Використання сулодексиду В пацієнтів з інвалідністю через цукровий діабет: систематичний огляд і метааналіз
Переклала й адаптувала канд. біол. наук Олександра Демецька
Мікро- та макросудинні ускладнення цукрового діабету (ЦД) займають одне з провідних місць серед захворювань у різних країнах світу [4]. Вони є причиною підвищеної смертності (головним чином серцево-судинної) та тяжкої інвалідності, яка загрожує якості життя, включно зі сліпотою, обмеженням рухів через кульгавість і діабетичну стопу, а також нирковою недостатністю, що потребує діалізу. Сулодексид є глікозаміногліканом, який може бути корисний для профілактики та лікування ЦД, включно з ускладненнями з боку нирок, очей і периферичних судин.
Протидіабетичні засоби: незадоволені клінічні потреби
Суворий контроль глікемії й артеріального тиску, зокрема за допомогою інгібіторів ангіотензинперетворювального ферменту (іАПФ) або блокаторів рецепторів ангіотензину (БРА), а також посилене багатофакторне лікування вважаються першим кроком до зниження ризику ускладнень ЦД, як-от інсульт [5], захворювання периферичних артерій (ЗПА) [6], ретинопатія [7] та нефропатія [8].
Терапевтичний арсенал для лікування ЦД було значно збагачено завдяки появі агоністів рецепторів глюкагоноподібного пептиду-1 (арГПП-1), інгібіторів дипептидилпептидази-4 й інгібіторів натрієзалежного котранспортера глюкози 2-го типу (іНЗКТГ-2).
Зазначені нові препарати було розроблено переважно для покращення контролю глікемії при ЦД, але для деяких з них, зокрема для арГПП-1 та іНЗКТГ-2, клінічний вплив на смертність від серцево-судинних захворювань і діабетичну нефропатію виходить далеко за межі їхнього впливу на метаболічний контроль. Водночас невідомо, як ці нові препарати впливають на діабетичну ретинопатію, ЗПА та діабетичну стопу, особливо враховуючи занепокоєння щодо ризику погіршення перебігу ЗПА через іНЗКТГ-2 канагліфлозин [9]. Отже, досі існує потреба в лікарських засобах, які ефективні для запобігання й лікування діабетичних захворювань та їхніх ускладнень.
Сулодексид – перспективний препарат для профілактики та лікування діабетичних ускладнень і загальної діабетичної інвалідності
Від моменту представлення гіпотези Стено щодо патогенезу діабетичних ускладнень [10] ендотеліальний глікокалікс вважають ключовим гравцем у перебігу ЦД та його комплікацій [11]. Отже, захисна дія сулодексиду, яку він чинить на глікокалікс [12-17], обґрунтовує доцільність застосування препарату для запобігання деградації ендотеліального глікокаліксу або для його відновлення при діабеті.
Сулодексид є глікозаміногліканом, який складається з двох фракцій: фракції швидкого гепарину (80%), що має спорідненість до антитромбіну III, та фракції дерматансульфату (20%), спорідненого до кофактора гепарину II [18].
Експериментальні дослідження продемонстрували сприятливий ефект сулодексиду в щурів із ЦД не тільки з приводу зменшення альбумінурії [19, 20], а й щодо захисту морфології та функції ендотелію [21-23]. Останнє може бути пов’язано із захисною та регенерувальною діями сулодексиду на глікокалікс як в експериментальних [24-27], так і в клінічних дослідженнях [28]. Установлено, що сулодексид чинить протизапальну [29-31], антипротеолітичну [32, 33] й антиоксидантну дії [25, 34, 35], включно з впливом на метаболічний і неметаболічний стрес [36]. Інгібування гепаранази [37, 38], імовірно, сприяє захисту ендотелію, а також зменшенню сигналізації, яка пов’язана з кінцевими продуктами глікації [39], запобіганню прогресуванню жорсткості судинної стінки [40], пригніченню синтезу фактора росту ендотелію судин [41] і сприятливому впливу на ендотеліальний оксид азоту [42, 43].
Сулодексид не впливає на метаболізм глюкози та глікемічний контроль; незважаючи на це, велике дослідження, проведене до того, як набули чинності поточні рекомендації щодо лікування інфаркту міокарда, котре охоплювало 10% пацієнтів з діабетом, повідомило про зниження ризику повторного інфаркту та смертності від серцево-судинних захворювань на тлі тривалого застосування сулодексиду [44].
Отже, сулодексид може бути одним із препаратів, ефективних у профілактиці та лікуванні діабетичних ускладнень, а також загальної діабетичної інвалідності.
У систематичному огляді та метааналізі було узагальнено доступну інформацію про вплив сулодексиду в пацієнтів із ЦД 1-го або 2-го типу щодо профілактики й лікування ускладнень, які вражають очі (діабетична ретинопатія), периферичний кровообіг (ішемія нижніх кінцівок з виразками або без них; кульгавість) і нирки (мікро- та макроальбумінурія). Загалом було проаналізовано 45 досліджень, у тому числі 25 рандомізованих клінічних досліджень (РКД), із загальною кількістю 2817 пацієнтів, які отримували сулодексид. Серед них 63% були чоловіками, середній вік становив 56,8 року, 85% страждали на ЦД 2-го типу. РКД включали 2074 пацієнтів, які отримували сулодексид (66% чоловіків, середній вік – 58,8 року, 91% пацієнтів із ЦД 2-го типу) [45].
Діабетична ретинопатія
Дослідження, проведені відповідно до належного плану та на досить великій вибірці уражених очей, повідомили про значне зменшення вираженості макулярних твердих ексудатів у пацієнтів з легкою та помірною непроліферативною діабетичною ретинопатією протягом 1 року лікування сулодексидом порівняно з контрольною групою. Також спостерігався регрес супутнього набряку макули.
Пацієнти, які отримували лікування сулодексидом, мали відношення шансів щодо покращення стану у 2,79 раза більше (95% довірчий інтервал (ДІ) 1,16-6,74) порівняно з контрольною групою (p=0,023) [64].
Загалом отримано достатньо доказів, щоби вважати, що терапія сулодексидом протягом 4-12 місяців сприяє зменшенню мікросудинних аномалій сітківки, твердих ексудатів і крововиливів за непроліферативної діабетичної ретинопатії.
Периферичні судинні ускладнення
ЗПА є тяжким довгостроковим ускладненням діабету, що призводить до інвалідності, основною причиною болю при фізичному навантаженні, хронічного болю, обмеження ходьби, ампутації кінцівок і гангрени [130].
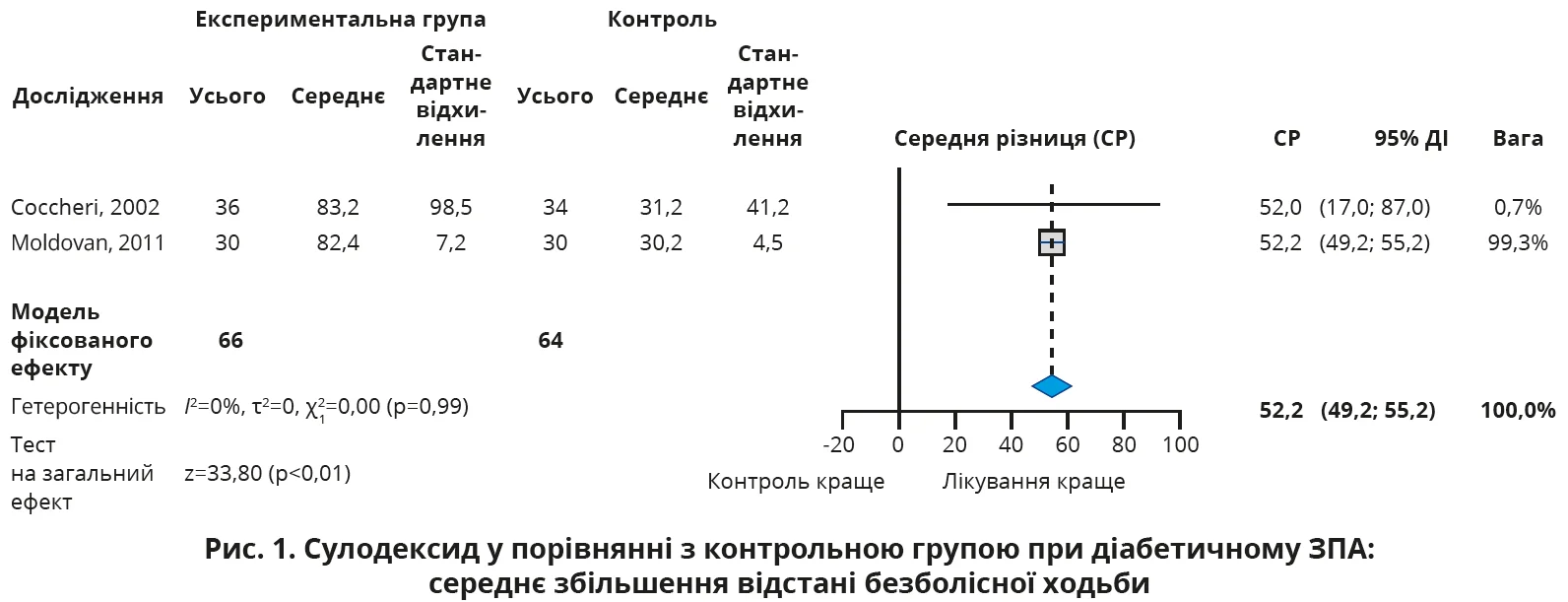
Кінцевими точками, які спостерігалися у відповідних дослідженнях, були дистанція ходьби без болю та максимальна дистанція ходьби. Лікування передбачало внутрішньом’язові ін’єкції щодня по 600 ЛО (ліпопротеїнліпазних одиниць) сулодексиду протягом 2-3 тижнів з подальшим пероральним лікуванням у дозі 250 або 500 ЛО сулодексиду двічі на день протягом загального періоду спостереження від 3 тижнів до 6 місяців (у середньому 22 тижні) в 119 пацієнтів.
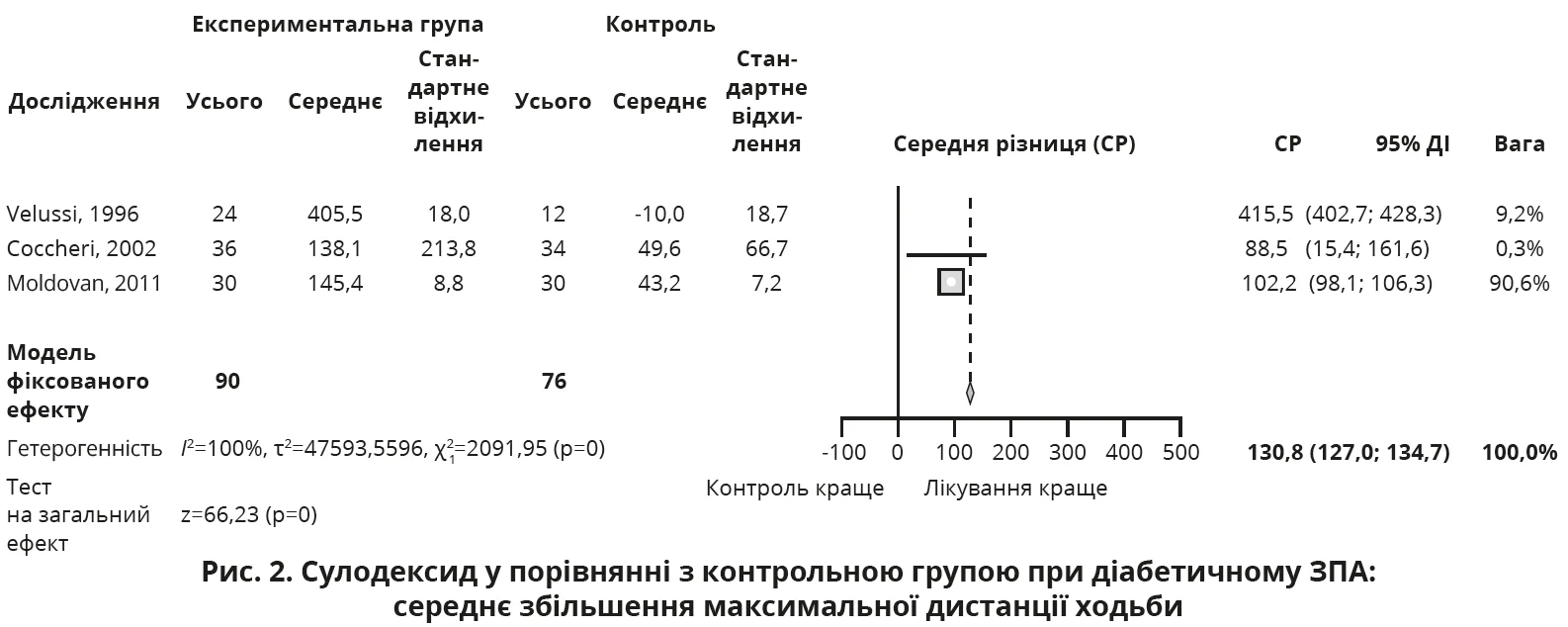
У якісних дослідженнях було отримано достатньо доказів того, що сулодексид збільшує дистанцію безболісної ходьби на 52 м (95% ДІ 49-55 м) і максимальну дистанцію ходьби на 130 м (95% ДІ 127-135 м) у пацієнтів з діабетом і периферичною ангіопатією та кульгавістю (рис. 1, 2).
Сприятливий вплив сулодексиду на ЗПА заслуговує на особливу увагу, оскільки жодне інтервенційне дослідження з «традиційними» та новими протидіабетичними препаратами досі не торкалося цього стану. Навпаки, висловлюються занепокоєння з приводу безпеки іНЗКТГ-2 щодо периферичної ангіопатії [9].
ЦД і трофічні виразки
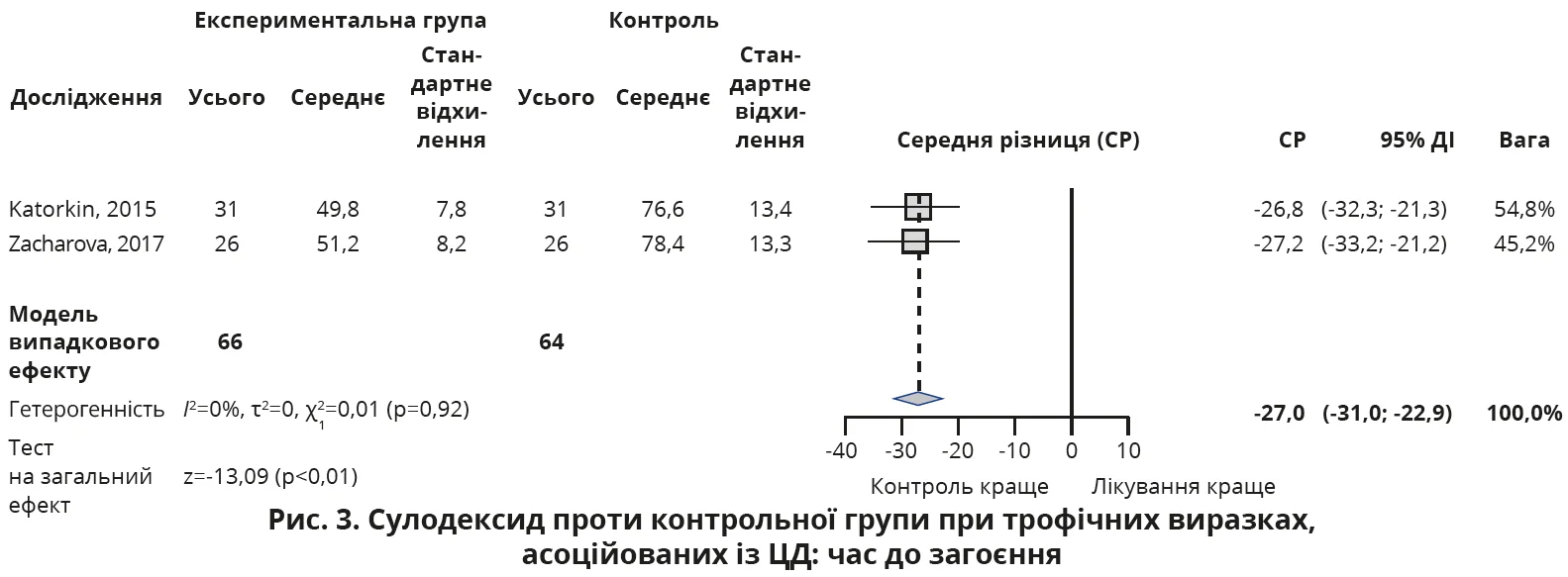
Кінцевими точками, які спостерігалися в трьох відповідних дослідженнях, були частка загоєних виразок і час до повної повторної епітелізації. Два з цих досліджень були спрямовані на пацієнтів із хронічною венозною хворобою класу C6 за CEAP (хронічні венозні виразки ніг) і ЦД 2-го типу.
Лікування проводилося з початковим періодом тривалістю 3 тижні з однією внутрішньом’язовою ін’єкцією 600 ЛО сулодексиду щодня, після чого протягом 4-7 тижнів перорально вводили 250-500 ЛО сулодексиду двічі на день протягом загального періоду спостереження 7,5 тижнів у 69 пацієнтів. Контрольна група включала 6 пацієнтів, які отримували плацебо згідно з подвійно сліпим дизайном, і 57 пацієнтів, які отримували стандартне лікування.
Загоювання трофічних виразок у пацієнтів, які отримували сулодексид, відбувалося в середньому на 27 днів раніше (95% ДІ 23-31; p<0,01), ніж в учасників контрольної групи (рис. 3).
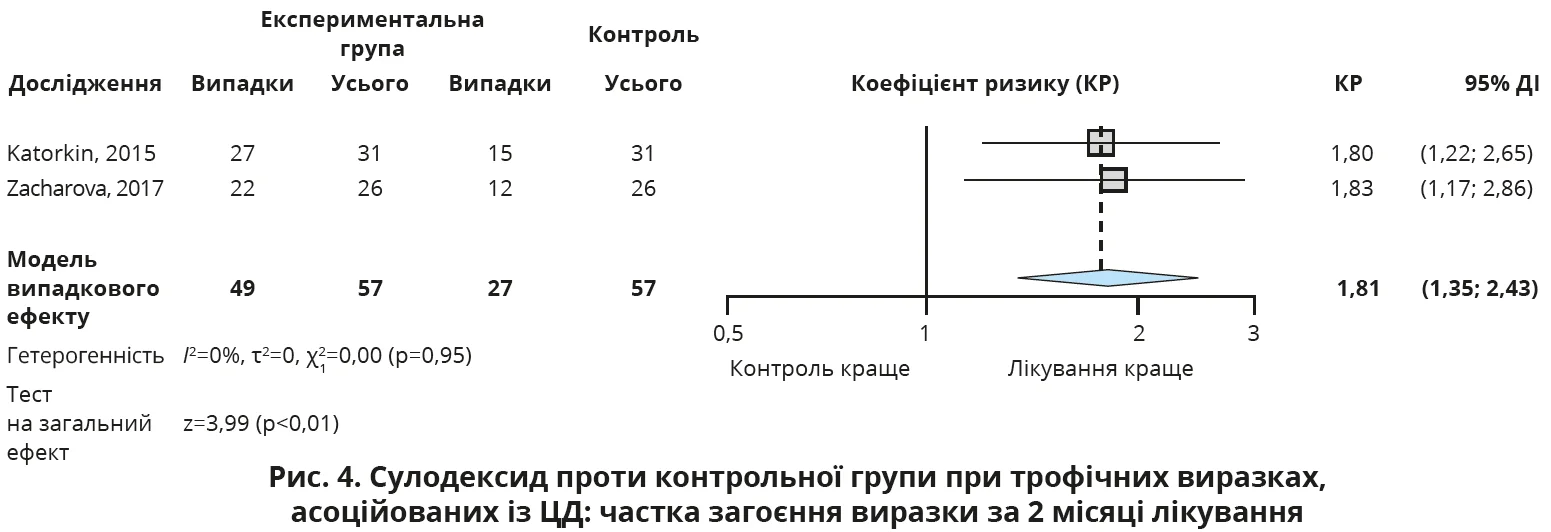
Щодо частки загоєння виразки протягом 2 місяців лікування, то пацієнти, які отримували сулодексид, мали ймовірність покращення стану в 1,8 раза (95% ДІ 1,4-2,4) більшу, ніж суб’єкти в контрольній групі (p<0,01; рис. 4).
Ознаки діабетичної нефропатії
Дослідження діабетичної нефропатії були численними, але різнорідними та різної якості. Лікування було урізноманітнено шляхом уведення (лише внутрішньом’язове; внутрішньом’язове/ внутрішньовенне введення з подальшим пероральним лікуванням; лише пероральне лікування); за дозою (від 600 до 2000 ЛО сулодексиду); за тривалістю (від 3 тижнів до 12 місяців) [93, 103].
Контрольованим результатом була швидкість виведення альбуміну. Загалом можна було спостерігати значний ефект лікування щодо зниження екскреції альбуміну із сечею. Порівняно з контрольною групою сулодексид знижував швидкість екскреції альбуміну із сечею на стандартизований розмір -1,28 (95% ДІ від -1,67 до -0,90).
Аналіз досліджень щодо впливу сулодексиду на лікування діабетичної нефропатії, котра контролюється як екскреція альбуміну із сечею, виявив, що сулодексид значно зменшує альбумінурію порівняно з контрольною групою.
Слід зазначити, що було зафіксовано сприятливий ефект на тлі застосування сулодексиду також при інших формах нефропатії (хронічний гломерулонефрит [128] і профілактика транзиторної нефропатії за допомогою контрастних речовин [129]).
Ефект лікування за типом діабету, схемою введення та супутнім застосуванням лікарських засобів
Метааналіз, розподілений за типом діабету, підтвердив неоднорідність популяцій, планів, графіків лікування й умов, продемонструвавши значну неоднорідність у загальному аналізі та в кожній із двох підгруп (ЦД 1-го та 2-го типів). Однак ефект сулодексиду був статистично значущим у підгрупах пацієнтів як із ЦД 1-го типу (p<0,01), так і з ЦД 2-го типу (p<0,01), а також у загальному аналізі (p<0,01).
Загалом ефект сулодексиду був достовірно більшим, аніж у контрольній групі, при ЦД 1-го та 2-го типів; у разі мікро- й макроальбумінурії; з або без одночасного застосування іАПФ/БРА та незалежно від дози препарату, шляху введення та тривалості лікування.
Одне з питань, яке періодично порушувалося щодо лікування сулодексидом, стосувалося найдоцільнішої схеми лікування. Схеми, перевірені в дослідженнях, залучених до аналізу, передбачали різні шляхи введення (лише парентеральне; парентеральне з подальшим пероральним прийманням; лише пероральне приймання), різні дози (від 600 ЛО сулодексиду щодня парентерально до 4000 ЛО сулодексиду щодня перорально) та різну тривалість лікування (від 3 тижнів до 24 місяців).
Існує достатньо вказівок на те, що парентеральне лікування при досліджуваних станах не має суттєвих переваг перед пероральним лікуванням [73, 86, 105, 131] і що ефект, імовірно, буде більшим за більшої тривалості лікування [90, 93]. Дози менш ніж 1000 ЛО сулодексиду на день, імовірно, будуть менш ефективними [89].
Профіль безпеки
Частоту побічних ефектів можна оцінити приблизно в 5% (95% ДІ 2-8%) із великою гетерогенністю. Гетерогенність здебільшого була спричинена відмінностями між РКД й іншими дослідженнями.
Натомість у порівняльних дослідженнях не було жодних доказів різної частоти побічних ефектів між групою сулодексиду та контрольною групою: співвідношення ризиків становило 0,907 (95% ДІ 0,699-1,176; p=0,46).
Висновки
Сулодексид є ефективним засобом для лікування периферичних судинних ускладнень у пацієнтів з діабетом, оскільки він поліпшує здатність ходити та прискорює загоєння виразок нижніх кінцівок.
Також наявні докази сприятливого впливу сулодексиду при непроліферативній діабетичній ретинопатії.
Сулодексид був корисним для лікування пацієнтів із ЦД 1-го та 2-го типів і різними ступенями нефропатії, оскільки він зменшував екскрецію альбуміну із сечею. Перспективними напрямами подальших досліджень є вивчення ефекту сулодексиду залежно від ступеня нефропатії та супутнього застосування іАПФ/БРА, а також тривалість ефекту після закінчення лікування.
За матеріалами:
Bignamini A.A., et al. Sulodexide for diabetic-induced disabilities: a systematic review and meta-analysis. Adv. Ther. 2021; 38 (3): 1483-1513. doi: 10.1007/s12325-021-01620-1.
Повний список літератури знаходиться в редакції.