Стан кісток за патології паращитоподібних залоз: перегляд доказів щодо епідеміології, хірургічного та медикаментозного лікування. Частина 2
Переклала й адаптувала канд. мед. наук Ольга Королюк
Вплив хірургічного лікування на патологію кісток, пов’язану з ПГПТ
Єдиним радикальним методом лікування ПГПТ є хірургічне видалення уражених ПЩЗ. Серед інших критеріїв (табл. 2) тяжкі ураження кісток з патологічними переломами, остеопорозом і рівнем кальцію в сироватці крові >0,25 ммоль/л (1 мг/дл) вище верхньої межі норми є вагомим показанням до операції. Основними цілями паратиреоїдектомії є відновлення нормального рівня кальцію, усунення симптомів гіперкальціємії, зниження ризику переломів і ниркових ускладнень. За умови проведення досвідченим хірургом операція є успішною в понад 95% випадків із частотою ускладнень <1%; інтраопераційний моніторинг ПТГ може бути корисним для оцінювання успішності резекції.
Відразу після операції спостерігається нормалізація рівнів ПТГ і кальцію; протягом кількох місяців знижується активність ремоделювання кісток і відзначається стійке покращення симптомів. У ретроспективному дослідженні оцінювали МЩКТ та ризик переломів після операції; незалежно від статі спостерігалося значне, хоча й тимчасове підвищення МЩКТ стегнової кістки протягом 2 років, однак через 5 років показники знижувалися нижче початкового рівня; втім, підвищення МЩКТ хребців було значним і стійким протягом 8 років. Інше дослідження показало виражене тривале покращення ремоделювання та структури губчастих кісток через 3 роки після операції. Кращий ефект у поперековому відділі хребта порівняно зі стегном пояснюється тим, що губчастим кісткам притаманне активніше ремоделювання, а отже, кращі умови для більшої та швидшої мінералізації після успішної операції. Результати досліджень щодо змін показника TBS суперечливі: одні демонструють покращення, інші не виявляють змін, що може пояснюватися різницею в складі досліджуваних груп, тяжкістю хвороби чи розміром вибірки.
Покращення МЩКТ після паратиреоїдектомії супроводжується істотним зниженням ризику переломів. У великому ретроспективному дослідженні з медіаною спостереження 6,5 років установлено, що паратиреоїдектомія незалежно асоціюється з меншою частотою переломів (коефіцієнт ризику 0,68).
Серед 1569 пацієнтів з ПГПТ операція зменшила 10-річний ризик перелому стегна на 8%, перелому руки – на 3% за відсутності впливу на переломи хребців, таза й інших ділянок нижніх кінцівок. Ризик переломів не асоціювався з рівнями кальцію та ПТГ. В іншому великому когортному дослідженні за участю понад 210 000 пацієнтів віком >65 років, серед яких 30% виконано паратиреоїдектомію протягом року після встановлення діагнозу, було виявлено, що операція асоціювалася з нижчим ризиком перелому стегна (коефіцієнт ризику 0,76) та будь-якого перелому (коефіцієнт ризику 0,78) порівняно з консервативним лікуванням. Абсолютне зниження ризику було значущим через 1, 2, 5 і 10 років після операції та зберігалося навіть після врахування таких чинників, як лікування остеопорозу, приймання цинакальцету чи стероїдів.
Відповідно, паратиреоїдектомія має клінічно значущий позитивний вплив на зниження ризику переломів у пацієнтів з ПГПТ.
Фіброзно-кістозний остеїт
Ретроспективне дослідження, що включало 51 пацієнта з ПГПТ та фіброзно-кістозним остеїтом після паратиреоїдектомії, виявило ранню ремінералізацію та приріст маси губчастих кісток, але не компактних кісток. Через 3 місяці після операції ділянки кістозних уражень, бурих пухлин і переломів були надмірно щільними. Маркери кісткового обміну показали швидке зниження рівня β-Cross Lap у сечі (CTX – C-кінцеві телопептиди колагену 1-го типу, що утворюються при розщепленні кісткової матриці остеокластами) в перший тиждень після операції та раннє підвищення ЛФ і остеокальцину, які зменшувалися через 6-9 місяців після втручання. В описі клінічного випадку видалення аденоми ПЩЗ сприяло нормалізації біохімічних показників, збільшенню МЩКТ та зникненню бурих пухлин. Описано також спонтанну регресію орбітальної пухлини через 2 роки після паратиреоїдектомії. У ретроспективному дослідженні спостерігалися нормалізація рівнів ПТГ і кальцію, а також цілковите зникнення бурих пухлин у середньому через 12 місяців (діапазон – 2-24 місяці) після операції.
Нормокальціємічний ПГПТ
За відсутності гіперкальціємії лікування залежить від ураження органів-мішеней. Пацієнти без значних кісткових чи ниркових змін мають перебувати під спостереженням. Успішна паратиреоїдектомія нормалізує рівень ПТГ; у пацієнтів з остеопорозом через 1 рік після операції підвищувалася МЩКТ хребців і стегнової кістки. За браком доказів сучасні настанови не рекомендують рутинну операцію при нкПГПТ.
Безсимптомний ПГПТ
Тривалі спостереження показали, що після паратиреоїдектомії біохімічні показники (рівні ПТГ і кальцію в сироватці крові, кальцію в сечі) залишалися нормальними, а МЩКТ зростала й утримувалася вище початкових рівнів протягом 15 років незалежно від часу проведення паратиреоїдектомії. Рандомізовані контрольовані дослідження (РКД) підтвердили значуще підвищення МЩКТ у поперековому відділі хребта та шийці стегнової кістки після операції порівняно зі спостережною тактикою. Систематичний огляд і метааналіз показали високоякісні докази біохімічного вилікування 96,1% пацієнтів з бсПГПТ після паратиреоїдектомії, а також значуще підвищення МЩКТ поперекових хребців і стегнової кістки. Водночас дані щодо ризику переломів і якості життя після операції залишаються невизначеними або низької якості. Інший систематичний огляд 8 РКД (447 дорослих з ПГПТ, переважно без симптомів) показав, що паратиреоїдектомія, ймовірно, значно підвищує відсоток вилікування порівняно зі спостереженням, але її вплив на серйозні побічні події мінімальний або відсутній, вплив на МЩКТ невизначений. У проспективній когорті 177 жінок з ПГПТ паратиреоїдектомія сприяла значному підвищенню МЩКТ у всіх ділянках скелета через 1 рік після операції. Приріст МЩКТ відзначався незалежно від початкової остеопенії чи остеопорозу, але в жінок з найбільшим приростом МЩКТ передопераційні рівні CTX та N-кінцевого пропептиду проколагену 1-го типу (P1NP) були вищими.
У скандинавському проспективному РКД порівнювали впливи паратиреоїдектомії та спостереження в пацієнтів з бсПГПТ. Через 5 років у групі оперативного втручання відзначено приріст МЩКТ у всіх ділянках (р <0,05 у поперековому відділі хребта), за винятком дистальної третини променевої кістки, а також зменшення рівнів P1NP (р >0,05) та CTX
(р <0,05). У групі спостереження МЩКТ знизилася в усіх ділянках, за винятком поперекового відділу хребта, що, на думку авторів, може бути зумовлено високою поширеністю прогресивного остеоартрозу хребта в досліджуваній групі. Десятирічне спостереження підтвердило позитивний вплив операції на МЩКТ поперекових хребців; у групі спостереження МЩКТ зменшилося в усіх ділянках. Дані щодо переломів були нульові; смертність і ризики серцево-судинних і ниркових ускладнень у групі спостереження не зростали. Отже, спостереження може бути безпечним варіантом для цієї категорії пацієнтів.
Метааналіз 5 РКД і 30 когортних досліджень (понад 238 000 пацієнтів, серед яких 73 778 – після паратиреоїдектомії) показав, що оперативне втручання знижує ризик переломів (особливо стегна) порівняно зі спостереженням, хоча приріст МЩКТ не був відповідним, що свідчить про інші механізми впливу. Автори відзначили проблеми достовірності через включення різних типів досліджень. Інший метааналіз порівнював впливи операції та медикаментозного лікування в пацієнтів з бсПГПТ: після операції рівні кальцію й ПТГ значно знизилися, тоді як у групі фармакотерапії рівні кальцію повернулися до початкових показників (імовірно, через низьку прихильність).
У пацієнтів на фармакотерапії показники МЩКТ поперекових хребців, стегнової кістки та кульшового суглоба були нижчими, ніж у прооперованих. Протягом близько 3,5 років спостереження різниці в частоті переломів між групами не було.
Є також дані про значне зростання показника TBS у пацієнтів з бсПГПТ через 24 місяці після паратиреоїдектомії, тоді як за консервативного ведення TBS мав тенденцію до зниження. Зменшення TBS корелювало з ризиком хребцевих переломів незалежно від МЩКТ.
Тож у пацієнтів з бсПГПТ паратиреоїдектомія забезпечує достовірне біохімічне вилікування та приріст МЩКТ в ділянках поперекового відділу хребта й шийці стегнової кістки. Дані щодо зниження ризику переломів залишаються суперечливими.
ПГПТ, пов’язаний з MEN1
Хірургічне втручання є методом вибору для пацієнтів з гіперкальціємією, спричиненою генетичним ПГПТ. Однак асинхронне ураження кількох залоз, що асоціюється з високими показниками рецидивної гіперкальціємії (20-60% у пацієнтів з MEN1 проти 4% за спорадичного ПГПТ), ускладнює втручання. Щодо післяопераційного стану кісток, є дані про середнє покращення МЩКТ шийки стегна на 5%, поперекового відділу хребта на 3% після операції. Інше повідомлення підтверджує статистично незначущий приріст кісткової маси після паратиреоїдектомії в усіх досліджуваних ділянках.
Синдром голодних кісток
Синдром голодних кісток є рідкісним, але серйозним ускладненням після успішної паратиреоїдектомії в пацієнтів з тяжким ураженням кісток. Характеризується швидкою, глибокою та тривалою гіпокальціємією, гіпофосфатемією, гіпомагніємією після операції внаслідок різкого зниження резорбції й посилення мінералізації кісток. Може потребувати внутрішньовенного введення кальцію. Лікування включає кальцій, вітамін D та магній, але універсальної стратегії немає. Дефіцит вітаміну D вважався фактором ризику, але передопераційна його корекція не запобігала ускладненню. До факторів ризику відносять: високі рівні ЛФ, ПТГ, кальцію, сечовини; старший вік; наявність бурих пухлин чи фіброзно-кістозного остеїту; великі або атипові пухлини; тривала операція. Деякі дані свідчать про можливий захисний ефект передопераційного призначення бісфосфонатів, але через ризик посилення гіпокальціємії та відсутність РКД
їх профілактичне застосування не схвалене.
Вплив фармакотерапії на асоційоване з ПГПТ ураження кісток
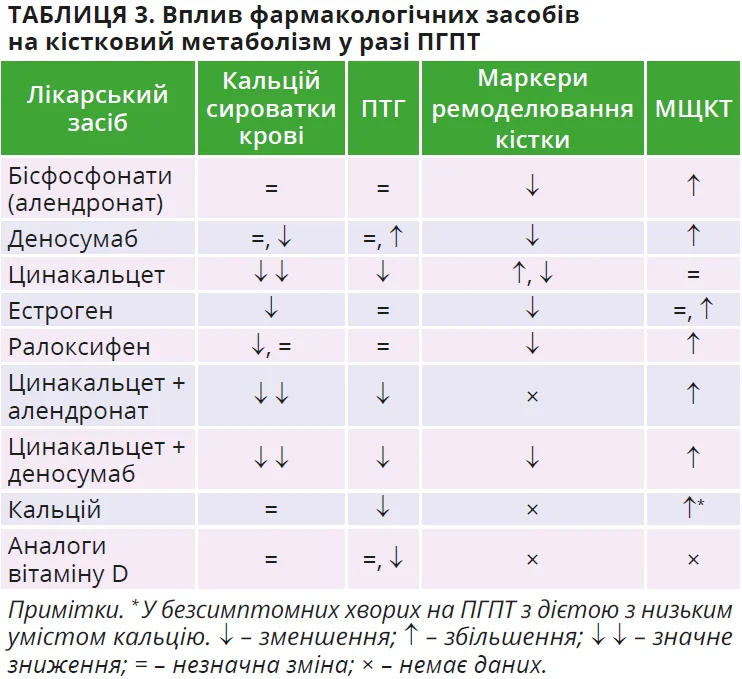
Через відсутність фармакотерапії, що забезпечує вилікування, нехірургічне лікування застосовується за наявності симптомів у пацієнтів, яким не показана операція, при складнощах локалізації збільшених ПЩЗ або в разі відмови від операції. Крім того, фармакотерапію можна розглядати за бсПГПТ. Вплив фармакотерапії на кістковий метаболізм узагальнено в таблиці 3.
Незалежно від вибору препарату слід дотримуватися загальних заходів: адекватна гідратація, щоб запобігти загостренню гіперкальціємії; уникнення тіазидних діуретиків (підвищують реабсорбцію кальцію в нирках) і препаратів літію (підвищують ПТГ); достатній рівень кальцію в раціоні, корекція дефіциту вітаміну D (цільовий рівень 25(OH)D >20-30 нг/мл).
Серед лікарських засобів найвивченішими є пероральні бісфосфонати, зокрема алендронат. Вони знижують маркери кісткового ремоделювання й підвищують МЩКТ у ділянках стегнової кістки, кульшового суглоба та хребців, хоча рівні кальцію та ПТГ залишаються незмінними; даних щодо зниження ризику переломів немає. Для внутрішньовенних бісфосфонатів доказів ефективності при ПГПТ поки що немає. Деносумаб показав позитивний вплив на МЩКТ у шийці стегна, кульшовому суглобі та поперековому відділі хребта, а також на показник TBS. Цинакальцет ефективно знижує рівні кальцію та ПТГ, але не впливає на МЩКТ. Гормональна терапія та селективні модулятори естрогенових рецепторів здатні підвищувати МЩКТ і зменшувати маркери ремоделювання кісток, але їхній вплив на кальцій і ПТГ мінімальний.
Нижче обговорюватимуться відповідні дані щодо впливу фармакотерапії на ураження кісток унаслідок ПГПТ.
Бісфосфонати
Бісфосфонати – аналоги пірофосфатів, потужні інгібітори резорбції кістки, що інактивують остеокласти через блокаду ферменту фарнезилдифосфатсинтази в холестериновому шляху, пригнічуючи ізопренілювання. Антирезорбтивна активність обґрунтовує їх використання при ПГПТ.
Найдослідженішим є алендронат. У 12 дослідженнях тривалістю до 2 років показано зниження кальцію та ПТГ у перші 6 місяців з подальшим поверненням до початкових рівнів; стабільне зниження біохімічних маркерів кісткового обміну; приріст МЩКТ переважно в губчастих кістках (поперековий відділ хребта, стегнова кістка) з мінімальним або відсутнім ефектом у дистальному відділі променевої кістки з переважно кортикальною структурою. Позитивний вплив алендронату на кістковий метаболізм підтверджено при всіх клінічних варіантах ПГПТ (класичному, легкому, нкПГПТ та бсПГПТ). Це робить його корисною альтернативою паратиреоїдектомії для пацієнтів з остеопорозом.
Застосування ризедронату продемонструвало значне гостре зниження кальцію в сироватці крові за відсутності впливу на МЩКТ та мінералізацію кістки.
Цікаво, що збільшення МЩКТ не супроводжувалося зниженням ризику переломів. Ретроспективний аналіз ефективності хірургічного лікування або застосування бісфосфонатів (алендронат у 92% випадків) порівняно зі спостереженням у 6272 пацієнтів з ПГПТ виявив, що підвищення МЩКТ внаслідок лікування бісфосфонатом не демонструвало переваг щодо ризику переломів. Ба більше, ризик переломів навіть збільшувався в тих, хто приймав бісфосфонати. Проте такі результати можуть бути зумовлені старшим віком і нижчою початковою МЩКТ у пацієнтів, які отримували бісфосфонати, порівняно з пацієнтами, які не лікувалися (середній вік – 71 проти 65 років; медіана МЩКТ – 0,56 проти 0,66 відповідно); крім того, не було даних щодо початкової поширеності переломів. У нещодавньому систематичному огляді та метааналізі також не спостерігалося значущого впливу бісфосфонатів на ризик переломів.
Деносумаб
Деносумаб – моноклональне антитіло людини, націлене на RANKL. Його застосування не лімітує швидкості клубочкової фільтрації (ШКФ), що важливо для літніх людей і пацієнтів з тяжким ураженням нирок. Деносумаб є безпечним і ефективним варіантом лікування для жінок після менопаузи з ПГПТ та легкою-помірною хронічною хворобою нирок (ХХН). Після 24 місяців лікування спостерігалося значне підвищення МЩКТ; крім того, в підгрупі з ХХН зафіксовано значне зниження рівня кальцію порівняно з підгрупою без ХХН. Ризик гіпокальціємії, особливо тяжкої, вищий на пізніх стадіях ХХН (3b-5) і в осіб з нижчими початковими рівнями кальцію.
Через 24 місяці лікування деносумабом жінок з остеопорозом унаслідок ПГПТ спостерігалося значуще підвищення МЩКТ у стегновій кістці, кульшовому суглобі та хребцях порівняно з початковими показниками, а також порівняно з пацієнтами з первинним остеопорозом за відсутності змін у сироваткових рівнях ПТГ, кальцію й ЛФ. У нещодавньому РКД лікування деносумабом достовірно підвищило МЩКТ у хребцях і кульшовому суглобі та знизило біохімічні маркери ремоделювання; в поєднанні із цинакальцетом деносумаб покращив біохімічні показники в пацієнтів з ПГПТ.
Впливи деносумабу й алендронату на кістковий метаболізм у пацієнтів з ПГПТ порівнювали в метааналізі. Деносумаб забезпечував швидке, але короткочасне зниження кальцію в сироватці крові; алендронат мав триваліший ефект (до 12 місяців), який зникав через 24 місяці. Обидва препарати не мали стійкого впливу на рівень ПТГ. Лікування деносумабом упродовж 12 місяців достовірно підвищувало МЩКТ у поперековому відділі хребта та шийці стегнової кістки. У ретроспективному дослідженні деносумаб 1 раз на 8 місяців виявився не менш ефективним за успішну паратиреоїдектомію щодо покращення МЩКТ та перевершував операцію щодо впливу на TBS хребта. Хоча впливу на рівні кальцію не продемонстровано, деносумаб може бути успішним містком до паратиреоїдектомії, забезпечуючи швидкий контроль гіперкальціємії в тяжких випадках. Водночас його слід застосовувати з обережністю через ризик гіпокальціємії, особливо за наявності таких чинників ризику, як ниркова недостатність, тривалий гіперпаратиреоз, рак ПЩЗ та дефіцит вітаміну D. Описано випадок вираженої гіпофосфатемії в пацієнта з нкПГПТ, що підкреслює необхідність адекватної корекції кальцію та вітаміну D.
Кальциміметики
Цинакальцет – перший препарат цієї групи, підвищує чутливість CaSR до циркулювального кальцію в клітинах ПЩЗ, знижуючи секрецію ПТГ і рівень кальцію. Спершу схвалений для лікування ВГПТ, згодом він став альтернативою паратиреоїдектомії при ПГПТ. Показання до його застосування при гіперпаратиреозі узагальнено в таблиці 4.
Великі дослідження підтвердили ефективність цинакальцету в нормалізації кальцію та зниженні ПТГ у пацієнтів з ПГПТ. У метааналізах показано: препарат добре переноситься, знижує та нормалізує рівні кальцію майже в 90% випадків, що супроводжується значним підвищенням фосфату. Попри зниження ПТГ, лише в 10% пацієнтів спостерігається його нормалізація. У багатоцентровому проспективному дослідженні PRIMARA (303 пацієнти з ПГПТ) 60% досягли зниження кальцію ≥1 мг/дл (≥0,25 ммоль/л) після
1 року лікування в дозі 30 мг/добу (медіана); основними побічними ефектами були легкі шлунково-кишкові симптоми. Цинакальцет ефективний за різних форм ПГПТ незалежно від ступеня тяжкості. У низьких дозах (30 мг/добу) лікування добре переноситься та може бути містком до операції в разі тяжкої гіперкальціємії й ураження кісток, у групах ризику виникнення післяопераційного синдрому голодних кісток. Додатково він впливає на рівні фосфору та кальцію в сечі, але на сьогодні немає доказів його позитивного впливу на покращення МЩКТ. Тому при вираженій кістковій патології доцільно поєднувати цинакальцет з антирезорбтивними засобами.
За даними досліджень, цинакальцет зменшує об’єм ПЩЗ при ВГПТ завдяки апоптозу паратиреоїдних клітин. У пацієнтів з ПГПТ 6-місячне лікування цинакальцетом зменшувало розмір аденом на ~29%, описано навіть випадки спонтанної ремісії. У разі ПГПТ, асоційованого з MEN1, частіше спостерігаються післяопераційні рецидиви й ускладнення; тому цинакальцет ефективний за персистенції ПГПТ та за наявності протипоказань до операції. У РКД за участю 15 пацієнтів з гіперпаратиреозом унаслідок MEN1 цинакальцет нормалізував сироваткові рівні кальцію, підвищував рівні фосфату та знижував ПТГ після 3 місяців терапії; в половини пацієнтів рівень ПТГ нормалізувався. Даних щодо здатності цинакальцету змінювати розміри ПЩЗ або впливати на МЩКТ немає.
Гормональна замісна терапія
Оскільки ПГПТ найчастіше трапляється в жінок після менопаузи, як фармакотерапію розглядали естрогени. Короткочасне застосування етинілестрадіолу чи норетистерону в пацієнток з легким ПГПТ сприяло зниженню рівнів кальцію в сироватці крові та сечі, а також маркерів резорбції кісток, але не впливало на рівні ПТГ. У 2-річному РКД за участю 42 жінок кон’юговані естрогени з медроксипрогестероном зменшували маркери кісткового метаболізму й рівні кальцію в сечі та значно підвищували МЩКТ в усіх ділянках. Побічні ефекти були легкими (масталгія, кровотечі). У 4-річному продовженні (23 пацієнтки з початкової когорти) відзначено невелике зниження кальцію в сироватці крові, зменшення маркерів ремоделювання кістки та приріст МЩКТ порівняно з плацебо (7,4 та 7,5% у шийці стегна й поперековому відділі хребта, 7% на передпліччі, 4,6% загалом у тілі). Початкове зниження рівня кальцію в сечі не зберігалося протягом 4 років.
Ралоксифен
Ралоксифен – селективний модулятор естрогенових рецепторів (SERM), що діє як агоніст естрогенів у метаболізмі кісток і ліпідів та як антагоніст у молочній залозі й матці. Це єдиний SERM, досліджений у разі ПГПТ. У 3 жінок у постменопаузі з легким безсимптомним ПГПТ терапія ралоксифеном у добових дозах 60 або 120 мг протягом 1 року сприяла підвищенню МЩКТ (поперековий відділ хребта +3,4%, шийка стегна +2,5%), істотному зниженню сироваткових рівнів кальцію та фосфату й рівнів дезоксипроліну та кальцію в сечі; але наприкінці дослідження рівні іонізованого кальцію й ПТГ повернулися до початкових значень. У більшому РКД (n=18) також відзначено зниження кальцію та NTX у сироватці крові, проте інші показники (ПТГ, фосфат, кальцитріол, ЛФ) не змінювалися; ефекти зникали після скасування препарату. Після скасування ралоксифену зміни кальцію та кісткових маркерів повертаються до попередніх значень. Порівняно з алендронатом ралоксифен слабше знижував кальцій, але обидва препарати однаково підвищували МЩКТ у поперековому відділі хребта після 12 місяців лікування.
Кальцій і вітамін D
Вищий рівень кальцію в раціоні пригнічує секрецію ПТГ, проліферацію клітин ПЩЗ та знижує ризик ПГПТ, що доведено в масштабному проспективному дослідженні тривалістю 22 роки. Обережна суплементація кальцію в пацієнтів з бсПГПТ і низьким споживанням кальцію зменшує ПТГ і покращує стан шийки стегна за даними DXA без істотного підвищення рівнів кальцію в крові та сечі. Проте через ризик гіперкальціємії/гіперкальціурії слід дотримуватися рекомендованих настановами норм і проводити ретельний моніторинг під час суплементації.
Поширеність недостатності вітаміну D у пацієнтів з ПГПТ вища, ніж у загальній популяції; крім того, зазвичай знижується загальний рівень 25(OH)D, тоді як рівень вільного 25(OH)D може бути подібним або навіть вищим, аніж у здорових людей. Дефіцит вітаміну D підвищує ризик гіпокальціємії/гіпоПТ після операції, потреби в кальцієвій підтримці та тривалій госпіталізації. Крім того, дефіцит вітаміну D асоціюється з більшою масою ПЩЗ, вищими рівнями ПТГ, кальцію й ЛФ, зниженням МЩКТ та гіршою геометрією кульшового суглоба в жінок після менопаузи. Водночас дані щодо зв’язку рівня вітаміну D з нефролітіазом, остеопорозом чи мікроархітектурою кістки суперечливі.
Клінічні дослідження та метааналізи дають неоднозначні результати щодо впливу суплементації вітамі-ну D: у пацієнтів з легким ПГПТ застосування добавок вітаміну D в осіб з його дефіцитом не забезпечувало значущих змін ПТГ, кальцію й фосфату в сироватці крові та рівнів кальціурії. Інший метааналіз указує на значуще зниження рівнів ПТГ й ЛФ без гіперкальціємії та гіперкальціурії. Отже, суплементація вітаміну D у пацієнтів з ПГПТ та дефіцитом вітаміну D є безпечною, але потребує ретельного моніторингу, із цільовим рівнем 25(OH)D 20-30 нг/мл.
Комбіноване лікування
Результати досліджень щодо застосування бісфосфонатів після паратиреоїдектомії суперечливі. У РКД, що порівнювало застосування золедронової кислоти та плацебо після операції, через 2 роки відзначено вищу МЩКТ у шийці стегнової кістки й поперековому відділі хребта та нижчі маркери ремоделювання кістки в групі, де використовували золедронову кислоту.
У великій когорті (n=1737) бісфосфонати підвищували МЩКТ, але зменшували позитивний вплив паратиреоїдектомії на ризик переломів. Інші дослідження не показали додаткової користі від бісфосфонатів після паратиреоїдектомії. Як указувалося вище, передопераційне застосування бісфосфонатів може знижувати ризик синдрому голодних кісток.
Антирезорбтивні препарати + цинакальцет: комбінація алендронату з цинакальцетом у 10 пацієнтів віком >50 років з явним ПГПТ і зниженням МЩКТ сприяла швидкому зниженню гіперкальціємії та гіперкальціурії, нормалізації сироваткових рівнів кальцію й ПТГ, підвищенню МЩКТ поперекових хребців (+9,6%); монотерапія цинакальцетом не впливала на МЩКТ. У РКД з деносумабом і цинакальцетом обидва препарати значно підвищували МЩКТ поперекових хребців і стегнової кістки; монотерапія деносумабом краще впливала на МЩКТ дистального відділу передпліччя. Було доведено, що деносумаб ефективно знижує ремоделювання кістки, а в поєднанні із цинакальцетом безпечно покращує біохімічний профіль пацієнтів з ПГПТ.
Отже, паратиреоїдектомія залишається найефективнішим варіантом щодо зниження ризику переломів. Бісфосфонати після паратиреоїдектомії покращують МЩКТ, але не знижують ризику переломів. Комбінація бісфосфонатів із цинакальцетом позитивно впливає на МЩКТ та рівень кальцію.
Карцинома ПЩЗ
Менш ніж 1% спорадичних випадків ПГПТ спричинені карциномою ПЩЗ. Карцинома може виникати спорадично або бути проявом генетичних синдромів HPT-JT, MEN1, MEN2A та сімейного гіперпаратиреозу. Наприклад, близько 15% пацієнтів з HPT-JT мають рак ПЩЗ. Пацієнти з карциномами зазвичай молодші, ніж з аденомами. Етіологія невідома, однак описані мутації генів HPRT2/CDC73, mTOR, KMT2D. Специфічні фактори ризику спорадичних карцином не визначені, але в анамнезі часто виявляють променеву терапію ділянки шиї, вторинний/третинний гіперпаратиреоз або аденому/гіперплазію ПЩЗ.
Зазвичай карцинома має повільний перебіг і низький ризик віддалених метастазів. Це функціональні пухлини з явним гіперпаратиреозом і гіперкальціємією, що проявляються загальними симптомами, ураженням кісток і нирок, аритміями та когнітивними розладами. Нормальний рівень кальцію в крові не виключає злоякісності. Описано також декілька випадків патологічних переломів як перших проявів хвороби. Рідкісні нефункціональні варіанти діагностуються пізно, після виникнення локальних або віддалених метастазів, оскільки в таких випадках ПТГ і кальцій тривало залишаються в межах норми.
Точний діагноз зазвичай установлюють після хірургічного видалення пухлини. Підозру на карциному викликають дуже високі рівні ПТГ (>1000 пг/мл) і кальцію (>14 мг/дл), великі ураження ПЩЗ з ознаками «злоякісності» при ультразвуковому дослідженні, осиплість голосу чи дисфагія, тяжкі ураження органів-мішеней. Тонкоголкова біопсія не рекомендована через ризик дисемінації.
Золотим стандартом лікування є резекція пухлини en bloc, але часті рецидиви потребують повторних операцій. У дослідженні NEKAR (n=83) рецидиви відзначено в 32 випадках; скелетні ускладнення – у ~23%, ниркові – у ~40%. Прогноз загалом сприятливий, але класичні ад’ювантні методи (променева терапія, хіміотерапія) малоефективні. При неоперабельних пухлинах ключове значення має контроль гіперкальціємії, яка є основною причиною смертності.
Ураження кісток за карциноми ПЩЗ
Ураження кісток за карциноми ПЩЗ загалом подібне до інших форм ПГПТ, але більшість пухлин гормонально активні та призводять до тяжкої гіперкальціємії. Гіперкальціємічна криза трапляється частіше, ніж при аденомах, і потребує невідкладної допомоги. На момент установлення діагнозу 80-90% пацієнтів уже мають ураження органів (нирок, кісток). У понад 40% спостерігається фіброзно-кістозний остеїт із субперіостальною резорбцією, ураження черепа на кшталт «сіль/перець» і бурі пухлини, що можуть імітувати метастази. Без лікування патологічні переломи виникають майже в 90% пацієнтів. У великому ретроспективному дослідженні в пацієнтів з карциномою спостерігалися значно вищі рівні кальцію, ПТГ і маркерів ремоделювання кістки, нижчі показники МЩКТ кульшового суглоба та шийки стегнової кістки порівняно з пацієнтами з аденомами або гіперплазією ПЩЗ.
Вплив хірургічного лікування при карциномі ПЩЗ
Основним методом лікування карциноми ПЩЗ є хірургічний. Золотим стандартом за підозри на злоякісність є радикальна резекція пухлини з широкими краями та видаленням усіх уражених структур. Відсутність точного діагнозу до чи під час операції ускладнює лікування, збільшує ризик рецидиву та потреби повторного втручання. Частим ускладненням після повної резекції пухлини є синдром голодних кісток, тому слід ретельно контролювати рівні кальцію та ПТГ. Успішне видалення пухлини сприяє зменшенню кісткових уражень, нормалізації біохімічних показників, підвищенню МЩКТ у стегновій кістці та поперекових хребцях, регресу рентгенологічних ознак і навіть зникненню бурих пухлин.
Вплив фармакотерапії при карциномі ПЩЗ
Захворюваність і смертність за карциноми ПЩЗ насамперед зумовлені гіперкальціємією. Пацієнтів з тяжкою гіперкальціємією чи кризою треба стабілізувати перед операцією. При неоперабельних або метастатичних пухлинах потрібна фармакотерапія хронічної гіперкальціємії. Крім гідратації та діуретиків, застосовують бісфосфонати (памідронат, золедронат), кальцитонін, октреотид, кортикостероїди, які дають тимчасовий ефект. Низка засобів не застосовується через нефротоксичність, зокрема мітраміцин, плікаміцин, нітрат галію. Деносумаб показав стійку ефективність у контролі гіперкальціємії при резистентності чи протипоказаннях до інших препаратів.
Цинакальцет
У багатоцентровому дослідженні за участю 29 неоперабельних пацієнтів з карциномою ПЩЗ поступове підвищення добової дози до 360 мг, яку розділяли на 4 прийоми, забезпечило значне та стійке зниження кальцію в сироватці крові (від 12,7±0,8 до 9,9±0,9 мг/дл) без істотних змін рівнів ПТГ й ЛФ. За неоперабельних, метастатичних чи рецидивних форм черезшкірне введення етанолу в пухлинні ураження сприяло тимчасовому зниженню ПТГ і кальцію в сироватці крові.
Імунотерапія
Імунотерапія – новий метод лікування гіперкальціємії при метастатичній карциномі ПЩЗ, вперше описана в 1999 р. Бардвеллом і Гарві. Використання синтетичних пептидів ПТГ (людських, бичачих) стимулювало утворення антитіл, які блокували дію високих рівнів ПТГ. У пацієнтів з тяжкою гіперкальціємією та резистентністю до стандартної терапії повторне введення синтетичних пептидів ПТГ забезпечувало клінічне й біохімічне покращення: зниження кальцію, нормалізацію ПТГ, регрес бурих пухлин, зменшення метастазів. Іноді після комбінації імунотерапії та хірургічного втручання досягали тривалої ремісії.
Останнім часом застосовуються інгібітори імунних контрольних точок. У пацієнтів з метастатичною карциномою ПЩЗ лікування пембролізумабом або ніволумабом сприяло біохімічній відповіді, зменшенню метастазів і виживанню без прогресування від 1 до 3 років. Наприклад, у жінки 46 років з метастазами через 12 років після первинної резекції карциноми ПЩЗ пембролізумаб нормалізував біохімічні показники; згодом їй було виконано хірургічну резекцію олігометастатичної хвороби черевних лімфатичних вузлів, що забезпечило щонайменше 3 роки без прогресування. У чоловіка 60 років із синдромом Лінча застосування пембролізумабу впродовж 4 місяців через тяжкий імунний коліт сприяло повній біохімічній відповіді та зменшенню легеневих метастазів; виживання без прогресування тривало щонайменше 2 роки. У жінки 64 років з рефрактерною гіперкальціємією внаслідок метастатичного ураження мозку та скелета через 6 місяців після першої хірургічної резекції імунотерапія ніволумабом забезпечила зникнення гіперкальціємії з виживанням без прогресування принаймні 1 рік.
Висновки
- Через високий рівень ПТГ у пацієнтів з ПГПТ посилюється ремоделювання кісток, порушується мінералізація, знижується мінеральна щільність кортикальних і трабекулярних кісток і підвищується ризик переломів.
- Успішна паратиреоїдектомія залишається основним методом лікування ПГПТ, що сприяє відновленню МЩКТ і зниженню ризику переломів; однак антирезорбтивні засоби (бісфосфонати, деносумаб) можуть зменшити резорбцію кісток і відновити МЩКТ.
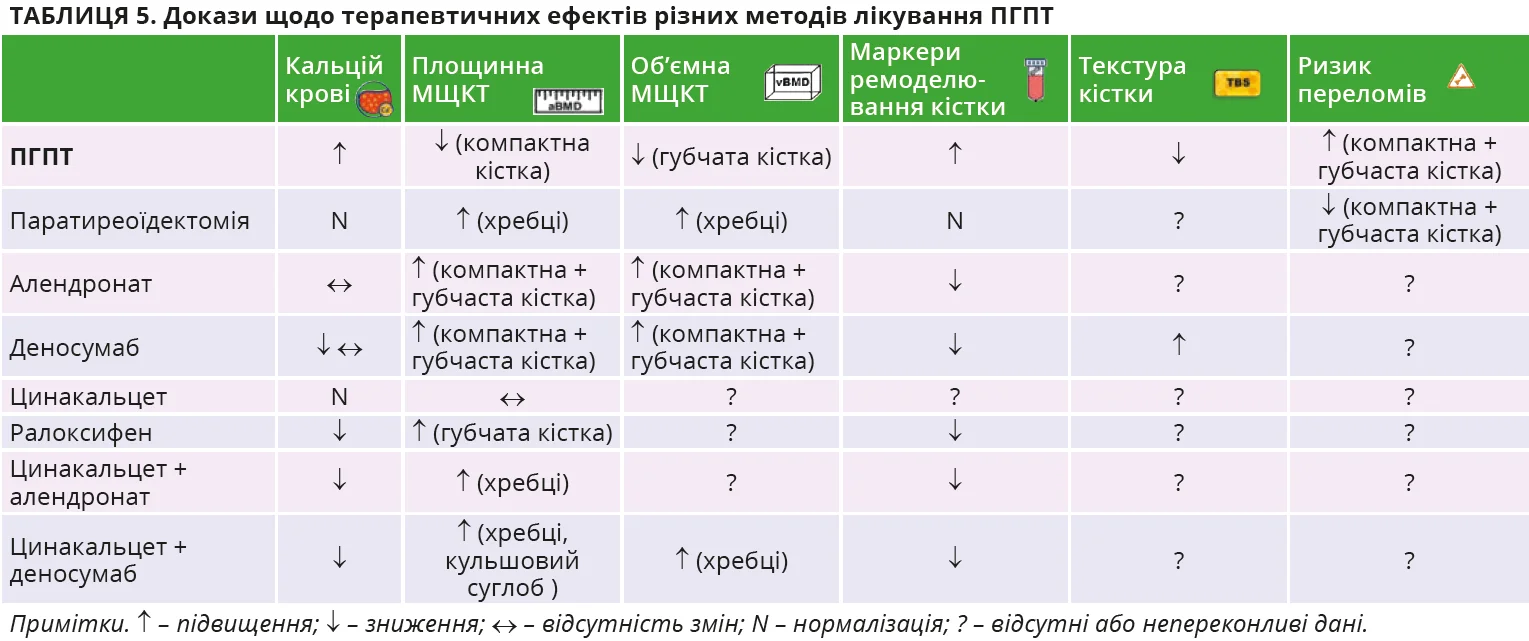
Основні ефекти доступних на сьогодні методів лікування ПГПТ підсумовуються в таблиці 5.