Скринінг діабетичної ретинопатії: нові можливості та виклики
Підготував д-р мед. наук Костянтин Бобришев
У світі поширеність сліпоти й інших порушень зору, спричинених діабетичною ретинопатією (ДР), із 1990 по 2015 р. зростала. Це пов’язано зі збільшенням поширеності цукрового діабету (ЦД) 2 типу, зокрема в бідних країнах і країнах із середнім рівнем доходу (Flaxman S. et al., 2017). Скринінг ДР потрібний для того, щоб виявляти осіб, які мають бути оглянуті спеціалістом. У результаті ці особи отримають своєчасне та повне офтальмологічне обстеження й лікування, що зможе запобігти постійній втраті зору. Крім того, візуалізація сітківки як складова скринінгу ДР дає змогу ідентифікувати осіб із ризиком серцево-судинних уражень і когнітивних порушень.
Чинники ризику ДР
Встановленими чинниками ризику ДР є велика тривалість ЦД, незадовільний контроль глікемії (збільшений рівень глікозильованого гемоглобіну), а також артеріальна гіпертензія. При цьому глікемія має більший вплив, аніж артеріальний тиск – АТ (Lachin J. et al., 2008; UKPDS Group, 1998; Chew E. et al., 2014; ACCORDION Eye Study Group, 2016).
Однак зв’язок між розвитком ДР і гіперглікемією / артеріальною гіпертензією не є абсолютним (Lachin J. et al., 2008). Існує чимало осіб із поганим контролем глікемії/АТ, в яких ДР не виникає. І навпаки, в деяких хворих із добрим контролем глікемії та нормальним АТ може виникнути ДР. Це пояснюється існуванням інших чинників ризику ДР: варіабельності глікемії (Lu J. et al., 2018; Zhao Q. et al., 2019), генетичної схильності (Arar N. et al., 2008; Hietala K. et al., 2008; Hallman D. et al., 2005; Monti M. et al., 2007), дисліпідемії, підвищеного індексу маси тіла, вагітності, статевого дозрівання й оперативного втручання з приводу катаракти (Yau J. et al., 2012).
Скринінг ДР: кого, коли та як
Сучасні рекомендації й інструментальне обстеження
Найновіші рекомендації щодо інструментального обстеження для скринінгу ДР було опубліковано у 2017-2018 рр. До них належать рекомендації Міжнародної ради з офтальмології – ICO (як частина настанов із догляду за оком у разі ЦД; Wong T.
et al., 2018) й Американської діабетичної асоціації – ADA (як частина програмної заяви з ДР; Solomon S. et al., 2017). Перше обстеження ока ADA рекомендує проводити вкрай ретельно. Час його здійснення визначається типом ЦД (табл. 1). Обсяг офтальмологічного обстеження за рекомендаціями ICO й ADA дещо відрізняється (табл. 2).


Мінімальний офтальмологічний скринінг має складатися з оцінки гостроти зору й обстеження сітківки, достатнього, щоб оцінити стадію ДР (Solomon S. et al., 2017). За класифікацією ICO (Wong T. et al., 2018), розрізняють п’ять стадій: відсутність ДР, м’яка непроліферативна ДР, середньотяжка непроліферативна, тяжка непроліферативна, проліферативна. Оновлена класифікація діабетичного макулярного набряку – ДМН (Wong T. et al., 2018) включає такі градації: відсутність ДМН; ДМН без залучення центра; ДМН із залученням центра.
Обстеження сітківки здійснюють за допомогою її фотографування та дослідження очного дна (офтальмоскопії). При ДР фотографія сітківки як без мідріазу, так і на його тлі продемонструвала кращу чутливість, аніж пряма чи непряма офтальмоскопія (Pugh J. et al., 1993; Harding S. et al., 1995). Результати багатопольової (три поля) візуалізації без мідріазу добре корелюють із результатами, отриманими при офтальмоскопії з дилатацією зіниць. Для одно- чи двопольової візуалізації під кутом у 45 градусів такої відповідності немає (Lee J. et al., 2019; Boucher M. et al., 2003). Досі невідомо, яка кількість ретинальних полів, досліджених за допомогою офтальмоскопії без дилатації зіниць, потрібна для коректного визначення ДР і ДМН та встановлення їхніх стадій у телемедичних скринінгових програмах. У минулому золотим стандартом вважали дослідження на дилатованих зірцях семи стандартних стерео-скопічних полів сітківки під кутом у 30 градусів (семипольове дослідження за протоколом ETDRS – Early Treatment Diabetic Retinopathy Study). Проте його проведення потребує тривалого часу, а саме дослідження є досить дорогим, і через це з метою скринінгу використовуватися не може. Отже, для скринінгу ДР і ДМН пропонували досліджувати меншу кількість полів: три, два й навіть одне центральне під кутами, що варіювали від 45 до 60 градусів (Bursell S. et al., 2001; Vujosevic S. et al., 2009; Scanlon P. et al., 2003; Williams G. et al., 2004). Дані свідчать, що у визначенні ДР і ДМН дослідження обмеженої кількості полів (від двох до чотирьох) порівняно з семипольовим протоколом ETDRS мають чутливість 80-98% і специфічність 86-100%. Таке саме зіставлення з дослідженням одного центрального поля продемонструвало нижчі чутливість (54-78%) і специфічність (88-89%) (Vujosevic S. et al., 2009; Aptel F. et al., 2008). Найбільша клінічна цінність скринінгу ДР полягає в тому, що він дає змогу своєчасно виявляти хворих, які потребують повного офтальмологічного дослідження й лікування, здатних запобігти постійній втраті зору. З огляду на це ефективний скринінг потребує високої чутливості (>80%). Саме тому фотографування під кутом у 45 градусів на недилатованих зірцях одного центрального поля не є підхожим для суспільної програми скринінгу (Solomon S. et al., 2017). Візуалізаційні системи надширокого поля, котрі покривають 200 градусів дна, також використовували для скринінгу ДР. Ці системи, якщо їх застосовують для оцінки поодинокого ушкодження сітківки, потребують фармакологічного мідріазу, котрий зменшує з 4,5 до 0% частку зображень, які не дають змоги визначити стадію процесу (Silva D. et al., 2013).
Щоби скринінгова програма виявилася корисною, вона має передбачати доступ до адекватної та своєчасної консультації офтальмолога.
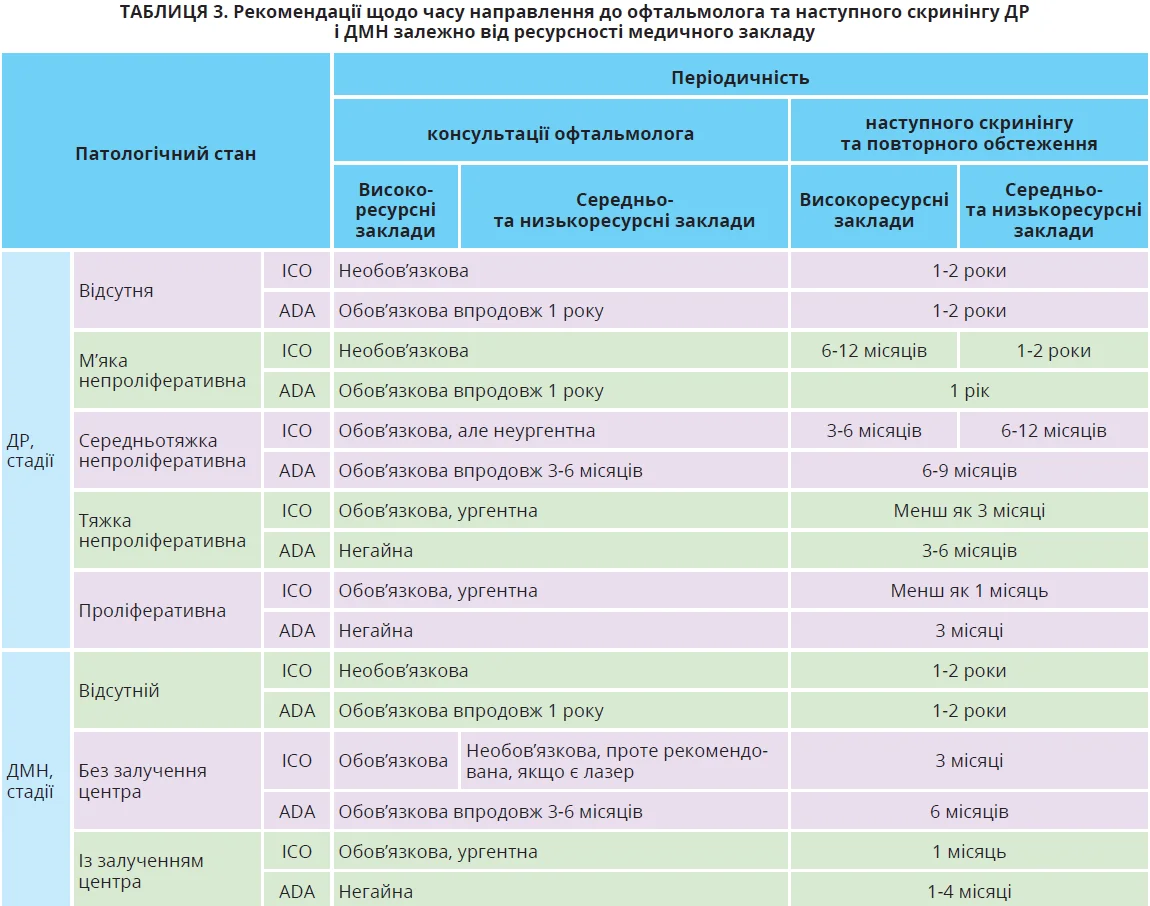
Час наступних візитів для скринінгу й офтальмологічної консультації залежно від ресурсності закладу наведено в таблиці 3.
Нові методи ретинальної візуалізації в офтальмологічних телемедичних програмах
Нещодавні технологічні розробки для скринінгу ДР можна поділити на три категорії: захоплення зображення, його аналіз та оцінка ризику. Новим методом захоплення зображення є використання сканувальних (лазерних) конфокальних камер, розташованих на офтальмоскопі та здатних відображати надшироке поле. Сканувальна конфокальна офтальмоскопія (з лазерами чи білим світлодіодним освітлювачем) потенційно може покращити якість зображення й огляд полів без потреби мідріазу (Silva P. et al., 2012). Також користуються конвенціональними камерами з деякими вдосконаленнями, наприклад портативними мобільними девайсами. Автоматичний аналіз зображень із застосуванням штучного інтелекту може зробити суттєвий внесок у телеофтальмологію. Це дасть змогу, по-перше, автоматично визначати ДР, а по-друге, ідентифікувати групи ризику серцево-судинних і нейродегенеративних уражень.
Скринінг ДР та інші ускладнення ЦД
Наявність у пацієнта ДР указує на розлад у нього мікроциркуляції з високим ризиком діабетичних мікроангіопатій, зокрема нефропатії та нейропатії (з можливим формуванням діабетичної стопи) (Pearce I. et al., 2019). За ДР також збільшується ризик розвитку макросудинних ускладнень (Rosenson R. et al., 2011).
Нині розробляється програмне забезпечення для автоматизованого аналізу зображень сітківки. При цьому користуються глибоким нейронним навчанням на основі штучного інтелекту. Ймовірно, аналіз структурно-функціональних змін мікроциркуляторного русла сітківки у хворих на ЦД дасть змогу краще визначати в них ризик серцево-судинних захворювань. Доведено, що моделі глибокого навчання на даних, що отримані із зображень очного дна, здатні передбачати кардіоваскулярні чинники ризику й основні серцеві події (Poplin R. et al., 2018).
Пацієнти з ЦД 2 типу мають значно вищий за середній ризик розвитку нейродегенеративних станів, зокрема хвороби Альцгеймера (Simo R. et al., 2017). У процесі ембріонального розвитку сітківка розвилася з тканин мозку. Саме тому око є своєрідним оглядовим вікном у мозок. Отже, існує можливість установлення нейродегенеративних змін мозку через нескладну, неінвазивну оцінку таких самих змін сітківки. Існують пацієнти з ЦД 2 типу з легкими когнітивними порушеннями, що є продромальною стадією хвороби Альцгеймера. Для ідентифікації таких хворих можна користуватися оптичною когерентною томографією в спектральному домені, котра дає змогу вимірювати товщину нейросітківки або шару її волокон (Cheung C. et al., 2017). Із цією метою також застосовують мікропериметрію, що оцінює чутливість сітківки (Ciudin A. et al., 2017) та фіксацію погляду (Simo-Servat O. et al., 2019). Наведені методи відкривають нові перспективи в підходах до скринінгу ДР в осіб віком понад 60 років. Тепер скринінг ДР можна використовувати не лише для запобігання станам, які загрожують розвитком сліпоти, але й для ідентифікації осіб із групи ризику тяжкої когнітивної дисфункції. Треба наголосити, що когнітивні порушення зменшують прихильність до лікування, зумовлюючи поганий контроль глікемії, збільшуючи кількість епізодів тяжкої гіпоглікемії та підвищуючи частоту госпіталізацій (Simo R. et al., 2017).
Література
Vujosevic S., Aldington S.J., Silva P., et al. Screening for diabetic retinopathy: new perspectives and challenges. Lancet Diabetes Endocrinol. 2020 Apr; 8 (4): 337-347.
