Рідкісна маніфестація тяжкого первинного гіпотиреозу: мікседема та масивний перикардіальний випіт
Переклала й адаптувала канд. мед. наук Ольга Федик
Первинний гіпотиреоз – це синдром недостатності тиреоїдних гормонів, зумовлений ураженням щитоподібної залози, найчастіше при хронічному автоімунному тиреоїдиті (тиреоїдиті Хашимото) або після радіойодтерапії / оперативного втручання. Діагноз зазвичай установлюють біохімічно: підвищений тиреотропний гормон (ТТГ) у поєднанні зі зниженим вільним тироксином (вТ4) вказують на маніфестний первинний гіпотиреоз [1, 2].
Клінічні прояви варіюються від мінімальних і неспецифічних скарг до багатосистемного ураження. У сучасній літературі підкреслюють типові симптоми (втома, сонливість, непереносимість холоду, збільшення маси тіла, сухість шкіри, закрепи), але вони не є специфічними, тому лабораторне підтвердження є вирішальним [1, 2]. Для первинного гіпотиреозу також характерні дисліпідемія, брадикардія, набряковий синдром, нейрокогнітивні порушення й анемія, а для частини пацієнтів – ураження серцево‑судинної системи (погіршення перебігу серцевої недостатності, підвищення серцево‑судинного ризику) [1, 2].
Етіологічно, крім автоімунного тиреоїдиту, важливими є медикаментозні причини (аміодарон, літій, інгібітори імунних контрольних точок), а також йодний дефіцит, який залишається значущим фактором у цілому світі [1, 2]. Додатковою проблемою є інтерпретація тиреоїдних тестів: зростає розуміння необхідності індивідуалізованих референтних інтервалів (вік, стать, особливі стани), щоб уникнути хибної діагностики та надмірного/недостатнього лікування [1, 3].
Лікуванням вибору при маніфестному первинному гіпотиреозі є левотироксин (L‑T4) у монотерапії з підбором дози за рівнем ТТГ і клінічною відповіддю. Контроль ТТГ рекомендують через 6-8 тижнів після старту або зміни дози, а після досягнення мети – періодично (часто раз на рік), щоб уникати як недостатньої замісної терапії, так і ятрогенного тиреотоксикозу [2]. Європейська тиреоїдна асоціація (ETA) в настанові 2025 р. акцентує на важливості врахування віку, супутньої патології та факторів, що впливають на абсорбцію L‑T4; у літніх пацієнтів лікування зазвичай рекомендують за стійкого ТТГ >10 мОд/л, а при ТТГ 7-10 мОд/л рішення має бути персоналізованим [3].
Субклінічний гіпотиреоз (підвищений ТТГ за нормального вТ4) є частою знахідкою, особливо в літніх людей, але ефективність лікування залежить від ступеня підвищення ТТГ, симптомів і коморбідності. За даними сучасних наукових досліджень, скринінг безсимптомних осіб загалом не рекомендується, натомість доцільним є цільове обстеження груп ризику (автоімунні хвороби, цукровий діабет 1-го типу, приймання аміодарону/літію, перенесені втручання на щитоподібній залозі) [2]. Європейські рекомендації також підкреслюють важливість визначення вікових референтних інтервалів для ТТГ, щоб не «переліковувати» фізіологічні вікові зсуви як патологію [3].
Підбір і ефективність замісної терапії L‑T4 значною мірою залежать від відповіді на лікування й умов приймання. У настанові ETA 2025 р. описується важливість чинників, які знижують біодоступність L‑T4: одночасне приймання з їжею, кальцієм/залізом, деякими сорбентами, а також гастроінтестинальні стани, що порушують абсорбцію [3].
Залишкові симптоми в частини пацієнтів на тлі нормалізованого ТТГ залишаються ще однією актуальною проблемою. За даними сучасних наукових досліджень, приблизно в 10% пацієнтів можуть зберігатися суб’єктивні скарги попри біохімічну компенсацію, що стимулює інтерес до альтернативних підходів до лікування (ліотиронін, висушений екстракт щитоподібної залози) [1]. Водночас ведуться дослідження більш фізіологічних форм трийодтироніну – T3 (зокрема повільного вивільнення) й інших перспективних підходів для підгруп пацієнтів з персистивними симптомами [7].
Отже, первинний гіпотиреоз слід розглядати як континуум: від «стертих» форм до тривалого дефіциту гормонів, який за наявності тригера може завершитися незворотною й загрозливою для життя декомпенсацією [4, 5].
Попри відносну рутинність діагностики та лікування, тривалий нелікований або недостатньо компенсований гіпотиреоз може призвести до тяжких ускладнень. Особливо небезпечним є декомпенсований гіпотиреоз (мікседематозна криза/кома) – рідкісний, але критичний стан з багатокомпонентною органною дисфункцією, що потребує інтенсивної терапії. За даними літератури, у 2012-2024 рр. смертність у разі мікседематозної кризи становила близько 38,8%, а причинами летальних наслідків часто були шок і мультиорганна недостатність [4]. Дані StatPearls підкреслюють: широкий діапазон летальності (приблизно 20-60%) вказує на те, що стан часто запускається стресорами (інфекція, холод, медикаменти), які зривають компенсаторні механізми при гіпотиреозі [5].
У контексті тяжкого гіпотиреозу на окрему увагу заслуговують серозити, зокрема перикардіальний випіт. Огляд перикардіальних уражень за гіпотиреозу показує, що перикардіальний випіт трапляється із частотою орієнтовно 3-37% і може призводити до тампонади в тяжких випадках; механізм пов’язують зі збільшенням проникності судин епікарда та зниженням лімфатичного дренажу альбуміну, через що рідина накопичується повільно й часто безсимптомно; це створює ризик недооцінювання тяжкості стану [6].
Тяжкий декомпенсований гіпотиреоз залишається клінічно недооціненим станом, особливо в осіб похилого віку, в яких його прояви можуть маскуватися під кардіологічну, неврологічну або геріатричну патологію. Мікседема, як крайній прояв тиреоїдної недостатності, характеризується багатосистемним ураженням і потенційно загрозливими для життя ускладненнями, серед яких перикардіальний випіт посідає особливе місце. Представлений клінічний випадок демонструє типову, проте водночас рідкісну сучасну маніфестацію нелікованого автоімунного гіпотиреозу.
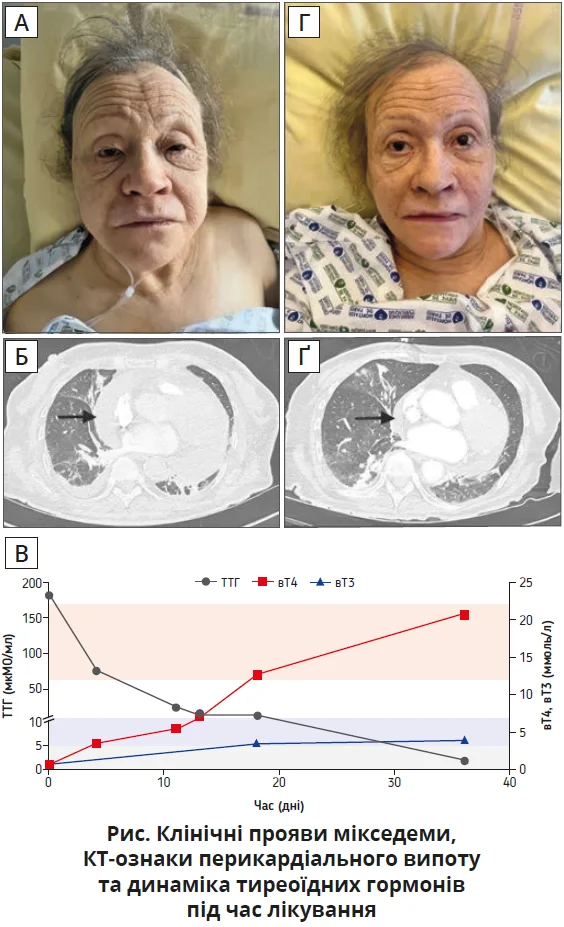
75-річна пацієнтка без відомої раніше ендокринної патології була госпіталізована до відділення невідкладної допомоги зі скаргами на прогресивну задишку. За словами родичів, протягом кількох місяців відзначалися поступова апатія, загальмованість, зниження когнітивної активності й уповільнення мовлення. Під час первинного огляду пацієнтка справляла враження виражено загальмованої, з брадипсихією та зниженою спонтанною мовленнєвою активністю (рис.).
При об’єктивному обстеженні: артеріальний тиск – 120/64 мм рт. ст., частота серцевих скорочень – 61 уд./хв, сатурація кисню – 80%, температура тіла – 37 °C.
При фізичному обстеженні виявлено характерні ознаки мікседеми: щільний набряк обличчя, пастозність повік, грубуватість рис обличчя (панель А). Шкіра була сухою, блідою та холодною на дотик, що відповідає типовим дерматологічним проявам вираженого гіпотиреозу.
Комп’ютерна томографія (КТ) органів грудної клітки з ангіографією виявила масивний циркулярний перикардіальний випіт товщиною близько 3 см (панель Б). Трансторакальна ехокардіографія підтвердила наявність значного випоту без гемодинамічних ознак тампонади.
Гормональний профіль демонстрував тяжкий первинний гіпотиреоз: ТТГ – 182,1 мМО/л (норма – 0,4-4,2 мМО/л), вТ4 – 0,04 пг/мл (критично знижений; норма – 0,96-1,76 пг/мл), вТ3 – 0,39 пг/мл (значно знижений; норма – 2,02-4,43 пг/мл) (рис.). Такий рівень ТТГ свідчить про тривалу декомпенсацію та повну втрату негативного зворотного зв’язку. Високий титр антитіл до тиреоглобуліну (4500 МО/мл, норма <33 МО/мл) у поєднанні з атрофією щитоподібної залози за даними ультразвукового дослідження підтверджував автоімунну природу хвороби, ймовірно, атрофічний варіант хронічного автоімунного тиреоїдиту.
З огляду на відсутність ознак тампонади було прийнято рішення про консервативну тактику. Пацієнтці призначено пероральний L‑T4 у стартовій дозі 75 мкг/добу з подальшим моніторингом.
Додатково пацієнтці проводили кисневу підтримку, а також внутрішньовенну діуретичну терапію, спрямовану на стабілізацію респіраторного стану та зменшення перевантаження рідиною.
Через місяць лікування, після досягнення біохімічної компенсації тиреоїдної функції (панель В), спостерігалися втрата маси тіла на 15 кг, істотний регрес мікседематозного набряку та перикардіального випоту (панелі Г, Ґ), а також стабілізація вітальних показників [1, 2].
У процесі лікування клінічний стан пацієнтки істотно покращився: поступово відновилися когнітивні функції, підвищилися фізична активність і загальна фізична витривалість.
Цей випадок демонструє, що навіть у сучасній клінічній практиці можливе пізнє виявлення тяжкого гіпотиреозу. Особливої уваги потребують пацієнти похилого віку, в яких симптоматика часто інтерпретується як вікові зміни. Перикардіальний випіт у разі гіпотиреозу має сприятливий прогноз за умови адекватної замісної терапії.
Тяжкий гіпотиреоз може тривалий час залишатися недіагностованим, оскільки його клінічні прояви часто є неспецифічними та можуть помилково трактуватися як прояви інших хронічних станів або вікових змін. Мікседема є мультисистемним станом з потенційно загрозливими ускладненнями. Перикардіальний випіт у більшості випадків регресує на тлі адекватної замісної терапії. Своєчасне призначення L‑T4 забезпечує повну клінічну компенсацію.
Представлений клінічний випадок добре ілюструє типову для ендокринних невідкладних станів проблему: тривале накопичення клінічних і лабораторних змін може маскуватися під кардіореспіраторну або інфекційну патологію, а декомпенсація настає після впливу тригера (переохолодження, інфекція, седативні препарати, декомпенсація супутніх хвороб). Саме тому в сучасних оглядах підкреслюють необхідність своєчасної діагностики та раннього переведення таких пацієнтів до відділення інтенсивної терапії [4, 5].
З позиції доказової бази важливо, що тяжкість мікседематозної кризи не завжди прямо корелює з абсолютними значеннями гормонів щитоподібної залози. Сучасні наукові дослідження зазначають: клінічна картина й ускладнення (шок, дихальна недостатність, кардіальні ускладнення) визначають прогноз більше, ніж цифри ТТГ/вТ4 самі по собі [4]. Це пояснює, чому рішення щодо інтенсивності лікування та моніторингу ґрунтується на сукупності показників гемодинаміки, температури тіла, свідомості, газообміну, натрію, глікемії, інфекційних маркерів.
Перикардіальний випіт у разі гіпотиреозу в цьому контексті слід розглядати як ускладнення повільного хронічного процесу. Через поступове накопичення рідини клінічні ознаки тампонади можуть бути «стерті», тому вирішальними є ехокардіографічні ознаки гемодинамічної компресії та динаміка стану під час замісної терапії [6]. У багатьох випадках корекція тиреоїдної недостатності сприяє регресу випоту, але при ознаках тампонади потрібна інвазивна тактика згідно з кардіологічними принципами [6].
Отже, розширений огляд первинного гіпотиреозу логічно підводить до розуміння того, як «звичайне» ендокринне захворювання може завершуватися життєзагрозливою декомпенсацією та чому клінічні випадки з поєднанням тяжкого гіпотиреозу й серозиту залишаються актуальними для практичної медицини.
Із клінічного погляду цей випадок підкреслює необхідність збереження високої настороженості щодо ендокринних причин неспецифічної симптоматики в пацієнтів похилого віку.
Поєднання поступового когнітивного зниження, брадикардії, набрякового синдрому та серозних випотів має спонукати лікаря до оцінювання тиреоїдної функції навіть за відсутності очевидного ендокринного анамнезу.
Своєчасна лабораторна діагностика та раннє призначення замісної терапії L‑T4 дають змогу не лише стабілізувати стан пацієнта, а й запобігти розвитку тяжких ускладнень, як-от мікседематозна криза, мультиорганна недостатність або кардіальні ураження.
Література
- Taylor P.N., Medici M.M., Hubalewska-Dydeychyk A., Boelart K. Hypothyroidism. The Lancet. 2024; 404 (10460): 1347-1364. doi: 10.1016/S0140-6736(24)01614-3. PMID: 39368843.
- Cheker L., Papaleontiou M. Hypothyroidism: a review. JAMA. 2025 Sep 3. Online ahead of print. doi: 10.1001/jama.2025.13559. PMID: 40900603.
- Chentanni M., Duntas L., Feldt-Rasmussen U., Kørle J., Peters R.P., et al. European Thyroid Association guideline on the use of levothyroxine sodium monotherapy to optimize the treatment of hypothyroidism. European Thyroid Journal. 2025; 14 (4): e250123. doi: 10.1530/ETJ-25-0123. PMID: 40622204.
- Zhang Y., Chu L., Han H. Myxedema crisis: challenges and future directions (systematic review). Thyroid Research. 2025. doi: 10.1186/s13044-025-00268-1.
- Elshimy G., Chippa V., Anastasopoulou C., Correa R. Myxedematous coma. StatPearls / NCBI Bookshelf. Update: 2023 (with summary of review data 2004-2024).
- Chahine J., Ala C.K., Gentry J.L., Pantalone K.M., Klein A.L. Pericardial diseases in patients with hypothyroidism (review). Heart (BMJ). 2019. doi: 10.1136/heartjnl-2018-314528. PMID: 30948517.
- Bianko A.K. New (emergent) approaches in the treatment of hypothyroidism. Annual Review of Medicine. 2024. doi: 10.1146/annurev-med-060622-101007. PMID: 37738506.