Рекомендації Міжнародної робочої групи з діабетичної стопи й Американського товариства інфекційних хвороб щодо лікування асоційованих із діабетом інфекцій стопи (IWGDF/IDSA, 2023)
Переклала й адаптувала д-р мед. наук Лариса Стрільчук
Поширеність цукрового діабету (ЦД) у всьому світі зростає. За даними Міжнародної федерації діабету, станом на 2021 р. у світі налічувалося 537 млн дорослих із цією хворобою. Паралельно з наростанням поширеності ЦД збільшується й кількість ускладнень із боку стопи. Асоційовані з діабетом інфекції стопи (АДІС) пов’язані зі значною захворюваністю, оскільки потребують частих відвідувань лікаря, щоденного догляду за раною, протимікробної терапії, хірургічних процедур і високих витрат на медичну допомогу. АДІС залишаються найпоширенішим ускладненням ЦД, яке призводить до госпіталізації, та провідною причиною ампутації нижніх кінцівок.
Систематичний доказовий підхід до ведення пацієнтів з АДІС покращує результати лікування та допомагає уникнути ускладнень. Медичну допомогу в таких випадках повинна надавати міждисциплінарна команда, яка має включати спеціаліста з інфекційних захворювань або фахівця з клінічної мікробіології. Лікування АДІС передбачає оптимальний місцевий догляд за раною (очищення, усунення детриту), зниження тиску на стопу, оцінку стану периферичних судин і метаболічний (зокрема глікемічний) контроль.
Інфекції шкіри та м’яких тканин у осіб із ЦД найчастіше виникають на тлі периферичної нейропатії та часто – на тлі хвороби периферичних артерій (ХПА). Дефект епідермісу, а іноді й дерми колонізує складний комплекс бактерій, які надалі розмножуються й індукують запальну відповідь. Оскільки всі рани заселяють мікроби, часто потенційно патогенні, ранову інфекцію не можна діагностувати на під-ставі результатів дослідження мікробної культури. Натомість АДІС діагностують клінічно, з огляду на ознаки запального процесу з утворенням рани на стопі (нижче кісточки). Варто пам’ятати, що в осіб із ЦД ознаки запалення можуть бути замасковані периферичною нейропатією, ХПА чи імунною дисфункцією.
Наявність ХПА збільшує ризик незадовільного загоєння й ампутації, тому слід оцінювати перфузію рани та за потреби проводити реваскуляризацію.
Хоча більшість АДІС є відносно поверхневими, мікроорганізми можуть поширюватися в підшкірні тканини, в тому числі фасції, сухожилки, м’язи, суглоби та кістки. Анатомія стопи, яка передбачає наявність кількох окремих, але сполучених компартментів, зумовлює проксимальне поширення інфекції та розвиток ішемічного некрозу тканин в ураженому компартменті. За відсутності швидкої діагностики та належного лікування АДІС прогресують, іноді швидко, тому в разі тяжкої АДІС спеціаліст із досвідом лікування інфекційних хвороб повинен оцінити стан пацієнта впродовж 24 годин після розвитку інфекції. Накопичення гнійних виділень, особливо за високого локального тиску або наявності некрозу, потребують швидкої (зазвичай протягом 24 годин) хірургічної декомпресії та дренування.
Примітка: проведіть неінвазивну діагностику ХПА біля ліжка хворого.
Діагностика
Рекомендація 1
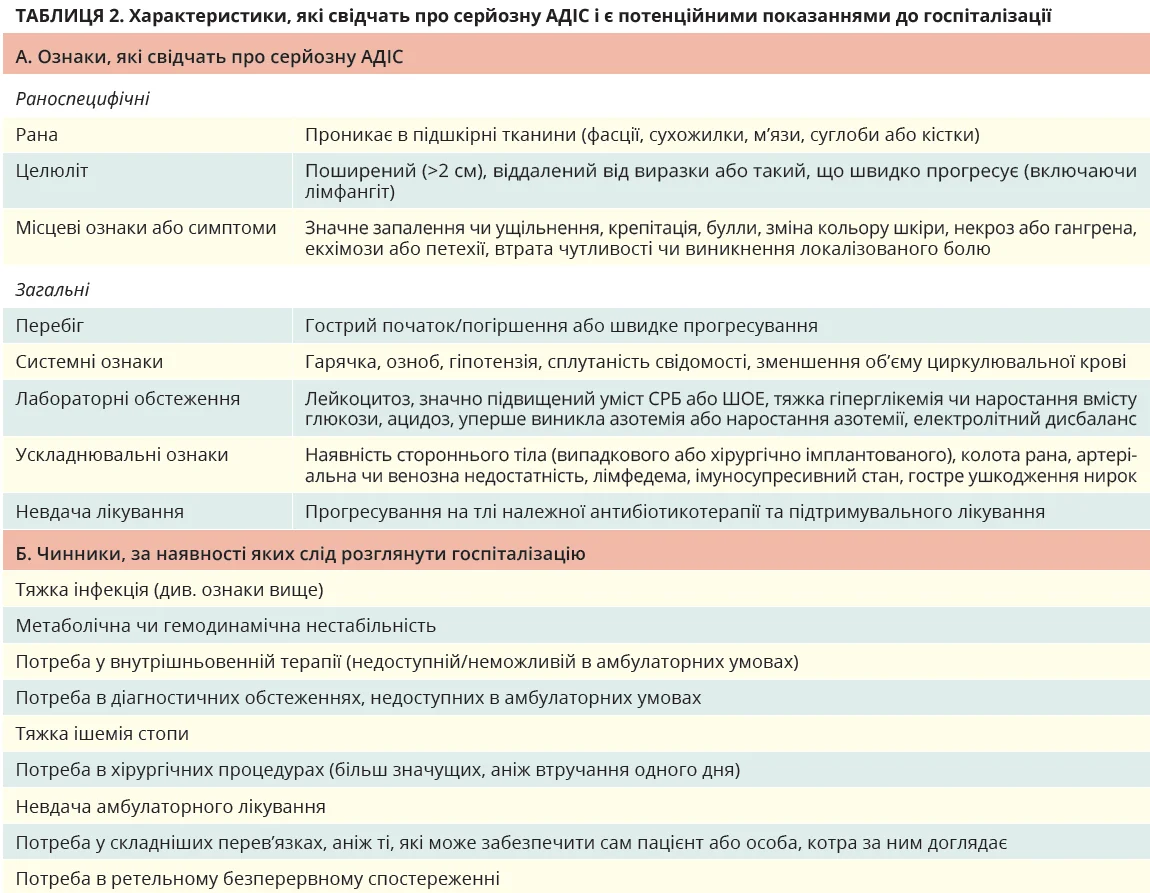
Діагностуйте асоційовані з ЦД інфекції м’яких тканин клінічно, з огляду на місцеві або системні ознаки та симптоми запалення. Оцінюйте тяжкість АДІС за допомогою класифікації Міжнародної робочої групи з діабетичної стопи й Американського товариства інфекційних хвороб (табл. 1).
Рекомендація 2
Розгляньте госпіталізацію для всіх осіб із ЦД й інфекцією стопи, в яких спостерігається тяжка інфекція стопи за класифікацією IWGDF/IDSA чи помірно тяжка інфекція, поєднана з ключовими коморбідностями.
У цих рекомендаціях діагностика АДІС ґрунтується на доказах наявності запалення та синдрому системної запальної відповіді. У зв’язку з вагомим впливом остеомієліту на перебіг процесу пропонується позначати наявність цього ускладнення літерою «О», яку додають до ступеня тяжкості.
Госпіталізація є дороговартісним ресурсом і для пацієнта асоціюється зі значними незручностями та ризиком нозокоміальних інфекцій. Утім, деякі пацієнти з АДІС однозначно потребують госпіталізації, наприклад особи з тяжкою інфекцією або значущими коморбідностями, як-от ХПА (табл. 2). Слід зауважити, що наявність остеомієліту не завжди потребує госпіталізації, оскільки значна кількість цих хворих є клінічно стабільними та можуть лікуватися пероральними антибіотиками.
Рекомендація 3
В осіб із ЦД та, ймовірно, інфікованою виразкою стопи, в яких результати клінічного огляду є неоднозначними або не підлягають інтерпретації, визначайте вміст запальних біомаркерів сироватки, зокрема С-реактивного білка (СРБ), швидкості осідання еритроцитів (ШОЕ) та прокальцитоніну.
Сироваткові тести на визначення маркерів запалення є широко доступними, легкими у виконанні й, окрім визначення прокальцитоніну, недорогими. Особливу увагу варто звернути на рівень лейкоцитів, який є одним із критеріїв тяжкості АДІС, хоча приблизно в половини пацієнтів із такими інфекціями вміст лейкоцитів є нормальним. ШОЕ є вищою в осіб з інфікованими виразками стопи порівняно з неінфікованими, але на рівень цього показника можуть впливати численні коморбідні стани, наприклад анемія й азотемія. Аналогічна тенденція спостерігається для СРБ і прокальцитоніну.
Запальні біомаркери застосовуються тоді, коли клінічна оцінка не дає можливості однозначно встановити діагноз.
Рекомендація 4
Для діагностики асоційованих із ЦД інфекцій м’яких тканин не рекомендується застосовувати оцінку температури стопи та кількісний мікробний аналіз.
Дані щодо цінності візуалізаційних досліджень при інфекціях м’яких тканин є суперечливими.
Інфрачервона чи цифрова термографія не покращує діагностику АДІС і не дає змоги прогнозувати клінічні наслідки.
Деякі автори пропонують застосовувати для диференційної діагностики інфікованих і неінфікованих виразок стопи велику кількість бактерій (≥105 колонієутворювальних одиниць) у культурі, але переконливі підтвердження такого методу відсутні. Загалом визначення так званого біотягаря рани є часозатратним і відносно дорогим.
Рекомендація 5
У людини з підозрою на АДІС розгляньте забір зразка м’яких тканин для вирощування культури причинних мікроорганізмів, бажано асептичний забір тканин із рани за допомогою кюретажу або біопсії.
У більшості випадків аналіз такого зразка надає цінну інформацію стосовно причинного патогена та його антибіотикочутливості, але в разі гострої нетяжкої АДІС у пацієнта, який нещодавно не отримував антибіотиків і не має чинників ризику наявності нетипової або антибіотикорезистентної флори, доцільним є емпіричний підбір лікування.
Рекомендація 6
Використовуйте звичайні, а не молекулярні, мікробіологічні методи для початкової ідентифікації патогенів зі зразків м’яких тканин або кісток пацієнтів з АДІС.
Для молекулярних і традиційних мікробіологічних методів дослідження продемонстровано високий відсоток збігів. Окрім того, молекулярні методи, як-от метагеномне секвенування нового покоління, не прискорюють ідентифікацію патогена та не дають можливості відрізнити мертві бактерійні клітини від живих, що може спричинити необґрунтоване застосування антибіотиків широкого спектра. Імовірно, молекулярні методи активно застосовуватимуться в майбутньому, але станом на сьогодні застосування їх у рутинній практиці не рекомендовано.
Рекомендація 7
Для діагностики остеомієліту стопи в осіб із діабетом розгляньте зондову пробу кістки в рані, рентгенографію та визначення ШОЕ, СРБ або прокальцитоніну.
Наявність інфекційного процесу в кістці значно підвищує ризик ампутацій. Велике значення в діагностиці остеомієліту має зондова проба, але на достовірність результату впливають досвід лікаря, локалізація й етіологія виразки. Кожному пацієнту з підозрою на інфекцію кістки слід виконувати рентгенографію стопи, оскільки цей метод є недорогим, широко доступним і безпечним. Доцільно повторювати обстеження раз на 2-3 тижні, оскільки гострий остеомієліт не завжди помітний на звичайній рентгенограмі.
Що стосується ШОЕ, СРБ і прокальцитоніну, то доцільно застосовувати ці методи в поєднанні з іншими діагностичними обстеженнями.
Рекомендація 8
Якщо діагноз асоційованого з ЦД остеомієліту стопи залишається сумнівним, незважаючи на результати клінічного обстеження, рентгенографії та лабораторних обстежень, виконайте магнітно-резонансну томографію (МРТ).
Рекомендація 9
Як альтернативу МРТ розгляньте позитронно-емісійну томографію, лейкоцитарну сцинтиграфію або однофотонну емісійну комп’ютерну томографію.
У багатьох пацієнтів для діагностики остеомієліту складні візуалізаційні методи не потрібні; найпоширенішим і найкраще вивченим із таких методів є МРТ. Збільшити точність методу можна за допомогою розгляду отриманих зображень іще одним спеціалістом.
Рекомендація 10
У разі підозри на остеомієліт стопи (до чи після лікування) розгляньте інтраопераційний або перкутанний забір зразка кістки (а не м’яких тканин) для дослідження культури бактерій.
Дослідження зразка кістки є золотим стандартом діагнозу остеомієліту та єдиним точним способом установлення причинного патогена. Для максимально точного результату слід уникати контамінації зразка кістки флорою шкіри, тобто забір має здійснюватися перкутанно через інтактну неінфіковану шкіру або інтраопераційно.
Лікування
Рекомендація 11
Не лікуйте клінічно неінфіковані виразки стопи системними чи місцевими антибіотиками з метою зниження ризику нових інфекцій або сприяння загоєнню виразок.
Рекомендація 12
Застосовуйте будь-які схеми системної антибіотикотерапії, котрі, за даними опублікованих рандомізованих клінічних досліджень, продемонстрували ефективність у стандартних дозах у лікуванні осіб із ЦД й інфекціями м’яких тканин стопи. Пацієнтам із діабетичною інфекцією шкіри або м’яких тканин стопи призначайте антибіотикотерапію на 1-2 тижні. Розгляньте продовження лікування (наприклад, до 3-4 тижнів), якщо вираженість інфекції знижується, але вона залишається широкою та зменшується повільніше, ніж очікувано, або якщо пацієнт має тяжку ХПА. Якщо докази наявності інфекції не зникли через 4 тижні адекватного лікування, повторно оцініть стан пацієнта та розгляньте потребу в подальших діагностичних дослідженнях чи альтернативному лікуванні.
Рекомендація 13
Обирайте антибіотик для лікування АДІС залежно від імовірного або доведеного причинного патогена та його антибіотикочутливості, клінічної тяжкості інфекції, опублікованих доказів ефективності цього засобу при інфікованій діабетичній стопі, ризику побічних ефектів, включаючи колатеральне знищення коменсальної флори, імовірності міжлікарських взаємодій, доступності та вартості засобу.
Рекомендація 14
В осіб з АДІС незначної тяжкості, які нещодавно не отримували антибіотикотерапії та проживають у Північній Америці або Західній Європі, обирайте препарати, що діють лише на аеробні грампозитивні патогени (β-гемолітичні стрептококи та золотисті стафілококи, включаючи метицилінорезистентні штами, якщо це показано).
Рекомендація 15
В умовах помірного клімату не призначайте емпірично антибіотикотерапію АДІС, спрямовану на Pseudomonas aeruginosa. В осіб із помірно тяжкою або тяжкою інфекцією, які проживають у Азії або Північні Африці, призначайте емпіричну антибіотикотерапію P. aeruginosa, якщо цю бактерію було ізольовано з культури, отриманої з ураженої ділянки впродовж кількох попередніх тижнів.
Призначення антибіотикотерапії при клінічно неінфікованих виразках не прискорює загоєння та не зменшує ризику розвитку клінічно явної інфекції. Культури бактерій із відкритих ран зазвичай виявляють мікроорганізми, деякі з яких є патогенними, але це не означає, що рана інфікована. У разі клінічно неінфікованих ран потенційні небезпеки призначення антибіотиків переважають над теоретичними перевагами.
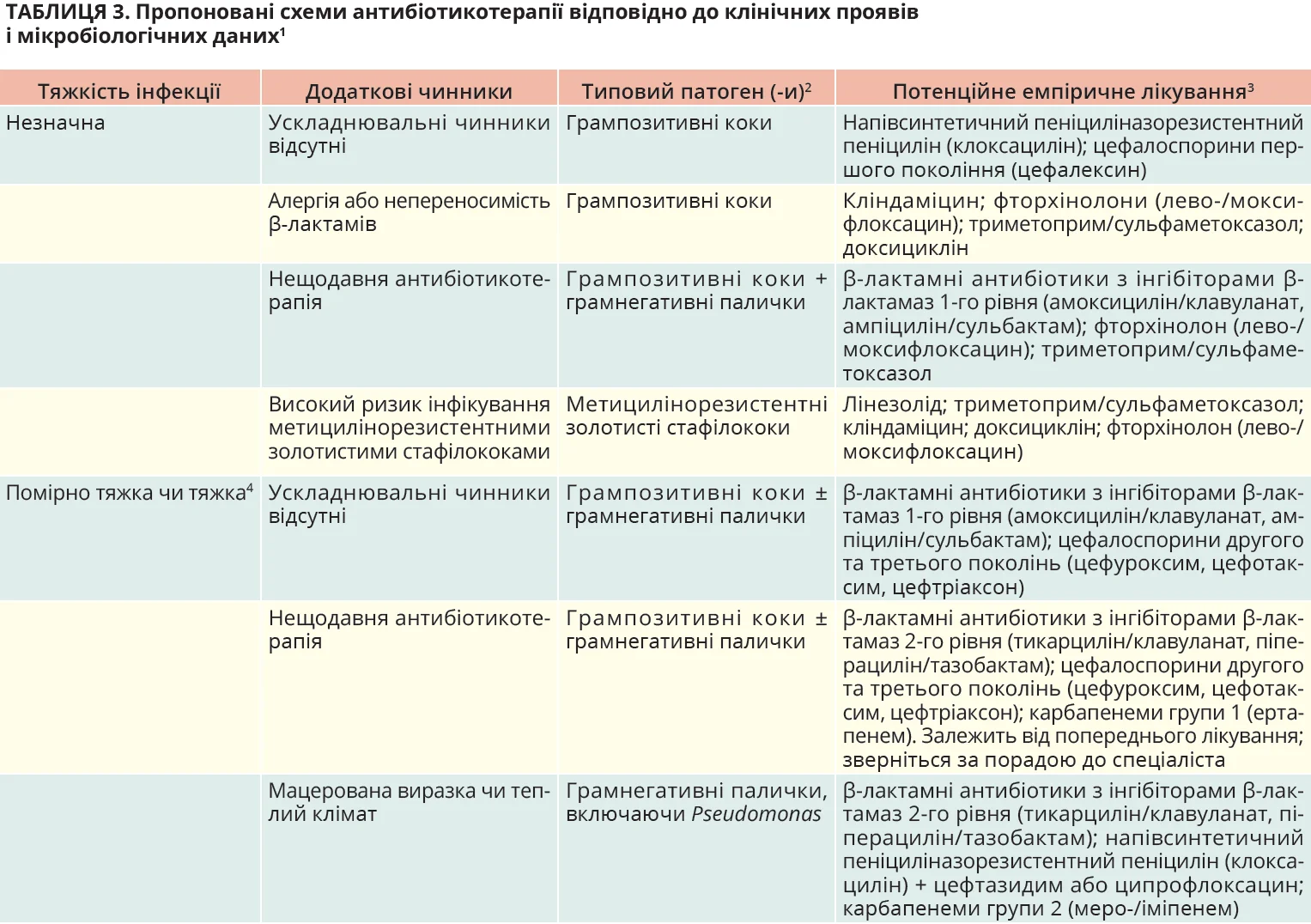
Дослідження показують, що лікування будь-яким адекватно підібраним пероральним або парентеральним препаратом із більшості класів антибіотиків здебільшого є ефективним. За нетяжких АДІС найімовірнішими причинними патогенами є грампозитивні бактерії. Якщо ж культура виявляє інші патогени, можна адаптувати антибіотикотерапію залежно від отриманих результатів. Пропоновані схеми антибіотикотерапії наведено в таблиці 3.
Бактерії роду Pseudomonas є рідкісними в Північній Америці та Європі й поширенішими в країнах із (суб-) тропічним кліматом.
Ураховуючи полімікробну природу АДІС, варто дотримуватися заходів профілактики антибіотикорезистентності: якщо змога, досягати контролю джерела інфекції за допомогою хірургічного втручання; розпочинати лікування з емпіричної антибіотикотерапії препаратом вузького спектра з найменшою кількістю побічних ефектів, найменшою тривалістю лікування, найбезпечнішим і найдешевшим способом уведення; переходити на прицільну (бажано пероральну) антибіотикотерапію препаратами, обраними на підставі дослідження культури бактерій.
Під час забору зразка слід максимально уникати звичайної колонізувальної флори, щоб обмежити ризик непотрібного призначення антибіотиків широкого спектра. У складних випадках, зумовлених нетиповими чи високорезистентними патогенами, клініцистам слід консультуватися з інфекціоністами або мікробіологами.
Переваг жодного з окремих препаратів або класів доведено не було, крім двох досліджень, в одному з яких було виявлено достовірну перевагу ертапенему над тайгецикліном, а в другому – невелику перевагу піперациліну/тазобактаму над ертапенемом. Зважаючи на недостатню кількість даних, рекомендовано застосовувати будь-яку схему системної антибіотикотерапії, що продемонструвала ефективність у лікуванні пацієнтів із ЦД й інфекцією м’яких тканин стопи. Дозування зазвичай є стандартним, хоча терапія остеомієліту може потребувати вищих доз.
Обираючи дозу, лікарю варто звернутися до національних рекомендацій. Ми радимо розглянути β-лактамні антибіотики (пеніциліни (з інгібіторами β-лактамази або без них), цефалоспорини, карбапенеми), метронідазол (у поєднанні з іншими антибіотиками), кліндаміцин, лінезолід, тетрацикліни, триметоприм/сульфаметоксазол, даптоміцин, фторхінолони або ванкоміцин, але не тайгециклін.
Після хірургічної обробки рани при помірно тяжких або тяжких АДІС рекомендується 10-денна антибіотикотерапія.
Рекомендація 16
Після невеликої ампутації з приводу асоційованого з діабетом остеомієліту стопи та позитивної культури з краю кістки розгляньте антибіотикотерапію тривалістю до 3 тижнів, а після асоційованого з діабетом остеомієліту стопи без резекції або ампутації кістки – до 6 тижнів.
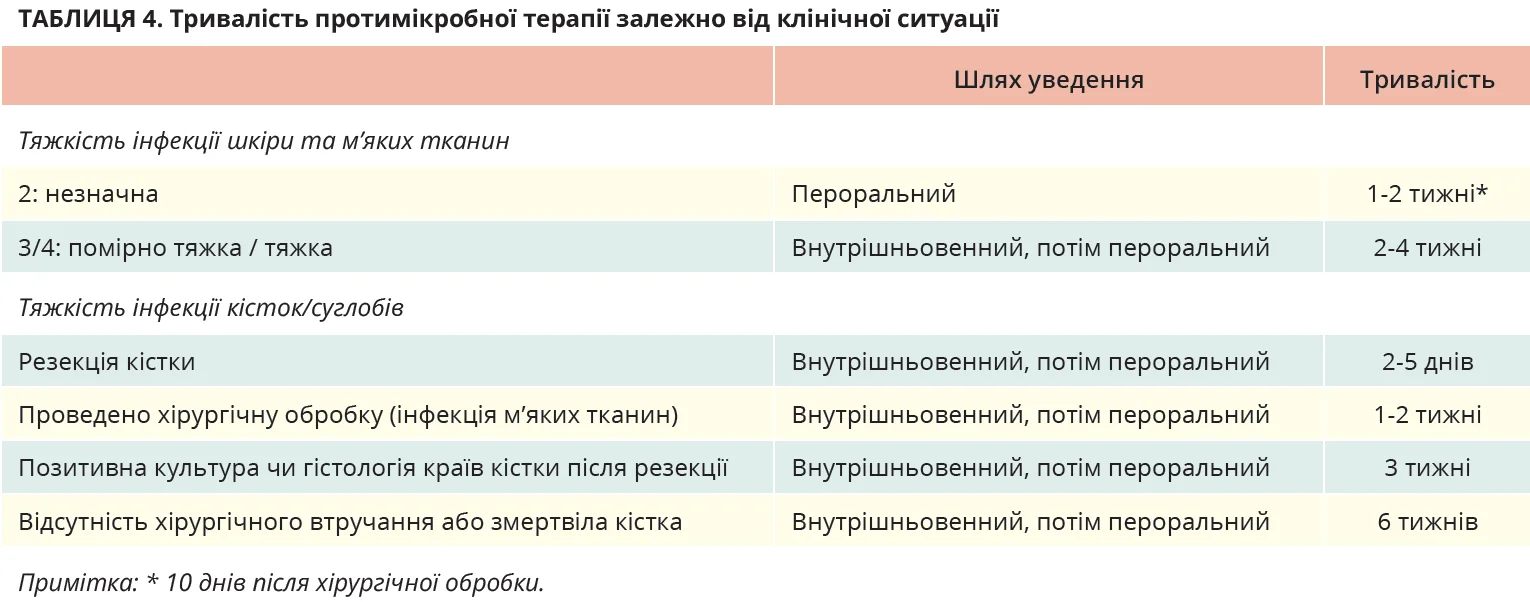
Призначаючи протимікробну терапію, слід забезпечити рівень препарату в сироватці, здатний гарантувати пенетрацію активної речовини в кістку. Зазвичай цього можна досягти при застосуванні антибіотиків у максимальних рекомендованих дозах і протягом тривалого часу (табл. 4).
За даними двох рандомізованих контрольованих досліджень, загальна тривалість антибіотикотерапії при діабетичному остеомієліті стопи, який не підлягає хірургічному лікуванню, не має перевищувати 6 тижнів, а при проведенні хірургічної обробки – ще менше. Для скорочення тривалості стаціонарного лікування застосовується перехід із внутрішньовенного на пероральне лікування.
Рекомендація 17
Для діагностики ремісії діабетичного остеомієліту стопи застосовуйте оцінку наслідків лікування щонайменше через 6 місяців після антибіотикотерапії.
У цій популяції пацієнтів необхідно проводити часті обстеження стоп протягом усього життя.
Рекомендація 18
У разі тяжкої інфекції або помірно тяжкої АДІС, ускладненої поширеною гангреною, некротизувальною інфекцією, ознаками глибокого (субфасціального) абсцесу, компартмент-синдрому чи тяжкої ішемії нижніх кінцівок варто провести невідкладну консультацію хірурга.
Рекомендація 19
У разі помірно тяжких і тяжких АДІС розгляньте раннє (протягом 24-48 годин) хірургічне втручання, покликане усунути інфіковані та некротизовані тканини, в поєднанні з антибіотиками.
Рекомендація 20
В осіб із ЦД, ХПА й виразкою стопи або гангрени з інфекцією, котра уражає будь-яку ділянку стопи, варто провести невідкладну консультацію хірурга й судинного хірурга, щоб визначити показання та тривалість дренування та/або потребу в реваскуляризації.
Ретроспективні дослідження свідчать, що ранні хірургічні втручання (зазвичай до 72 годин після виникнення симптомів) забезпечують меншу кількість великих ампутацій нижніх кінцівок порівняно з відтермінованими (протягом 3-6 днів після госпіталізації). У разі тяжких АДІС і станів, за яких нехірургічне лікування, ймовірно, не досягне результату, рекомендовано розглянути хірургічне втручання.
У разі інфекції потрібно також оцінити стан пацієнта щодо наявності й тяжкості ХПА. Оскільки результат клінічної оцінки часто є ненадійним, важливо провести неінвазивні дослідження, зокрема доплерографію та вимірювання артеріального тиску на гомілці.
Рекомендація 21
В осіб із діабетичним остеомієлітом стопи розгляньте проведення хірургічної резекції інфікованої кістки в поєднанні із системними антибіотиками.
Рекомендація 22
Розгляньте антибіотикотерапію без хірургічного втручання в разі остеомієліту передньої частини стопи без негайної потреби в розрізі та дренуванні для контролю інфекції; в осіб без ХПА та в осіб без ділянок відкритої кістки.
Хірургічна резекція інфікованої кістки протягом тривалого часу виступала стандартом лікування остеомієліту, але протягом останніх двох декад докази свідчать, що в певних категорій пацієнтів для ремісії діабетичного остеомієліту достатньо антибіотикотерапії. Слід зауважити, що з більшості досліджень виключали пацієнтів, які однозначно потребували хірургії (мали відкриту кістку, компартмент-синдром, недренований абсцес). Якщо перфузія стопи значно порушена, слід завжди проводити реваскуляризацію.
Рекомендація 23
При лікуванні АДІС не рекомендовано застосовувати додаткове лікування гранулоцитарно-макрофагальним стимулювальним фактором, топічними антисептиками, препаратами срібла, медом, бактеріофагами чи негативним тиском (з інстиляціями чи без них).
Рекомендація 24
Застосування топічних АБ (у формі просякнутих губок, цементу чи крему) в поєднанні із системними АБ для лікування інфекцій м’яких тканин або остеомієліту стопи в пацієнтів із ЦД не рекомендовано.
Топічна протимікробна терапія має низку теоретичних переваг, але в дослідженнях топічних антибіотиків як додатка до системної антибіотикотерапії було отримано суперечливі результати. Крім того, якість досліджень на цю тему була незадовільною, що не дафє змоги зробити чіткий висновок щодо клінічних переваг додавання топічної протимікробної терапії до системної.
Рекомендація 25
Не рекомендовано застосовувати гіпербаричну оксигенацію або топічну оксигенотерапію як додаткове лікування, якщо єдиним показанням є лікування діабетичної інфекції стопи.
Зважаючи на відсутність надійних даних на підтримку сприятливого впливу цих методів лікування, асоційовані з ними витрати та незручності переважають над теоретичними перевагами.
Література
Senneville É., Albalawi Z., van Asten S.A., Abbas Z.G., Allison G., Aragón-Sánchez J., Embil J.M., Lavery L.A., Alhasan M., Oz O., Uçkay I., Urbančič-Rovan V., Xu Z.-R., Peters E.J.G. IWGDF/IDSA guidelines on the diagnosis and treatment of diabetes-related foot infections (2023). Clinical Infectious Diseases. 2023; ciad527. doi: 10.1093/cid/ciad527.