Подагра у практиці ендокринолога
Підготувала канд. мед. наук Ольга Королюк
Подагра – найпоширеніша форма запального артриту у світі. За останні 20 років захворюваність на подагру зросла більш ніж удвічі [1]. Ризик захворюваності збільшується з віком. Хвороба виникає внаслідок стійкого підвищення рівня сечової кислоти (СК) у сироватці крові. Період безсимптомної гіперурикемії може тривати багато років. Важливість гіперурикемії як чинника ризику виникнення подагри підтверджена багатьма дослідженнями. Зокрема, метааналіз результатів 4 когортних досліджень за участю 18 889 осіб, які на початковому етапі не хворіли на подагру, виявив, що 15-річна кумулятивна захворюваність на подагру становить 1,1% (95% довірчий інтервал, ДІ 0,9-1,4%) в осіб із рівнем СК <6 мг/дл порівняно із 49% (95% ДІ 31-67%) в осіб із рівнями ≥10 мг/дл [2]. Однак у певної частки осіб із гіперурикемією навіть протягом тривалого періоду спостереження не виникає подагри. За відсутності типових клінічних проявів або наявності кристалів під час мікроскопії аспірованої із суглоба рідини гіперурикемія не дає змоги встановити діагноз подагри.
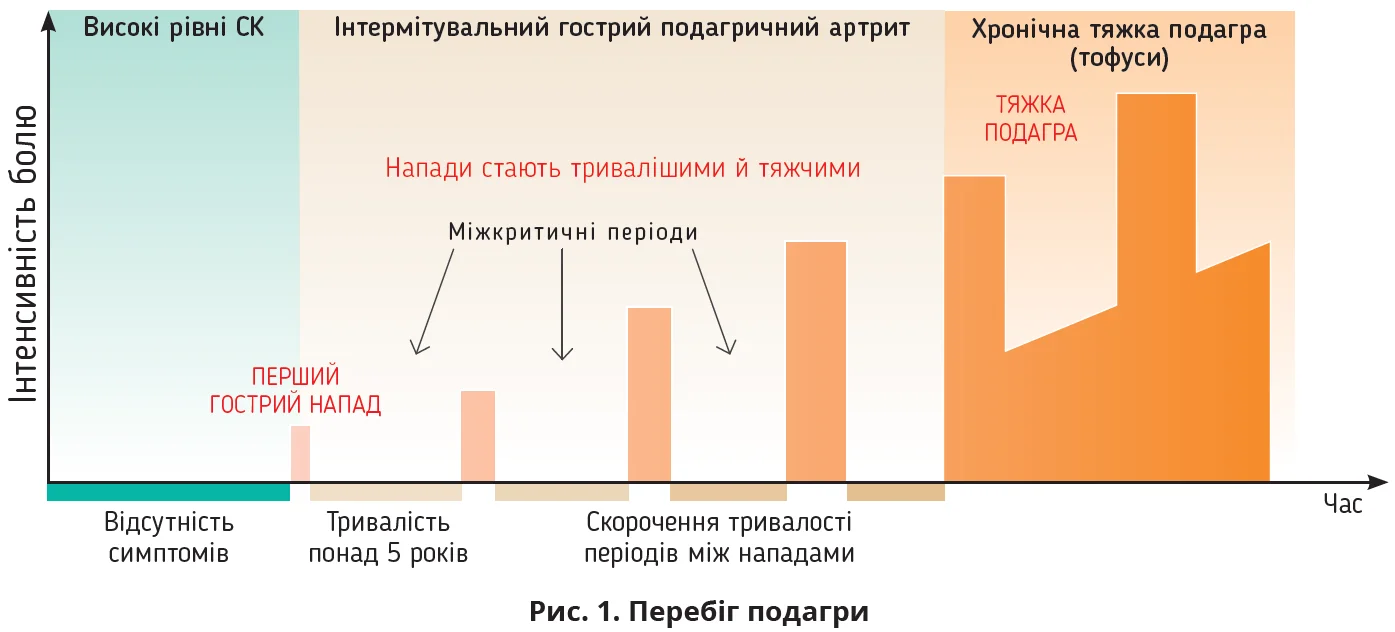
Із часом кристали моноурату натрію відкладаються в суглобах, сухожиллях та інших тканинах, що спричиняє повторювані епізоди вираженого гострого запалення, відомі як напади подагри (рис. 1). Підозрювати хворобу варто в пацієнтів із раптовим сильним болем в одному або обох перших метатарсофалангових суглобах, що супроводжується почервонінням і набряком і часто виникає вночі. До ознак, які збільшують імовірність подагри, відносять тофуси й аналогічний біль в інших суглобах, як-от середина стопи, кісточки, коліна, кисті, зап’ястя або лікті. Хронічний запальний біль в уражених суглобах указує на хронічний подагричний артрит.
Збираючи анамнез і проводячи обстеження, варто звернути увагу на низку ознак, притаманних фенотипу пацієнта з подагрою, зокрема демографічні чинники, особливості способу життя, супутні хвороби та застосування ліків, які підвищують рівень СК (рис. 2).

Важливу роль відіграють дієтичні чинники. Споживання їжі з високим умістом білка, червоного м’яса, морепродуктів, молюсків, фруктози, підсолоджених безалкогольних і алкогольних напоїв, зокрема пива, підвищує ризик подагри, тоді як нежирні молочні продукти, вітамін С та кава, навпаки, захищають від хвороби [3-6]. Дієта DASH (Dietary Approaches to Stop Hypertension) із низьким умістом загальних і насичених жирів включає фрукти, овочі, нежирні молочні продукти. Впродовж 26 років спостереження чоловіки, які дотримувалися дієти DASH, мали менший ризик виникнення подагри [7].
Із меншим ризиком асоціюється також і вегетаріанська дієта [8].
Зв’язки між подагрою, гіперурикемією та супутніми хворобами доволі складні. Деякі хвороби спричиняють виникнення гіперурикемії та/або подагри, інші виникають унаслідок подагри [3]. Ожиріння – вагомий чинник ризику подагри й один з основних чинників збільшення її поширеності. Нещодавній метааналіз показує, що ожиріння асоціюється з більш ніж удвічі вищим ризиком подагри порівняно з особами з індексом маси тіла <30 кг/м2 [9].
У великому дослідженні даних Сполученого Королівства CPRD (Clinical Practice Research Datalink) вивчали часові зв’язки між появою супутніх захворювань до та після встановлення діагнозу подагри [10]. Встановлено, що артеріальна гіпертензія (АГ), гіперліпідемія та хронічна хвороба нирок (ХХН) є чинниками ризику подагри; підтверджено зв’язок подагри з наступними серцево-судинними захворюваннями (ССЗ) та хворобами нирок. Метааналіз когортних досліджень підтвердив, що АГ та застосування діуретиків спричиняють виникнення подагри [9]. Метаболічний синдром, що включає ожиріння, дисліпідемію, АГ та резистентність до інсуліну (діабет, предіабет), істотно підвищує ризик подагри.
У цій когорті її поширеність становить 51-63% [11, 12].
Дослідження у Великій Британії, США й Канаді підтвердили двосторонній зв’язок між подагрою та ХХН [13-16]. Нещодавно з’явилися докази, що подагра асоціюється з вищим ризиком розвитку фібриляції передсердь [17-19], захворювань периферичних артерій [20], венозної тромбоемболії [21-23], обструктивного апное уві сні [24, 25], еректильної дисфункції [26-28], остеопорозу та переломів
у жінок [29-32].
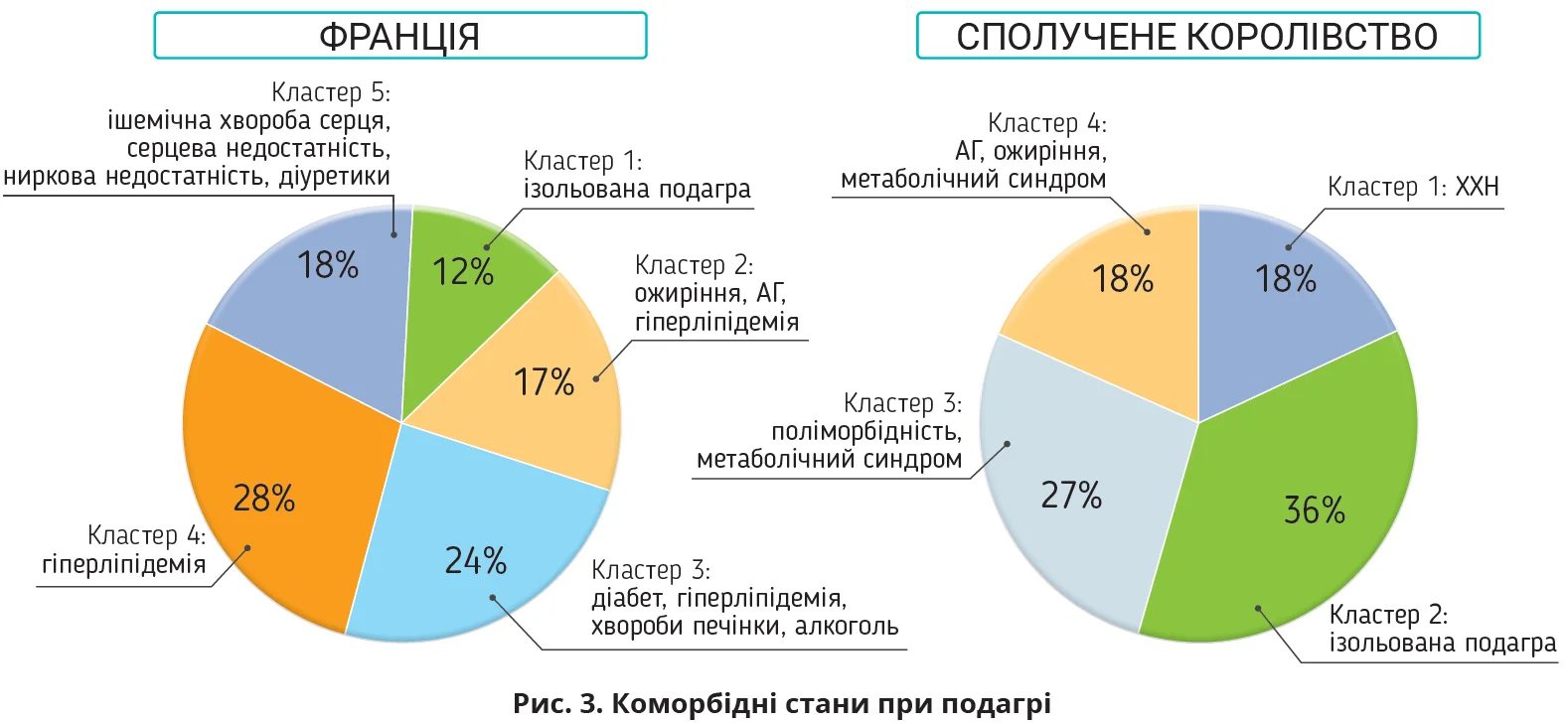
Спроби кластеризувати коморбідність у разі подагри проведено у Франції [33] та Сполученому Королівстві [34]. Обидва дослідження виявили кластер з ізольованою подагрою (12 та 36% відповідно), решта кластерів асоціювалася з латентними або явними супутніми розладами, причому принаймні один із них включав тяжкий перебіг подагри та поліморбідність (рис. 3). У Сполученому Королівстві до кластера ізольованої подагри увійшли пацієнти наймолодші за віком на момент початку хвороби, що вказує на високу ймовірність генетичних чинників у патогенезі подагри в цій когорті [34].
Нещодавнє дослідження, проведене в США, порівнювало коморбідність на момент встановлення діагнозу подагри за період 2009-2010 рр. порівняно з 1989-1992 рр. Встановлено вищу поширеність АГ (69 проти 54%), ХХН (28 проти 11%), гіперліпідемії (61 проти 21%), патологічного ожиріння (29 проти 10%) та цукрового діабету – ЦД (25 проти 6%) [1].
За останні 20 років кількість випадків госпіталізації з приводу подагри у Великій Британії, США та Швеції зросла на 50-100% [35-38]. Значною мірою цьому сприяє асоційована з подагрою коморбідність. Серед 54 215 госпіталізацій в Австралії та Новій Зеландії за період із 2009 по 2014 р. подагра була основною причиною госпіталізації у 36,5% випадків, решта випадків були зумовлені ускладненнями, як-от ССЗ, інсульти, аритмії та ЦД [39]. Проспективне когортне дослідження за участю пацієнтів із випробування NHANES із подальшим метааналізом встановило асоціацію гіперурикемії та смертності від усіх причин і від ССЗ в осіб із діабетом (рис. 4) [40].

Настанови Національного інституту здоров’я та вдосконалення клінічної практики Великої Британії (NICE, 2022) щодо діагностики й лікування подагри наголошують на важливості застосування уратознижувальної терапії (УЗТ) у тривалому менеджменті (рис. 5) [41].

Незважаючи на те що подагра є одним із небагатьох «виліковних» ревматичних захворювань, на сучасному етапі терапія є часто неадекватною через низький рівень призначення УЗТ і прихильності пацієнтів до лікування [42]. Нещодавнє дослідження вивчало прихильність до лікування алопуринолом у 22 056 пацієнтів із діабетом і подагрою впродовж 3 років після першого призначення. Встановлено, що 41,2% пацієнтів не постійно застосовували препарат, особливо жінки, пацієнти з деменцією та нетяжкими нападами подагри. Перервали лікування 20,9%, повністю припинили – 20,3%. Переривання та припинення прийому УЗТ частіше асоціювалося з тяжкою формою подагри й більшою ймовірністю призначення преднізону. Автори зазначають, що субоптимальна УЗТ не тільки підвищує ризик ускладнень подагри в цій популяції, але й потенційно збільшує можливість ускладнень діабету через негативний вплив кортикостероїдів на глікемічний контроль [43].
До препаратів першої лінії УЗТ тепер відносять фебуксостат [41]. Це потужний селективний непуриновий інгібітор ксантиноксидази – ферменту, що каталізує обидві стадії перетворення гіпоксантину на СК. Препарат має здатність пригнічувати активність як окисненої, так і відновленої форми ксантиноксидази без впливу на інші ферменти, що беруть участь у метаболізмі пуринів і піримідинів. Ефективність фебуксостату підтверджена у фазі III рандомізованих контрольованих досліджень APEX (Allopurinol and Placebo-Controlled Efficacy Study of Febuxostat), FACT (Febuxostat Allopurinol Controlled Trial) і CONFIRMS за участю 4101 пацієнта з гіперурикемією та подагрою. У кожному з досліджень фебуксостат продемонстрував ефективніше зниження СК та підтримку її належного рівня порівняно з алопуринолом [44-46]. На вітчизняному фармацевтичному ринку фебуксостат представлений препаратом Подафеб, який виробляє АТ «Київський вітамінний завод». Випускається в таблетках із двома варіантами дозування – по 80 і 120 мг, що полегшує титрування. Подафеб – єдиний фебуксостат українського виробництва повного циклу. Препарат пройшов дослідження біоеквівалентності та відповідає оригінальну фебуксостату. Крім того, вітчизняний препарат має оптимальне співвідношення «ціна/якість», що часто є вирішальним чинником у прихильності пацієнтів до лікування.
Висновки
- Подагра – хронічна прогресивна хвороба, що виникає на тлі тривалої гіперурикемії та характеризується відкладанням кристалів моноурату натрію в суглобах, сухожиллях та інших тканинах.
- Залежно від досліджуваної популяції на подагру хворіє від 1 до 6,8% населення. Поширеність і захворюваність прогресивно збільшуються.
- Здебільшого дебютом хвороби є гострий запальний моно-/олігоартрит типової локалізації. Характерні повторні атаки артриту зі скороченням тривалості безсимптомних періодів і втягненням нових суглобів. Із часом хвороба переростає в хронічний подагричний поліартрит із деструкцією суглобів, формуванням тофусів у м’яких тканинах і можливим ураженням нирок (сечокам’яна хвороба).
- Подагра часто супроводжується коморбідними станами, як-от ССЗ, ХХН, ожиріння та ЦД 2 типу. Ожиріння й супутні захворювання є важливими чинниками ризику подагри, збільшення її поширеності та несприятливого перебігу.
- Менш як половина пацієнтів отримують УЗТ, що має вирішальне значення в лікуванні хвороби. Прихильність до УЗТ здебільшого погана, з високими показниками непостійності.
- Сучасні міжнародні рекомендації наголошують на важливості ранньої тривалої УЗТ із використанням препаратів першої лінії – алопуринолу або фебуксостату, який забезпечує ефективніше зниження СК та підтримку її цільових рівнів.
- Подафеб – новий препарат фебуксостату вітчизняного виробника, який пройшов дослідження біоеквівалентності та разом із препаратом Алопуринол-КВ відіграє важливу роль у тривалій терапії пацієнтів із подагрою.
Література
- Elfishawi M., et al. The rising incidence of gout and the increasing burden of comorbidities: a population-based study over 20 years. J. Rheumatol. 2018; 45 (4): 574-579.
- Dalbeth N., et al. Relationship between serum urate concentration and clinically evident incident gout: an individual participant data analysis. Ann. Rheum. Dis. 2018; 77: 1048-1052.
- Kuo C., Grainge M., Zhang W., Doherty M. Global epidemiology of gout: prevalence, incidence and risk factors. Nat. Rev. Rheumatol. 2015; 11: 649-662.
- Teng G., Pan A., Yuan J.-M., Koh W.-P. Food sources of protein and risk of incident gout in the Singapore Chinese Health Study. Arthritis Rheumatol. 2015;
67: 1933-1942. - Ayoub-Charette S., et al. Important food sources of fructose-containing sugars and incident gout: a systematic review and meta-analysis of prospective cohort studies. BMJ Open. 2019; 9: e024171.
- Jamnik J., et al. Fructose intake and risk of gout and hyperuricemia: a systematic review and meta-analysis of prospective cohort studies. BMJ Open. 2016;
6: e013191. - Rai S.K., et al. The Dietary Approaches to Stop Hypertension (DASH) diet, Western diet, and risk of gout in men: prospective cohort study. BMJ. 2017; 357: j1794.
- Chiu T.H.T., Liu C.-H., Chang C.-C., Lin M.-N., Lin C.-L. Vegetarian diet and risk of gout in two separate prospective cohort studies. Clin. Nutr. 2020; 39: 837-844.
- Evans P.L., et al. Obesity, hypertension and diuretic use as risk factors for incident gout: a systematic review and meta-analysis of cohort studies. Arthritis Res. Ther. 2018; 20: 136.
- Kuo C.-F., Grainge M.J., Mallen C., Zhang W., Doherty M. Comorbidities in patients with gout prior to and following diagnosis: case-control study. Ann. Rheum. Dis. 2016; 75: 210-217.
- Jung J.H., et al. Metabolic syndrome: prevalence and risk factors in Korean gout patients. Korean J. Intern. Med. 2018; 33: 815-822.
- Choi H.K., Ford E.S., Li C., Curhan G. Prevalence of the metabolic syndrome in patients with gout: the Third National Health and Nutrition Examination Survey. Arthritis Rheum. 2007; 57: 109-115.
- Jaffe D.H., et al. Incident gout and chronic kidney disease: healthcare utilization and survival. BMC Rheumatol. 2019; 3: 11.
- Roughley M., et al. Risk of chronic kidney disease in patients with gout and the impact of urate lowering therapy: a population-based cohort study. Arthritis Res. Ther. 2018; 20: 243.
- Singh J., Cleveland J. Gout is associated with a higher risk of chronic renal disease in older adults: a retrospective cohort study of U.S. Medicare population. BMC Nephrol. 2019; 20: 93.
- Tan V.S., et al. The 3-year incidence of gout in elderly patients with CKD. Clin. J. Am. Soc. Nephrol. 2017; 12: 577-584.
- Singh J.A., Cleveland J.D. Gout and the risk of incident atrial fibrillation in older adults: a study of US Medicare data. RMD Open. 2018; 4: e000712.
- Kuo Y.J., et al. The risk of atrial fibrillation in patients with gout: a nationwide population-based study. Sci. Rep. 2016; 6: 32220.
- Kim S.C., Liu J., Solomon D.H. Risk of incident atrial fibrillation in gout: a cohort study. Ann. Rheum. Dis. 2016; 75: 1473-1478.
- Clarson L.E., et al. Increased risk of vascular disease associated with gout: a retrospective, matched cohort study in the UK Clinical Practice Research Datalink. Ann. Rheum. Dis. 2015; 74: 642-647.
- Chiu C.C., et al. Association between previous history of gout attack and risk of deep vein thrombosis – a nationwide population-based cohort study. Sci. Rep. 2016; 6: 26541.
- Li L., et al. Trends of venous thromboembolism risk before and after diagnosis of gout: a general population-based study. Rheumatology. 2020; 59: 1099-1107.
- Sultan A.A., et al. Venous thromboembolism in patients with gout and the impact of hospital admission, disease duration and urate-lowering therapy. CMAJ. 2019; 191: E597-E603.
- Singh J., Cleveland J. Gout and the risk of incident obstructive sleep apnea in adults 65 years or older: an observational study. J. Clin. Sleep. Med. 2018; 14: 1521-1527.
- Blagojevic-Bucknall M., et al. The risk of gout among patients with sleep apnea: a matched cohort study. Arthritis Rheumatol. 2019; 71: 154-160.
- Abdul Sultan A., et al. Gout and subsequent erectile dysfunction: a population-based cohort study from England. Arthritis Res. Ther. 2017; 19: 123.
- Chen Y.F., et al. Gout and a subsequent increased risk of erectile dysfunction in men aged 64 and under: a nationwide cohort study in Taiwan. J. Rheumatol. 2015; 42: 1898-1905.
- Hsu C., Lin C., Kao C. Gout is associated with organic and psychogenic erectile dysfunction. Eur. J. Intern. Med. 2015; 26: 691-695.
- Wang Y., et al. Association of gout with osteoporotic fractures. Int. Orthop. 2018; 42: 2041-2047.
- Tzeng H.-E., Lin C.-C., Wang I.K., Huang P.-H., Tsai C.-H. Gout increases risk of fracture: a nationwide population-based cohort study. Medicine. 2016; 95: e4669.
- Paik J.M., et al. Gout and risk of fracture in women: a prospective cohort study. Arthritis Rheumatol. 2017; 69: 422-428.
- Kok V.C., et al. Gout as a risk factor for osteoporosis: epidemiologic evidence from a population-based longitudinal study involving 108,060 individuals. Osteoporos. Int. 2018; 29: 973-985.
- Richette P., Clerson P., Périssin L., Flipo R.-M., Bardin T. Revisiting comorbidities in gout: a cluster analysis. Ann. Rheum. Dis. 2015; 74: 142-147.
- Bevis M., Blagojevic-Bucknall M., Mallen C., Hider S., Roddy E. Comorbidity clusters in people with gout: an observational cohort study with linked medical record review. Rheumatology. 2018; 57: 1358-1363.
- Han G.-M., Michaud K., Yu F., Watanabe-Galloway S., Mikuls T.R. Increasing public health burden of arthritis and other rheumatic conditions and comorbidity: results from a Statewide Health Surveillance System, 2007-2012. Arthritis Care Res. 2016; 68: 1417-1427.
- Kiadaliri A., Englund M. Temporal trends and regional disparity in rheumatoid arthritis and gout hospitalizations in Sweden, 1998-2015. Clin. Rheumatol. 2018; 37: 825-830.
- Lim S.Y., et al. Trends in gout and rheumatoid arthritis hospitalizations in the United States, 1993-2011. JAMA. 2016; 315: 2345-2347.
- Russell M., et al. Rising incidence of acute hospital admissions due to gout. J. Rheumatol. 2020; 47: 619-623.
- Robinson P., Kempe S., Tebbutt I., Roberts L. Epidemiology of inpatient gout in Australia and New Zealand: temporal trends, comorbidities and gout flare site. Int. J. Rheum. Dis. 2017; 20: 779-784.
- Li B., Chen L., Hu X., Tan T., Yang J., Bao W., Rong S. Association of serum uric acid with all-cause and cardiovascular mortality in diabetes. Diabetes Care. 2023; 46 (2): 425-433.
- Gout: diagnosis and management. London: National Institute for Health and Care Excellence (NICE); 2022 Jun 9. Available at: https://www.nice.org.uk/guidance/ng219.
- Dehlin M., Jacobsson L., Roddy E. Global epidemiology of gout: prevalence, incidence, treatment patterns and risk factors. Nat. Rev. Rheumatol. 2020; 16 (7): 380-390.
- Weisman A., Tomlinson G.A., Lipscombe L.L., Perkins B.A., Hawker G.A. Allopurinol adherence, persistence and patterns of use in individuals with diabetes and gout: a retrospective, population-based cohort analysis. Semin. Arthritis Rheum. 2021; 51 (6): 1162-1169.
- Becker M.A., Schumacher H.R. Jr, Wortmann R.L., MacDonald P.A., Palo W.A., Eustace D., et al. Febuxostat, a novel non-purine selective inhibitor of xanthine oxidase: a twenty-eight day, multicenter, phase II, randomized, double-blind, placebo-controlled, dose-response clinical trial examining safety and efficacy in patients with gout. Arthritis Rheum. 2005b; 52: 916-923.
- Schumacher H.R. Jr, Becker M.A., Wortmann R.L., Macdonald P.A., Hunt B., Streit J., Lademacher C., Joseph-Ridge N. Effects of febuxostat versus allopurinol and placebo in reducing serum urate in subjects with hyperuricemia and gout: a 28-week, phase III, randomized, double-blind, parallel-group trial. Arthritis Rheum. 2008; 59 (11): 1540-8.
- Becker M.A., Schumacher H.R., Espinoza L.R., Wells A.F., MacDonald P., Lloyd E., Lademacher C. The urate-lowering efficacy and safety of febuxostat in the treatment of the hyperuricemia of gout: the CONFIRMS trial. Arthritis Res. Ther. 2010; 12 (2): R63.
