Ожиріння-2025: нова мова, нові алгоритми. Огляд рекомендацій комісії Lancet і ААСЕ
Підготувала канд. мед. наук Тетяна Можина
Минулий 2025 рік став роком перегляду підходів до номенклатури, концепції ожиріння й уявлень щодо його лікування. Одночасно з розширенням терапевтичних можливостей у центрі уваги опинилися практичні питання: кого саме треба вважати пацієнтом з ожирінням, коли надлишкова маса тіла стає хворобою, а коли залишається станом підвищеного ризику та за якими критеріями варто вибирати інтенсивність медикаментозних і хірургічних утручань.
Міжнародна комісія Lancet: доклінічне та клінічне ожиріння
Важливий крок на шляху змін зробила міжнародна комісія Lancet з ожиріння, котра критично переглянула традиційний підхід до діагностики ожиріння, заснований переважно на визначенні індексу маси тіла (ІМТ). Відповідно до погодженої думки 58 експертів із 75 країн, які увійшли до складу комісії Lancet, застосування ІМТ корисно для виявлення осіб з підвищеним ризиком несприятливих наслідків для здоров’я, але цей показник не дає змоги безпосередньо виміряти кількість жирової тканини, не відображає розподілу жиру в організмі та не допомагає визначити, коли надлишок жирової тканини стає причиною порушення здоров’я [1].
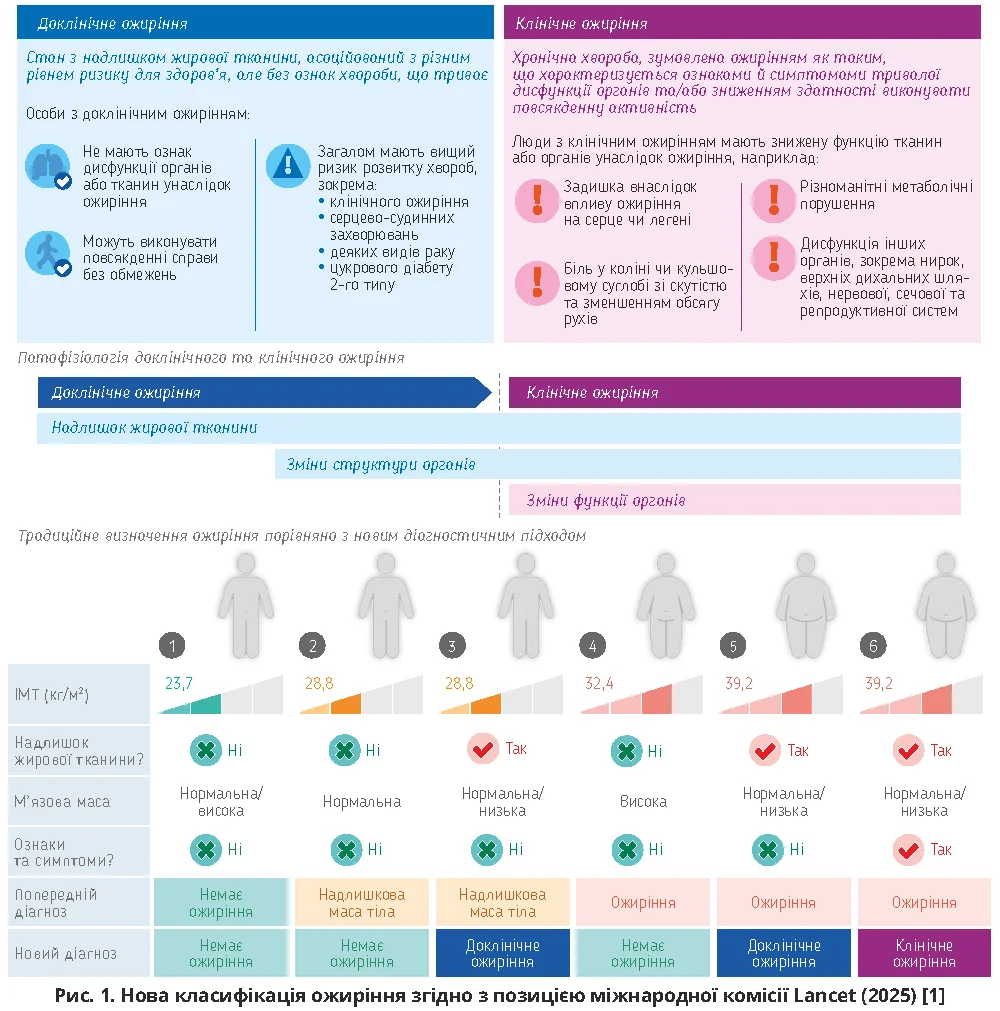
З огляду на ці обмеження комісія Lancet запропонувала нові поняття – «доклінічне/клінічне ожиріння», що тісно пов’язані з терміном «адипозність» і категорією «асоційовані з ожирінням ускладнення та захворювання» (АОУЗ). Адипозність характеризує кількість, розподіл і функціональний стан жирової тканини; при цьому вона не тільки оцінює, скільки жиру в організмі, а й ураховує, де він накопичується та як поводиться метаболічно. Згідно з позицією комісії Lancet термін «доклінічне ожиріння» слід використовувати для позначення стану надлишкової адипозності без наявності АОУЗ, тоді як «клінічне ожиріння» відображає вже сформовані ускладнення, що визначають як зміни структури та/або функції органів, які зазвичай проявляються симптомами й виникають саме через надлишкову адипозність (рис. 1) [2].
Саме такий підхід пояснює, чому пацієнти з однаковим ІМТ можуть мати принципово різний ризик ускладнень, який залежить від фенотипу адипозності. Найбільш клінічно значущими визнано надлишок вісцеральної жирової тканини, ектопічне відкладання жиру (наприклад, у печінці), а також дисфункцію жирової тканини як ендокринного органа (зміни у виробленні адипокінів, хронічне низькоінтенсивне запалення, інсулінорезистентність). Зберігаючи використання ІМТ як важливого скринінгового показника, комісія Lancet підкреслює недостатність його «моновикористання» для повного клінічного оцінювання та рекомендує доповнювати визначення ІМТ оцінюванням проявів, ускладнень і супутніх захворювань [1].
ААСЕ-2025: від нових термінів до нових алгоритмів
Наприкінці 2025 року Американська асоціація клінічної ендокринології (AACE) опублікувала оновлену консенсусну заяву й алгоритми з діагностики та лікування ожиріння в дорослих [3]. На відміну від попередніх версій, у яких ключовим орієнтиром були антропометричні критерії (насамперед ІМТ), за допомогою яких установлювали діагноз і вибирали тактику ведення, оновлена настанова запроваджує ключову термінологічну новацію – поняття «хронічна хвороба, зумовлена адипозністю» (ХХЗА) – та підтримує необхідність використання терміна «АОУЗ».
Експерти ААСЕ розглядають ХХЗА як парасольковий термін, що об’єднує спектр станів від надлишкової адипозності без поточних клінічних наслідків до форм з наявними ускладненнями, які й визначають клінічні цілі лікування [3]. Такий термінологічний зсув відображає патофізіологічний підхід, який підкреслює, що клінічно значущою є не вага сама по собі, а адипозність і пов’язані з нею наслідки для здоров’я. Водночас представники ААСЕ підтримують використання термінів, запропонованих комісією Lancet (рис. 2).
Запровадження термінів «доклінічне/клінічне ожиріння», «ХХЗА», «АОУЗ» змінило не лише мову, а й клінічну логіку. Нині вибір тактики дедалі більше визначають два запитання: чи має пацієнт АОУЗ і наскільки вони виражені, а також на які результати очікує сам пацієнт і що для нього прийнятне в довгостроковій перспективі? На цьому ґрунтуються два взаємопов’язані принципи, які AACE формулює як «ускладнення- та людиноцентричний підходи». Ускладненняцентричний підхід означає, що інтенсивність лікування визначають насамперед наявністю й тяжкістю АОУЗ, їхнім впливом на функцію органів, симптоми та прогноз. Людиноцентричний підхід передбачає формування цілей лікування разом з пацієнтом, персоналізацію плану з урахуванням пріоритетів пацієнта, ресурсів і можливих бар’єрів [3]. Разом ці принципи переводять ведення ожиріння від ІМТ-центричної моделі до персоналізованої тривалої допомоги, де успіх оцінюють не лише зміною маси тіла, а й динамікою ускладнень, симптомів і якості життя.
Діагностика: антропометричний і клінічний компоненти
Ще однією особливістю оновленої настанови AACE є двокомпонентний підхід до діагностики ожиріння/ХХЗА, який передбачає виділення антропометричного та клінічного компонентів. Антропометричний компонент покликаний дати відповідь на запитання «чи є надлишкова/аномальна адипозність», тоді як клінічний компонент має визначити тяжкість хвороби й те, як саме адипозність впливає на здоров’я, якість життя.
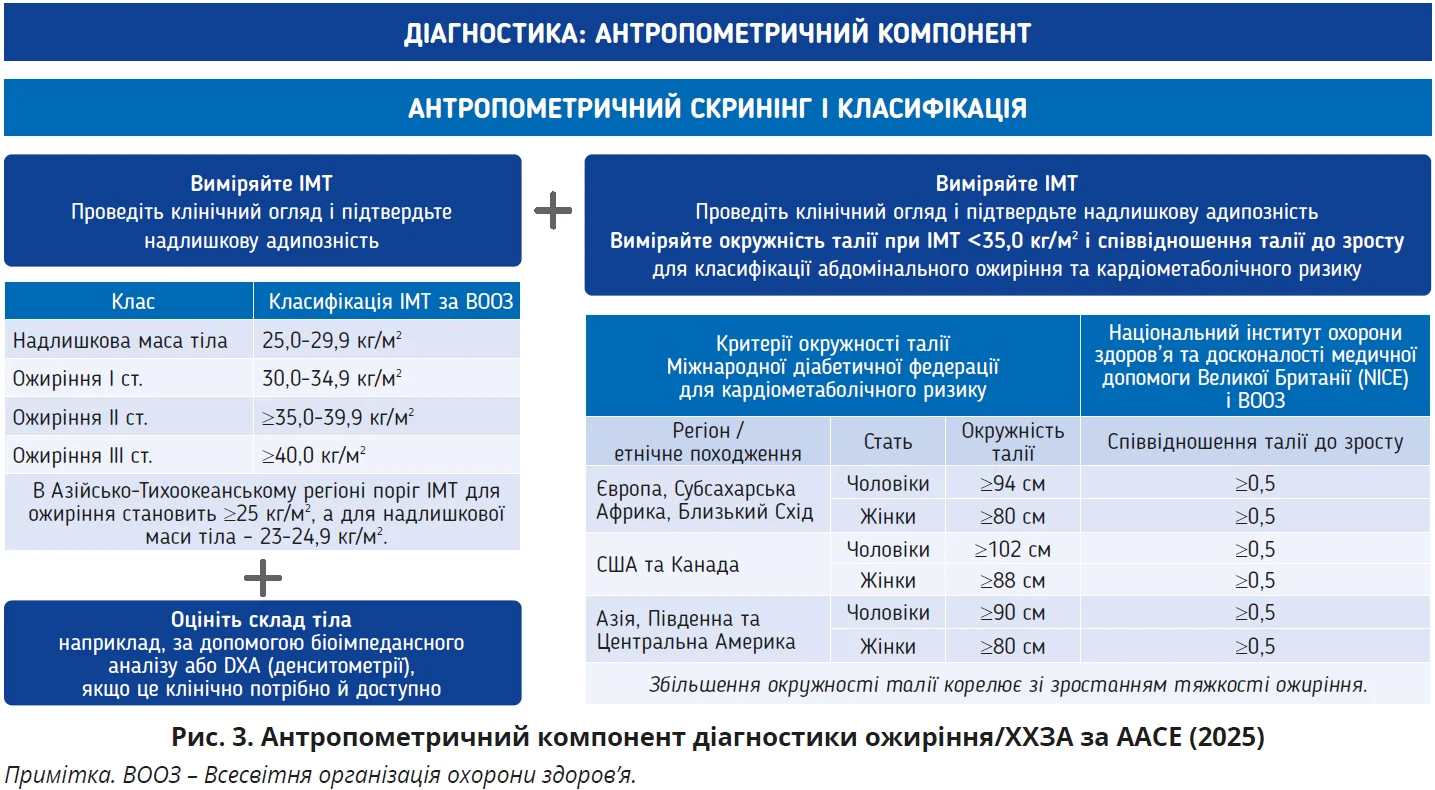
Діагностика ожиріння/ХХЗА розпочинається з антропометрії та скринінгу за ІМТ (рис. 3), але експерти AACE підкреслюють, що ІМТ сам по собі не є підтвердженням надлишкової адипозності, тому його значення потрібно верифікувати за допомогою огляду та фізичного обстеження. Рекомендується оцінювати не лише масу тіла, а й розподіл жирової тканини, вимірюючи окружність талії та визначаючи співвідношення талія/стегна й талія/зріст; причому інтерпретувати отримані дані слід з урахуванням віку, статі й етнічних особливостей [3]. Підкреслюється ще один важливий практичний момент: аналізуючи значення ІМТ, варто взяти до уваги м’язову масу, набряки/гіпергідратацію, саркопенію / саркопенічне ожиріння, за потреби – діагностувати їх за допомогою двохенергетичної рентгенівської абсорбціометрії (DXA), біоімпедансу, магнітно-резонансної томографії.
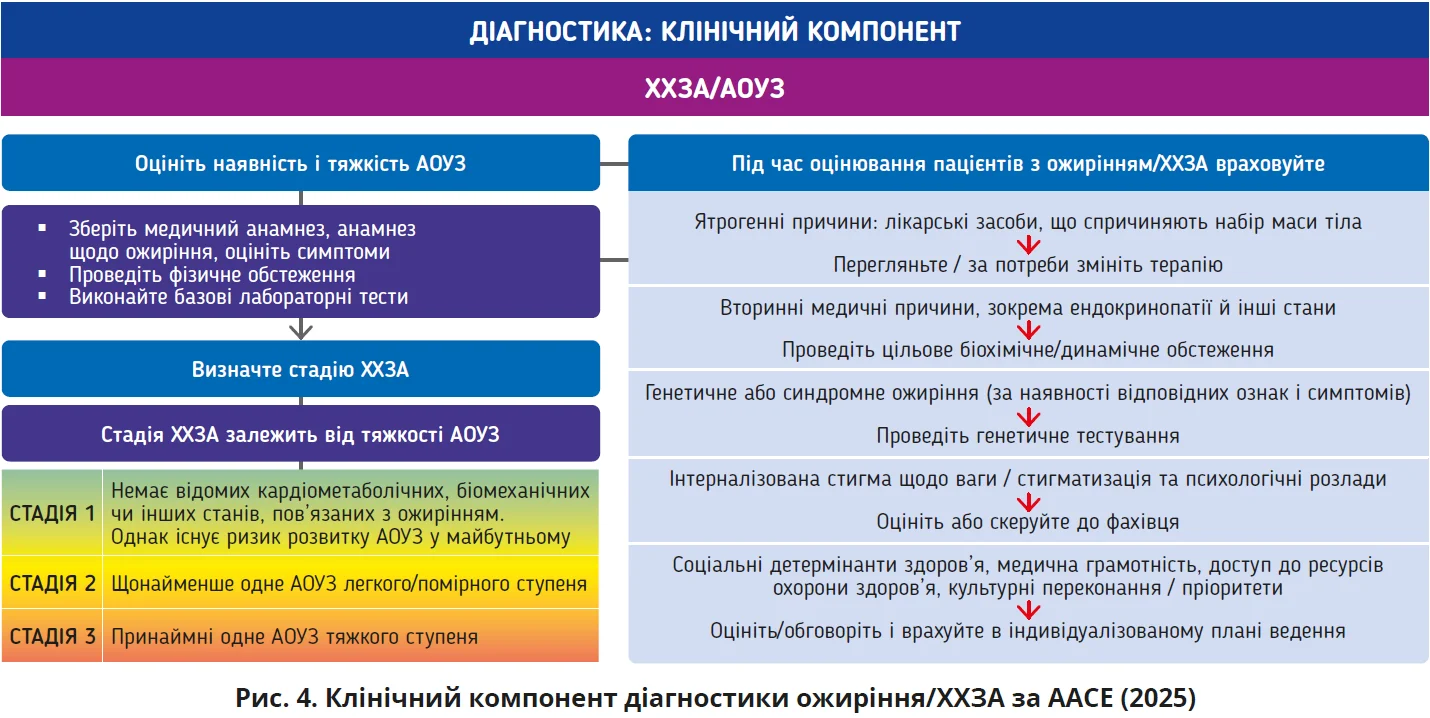
Клінічний компонент фокусується на встановленні наявності та тяжкості АОУЗ, оскільки саме вони визначають стадію ХХЗА й інтенсивність терапії. Визначення стадії ХХЗА потребує повноцінного клінічного оцінювання: збору анамнезу (включно з попередніми спробами лікування), огляду та фізичного обстеження, визначення базових лабораторних показників і, за потреби, проведення додаткових тестів / візуалізації для уточнення конкретних АОУЗ (рис. 4). Відповідно до цього підходу пропонується проста класифікація: стадія 1 – АОУЗ відсутні (аналог «доклінічного ожиріння»), стадії 2-3 – АОУЗ наявні (від легких/помірних до тяжких), що відповідає «клінічному ожирінню»; при цьому навіть стадія 1 розглядається як частина спектра ХХЗА та може потребувати активних утручань для запобігання прогресуванню [3].
Первинне обстеження: обов’язкові та додаткові компоненти
Наступним кроком є проведення первинного обстеження, котре AACE розглядає як стандартизований фундамент збору даних для виявлення АОУЗ і планування подальшої тактики ведення пацієнта. Первинне обстеження включає кілька обов’язкових компонентів. По-перше, збір медичного анамнезу й анамнезу зміни маси тіла протягом життя з урахуванням попередніх спроб зниження маси тіла, проведення фізичного обстеження. По-друге, сімейний і соціальний анамнез (харчові вподобання, рівень фізичної активності, соціальні детермінанти здоров’я, куріння) та структуроване опитування, спрямоване на виявлення симптомів можливих АОУЗ – від кардіореспіраторних (задишка, ортопное, біль у грудях, синкопе) та порушень сну до поліурії, суглобового болю, обмеження мобільності, втоми, тривоги/депресії, досвіду стигматизації [3]. Частину цих даних AACE пропонує збирати за допомогою опитувальників, щоби зробити оцінку відтворюваною та менш залежною від часу приймання (рис. 5).
Окремий блок первинного обстеження становлять базові лабораторні тести для скринінгу кардіометаболічного ризику й супутніх станів: глюкоза натще та/або глікований гемоглобін (HbA1c), ліпідограма, креатинін з розрахунком швидкості клубочкової фільтрації (ШКФ), а також АЛТ/АСТ і тромбоцити для розрахунку індексу FIB-4 (як стартової оцінки ризику фіброзу при супутній метаболічно-асоційованій стеатотичній хворобі печінки).
Принципова позиція AACE полягає в тому, що подальші обстеження виконують лише за показаннями, зважаючи на дані первинного оцінювання: наприклад, 2-годинний оральний глюкозотолерантний тест, ехокардіографію, добове моніторування артеріального тиску (АТ), еластографію печінки / біопсію, психологічне обстеження, генетичне тестування або спрямування до суміжних фахівців призначають за наявності відповідних змін [3]. Такий підхід дає змогу відразу пов’язати діагностику із завданнями ускладненняцентричного підходу: не «обстежити все», а цілеспрямовано підтвердити/уточнити ті АОУЗ, які визначатимуть стадію ХХЗА й інтенсивність лікування.
Лікування: цільові показники та модифікація способу життя
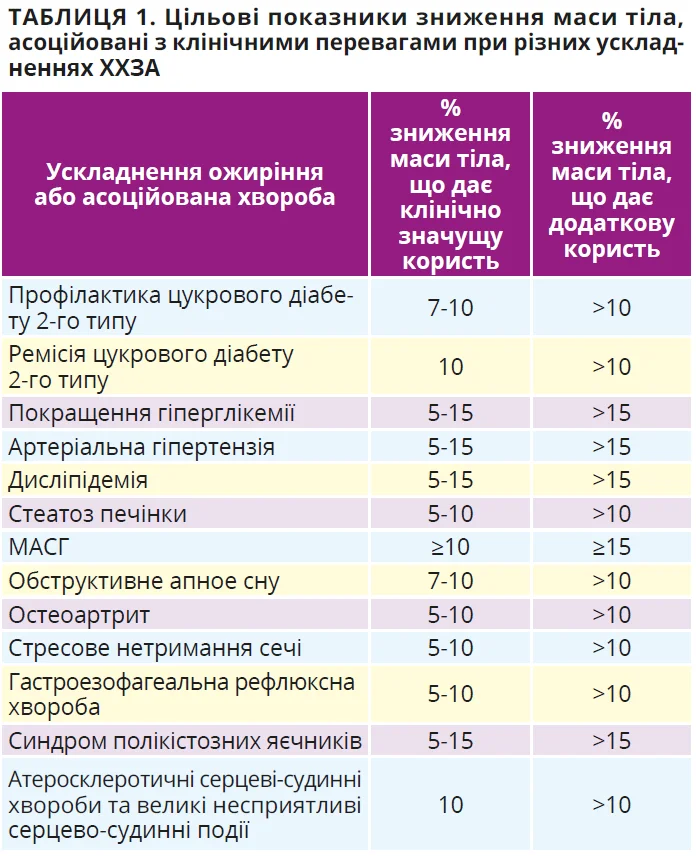
Лікувальна стратегія в оновленій настанові AACE спирається на стадію ХХЗА та наявні АОУЗ: інтенсивність утручань визначають за конкретними клінічними цілями, а не лише за показниками ІМТ. При цьому бажаний відсоток зниження маси тіла розглядають як практичний орієнтир, своєрідний біомаркер відповіді, який пов’язують із прогнозованим покращенням окремих АОУЗ і використовують для своєчасної корекції тактики (табл. 1).
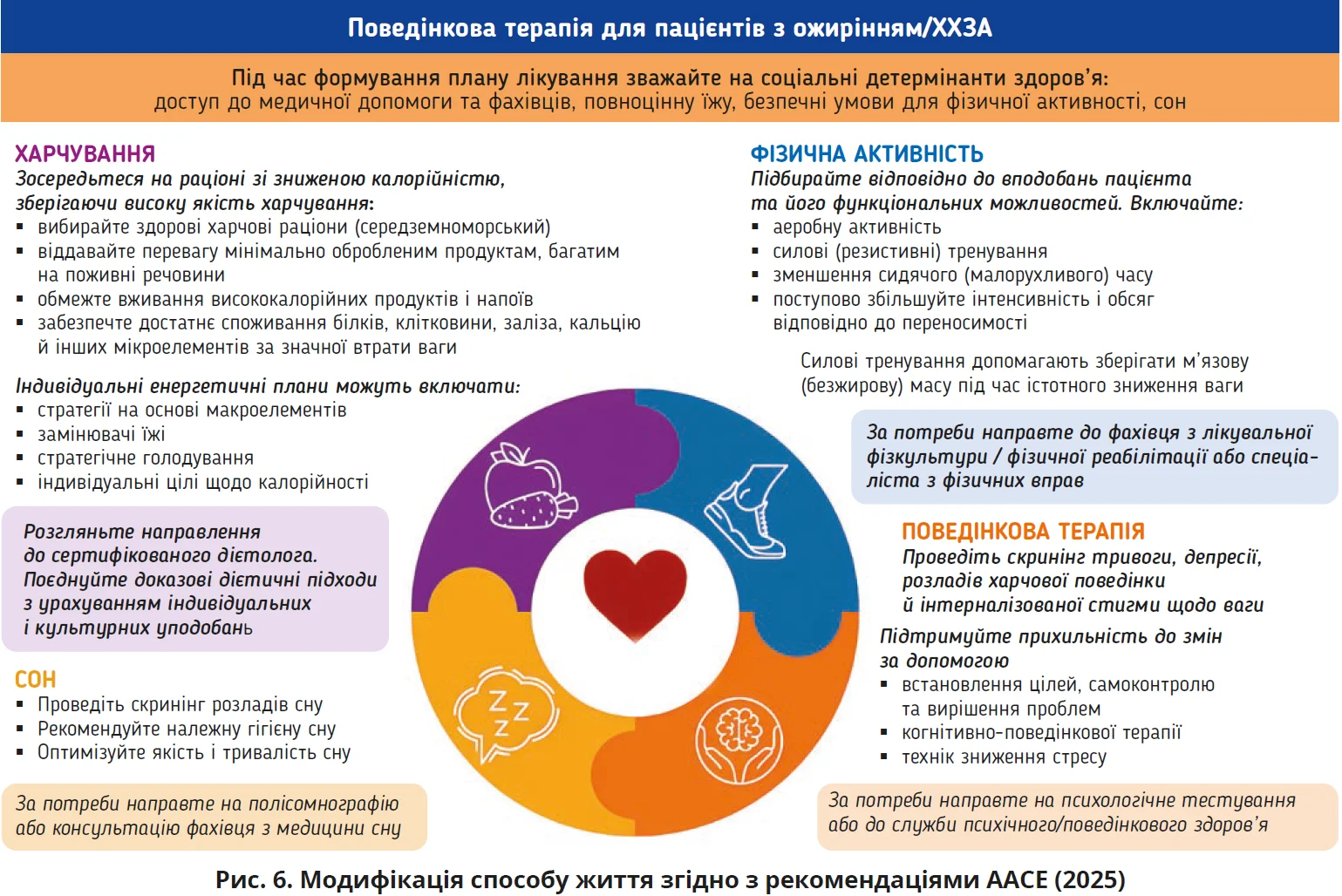
Фундаментом лікування ожиріння/ХХЗА в алгоритмі AACE залишається модифікація способу життя, однак подана вона не як «універсальна порада», а як керований інструмент під конкретні цілі та можливості пацієнта. Харчування насамперед має створювати стійкий енергетичний дефіцит, але ключовим стає не жорстка дієта, а відтворюваний план, який людина здатна підтримувати місяцями й роками (рис. 6) [3]. Тому акцент зміщується на якість раціону та нутритивну щільність: більше продуктів, що дають ситість і водночас забезпечують білок, клітковину, мікронутрієнти; менше енергетично щільних і ультраперероблених страв. На практиці це означає: порції менші, ритм харчування регулярніший, білок присутній у кожному основному прийомі їжі, а «калорійні тригери» (особливо жирні страви та великі порції) слід ретельно контролювати, зокрема тому, що вони часто погіршують гастроінтестинальні симптоми в пацієнтів, які отримують сучасну фармакотерапію. Окремий принцип полягає в збереженні м’язової маси під час зниження ваги: достатня кількість білка та продумана структура харчування знижують ризик небажаної втрати безжирової маси, що напряму впливає і на метаболічні результати, і на здатність утримувати досягнуте.
Безперечно, підкреслюється значущість фізичної активності: нині її розглядають з погляду покращення чутливості до інсуліну, поліпшення композиції тіла, зменшення кардіометаболічних факторів ризику, покращення самопочуття та підтримання ваги. AACE пропонує стартувати з реальної для пацієнта вихідної точки, роблячи рух частиною щоденної рутини й застосовуючи прийнятні активності (ходьба, плавання, їзда на велосипеді) з поступовим нарощуванням частоти, інтенсивності та тривалості. Оптимальним орієнтиром вважають щонайменше 150 хвилин на тиждень помірної інтенсивності або 75 хвилин – високої; для утримання зниження маси тіла часто потрібні більші обсяги руху. Окремо підкреслюється пріоритет силових/резистивних тренувань, особливо в пацієнтів, які отримують фармакотерапію та/або перенесли баріатричне втручання: саме вони допомагають зберігати м’язову масу, підтримувати функціональність і роблять результат лікування стійкішим.
Ефективність модифікації способу життя рекомендується оцінювати одночасно за двома компонентами: антропометрично (відсоток зниження маси тіла) та клінічно (динаміка АОУЗ/симптомів, даних лабораторних/функціональних обстежень). Час оцінювання ефективності перелічених заходів строго не регламентований: він визначається індивідуально, в спільному рішенні лікаря та пацієнта, залежно від стадії ХХЗА й наявних АОУЗ. Такий підхід потрібен не лише для фіксації прогресу, а й для своєчасного рішення про корекцію або ескалацію лікування. Якщо за визначений інтервал відповідь є недостатньою або ризик, зумовлений АОУЗ, залишається високим, алгоритм передбачає додавання специфічної фармакотерапії.
Фармакотерапія: ієрархія препаратів і покращення переносимості
Представники ААСЕ розглядають фармакотерапію як спосіб ескалації лікування, котрий застосовують разом з модифікацією способу життя для досягнення персоналізованих цілей. Важливо, що вибір препарату зумовлений не тільки очікуваним зниженням маси тіла, а й провідними/наявними АОУЗ. Саме тому в контексті ускладненняцентричного підходу експерти вперше запропонували так звану ієрархію препаратів переваги на підставі даних клінічних досліджень (рис. 7). Першу сходинку в ієрархії за наявності кардіометаболічного профілю патологічних змін у більшості випадків займають сучасні інкретин-міметики (семаглутид і тирзепатид), тоді як ліраглутид визнано препаратом другої лінії [3]. Третю сходинку в ієрархії в багатьох випадках займають орлістат, налтрексон, бупропіон. За наявності біомеханічних ускладнень можливе застосування тирзепатиду, семаглутиду та фентерміну/топірамату. Такий розподіл препаратів у «ієрархії переваги» відображає насамперед різницю в очікуваній ефективності та силі доказів щодо впливу на ключові АОУЗ.
Перевага віддається семаглутиду, тирзепатиду через їхню здатність забезпечити найбільше зниження середньої маси тіла та покращити кардіометаболічний профіль.
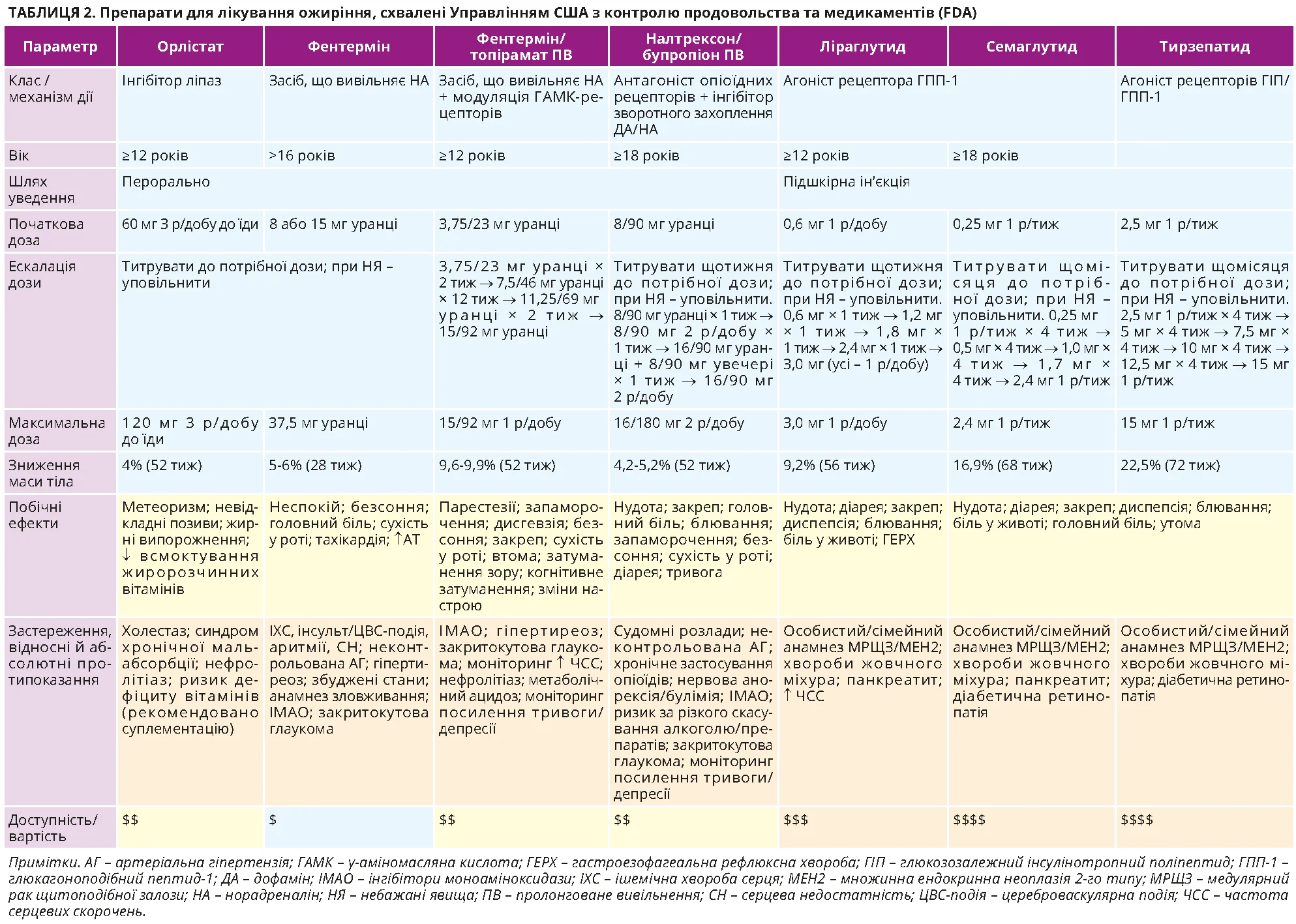
Переносимість у цій ієрархії також урахована. Найпоширенішою причиною скасування інкретинових препаратів (ліраглутид, семаглутид, тирзепатид) є небажані гастроінтестинальні симптоми, які часто виникають саме на етапі підвищення дози. Тому експерти AACE радять застосовувати такі правила: починати з мінімальної дози й титрувати «за переносимістю», тобто за потреби затримувати ескалацію, довше утримувати попередній крок або тимчасово повернутися до дози, яку пацієнт добре переносить (табл. 2). Водночас слід рекомендувати немедикаментозні заходи: повільно приймати їжу, вживати менші порції, уникати дуже жирних страв і рясного застілля, пити достатню кількість води. Якщо виникає блювання або діарея, важливо оцінити ризик дегідратації та ймовірність погіршення функції нирок, розглянути можливість паузи чи зробити крок назад під час титрації дози.
Переносимість інших препаратів (фентермін або фентермін/топірамат) не така добра, їх приймання пов’язане з виникненням системних ефектів (серцево-судинні ризики, психіатричний профіль) і менше залежить від темпу титрації. Отже, місце кожного препарату в ієрархії визначає баланс між імовірністю досягнення цільового зниження маси тіла, зменшення АОУЗ та обмеженнями переносимості й безпеки для конкретного пацієнта. Саме тому AACE підкреслює необхідність персоналізації: вибирати терапію за домінувальними ускладненнями, протипоказаннями, супутньою фармакотерапією та здатністю пацієнта тривало дотримуватися вибраного режиму.
На відміну від невизначеного часу оцінювання ефективності модифікувальної терапії, результативність фармаколікування рекомендується перевіряти в чіткій контрольній точці: приблизно через 3 місяці перебування на терапевтичній (цільовій) дозі. Відповідь оцінюють за відсотком зниження маси тіла, використовуючи значення ІМТ: ≤5% вважають неповною відповіддю, від >5 до <15% – доброю, ≥15% – відмінною. Якщо через 3 місяці на цільовій дозі зниження ІМТ становить <5%, довгострокова ефективність, імовірно, буде недостатньою, тому потрібна зміна підходу: інтенсифікація модифікації способу життя, заміна препарату або перехід до комбінації декількох засобів проти ожиріння. Якщо досягнуто зниження ІМТ на ≥5%, терапію продовжують. Під час подальшого спостереження передбачається ескалація лікування, якщо цілі щодо АОУЗ не досягаються.
Висновки
У 2025 році дискусія про ожиріння вийшла за межі ІМТ і «зайвих кілограмів»: на перший план вийшли адипозність, її фенотип і конкретні наслідки для здоров’я. Комісія The Lancet запропонувала розмежування доклінічного та клінічного ожиріння, а AACE закріпила це мислення в практичних алгоритмах, запровадивши рамку ХХЗА та поняття АОУЗ як ключ до стадіювання й вибору інтенсивності лікування. Двокомпонентна діагностика (антропометрична та клінічна) разом зі стандартизованим первинним обстеженням допомагає швидко перейти від оцінювання ваги до оцінювання ризиків і цілей терапії. У лікуванні центральними стають ускладнення- та людиноцентричний підходи: успіх вимірюють не лише відсотком зниження маси тіла, а й регресом АОУЗ, покращенням симптомів і якості життя, з готовністю своєчасно ескалувати тактику, коли цього потребує клінічна картина.
Література
- Rubino F., Cummings D.E., Eckel R.H., et al. Definition and diagnostic criteria of clinical obesity. Lancet Diabetes Endocrinol. 2025; 13 (3): 221-262. doi: 10.1016/s2213-8587(24)00316-4.
- The Lancet (2025). Diagnosing clinical obesity. Available at: https://www.thelancet.com/pb-assets/Lancet/infographics/clinical-obesity/image-1736175271690.pdf.
- Nadolsky K., Garvey W.T., Agarwal M., et al. American Association of Clinical Endocrinology Consensus Statement: algorithm for the evaluation and treatment of adults with obesity / adiposity-based chronic disease – 2025 update. Endocr. Pract. 2025 Nov; 31 (11): 1351-1394. doi: 10.1016/j.eprac.2025.07.017.