Метаболічна роль і терапевтичний потенціал мікробіому
Переклала й адаптувала канд. мед. наук Тетяна Можина
Протягом останніх двох десятиліть значна увага вчених прикута до кишкової мікробіоти (КМ). Нині КМ вважається важливим модулятором фізіології організму хазяїна (ОХ), який здатний спричиняти розвиток захворювань у людей. КМ можна розглядати як ендокринний орган, що метаболізує поживні речовини раціону й виробляє численні метаболіти. Ці метаболіти можуть всмоктуватися та впливати на рецептори багатьох органів, включаючи кишківник, печінку, коричневу й білу жирову тканину, центральну нервову систему. Більшість таких важливих метаболічних захворювань (МЗ), як ожиріння, цукровий діабет (ЦД) 2 типу, серцево-судинні захворювання (ССЗ), стеатоз печінки, модулюється мікробними продуктами та метаболітами; доказові дані підтверджують важливу роль КМ у виникненні цих захворювань. У цій статті розглянуто, яким чином мікробіота з’являється в організмі під час народження, розвивається та функціонує як складна мікробна екосистема; обговорюються зміни бактеріального складу кишківника при різноманітних МЗ.
Кишкова мікробіота
Немовлята, народжені природним шляхом, колонізуються мікроорганізмами з піхви та кишківника матері при народженні, тоді як немовлята, народжені завдяки кесареву розтину, колонізуються мікроорганізмами зі шкіри та навколишнього середовища. Схема колонізації є однаковою в усіх дітей, але кінетика колонізації різниться. Вона відбувається в певній послідовності: деякі мікроби можна вважати ранніми колонізаторами, тоді як інших слід віднести до пізніх. Ранні колонізатори, включаючи рід Bifidobacterium, який є найпоширенішим до 4 місяців життя, процвітають завдяки олігосахаридам жіночого молока. Ці ранні колонізатори забезпечують розвиток невеликого середовища й таким чином створюють умови для появи більшої кількості анаеробних мікроорганізмів, чисельність яких починає швидко збільшуватися при переході дитини з грудного вигодовування до споживання твердої їжі, що сприяє значній мікробній різноманітності протягом перших 5 років життя.
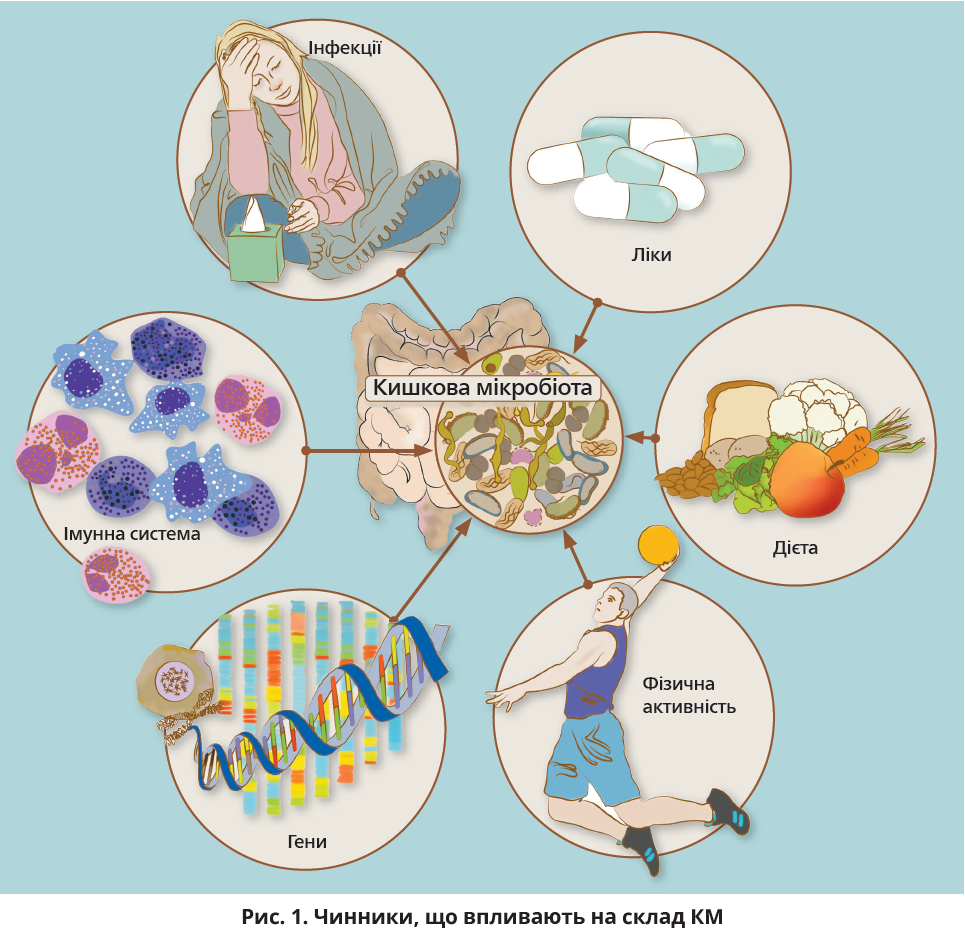
Дослідження, проведені за участю здорових осіб і в загальній популяції, демонструють, що чинники зовнішнього середовища та генетичні особливості ОХ впливають на склад КМ людини (рис. 1). Багато досліджень довели вплив дієти на склад мікробіоти. Наприклад, припинення грудного вигодовування потрібно для дозрівання дитячої мікробіоти та набуття рис, притаманних мікробіоті дорослих: збільшення кількості Bacteroides, Bilophila, Roseburia, Clostridium, Anaerostipes. У дорослих дієта впливає на склад КМ, перемикання між тваринною й рослинною дієтами зумовлює швидкі та відтворювані зміни в КМ. Ці зміни залежать від здатності мікробів метаболізувати та використовувати різні компоненти їжі для власного росту. Різні чинники, включаючи фізичну активність, імунну систему, інфекції, а також антибіотики й інші ліки, впливають на склад КМ. Окрім чинників навколишнього середовища, певну роль мають генетичні особливості хазяїна. Проте вплив генетичних характеристик хазяїна на формування КМ є, ймовірно, незначним, тоді як чинники довкілля вважають впливовішими детермінантами.
КМ не являє собою сукупність незалежних мікроорганізмів, навпаки: вона є складною мікробною екосистемою, в якій мікроорганізми комунікують, впливають один на одного, рекомбінують і коеволюціонують. Залежно від складу харчового раціону формується масив мікробних метаболітів. Це означає, що, навіть якщо дві особи мають однаковий харчовий раціон, синтезовані метаболіти можуть істотно відрізнятися залежно від індивідуального складу мікробіому. Особи із зіставною КМ, але різною харчовою поведінкою, також мають різні мікробні метаболіти. Ці метаболіти важливі для мікробної взаємодії, але вони також можуть впливати на фізіологію ОХ завдяки зв’язуванню з рецепторами.
Колонізація коменсальними мікробами та взаємодія між ними й хазяїном потрібна для здорового розвитку ОХ. Благотворний вплив КМ передбачає дозрівання імунних тканин і тонке налаштування імунної відповіді. Різноманітні мікробні метаболіти та компоненти діють локально, але також у віддалених відділах організму, модулюючи імунну функцію й інші фізіологічні процеси. Крім їхнього впливу на імунну систему, коменсальні мікроби відіграють важливу роль у запобіганні потраплянню патогенів в ОХ шляхом обмеження простору й поживних речовини, доступних для патогенів. Симбіоз «хазяїн – мікроб» також необхідний для здорового метаболізму. Мікроби синтезують вітаміни, що є надзвичайно важливим через обмежену здатність організму людини біосинтезувати більшість вітамінів. Незважаючи на наявність вітамінів у продуктах харчування, дефіцит вітамінів виникає через недоїдання або погані харчові звички. Отже, мікроорганізми виробляють вітаміни, що може бути метаболічно корисно для господаря. КМ впливає на метаболічні функції різних органів, включаючи шлунково-кишковий тракт (ШКТ), печінку, білу й коричневу жирову тканину, скелетні м’язи та мозок.
КМ чинить локальний і периферичний метаболічні впливи
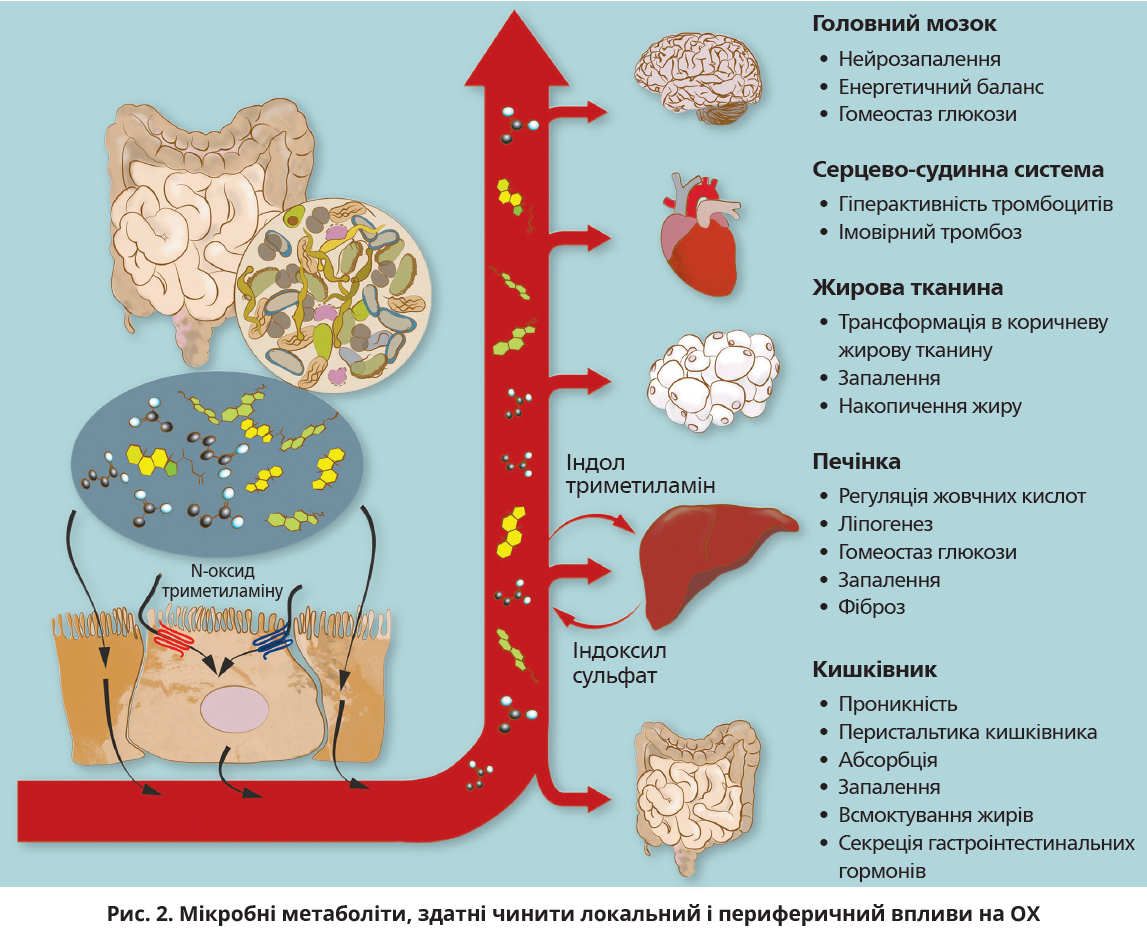
КМ чинить локальний метаболічний вплив усередині ШКТ, де вона впливає на здатність перетравлювати їжу, видобувати енергію, поглинати поживні речовини, виводити продукти обміну споживаної їжі. Функції, які модулює КМ, включають інтестинальну проникність, перистальтику кишківника та секрецію гастроінтестинальних гормонів. Однак КМ не тільки чинить локальний вплив у кишківнику (рис. 2). Мікроби синтезують численні невеликі молекули, котрі можуть впливати на фізіологію ОХ, як у кишківнику, так і в інших органах. Уміст цих метаболітів може досягати мілімолярних концентрацій і значно варіювати в окремих осіб, що свідчить про значні міжіндивідуальні варіації в метаболіт-рецепторній сигналізації. Оскільки кишківник безпосередньо пов’язаний із печінкою через ворітну вену, переважна більшість синтезованих метаболітів абсорбується в ШКТ і надходить у кровообіг через ворітну вену, даючи змогу печінці діяти як другий етап захисту від шкідливих речовин, які всмоктуються в кишківнику. Проте деякі метаболіти уникають деградації в печінці; інші метаболіти можуть бути трансформовані печінковими ферментами в біологічно активні метаболіти. Відповідно, КМ здатна чинити метаболічний вплив у інших частинах тіла завдяки мікробним метаболітам і метаболіт-індукованому вивільненню гормонів у кишківнику.
Терапевтичний потенціал мікробіому
Збільшується кількість доказів, які демонструють взаємозв’язок між КМ, її мікробними продуктами та метаболітами в розвитку МЗ, що відкриває можливість спрямованого впливу на КМ за цих захворювань. Існує кілька способів, завдяки яким можна модулювати склад і функції КМ: корекція дієти, пре-, про- та постбіотики, перенесення мікробіоти, призначення певних ліків.
Корекція дієти
Дієта є одним із найважливіших чинників навколишнього середовища, що впливає на склад мікробіому. Однак якщо короткотривалі екстремальні зміни харчування здатні швидко й істотно змінити склад мікробіому, то незначна корекція дієти призводить лише до незначних змін КМ. Згідно з результатами дослідження, різні люди по-різному реагують на зміни дієти, тому можуть потребувати персоніфікованих рекомендацій.
Трансплантація фекальної мікробіоти (ТФМ)
Іншим способом змінення КМ є перенесення фекальної мікробіоти від здорового донора до хворого реципієнта. Нині такий вид лікування схвалений лише для рецидивів інфекції Clostridium difficile у зв’язку з доведеною ефективністю. ТФМ раніше виконували шляхом дуоденальної інфузії або колоноскопії, але тепер вона може бути проведена за допомогою капсул, які містять ліофілізований кал. Вивчається також здатність ТФМ покращувати метаболічні показники. Vrieze та співавт. продемонстрували, що чутливість до інсуліну збільшується в осіб з ожирінням і метаболічним синдромом через 6 тижнів після інфузії мікробіоти від худих донорів. Натомість інфузія автологічної мікробіоти не покращувала чутливості до інсуліну. Проте, хоча таке лікування короткочасно покращувало метаболічні показники, позитивний ефект був транзиторним.
Пре-, про-, пост-, синбіотики та мікробні метаболіти
Пребіотик визначають як «субстрат, що селективно використовується мікроорганізмами ОХ, забезпечуючи користь для здоров’я». До поширених пребіотиків відносять такі ферментовані волокна, як інулін, фруктоолігосахариди та галактоолігосахариди. Ці пребіотики використовувалися в дослідженнях для визначення благотворного впливу на МЗ. Застосування інуліну або ефіру інулін-пропіонату в осіб із надмірною вагою або ожирінням сприяло зменшенню інсулінорезистентності.
Пробіотики визначають як «живі мікроорганізми, котрі при введенні в адекватній кількості сприяють здоров’ю ОХ». Незважаючи на те що Bifidobacterium (adolescentis, animalis, bifidum, reuteri, breve та longum) і Lactobacillus (acidophilus, casei, fermentum, gasseri, johnsonii, paracasei, plantarum, rhamnosus і salivarius) широко використовують як пробіотики, ні Управління з контролю продуктів харчування та лікарських засобів США (FDA), ні Європейська агенція з безпеки харчових продуктів (EFSA) не схвалили будь-якої заявки щодо пробіотиків. Декілька рандомізованих плацебо-контрольованих досліджень, проведених за участю хворих на ЦД 2 типу з переважним застосуванням штамів Lactobacillus і Bifidobacterium, і метааналізів підтверджують, що використання пробіотиків здатне покращити гомеостаз глюкози у хворих на ЦД 2 типу.
Синбіотик визначають як «суміш, що містить живі мікроорганізми та субстрати, котрі використовуються мікроорганізмами ОХ і приносять користь його здоров’ю». Лікування синбіотиками недавно досліджувалося у хворих на ЦД 2 типу. У цьому дослідженні доведено, що 12-тижневий прийом синбіотика, що містив інулін, Akkermansia muciniphila, Clostridium beijerinckii, Clostridium butyricum, Bifidobacterium infantis і Anaerobutyricum hallii, покращує метаболізм глюкози після стандартного 3-годинного тесту толерантності їжі. Застосування синбіотика асоційоване зі зміною складу фекальної мікробіоти та специфічним послідовним підвищенням рівня фекальних A. muciniphila і B. infantis.
Міжнародна наукова асоціація пробіотиків і пребіотиків (ISAPP) нещодавно визначила постбіотики як «препарати з неживими мікроорганізмами та/або їхніми компонентами, котрі є корисними для здоров’я ОХ». ISAPP стверджує, що «ефективні постбіотики мають містити інактивовані мікробні клітини або клітинні компоненти, з/без метаболітів, які сприяють спостережуваним перевагам для здоров’я». Також можна застосовувати очищені мікробні метаболіти. Окреме або комбіноване використання бутирату разом з інуліном чинить певний сприятливий вплив на активність запалення та кардіометаболічні фенотипи.
Висновки
МЗ, як-от ожиріння, ЦД 2 типу та ССЗ, являють собою гетерогенні нозології, етіологія та клінічні ознаки яких різняться в різних пацієнтів. Якщо такі особливості дієти, як західний стиль харчування або споживання великої кількості червоного м’яса, вже давно вважаються чинниками ризику кардіометаболічних захворювань, то значення та важливість КМ визнані тільки нещодавно. Ми розглядаємо КМ як ендокринний орган, що діє як фільтр, котрий мають подолати проковтнуті поживні речовини. Взаємодія «дієта – КМ» визначає, які метаболіти будуть утворюватися й абсорбуватися. Доведено, що багато ключових МЗ, включаючи інсулінорезистентність, атерогенні зміни ліпідного профілю сироватки, гіперреактивність тромбоцитів, імовірність тромбоутворенн та низькоінтенсивне запалення, модулюються мікробними продуктами й метаболітами, тобто склад КМ здатний спричиняти виникнення різних за етіологією кардіометаболічних захворювань. Різні чинники, в тому числі генетична схильність, дієта, фізична активність, куріння, стрес і склад КМ, можуть взаємодіяти та призводити до унікального профілю захворювання в кожної людини.
Література
Olofsson L.E., Bäckhed F. The metabolic role and therapeutic potential of the microbiome. Endocr. Rev. 2022 Sep 26; 43 (5): 907-926. doi: 10.1210/endrev/bnac004.
Коментар фахівця
 Анастасія Соколова
Анастасія Соколова
лікарендокринолог першої категорії, лікардієтолог, Національний медичний університет імені О.О. Богомольця, м. Київ
Для кращого розуміння теми кишкової мікробіоти та її впливу на людський організм насамперед потрібно дати визначення співзвучним термінам: мікробіота та мікробіом.
Мікробіота кишкова – це спільнота мікроорганізмів, якими заселений кишківник людини, вона включає бактерії, дріжджі та віруси. Домінувальними типами кишкових мікробів є Firmicutes, Bacteroidetes, Actinobacteria, Proteobacteria, Fusobacteria та Verrucomicrobia, з яких перші два становлять 90% мікробіоти кишківника. Тип Firmicutes складається з понад 200 різних родів, як-от Lactobacillus, Bacillus, Clostridium, Enterococcus і Ruminococcus. Саме на покращення та розростання цих родів мікроорганізмів практична медицина робить акцент.
Мікробіом – це збірне та загальне поняття, що поєднує власне мікроорганізми (мікробіоту) та їхні функціональні елементи: структурні особливості, метаболіти, сигнальні молекули й умови навколишнього середовища. Саме тому на практиці ми говоримо про конкретні види мікроорганізмів (мікробіоту), але маємо на увазі їхній вплив на організм хазяїна (тобто мікробіом).
Сьогодні наукові дослідження, спрямовані на вивчення багатовекторного впливу мікробіому на організм людини, стають дедалі глибшими та практичнішими. Є переконливі дані, які свідчать, що для хронічних метаболічних захворювань характерними є особливі співвідношення мікробіоти кишківника. Мікробні метаболіти здатні чинити локальний і периферичний впливи на організм людини. Тому такі хвороби, як ожиріння, цукровий діабет 2 типу, стеатогепатоз, мають у своєму патогенезі додаткову складову – мікробіом.
Наукові дослідження в цій галузі покликані звернути увагу на важливість модифікації мікробіоти кишківника як складової ефективного лікування метаболічних захворювань.
В арсеналі лікаря-практика є такі інструменти: модифікація харчування та харчових звичок, раціональне призначення антибіотикотерапії, оптимізація медикаментозного лікування, просвітницька діяльність щодо впливу шкідливих звичок на мікробіоту кишківника, застосування пре-, про- та постбіотиків.
У харчуванні важливо звернути увагу на кількість клітковини в раціоні, передусім зелених листових овочів; обмеження простих цукрів та їх заміну на продукти із цільного зерна; вживання кисломолочних продуктів; збагачення раціону моно- та поліненасиченими жирними кислотами. Для людей із цукровим діабетом 2 типу рекомендована кількість клітковини становить 14 г на кожні 1000 кКал. Важливим є тривале дотримання збалансованого харчування задля позитивно функціонального та стабільного мікробіому.
Незважаючи на те що пре-, про- та постбіотики у вигляді медикаментозних таблетованих препаратів дають швидкий ефект, без регулярного збалансованого та різноманітного раціону цей ефект не буде тривалим. Наразі проводяться дослідження для вивчення пробіотичних препаратів як додаткової ланки лікування ожиріння та цукрового діабету 2 типу, але конкретних кроків у алгоритмі лікування ще не має.
Отже, вплив на мікробіом кишківника є безпечним і потенційно ефективним кроком у компенсації хронічних метаболічних захворювань. Корекція всіх ланок здорового способу життя є базовою потребою для ефективного впливу на мікробіом.
