Механомедицина скелетних м’язів як новітній напрям у діагностиці та терапії інсулінорезистентності
Підготувала Ганна Гаврюшенко
Інсулінорезистентність (ІР) характеризується хронічно підвищеним рівнем інсуліну, необхідним для підтримання нормоглікемії, та відіграє ключову роль у розвитку метаболічних порушень, у тому числі цукрового діабету 2-го типу, неалкогольної жирової хвороби печінки й саркопенії. Оскільки скелетні м’язи забезпечують близько 80% інсулінозалежного поглинання глюкози, саме вони є основним периферичним локусом ІР і важливою мішенню для діагностики та терапії ІР. Відповідно, поліпшення функції скелетних м’язів має значний потенціал для зменшення ІР і пов’язаних з нею метаболічних ускладнень.
Традиційні дослідження ІР у скелетних м’язах зосереджувалися переважно на біохімічних механізмах, зокрема порушеннях інсулінового сигналінгу, запаленні та змінах ліпідного обміну. Однак останніми роками зростає інтерес до механосенситивних характеристик м’язової тканини, що відкриває нові перспективи в галузі механомедицини. Цей матеріал узагальнює сучасні уявлення про біомеханічні й механобіологічні зміни скелетних м’язів при ІР, а також розглядає наявні та перспективні механомедичні стратегії, спрямовані на діагностику й лікування ІР.
Біомеханіка та механобіологія жорсткості скелетних м’язів при ІР
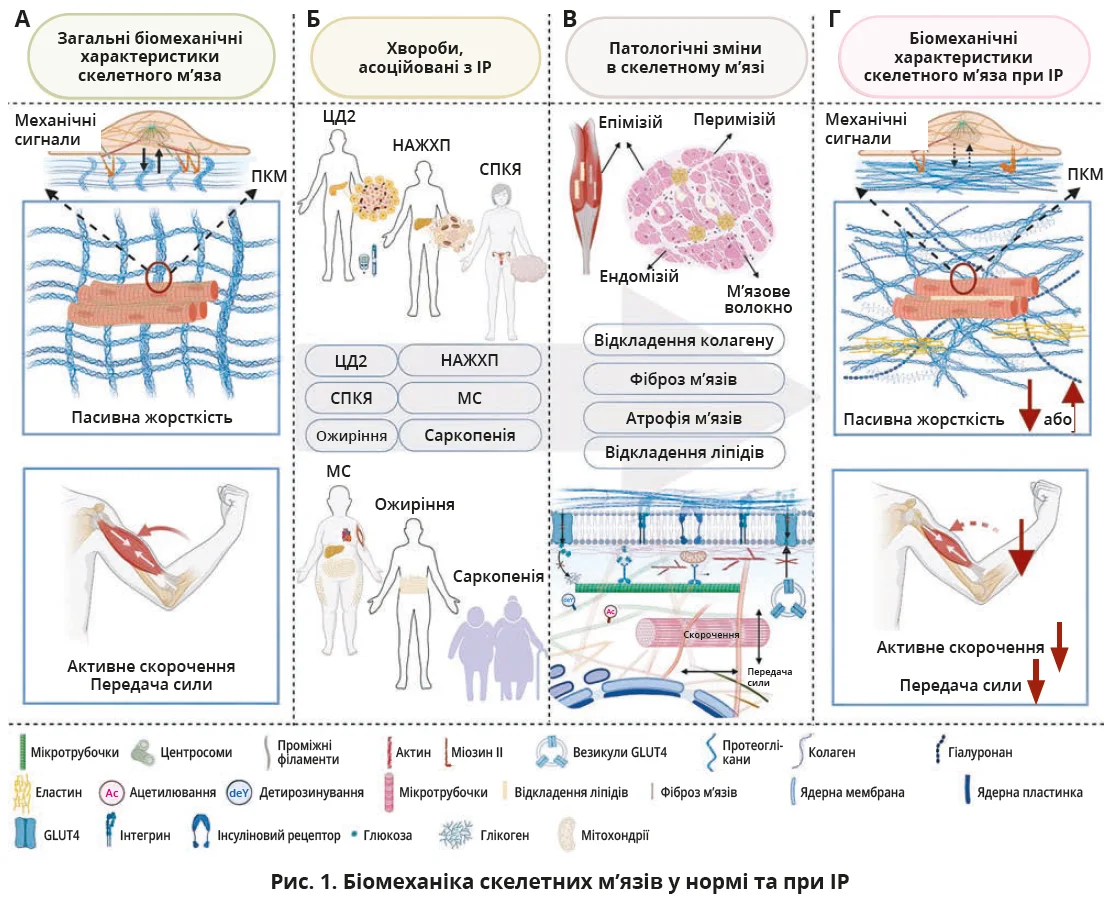
Біомеханічні зміни жорсткості скелетних м’язів при ІР відображають патологічні процеси на органному, тканинному та клітинному рівнях і тісно пов’язані з порушеннями механобіології м’язів (рис. 1). На органному рівні на жорсткість впливають жирова інфільтрація, набряки, втрата м’язової маси та зниження фізичної активності. Більшість досліджень свідчать про зниження м’язової жорсткості в пацієнтів із цукровим діабетом 2-го типу, особливо за наявності ускладнень, тоді як цироз печінки часто супроводжується її підвищенням.
Примітки. МС – метаболічний синдром; НАЖХП – неалкогольна жирова хвороба печінки; СПКЯ – синдром полікістозних яєчників; ЦД2 – цукровий діабет 2-го типу. А. Біомеханіка скелетних м’язів у нормальних фізіологічних умовах. Б. Хвороби, асоційовані з ІР скелетних м’язів. В. Патологічні зміни в скелетних м’язах з ІР. На тканинному рівні ці зміни охоплюють відкладення колагену, фіброз, атрофію та відкладення ліпідів, а на клітинному рівні – детирозинування й ацетилювання цитоскелета, утворення розгалуженого F-актину, інактивацію інтегрину та зменшення транслокації GLUT4 до плазматичної мембрани. Г. Зміни в біомеханічних сигналах скелетних м’язів при ІР, включно зі зміненою жорсткістю та зниженою скоротливістю.
На тканинному рівні жорсткість м’язів визначається переважно позаклітинним матриксом (ПКМ), який зазнає патологічної перебудови внаслідок ІР. Надмірне відкладення колагену, накопичення ліпідів, фіброз, хронічне запалення й утворення кінцевих продуктів глікації підвищують жорсткість ПКМ і порушують нормальну архітектоніку м’язів, формуючи змінене механічне середовище для м’язових клітин.
На клітинному рівні ІР асоціюється з підвищеною жорсткістю міоцитів, зумовленою перебудовою цитоскелета. Ущільнення актинової сітки та зміни мікротрубочок обмежують транспортування глюкозних транспортерів (GLUT) до плазматичної мембрани та знижують поглинання глюкози міоцитами. Реакція клітин на зміни позаклітинної жорсткості опосередкована механотрансдукційними шляхами за участю інтегринів і фокальних сайтів адгезії, які поєднують ПКМ із цитоскелетом і регулюють структурні й метаболічні сигнали.
Зміни жорсткості також впливають на мітохондрії та клітинне ядро. Механічні сигнали, що передаються через цитоскелет, регулюють мітохондріальну динаміку й енергетичний обмін, тоді як надмірна чи аномальна жорсткість порушує внутрішньоклітинний транспорт і знижує чутливість до інсуліну. Передача механічної сили до ядра через зв’язки між цитоскелетом і ядерними структурами призводить до змін жорсткості й організації ядра, що порушує експресію генів, спричиняє запалення та посилює метаболічну дисфункцію. Отже, порушена механічна сигналізація від ПКМ до цитоскелета, мітохондрій і ядра є ключовим чинником ІР скелетних м’язів і перспективною терапевтичною мішенню.
Біомеханіка та механобіологія активного скорочення скелетних м’язів при ІР
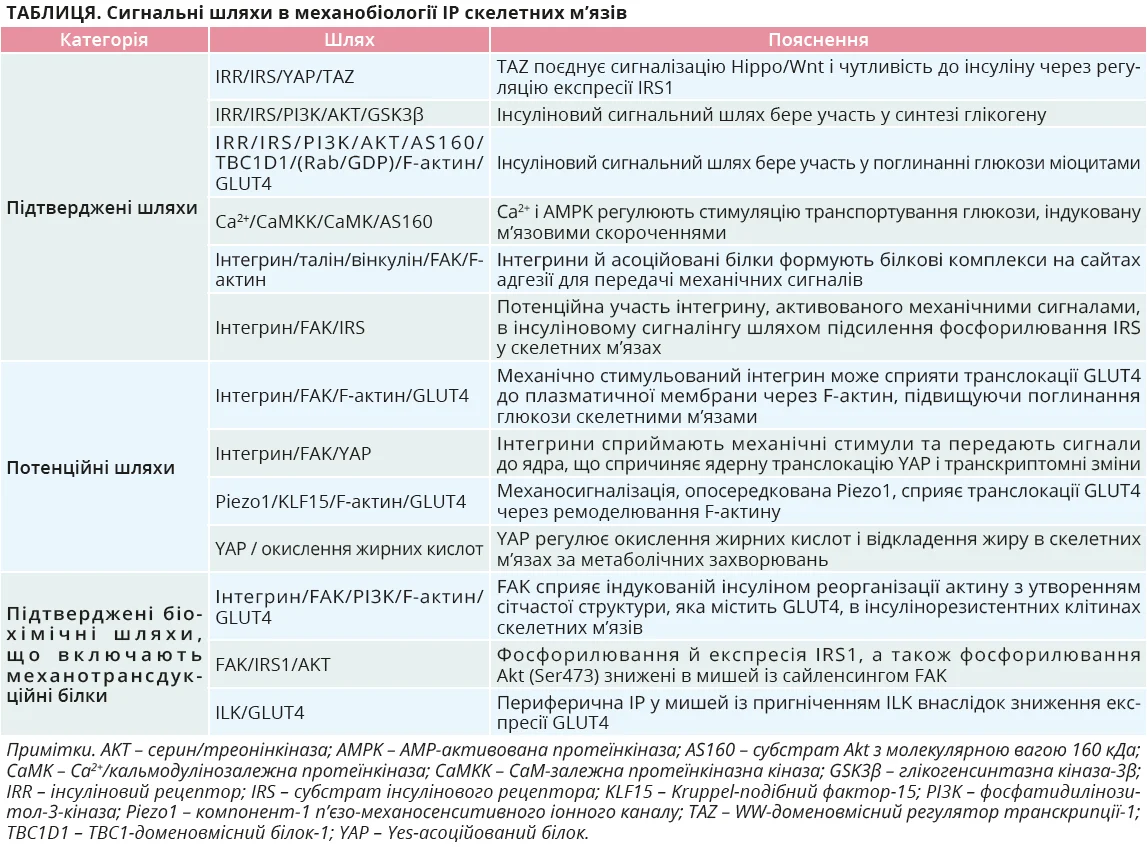
Активне скорочення скелетних м’язів тісно пов’язане з метаболізмом глюкози й істотно порушується при ІР (табл.). У здоровому м’язі сила скорочення генерується взаємодією актину та міозину й передається через цитоскелет до клітинної мембрани та ПКМ, забезпечуючи координацію між скороченням і поглинанням глюкози. За умов ІР м’язові волокна оточені патологічно ремодельованим матриксом з надлишком колагену та жировою інфільтрацією, що порушує цілісність волокон, послаблює генерацію сили та погіршує її передачу. Це призводить до зниження скоротливої здатності м’язів, що стабільно підтверджується дослідженнями in vivo й ex vivo.
У нормі активне скорочення стимулює поглинання глюкози через кальціє- й AMPK-залежні сигнальні шляхи, які забезпечують транслокацію GLUT4 незалежно від інсуліну. Порушення кальцієвого гомеостазу в інсулінорезистентних м’язах послаблює скорочення та знижує інсулінонезалежне поглинання глюкози. Механічні сигнали з ПКМ передаються в клітини через механочутливі адгезійні комплекси, насамперед інтегрини, які координують структурну та метаболічну сигналізацію. Зміни інтегринових шляхів разом зі зниженою активністю інтегрин-асоційованої кінази (ILK) і фокально-адгезійної кінази (FAK) порушують організацію цитоскелета, функцію мітохондрій та інсулінову сигналізацію, що призводить до подальшого погіршення метаболізму глюкози.
Інші механочутливі механізми, зокрема іонні канали Piezo1 і транскрипційні регулятори YAP і TAZ, є посередниками між механічним навантаженням і надходженням у клітину кальцію, регуляцією генів і метаболічною адаптацією. Враховуючи вищезазначене, можна зробити висновок, що ІР водночас є причиною та наслідком дефектного м’язового скорочення й порушень механотрансдукції. Ослаблення генерації та передачі сили й аномальна механочутлива сигналізація формують хибне коло, що спричиняє прогресування метаболічної дисфункції.
Механодіагностика ІР скелетних м’язів
Механодіагностика ІР скелетних м’язів є обмеженою, оскільки надійне вимірювання механічних змін у живій м’язовій тканині є технічно складним. Традиційні методи, як-от атомно-силова мікроскопія, забезпечують високу точність оцінювання жорсткості, проте використовують м’язові біоптати та відображають властивості лише невеликих локальних ділянок, що значно обмежує їх клінічне застосування. Натомість неінвазивні методи візуалізації, як-от ультразвукова еластографія зсувних хвиль і магнітно-резонансна томографія (МРТ), дають змогу оцінювати жорсткість скелетних м’язів in vivo й уже застосовуються в клінічних дослідженнях осіб з ІР. Наприклад, ультразвукова еластографія демонструє чіткі відмінності в жорсткості м’язів між інсулінорезистентними пацієнтами та здоровими особами, що робить її перспективним інструментом діагностики. МРТ надає додаткову інформацію, особливо щодо глибоких м’язових груп, однак її результативність сильно залежить від протоколів сканування та методів інтерпретації. Розроблення й упровадження уніфікованих протоколів для ультразвукової еластографії та МРТ істотно підвищать відтворюваність і клінічну цінність оцінювання жорсткості м’язів, що сприятиме використанню цих методів для діагностики та контролю перебігу ІР.
Перспективні методи механодіагностики відкривають можливості для більш раннього й точного виявлення ІР шляхом фіксації біомеханічних змін, пов’язаних з метаболічними порушеннями. Оптоакустична мезоскопія забезпечує глибоке високороздільне зображення м’язової тканини й дає змогу виявляти атрофію м’язів і накопичення колагену внаслідок ІР. Використання штучного інтелекту (ШІ) може розширити можливості механодіагностики, інтегруючи й аналізуючи дані ультразвукової еластографії, МРТ й інших методів, підвищуючи точність діагностики та прогнозування ризиків. Окрім того, поєднання алгоритмів ШІ з використанням імплантованих сенсорів або інтелектуальних біоматеріалів відкриває можливості безперервного моніторингу механічних властивостей м’язів у реальному часі. Натільні пристрої для неінвазивного оцінювання жорсткості та скоротливості м’язів також є перспективним інструментом раннього виявлення й довготривалого спостереження при ІР.
Механотерапія ІР скелетних м’язів
Механотерапевтичні методи використовуються для корекції ІР шляхом впливу на механічні чинники, що регулюють метаболізм м’язів. Основні підходи механотерапії спрямовані на зменшення жорсткості ПКМ, відновлення механочутливої сигналізації та посилення зв’язку між м’язовим скороченням і утилізацією глюкози. Ці стратегії охоплюють як системні втручання, зокрема фізичні вправи, так і клітинні та молекулярні методи лікування.
Фізична активність є базовим елементом механотерапії. Аеробні та силові тренування знижують надлишкове відкладення колагену, ліпідів і рівень запалення в м’язах, водночас відновлюючи скоротливу здатність і регулюючи кальцієвий обмін. Пасивне розтягнення також здатне покращувати чутливість до інсуліну та підвищувати поглинання глюкози завдяки механічній стимуляції м’язової тканини навіть без активних рухів. Пристрої, що імітують фізичні вправи, зокрема вібраційні платформи або апарати для допоміжних рухів і симуляції вправ, можуть покращувати регуляцію жорсткості м’язів і глікемічний контроль, особливо в осіб з обмеженою рухливістю.
Різноманітні стратегії, спрямовані на зниження маси тіла, істотно впливають на механобіологію м’язів і чутливість до інсуліну. Корекція дієти, баріатрична хірургія, фармакотерапія та фізичні вправи зменшують жирову інфільтрацію й запалення, покращують інсулінову чутливість, сприяють ремоделюванню ПКМ і відновленню скоротливої функції м’язів. Препарати для зниження маси тіла, зокрема агоністи рецепторів глюкагоноподібного пептиду-1, зменшують накопичення ліпідів у м’язах і покращують чутливість до інсуліну. Важливо поєднувати дієтичні, баріатричні та фармакотерапевтичні підходи з фізичними навантаженнями, зокрема силовими тренуваннями, оскільки істотне обмеження надходження калорій і нутрієнтів негативно впливає на м’язову масу та силу.
На молекулярному рівні перспективні підходи спрямовані на модифікацію м’язової жорсткості та механочутливих сигнальних шляхів, що сприяє поліпшенню метаболічного здоров’я. Вивчаються групи препаратів, що здатні зменшити накопичення колагену та жорсткість ПКМ, а також покращують сигналінг і функцію механочутливих білків (зокрема, інтегринів), підсилюють поглинання глюкози міоцитами. Фармакоміметики фізичних навантажень і ультразвукова терапія мікровезикулами з адипонектином демонструють багатонадійні результати, однак для їх повноцінного клінічного впровадження потрібне глибше розуміння механобіології м’язів.
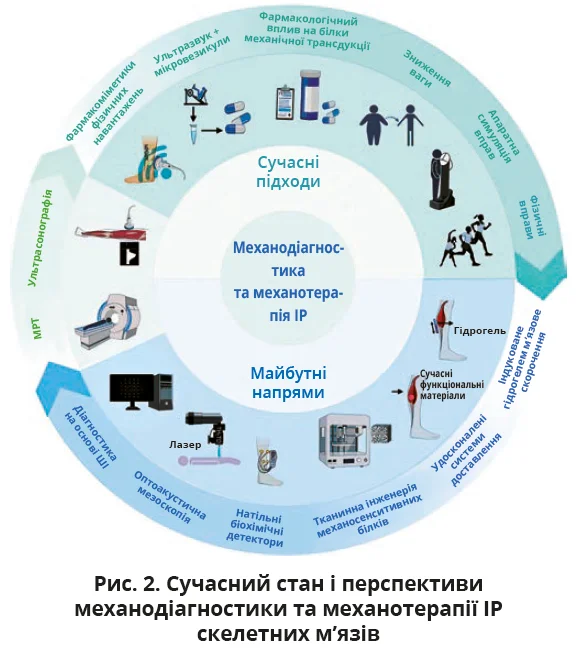
Перспективні механотерапевтичні стратегії орієнтовані на безпосередню модифікацію біомеханіки та механобіології м’язів для підвищення чутливості до інсуліну. Гідрогелеві імпланти можуть забезпечувати контрольоване розтягування або скорочення м’язів відповідно до механічних властивостей здорової тканини. Крім того, такі системи здатні локально доставляти препарати для зменшення фіброзу й жирового відкладення в м’язах. До інших інноваційних підходів належать робототехнічні системи для механічної стимуляції м’язів, а також тканинна інженерія м’язів для посилення механосенситивної сигналізації та потенційного відновлення чутливості до інсуліну. Огляд наявних і перспективних методів механодіагностики та механотерапії ІР скелетних м’язів представлено на рисунку 2.
Зверху представлено сучасні методи механотерапії ІР скелетних м’язів, як-от фізичні вправи, апаратна імітація фізичних вправ, препарати, що впливають на механосенситивні білки, фармакоміметики фізичних навантажень і терапія мікровезикулами за допомогою ультразвуку. Методи механодіагностики, як-от ультрасонографія та МРТ, показані зліва. У нижній частині представлено перспективні підходи, що включають гідрогелеві системи доставлення активних речовин, оптоакустичну мезоскопію, натільні біохімічні детектори, тканинну інженерію для підсилення активності механосенситивних рецепторів і механотерапевтичні та діагностичні методи на основі ШІ.
Висновки
З біомеханічного погляду ІР супроводжується змінами жорсткості м’язів, зниженням сили та порушенням її передачі під час м’язового скорочення. Модифікація жорсткості ПКМ впливає на механочутливі рецептори, зокрема інтегрини, змінюючи метаболізм глюкози, структуру ядра та регуляцію генів. Зниження скоротливої сили й ефективності механічної сигналізації тісно пов’язані з порушенням утилізації глюкози, що підкреслює тісний зв’язок між механікою м’язів і метаболічною дисфункцією при ІР.
Розвиток механомедицини відкриває нові можливості як для діагностики, так і для терапії ІР скелетних м’язів, даючи змогу оцінювати та модулювати стан тканин на підставі їхніх біомеханічних і механобіологічних характеристик. Використання методів візуалізації, як-от ультразвукова еластографія та МРТ, у поєднанні з дієтотерапією, фізичними вправами й іншими механічними та фармакологічними втручаннями являє собою принципово новий і перспективний підхід до діагностики й лікування ІР і асоційованих з нею метаболічних порушень.
Література
Wang L., Chang L., Ma Y., et al. Mechanomedicine for addressing skeletal muscle insulin resistance. Endocrine Reviews. 2025 Oct; 46 (5): 652-669. doi: 10.1210/endrev/bnaf012.