Конгрес Європейської асоціації з вивчення діабету (2022)
Підготувала канд. мед. наук Лариса Стрільчук
Цьогорічний конгрес Європейської асоціації з вивчення діабету відбувся 19-23 вересня в гібридному форматі; очна частина проходила в Стокгольмі (Швеція). У заході взяли участь близько 20 тисяч учасників зі 130 країн. У ході роботи конгресу учасники мали змогу прослухати виступи спікерів, які стосувалися різноманітних теоретичних і практичних аспектів діагностики, лікування та профілактики цукрового діабету (ЦД), а також інновацій у галузі діабетології. У цьому матеріалі коротко подано вибрані матеріали конгресу практичної спрямованості.
Інтенсивна глюкозознижувальна терапія та поліпрагмазія в осіб похилого віку із ЦД 2 типу (B. Bongaerts і співавт.)
В осіб похилого віку ЦД 2 типу є дуже поширеним. Цей контингент є вразливішим до гіпоглікемій, причому тяжкі гіпоглікемії можуть призводити до падінь і переломів, кардіоваскулярних подій, погіршення когнітивної функції. Відповідно до рекомендацій Американської діабетологічної асоціації (2022), особи похилого віку потребують індивідуалізованого підходу до цільових показників і лікування залежно
від загального стану здоров’я (табл.).
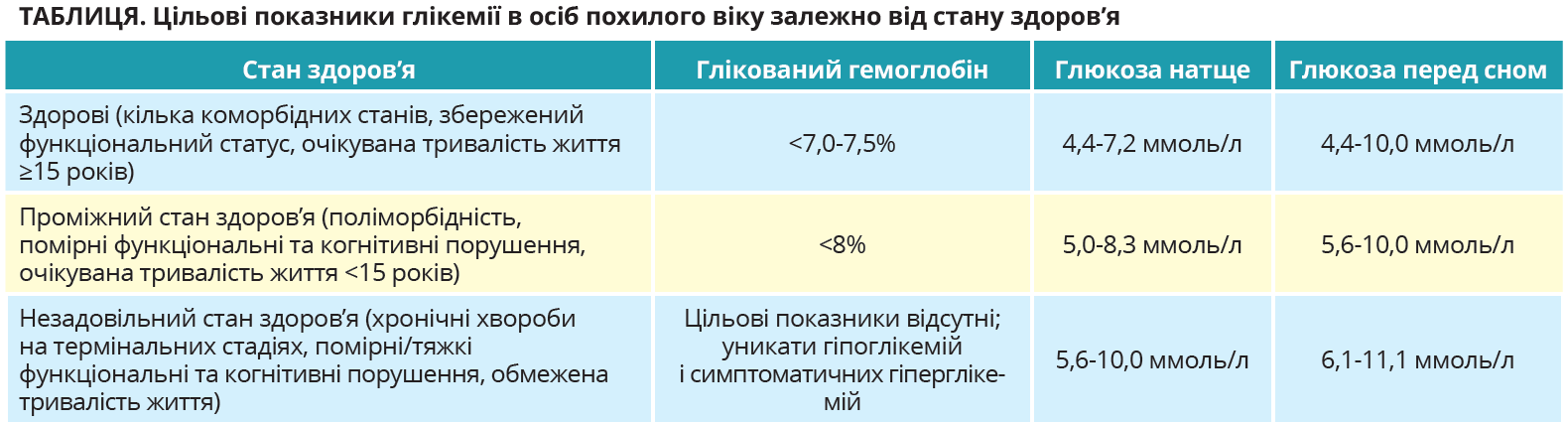
Незважаючи на ці рекомендації, в осіб похилого віку із ЦД 2 типу часто спостерігається надмірне лікування. Зокрема, вивчення даних понад 100 тисяч пацієнтів віком ≥75 років показало, що в 61% було застосовано інтенсивний глікемічний контроль із цільовим показником глікованого гемоглобіну (HbA1c) ≤7,0% (Lega I.C. et al., 2021). Подібні дані було отримано й іншими авторами. Отже, можна сказати, що такі хворі потребують деінтенсифікації лікування, тобто його деескалації внаслідок скасування препаратів, зменшення доз, заміни потужніших препаратів на менш потужні. Метою цього є покращення наслідків лікування для пацієнта й уникнення поліпрагмазії.
Як показують опитування, більшість лікарів (близько 80%) погоджуються з концепцією індивідуальних цільових показників HbA1c, однак реально практикують це близько 68%. Ситуація утруднюється ще й тим, що рекомендації зазвичай акцентують на інтенсифікації, а не на деінтенсифікації, яка, втім, є дуже важливою для пацієнтів похилого віку. Відповідно до огляду M.P. Oktora та співавт. (2021), деескалація є успішною в 57-100% випадків: рівні HbA1c зростають мінімально, а частота гіпоглікемій, особливо небезпечних для цього контингенту хворих, знижується. За даними іншого систематичного огляду, повне скасування, припинення або деінтенсифікація терапії не призводять до збільшення HbA1c, підвищення частоти госпіталізацій і мікроваскулярних подій, але покращують якість життя (Seidu S. et al., 2019).
Висновок: надмірне лікування є частим явищем у терапії ЦД 2 типу в осіб похилого віку. Надмірне лікування підвищує ризик розвитку гіпоглікемій та їхніх несприятливих наслідків, але деінтенсифікація терапії залишається малопоширеним явищем у клінічній практиці. За даними досліджень, деінтенсифікація не лише не призводить до різкого зростання HbA1c, а й має низку сприятливих наслідків.
Харчування та патерни дієти в пацієнтів із ЦД (J. Sievenpiper і співавт.)
На ранніх етапах розвитку дієтології провідну позицію в цій науці посідали редукціоністські погляди, які були дещо обмеженими і примітивними та ґрунтувалися переважно на знаннях щодо вітамінодефіцитів.
Натомість у наш час у фокусі перебувають раціони й харчові звички загалом. Значна увага приділяється також окремим групам продуктів. Наприклад, метааналіз 6 досліджень і 28 когорт пацієнтів виявив, що вживання бобових зменшує кількість кардіометаболічних подій, сприяючи зниженню HbA1c на 0,5%, холестерину ліпопротеїнів низької щільності (ХС ЛПНЩ) – на 5%, маси тіла – на 0,5 кг, систолічного артеріального тиску – на 2 мм рт. ст. (Viguiliouk Е. et al., 2018).
Однією з найвивченіших терапевтичних дієт є середземноморська, вперше описана в 1960-х рр.
В основі цієї дієти лежать такі принципи: високий рівень споживання овочів, фруктів, бобових, горіхів, насіння, цільнозернових продуктів; уживання оливкової олії як основного джерела жирів; незначне/помірне споживання молочних продуктів, риби та птиці; низький рівень споживання червоного м’яса; незначне/помірне споживання червоного вина, переважно під час їди. За даними дослідження PREDIMED, середземноморська дієта в поєднанні з 30 г горіхів на день дає змогу зменшити кількість кардіоваскулярних подій (Estruch et al., 2018). Великий метааналіз показав, що середземноморський патерн раціону асоціюється зі зниженням смертності від серцево-судинних захворювань (ССЗ) на 33%, смертності від ішемічної хвороби серця – на 67%, інсульту – на 42%, інфарктів міокарда – на 35% (Beсerra-Tomas et al., 2020).
Концепції середземноморської та DASH-дієти, спрямованої на зниження артеріального тиску, відповідає й нордична (дієта Балтійського моря). Їй властиві високий рівень споживання цільнозернових продуктів (передусім із жита, ячменю та вівса), ягід, фруктів кліматичних зон із помірним кліматом (яблук, груш), овочів, бобових, жирної риби, горіхів і знежирених молочних продуктів. Нордичний патерн раціону також дає змогу покращити кардіометаболічний статус пацієнта (Massara et al., 2022). Ще однією дієтою, заснованою переважно на рослинних продуктах, є дієта портфоліо, яка передбачає вживання 45 г горіхів, 20 г клітковини (вівсянка, ячмінь, псиліум, баклажани, фрукти кліматичних зон із помірним кліматом), 45 г рослинного білка (соя, бобові) та до 2 г рослинних стеролів (маргарин, олія) на добу. Дієта портфоліо вже через 1-6 місяців дає можливість знизити рівень ХС ЛПНЩ приблизно на 27%, причому зниження продемонстровано і для осіб із ЦД.
Висновок: як і запропоновано в концепціях трьох описаних вище дієт, пацієнтам із ЦД рекомендовано вживати мінімально оброблені цільнозернові продукти, овочі, фрукти, бобові, горіхи й насіння. Ці продукти дають змогу покращити контроль глікемії, зменшити кардіоваскулярні чинники ризику, знизити ймовірність розвитку ССЗ. Глікемічний контроль можна також покращити за допомогою вегетаріанської дієти.
Механізм дії емпагліфлозину в пацієнтів із ЦД 2 типу та серцевою недостатністю (A. Elrakaybi та співавт.)
ЦД є чинником ризику серцевої недостатності (СН), яка за умови діабету трапляється вдвічі частіше, ніж у нормоглікемічних осіб. У пацієнтів із ЦД 2 типу та СН прогноз є гіршим, а смертність від ССЗ – вищою. Показано, що інгібітори натрійзалежного котранспортера глюкози 2 типу (іНЗКТГ-2) зменшують частоту госпіталізацій із приводу СН і кардіоваскулярну смертність незалежно від наявності діабету (Crabtree, Ryder, 2021).
Запропоновано кілька основних механізмів, які можуть пояснювати цей феномен. Ці механізми можна поділити на 4 основні групи: зменшення активності ренін-ангіотензин-альдостеронової
системи, пригнічення симпатичної нервової системи, зменшення запалення, зниження окисного стресу. За даними досліджень EFFORT-1 та EFFORT-2, емпагліфлозин покращував параметри серця при його ремоделюванні незалежно від фракції викиду (зменшував товщину задньої стінки лівого шлуночка та його кінцеводіастолічний розмір) і знижував уміст KIM-1 – маркера тубулярного ушкодження нирок. Протизапальних ефектів емпагліфлозину виявлено не було.
Висновок: іНЗГКТ-2 можуть запобігати розвитку СН завдяки протидії несприятливому ремоделюванню серця. Позитивний ефект іНЗГКТ-2 не залежить від наявності ЦД.
Кардіометаболічне та психічне здоров’я в жінок із раннім гестаційним діабетом: проспективне когортне дослідження (J. Puder і співавт.)
Американська діабетологічна асоціація рекомендує проводити скринінг гестаційного діабету (ГД) у терміні 24-28 тижнів вагітності. У 15-70% жінок із ГД іще до встановлення діагнозу відзначається гіперглікемія.
Консенсус щодо скринінгу та діагностичних критеріїв раннього ГД дотепер відсутній: різні фахові організації й автори пропонують різні терміни обстеження (переважно застосовується <20 тижнів гестації) та різні порогові значення глікемії. За даними 13 когортних досліджень, ранній ГД супроводжується більш несприятливими перинатальними наслідками, ніж класичний. Раннє виявлення ГД дає можливість раннього втручання та створює додаткове терапевтичне вікно перед пологами, однак існує певний ризик гіпердіагностики та надмірного лікування.
Порівняння груп раннього та класичного ГД показало, що за умови раннього ГД відзначається достовірно більша ймовірність народження плодів, занадто великих для гестаційного віку. У жінок із раннім ГД спостерігалися на 2 кг менший набір маси при вагітності, але більша потреба в інсуліні. Крім того, пацієнток із раннім ГД відрізняли більш атерогенний ліпідний профіль і вища частота розвитку ЦД після вагітності.
Висновок: у жінок із раннім ГД спостерігається більша поширеність несприятливих кардіометаболічних наслідків. Відмінностей у психічному здоров’ї між групами раннього та класичного ГД виявлено не було.
Комбінація езетимібу та статину в лікуванні неалкогольної жирової хвороби печінки: рандомізоване контрольоване дослідження ESSENTIAL (Y. Kim і співавт.)
Неалкогольна жирова хвороба печінки (НАЖХП), яка є загальносвітовою проблемою, підвищує ризик серцево-судинних ускладнень і смертність від усіх причин. Переваги застосування статинів при НАЖХП досить обмежені, що зумовлює потребу в пошуку нових засобів для лікування цієї хвороби.
Існують дані, що езетиміб здатен зменшувати вміст вісцерального жиру та вираженість неалкогольного стеатогепатиту в експериментальних моделях. За даними авторського дослідження (Корея), поєднання езетимібу та розувастатину дало змогу достовірно зменшити стеатоз печінки в осіб із НАЖХП. На комбіновану терапію добре відповідали особи з вищим індексом маси тіла, ЦД 2 типу, інсулінорезистентністю й тяжким фіброзом печінки.
Висновок: поєднання езетимібу й розувастатину є безпечним і ефективним методом лікування пацієнтів із НАЖХП та дисліпідемією.
Ефективність метформіну в запобіганні прогресуванню предіабету до діабету (L. Zhang і співавт.)
Метформін має найпотужнішу доказову базу щодо профілактики переходу порушення толерантності до глюкози (ПТГ) у клінічно виражений ЦД. У авторському дослідженні взяли участь 1706 осіб із ПТГ, яких було рандомізовано в групи модифікації способу життя та модифікації способу життя в поєднанні з метформіном. У другій групі ПТГ прогресували до діабету достовірно пізніше, крім того, відзначалося вираженіше зниження маси тіла (на 2,43±0,28 кг порівняно з 1,40±0,27 кг у групі модифікації способу життя без фармакотерапії).
Висновок: додавання метформіну до модифікації способу життя зменшує ймовірність прогресування ПТГ до ЦД.
Застосування ІНЗКТГ-2 й арГПП-1 асоціюється з нижчою смертністю в молодих осіб із ЦД 2 типу та першим інфарктом міокарда (дані за період 2016-2020 рр.) (M. Londahl і співавт.)
У пацієнтів із ЦД 2 типу спостерігаються вищі показники смертності від усіх причин, хоча порівняно з 1998-2003 рр. спостерігається певний спад смертності й у осіб із ЦД, й у осіб із нормальною толерантністю до глюкози.
Нові класи глюкозознижувальних препаратів – іНЗКТГ-2-2 й агоністи рецепторів глюкагоноподібного пептиду-1 (арГПП-1), які доведено покращують виживаність (дослідження EMPA-REG, LEADER), –
мають деякі відмінності за своїми ефектами. Наприклад, арГПП-1 забезпечують вираженіше зниження HbA1c та маси тіла й можуть призначатися за швидкості клубочкової фільтрації (ШКФ) до 15 мл/хв,
але є дорожчими, натомість іНЗКТГ-2 забезпечують помірне зниження HbA1c та маси тіла, можуть призначатися за ШКФ ≥45 мл/хв, але є доступнішими за ціною.
Аналіз Шведської національної медичної бази даних дав змогу включити до популяції дослідження 9722 особи віком 40-69 років із ЦД 2 типу й інфарктом (-ами) міокарда, причому перший інфаркт було перенесено у 2016-2020 рр. Виявилося, що прийом арГПП-1 та іНЗКТГ-2 достовірно зменшував 5-річну смертність (відношення ризиків 0,57 та 0,37 відповідно, обидва р<0,0001). Натомість із підвищеною смертністю асоціювалися ниркова та серцева недостатність, хвороба периферичних артерій, інсульти в анамнезі. Кумулятивна смертність за умови прийому засобів будь-якого/обох нових класів глюкозознижувальних препаратів (арГПП-1, іНЗКТГ-2) становила 5,5%, а в пацієнтів, які їх не приймали, – 13%.
Висновок: арГПП-1 та іНЗКТГ-2 сприятливо впливають на виживаність пацієнтів із ЦД 2 типу й інфарктом міокарда. Незважаючи на доказову базу із цього питання, що охоплює низку досліджень починаючи з 2015 р., частка осіб із ЦД 2 типу молодше 70 років є недостатньою (49%).
Лікування гіперглікемії при ЦД 2 типу: консенсус Американської діабетологічної асоціації та Європейської асоціації з вивчення діабету (M.J. Davies, P. Rossing, B. Collins і співавт.)
Для контролю глікемії застосовуються три основні групи методів: поведінкові підходи, фармакотерапія та метаболічна хірургія. Велике значення в лікуванні діабету має нормалізація маси тіла. За даними дослідження DiRect, схуднення на 10 кг протягом 2 років спостереження забезпечувало ремісію діабету в 64% випадків.
Великий акцент у фармакотерапії припадає на нові групи препаратів. Наприклад, у осіб зі встановленим діагнозом ССЗ для зниження ймовірності значущих кардіоваскулярних подій мають застосовуватися арГПП-1 із доведеними перевагами або для зниження ймовірності значущих кардіоваскулярних подій і розвитку СН – іНЗКТГ-2 з доведеними перевагами. Аналогічна тактика застосовується для осіб без встановленого діагнозу ССЗ, але з численними факторами кардіоваскулярного ризику (вік ≥55 років, ожиріння, артеріальна гіпертензія, куріння, дисліпідемія, альбумінурія). Слід зазначити, що в осіб
із СН, хронічною хворобою нирок, встановленим діагнозом ССЗ або численними факторами ризику ССЗ рішення призначити арГПП-1 чи іНЗКТГ-2 з доведеними перевагами не має залежати від фонового застосування метформіну чи вихідного рівня HbA1c.
Висновок: лікування хворих на ЦД 2 типу має бути пацієнтоцентрованим і проводитися мультидисциплінарною командою з активним залученням до цього процесу самого пацієнта. Важливе значення має застосування нових класів препаратів (арГПП-1, іНЗКТГ-2).
