Інновації в лікуванні діабетичних виразок: сучасні біоматеріали, біосенсори та смарт-системи
Підготувала канд. мед. наук Тетяна Можина
Цукровий діабет (ЦД) давно вийшов за межі суто метаболічної проблеми: через значну поширеність з ним регулярно стикаються лікарі різних спеціальностей, а його ускладнення визначають прогноз та якість життя пацієнта. При неконтрольованому перебігу ЦД порушення мікро- та макроциркуляції, нейропатія, імунна дисрегуляція впливають не лише на внутрішні органи, а й на периферичні тканини, створюючи умови для розвитку діабетичних виразок на нижніх кінцівках (ДВНК).
Саме ДВНК становлять істотну частку тягаря ускладнень: за даними літератури, з ними протягом життя стикається майже 7% хворих на ЦД 1-го та 2-го типів [11]. ДВНК істотно погіршують якість життя й асоціюються із частими та тривалими госпіталізаціями внаслідок інфікування, розвитку гангрени, необхідністю виконання ампутації [6] та збільшенням ризику смерті [8]. На практиці ведення таких пацієнтів залишається складним: рани часто загоюються повільно, рівень глікемії може бути далеким від цільового, а локальне мікросередовище виразки підтримує хронічне запалення й персистенцію інфекції.
Усе це сприяє стрімкій появі інноваційних способів лікування ДВНК. Поряд із класичними принципами активно застосовуються сучасні біоматеріали, біосенсори та смарт-системи, що дають змогу моніторувати стан рани й у перспективі забезпечувати терапію «на вимогу».
ЦД та рановий процес: значущі особливості
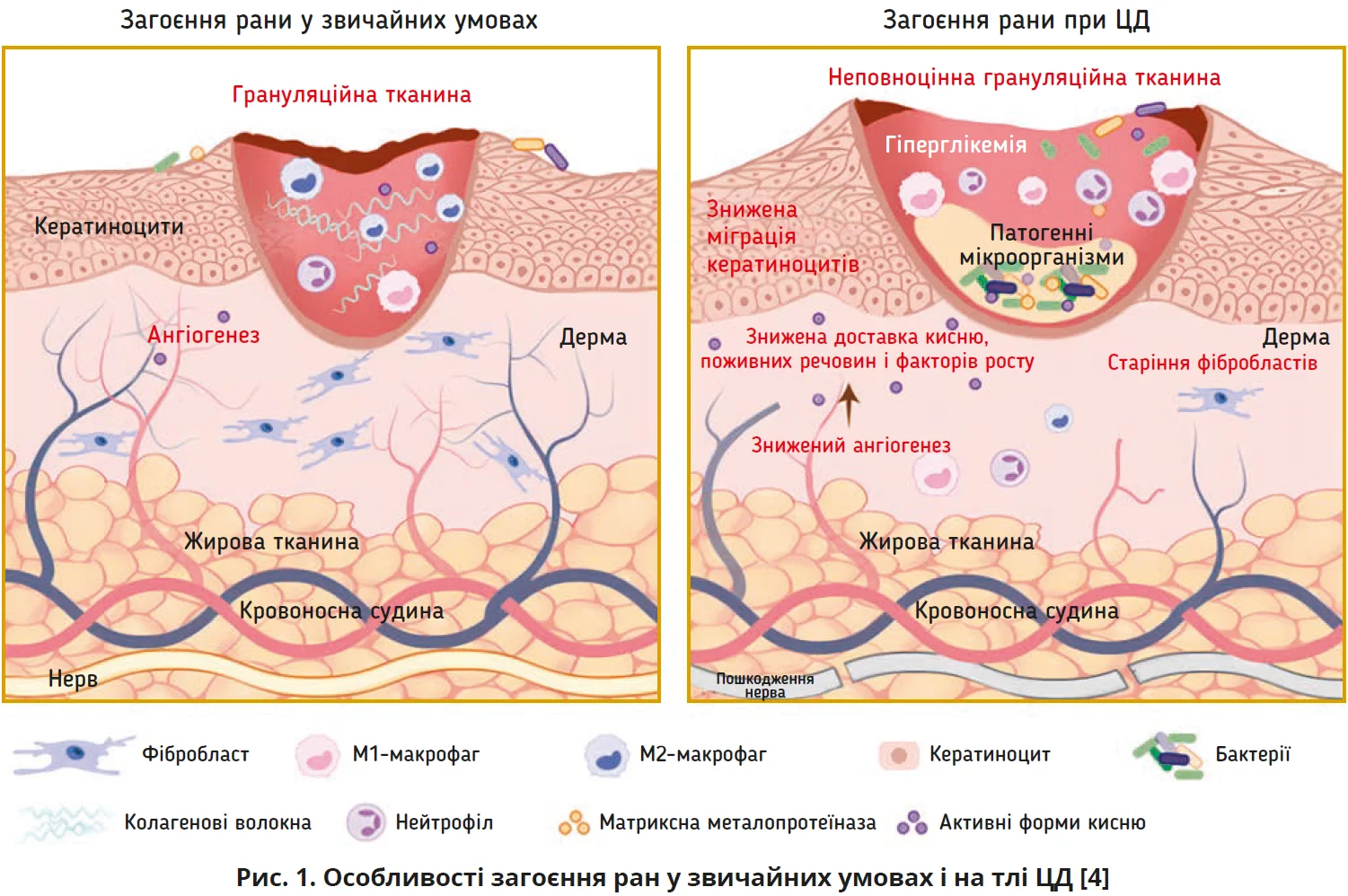
Загоєння будь-якої рани у хворих на ЦД має свої особливості. Якщо в типовій ситуації рана проходить послідовні етапи – гемостаз, запалення, проліферацію та ремоделювання (рис. 1), то при ЦД цей сценарій часто збивається вже на ранніх кроках [3]. Найуразливішою ланкою є фаза запалення: вона може затягуватися через персистивну гіперглікемію, оксидативний стрес, порушення мікроциркуляції, нейропатію, недостатній ангіогенез і високий ризик бактерійної контамінації [2, 4].
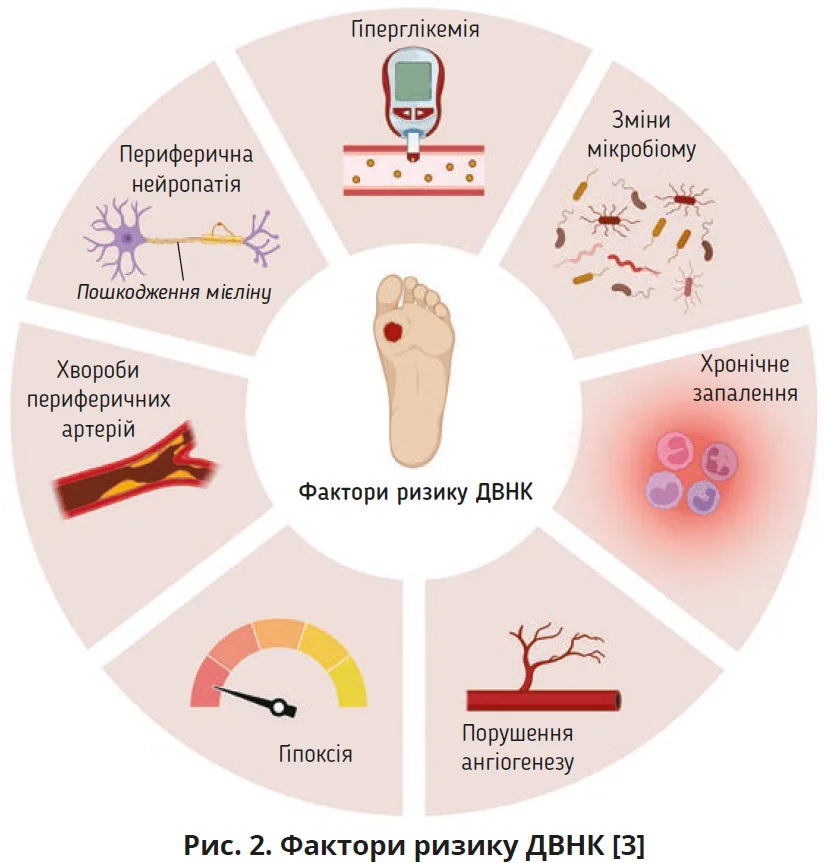
Порушення детоксикації активних форм кисню та синтезу оксиду азоту спричиняє прогресування нейропатії; ішемія на тлі мікроангіопатії обмежує доставлення кисню й нутрієнтів у ранове ложе. Гіперглікемія та метаболічні зсуви порушують імунну відповідь: ефективність нейтрофілів/макрофагів знижується, запалення стає більш тривалим і деструктивним (рис. 2). Це створює умови для персистування інфекції та формування біоплівок, що додатково підтримують хронізацію [9].
У результаті рана довше залишається в «режимі оборони», підтримуючи надлишкову активність протеаз і медіаторів запалення, що гальмує формування зрілої грануляційної тканини й епітелізацію [9].
Згідно із сучасними поглядами на ведення ДВНК ефективне загоєння потребує не лише нормалізації рівня глікемії та закриття рани, але й забезпечення низки умов у рановому ложі, що можна забезпечити за допомогою сучасних пов’язок. Вони мають підтримувати вологе середовище та контрольовану абсорбцію ексудату, забезпечувати газопроникність і механічний захист, створювати бар’єр для мікроорганізмів, бути нетоксичними для здорових тканин, а також бажано мати протизапальні властивості та бути зручними в застосуванні [3, 4]. Це особливо важливо при веденні ДВНК, оскільки надмірне пересушування, травматичне зняття, мікробний ріст, формування біоплівок легко зводять нанівець прогрес загоєння.
Пов’язки: від «простих і пасивних» до смарт-технологій
Лікування виразок на шкірних покривах, незалежно від епохи й технологій, завжди має два послідовні етапи: очищення рани та її закриття за допомогою пов’язки. Протягом століть погляди на ядро ранової хірургії – первинну хірургічну обробку – залишалися майже незмінними: огляд і знеболення, санація (дебридмент) з видаленням сторонніх тіл і нежиттєздатних тканин, промивання, створення чистого ложа для загоєння, резекція країв, гемостаз і антисептика. Значних змін зазнав останній етап – накладання пов’язки або дренування. Фокус змістився від принципу простого закриття рани до керування її локальним середовищем. Тепер пов’язка має особливе «технічне завдання»: контролювати ексудат, підтримувати баланс вологості, добре виконувати бар’єрну функцію та забезпечувати ефективне зниження ризику інфекційних ускладнень [2-4].
Становлення десмургії починалося зі спроб знайти в природному оточенні речовини з антибактерійними, антисептичними та ранозахисними властивостями. Спочатку із цією метою використовували вино й оцет, смоли та мед, мох і павутину, глину та листя рослин, льон і полотно. Усі вони, відповідно до свого часу, вирішували ключову проблему: зменшували контамінацію та створювали хоча б мінімальний бар’єр між раною й зовнішнім середовищем.
Протягом довгих років ранова медицина використовувала принцип «що сухіше, то краще». Класичні пов’язки, насамперед марлеві, були визнані універсальним інструментом догляду за раною: доступні та прості, вони добре вбирають ексудат, дають змогу проводити часті огляди й заміну. Сухий метод має очевидні практичні переваги: він сприяє зменшенню мацерації, дає змогу пасивно контролювати ексудат і здійснювати механічне очищення під час перев’язки. Але ці самі переваги мають і зворотний бік. Суха марля легко прилипає до ранового ложа, а при знятті може травмувати грануляції й епітелій, провокувати повторну кровоточивість і відкидати загоєння назад. Пересушування змінює локальні репаративні процеси: клітини мігрують гірше, а формування нової епітеліальної тканини сповільнюється. Отже, суха пов’язка добре виконує роль пасивного захисника, проте рідко стає справжнім союзником активної репарації.
Саме така особливість сухих пов’язок зумовила роботу над пов’язками нового покоління. Уже розроблено функціональні пов’язки за концепцією вологого загоєння, при якій акцент зміщується із «закрити» на «керувати мікросередовищем». На практиці це означає використання матеріалів, які підтримують оптимальну вологість, температуру та рН, забезпечують газообмін, знижують бактерійне навантаження, а ще локально доставляють протимікробні чи протизапальні агенти та навіть підлаштовуються під стан рани.
Нині технології крокують далі – створюються «інтелектуальні» пов’язки. Їхня ідея проста: мікросередовище хронічної рани може суттєво змінюватися в інтервалах між перев’язками, тому контролювання її лише під час огляду дає недостатню, вибіркову картину. За 1-3 доби, які минають до наступної перев’язки, під пов’язкою можуть коливатися рН та об’єм/склад ексудату, змінюватися активність оксидативного стресу, протеолітична активність і бактерійне навантаження, а також формуватися біоплівки. Ці процеси не завжди помітні при поверхневому огляді, але саме вони визначають, чи рана переходить до грануляції й епітелізації, чи знову триває хронічне запалення та зростають інфекційні ризики. Тому інтелектуальна пов’язка має не тільки реєструвати ключові сигнали (pH, температуру, кількість ексудату, біомаркери запалення/інфекції), але й відповідати на них, наприклад, зміною кольору, сигналізуванням медперсоналу або початком вивільнення відповідних лікарських засобів. У такій концепції пов’язка продовжує обрану лікувальну стратегію між перев’язками, даючи змогу контролювати стан рани не епізодично, а майже безперервно.
Смарт-біоматеріали: акцент на гідрогелі
Сучасна концепція вологого загоєння зміщує акцент із «закрити рану» на «керувати умовами»: підтримувати оптимальні вологість, температуру та pH, мінімізувати зовнішню контамінацію й забезпечувати нетравматичну зміну пов’язки. Однак за діабетичних виразок цього часто недостатньо: на тлі хронічного запалення, оксидативного стресу, порушеного ангіогенезу та високого ризику інфекції потрібні матеріали, які не лише підтримують середовище, а й активно модулюють ключові патогенетичні ланки.
Тому розробляються інноваційні біоматеріали, що забезпечують протимікробний захист, контролюють запалення та підтримують регенерації. Одним з найперспективніших рішень вважають смарт-
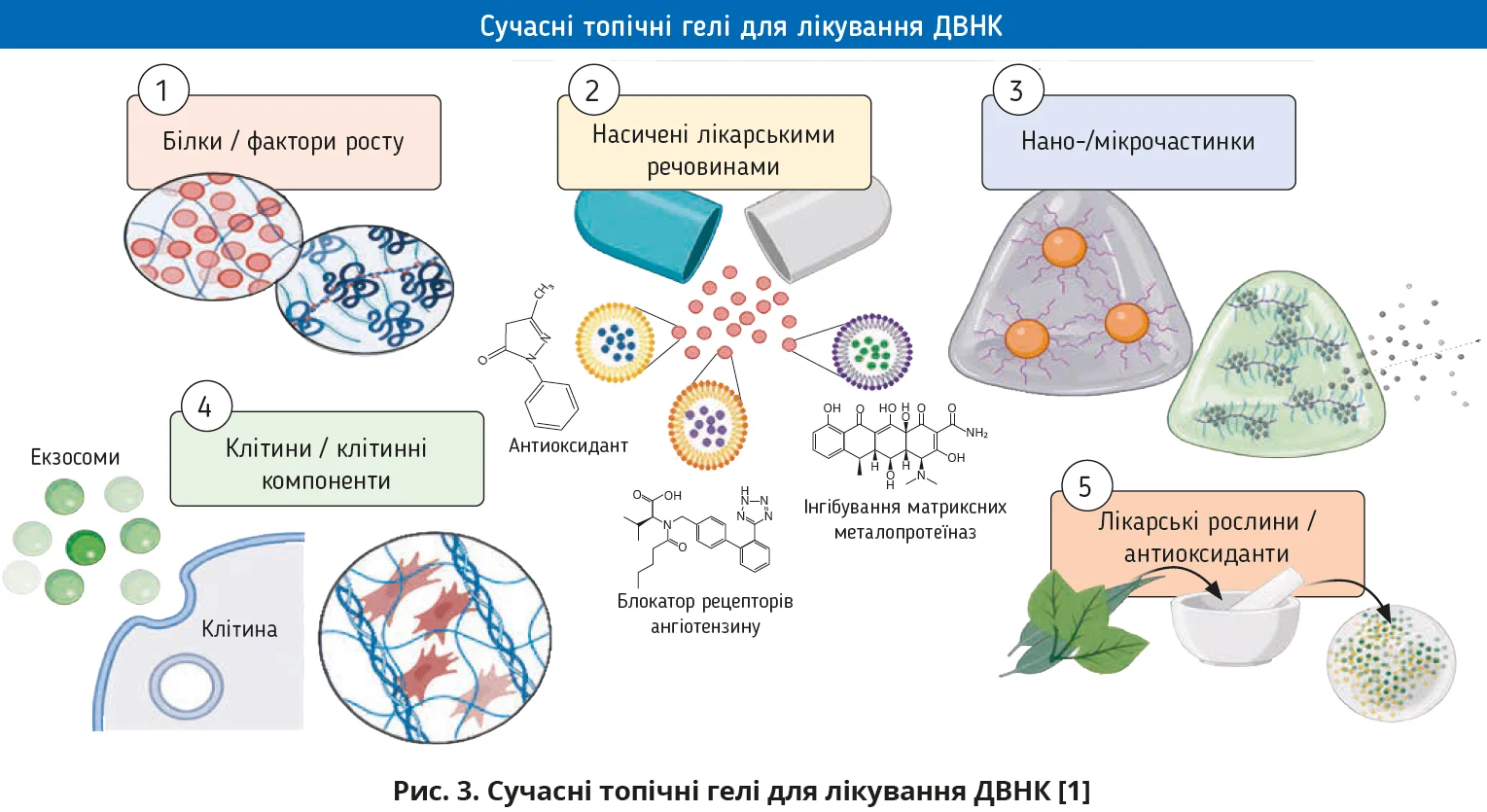
біоматеріали, передусім гідрогелі: вони біосумісні, утримують вологу, можуть бути прозорими для візуального контролю та слугують матрицею для локального доставлення активних речовин [1, 5]. Завдяки цьому гідрогель перетворюється з пасивного покриття на терапевтичну платформу. Гідрогелі можуть містити білки / фактори росту, ліки й лікарські рослини, клітини та клітинні компоненти, нано- та мікрочастинки (рис. 3).
Гелеві покриття можуть розміщувати на природних або синтетичних матрицях (часто у вигляді композитів), і вибір матриці визначає, наскільки добре система утримує вологу, абсорбує ексудат, забезпечує газообмін, адгезію клітин і механічну стабільність [1, 5]. Природні матриці можуть бути представлені найрізноманітнішими компонентами:
- альгінат добре гелюється й утримує вологе середовище, корисний при ексудативних ранах;
- целюлоза підсилює сорбцію ексудату та стабілізує гель;
- хітозан цінують за біоадгезивність, гемостатичні та власні протимікробні властивості;
- колаген як компонент екстрацелюлярного матриксу покращує прикріплення клітин і підтримує формування грануляційної тканини;
- декстран підвищує гідратацію та зручний для хімічної модифікації;
- фібрин відтворює ранній каркас загоєння та сприяє клітинній міграції;
- желатин додає еластичності та є сприятливим субстратом для клітин;
- гіалуронова кислота підтримує міграцію клітин і модуляцію запалення;
- пектин покращує гелеутворення й бар’єрні властивості [3].
Водночас природні полімери часто мають слабші механічні характеристики, тому їх зшивають або комбінують із синтетичними матрицями. Синтетичні полімери (полі-ε-капролактон, поліетиленгліколь/поліетиленоксид, полімолочна кислота, полівініловий спирт, повідон) дають відтворювану якість і керовану міцність/деградацію:
- полі-ε-капролактон забезпечує каркас і міцність, але потребує підвищення гідрофільності;
- поліетиленгліколь формує гідрофільні гелі з прогнозованою реологією;
- полімолочна кислота зручна для контрольованої деградації та доставлення агентів;
- полівініловий спирт посилює механіку та стабільність гелю;
- повідон покращує змочуваність і адгезію, а також підходить для систем із пролонгованим вивільненням [3].
Активні агенти, які вбудовують у гелеву матрицю, підбирають під ключові вузькі місця діабетичної рани: мікробне навантаження, персистивне запалення, дисбаланс протеаз, оксидативний стрес і дефіцит репаративних сигналів. Для контролю інфекції використовують антибіотики (вони локально знижують бактерійну контамінацію, а матриця забезпечує їх утримання в рані та пролонговане вивільнення) й антисептики / йодовмісні комплекси, що дають ширший протимікробний ефект. Додатково застосовують протимікробні пептиди, які можуть зменшувати ризик персистенції біоплівок. Для корекції мікросередовища використовують антиоксиданти та «поглиначі» активних форм кисню: вони зменшують оксидативний стрес, який гальмує проліферацію клітин і підтримує хронічне запалення. Окремою мішенню є протеолітичний дисбаланс: інгібітори матриксної металопротеїнази або матеріали, що знижують надмірну активність протеаз, допомагають зберігати позаклітинний матрикс і фактори росту [1, 5]. Для стимуляції репарації до гелів додають фактори росту (підсилюють ангіогенез, проліферацію фібробластів і реепітелізацію), але вони потребують додаткової стабілізації носієм і контрольованого вивільнення. У складніших рішеннях застосовують клітинні компоненти, які забезпечують паракринні сигнали для імуномодуляції та регенерації, а матриця підвищує їхню локальну біодоступність. Нарешті, нано-/мікрочастинки можуть виступати як носії для антибіотиків/антиоксидантів або як самостійні біоактивні добавки (наприклад, із протимікробними властивостями), забезпечуючи керованіше доставлення та триваліший ефект у рані [3].
Смарт-моніторинг за допомогою гідрогелевих біосенсорів
Окрім створення різноманітних біоматеріалів активно розроблюють гідрогелеві біосенсори, адже при веденні діабетичних виразок потрібно не лише застосовувати оптимальне покриття, а й учасно помітити, що рана переходить у несприятливу фазу: зростає ризик інфекції, посилюється запалення, погіршується перфузія, формується хронізація. Так виник окремий напрям: стратегії смарт-моніторингу, де гідрогель працює не лише як вологе середовище, а і як платформа для біосенсорів.
Суть підходу полягає в інтегруванні в пов’язку сенсорних компонентів, які вловлюють зміни мікросередовища рани (pH, глюкоза, температура, вологість тощо) та перетворюють їх на сигнал, придатний для швидкої інтерпретації. Це може бути проста кольорова індикація або спеціальний індикатор для кількісного зчитування пристроєм/камерою, який потім передає інформацію в цифрову систему.
Візуальні (колориметричні) сенсори являють собою найпростіший тип гідрогелевих сенсорів. Вони швидко реагують на зміни в рані за допомогою індикатора, який змінює колір у відповідь на коливання pH або інший показник. Їхня велика перевага полягає в простоті оцінювання результату – досить візуального огляду або погляду через камеру смартфона. Напівкількісний сигнал, залежність від освітлення, «зашумленість», які створюють ексудат і домішки, є типовими недоліками цього типу сенсорів.
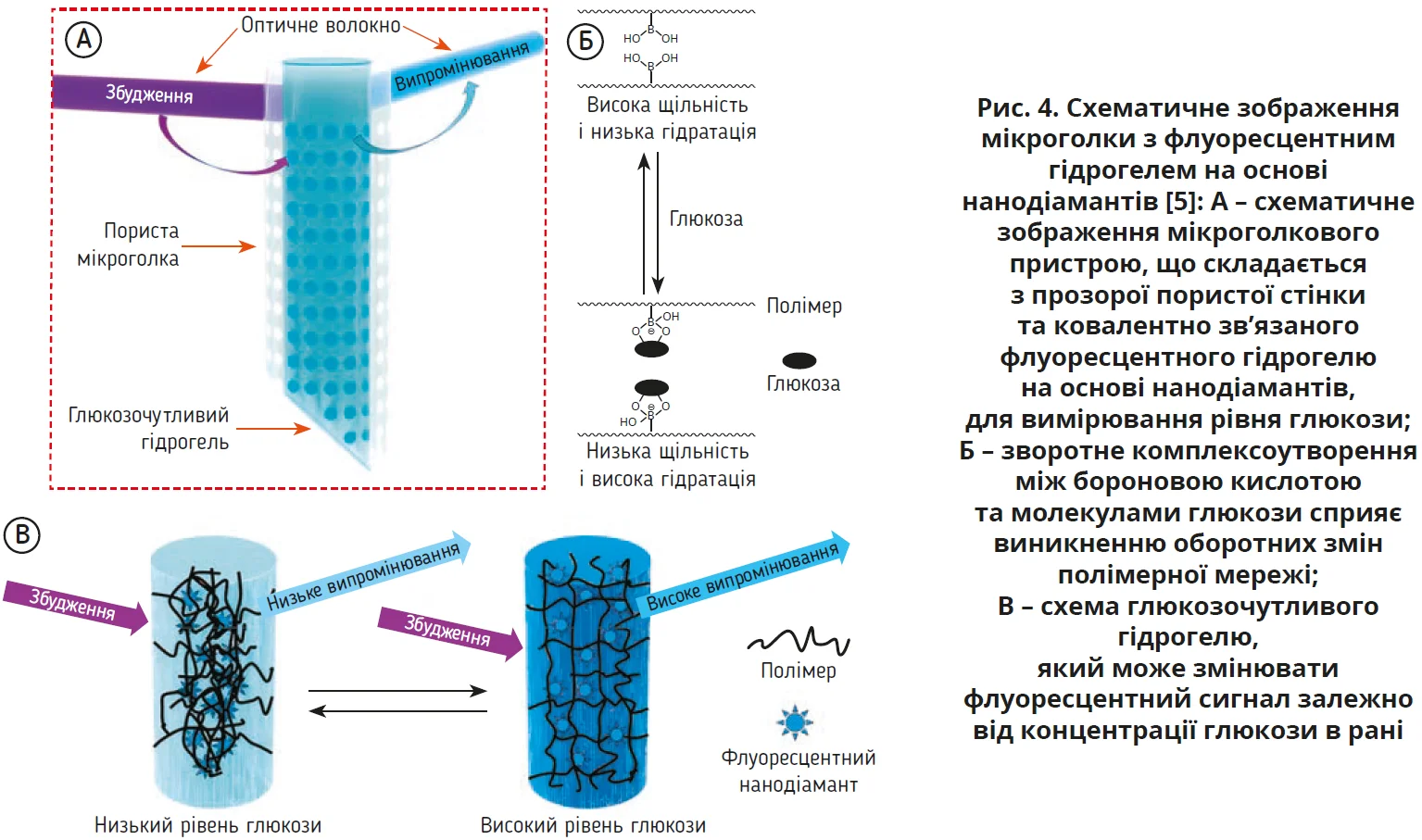
Є ще флуоресцентні сенсори (рис. 4). Вони точніші та здатні перетворювати коливання вмісту глюкози чи pH на зміну світіння вбудованого флуорофора. Технічно таку здатність реалізують або через молекули, що вибірково зв’язують глюкозу (наприклад, боронатні групи), або через ферментні системи (часто на основі глюкозооксидази). Флуоресценція дає змогу отримувати чутливіший сигнал і відстежувати його в динаміці, а для зменшення залежності від зовнішніх умов інколи застосовують раціометричний підхід: у пов’язку вбудовують сенсор, який навмисно формує два флуоресцентні канали (наприклад, два барвники або два піки випромінювання одного зонда), й оцінюють не абсолютну яскравість, а їх співвідношення. Альтернатива – часовий режим, коли аналізують не інтенсивність, а тривалість світіння після підсвічування; це також робить результат менш чутливим до освітлення, товщини пов’язки чи кількості ексудату. Обмежують цей метод необхідність підсвічування та зчитування (потрібна камера смартфона / спеціальний зчитувач), а також високі вимоги до стабільності сенсорного шару в рановому ексудаті. Поверхня сенсору також може «обростати» білками, клітинами та мікроорганізмами (інколи з формуванням біоплівки), через що сигнал слабшає або спотворюється (так званий біофулінг); інколи явище біофулінгу призводить до руйнування сенсора.
Альтернативу оптичним сенсорам становлять електрохімічні сенсори, в яких зміни глюкози переводяться в електричний сигнал. Вони бувають ензимні (з глюкозооксидазою або дегідрогеназою) та неензимні (з каталізаторами на електроді) [5]. Такі системи здатні давати кількісні значення в реальному часі й добре поєднуються з мініелектронікою; натомість потребують контролю стабільності (особливо ензимні), калібрування та захисту від біофулінгу. Часто їх інтегрують у мікроголкові платформи для стабільного доступу до інтерстиційної рідини.
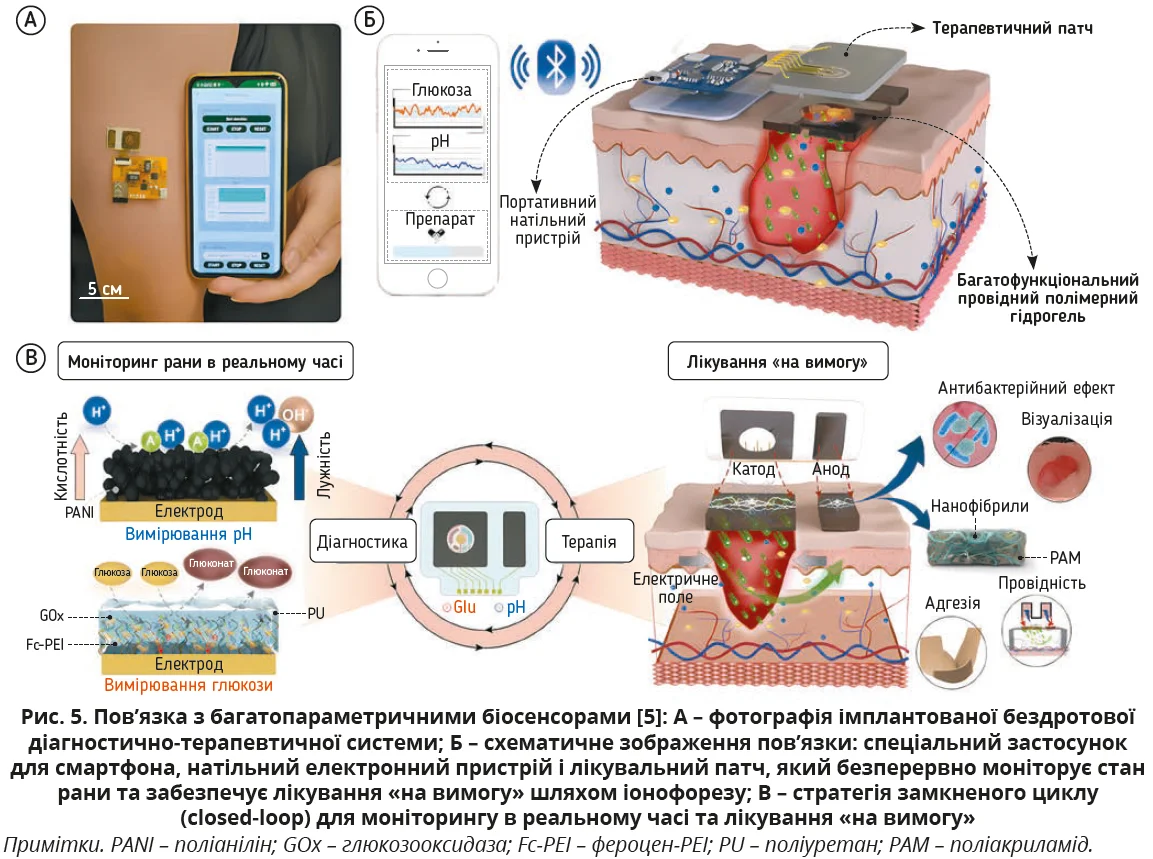
Найтехнологічнішими є багатопараметричні пов’язки, котрі одночасно відстежують глюкозу, pH, температуру, вологість або механічний тиск. До їхнього складу входить натільний електронний пристрій, який збирає дані із сенсорів та отримує команди від мобільного застосунку на смартфоні, за допомогою якого подається команда щодо введення потрібного препарату (рис. 5). Такі пов’язки максимально повно відображають стан діабетичної рани, однак є значно складнішими у виготовленні й інтерпретації. Більшість таких систем поки що перебуває на етапі досліджень і пілотних розробок.
Висновки
Класичні підходи до лікування ДВНК суттєво трансформуються: поряд з базовими принципами ведення зростає акцент на керований вплив на мікросередовище рани та персоналізацію місцевої терапії. Значні перспективи мають гідрогелі, оскільки вони поєднують біосумісність, підтримання вологого середовища з можливістю бути платформою для локального доставлення лікарських засобів з наступним їх смарт-вивільненням «за сигналом» з рани. Особливі надії пов’язують з біосенсорами, здатними фіксувати несприятливі зміни в рані між перев’язками та підвищувати керованість лікування. У перспективі це відкриває шлях до розширення використання підходів test-and-treat і впровадження діагностично-терапевтичних систем, які здатні самостійно визначати мінімальні зміни в діабетичній рані та «на вимогу» вводити потрібні медикаменти. Загалом майбутнє ведення ДВНК видається дедалі технологічнішим з фокусом на використання біоматеріалів, смарт-моніторингу та цільової локальної терапії.
Література
- Bardill J.R., Laughter M.R., Stager M., et al. Topical gel-based biomaterials for the treatment of diabetic foot ulcers. Acta Biomater. 2022; 138: 73-91. doi: 10.1016/j.actbio.2021.10.045.
- Bielska B., Miłowska K. Therapeutic potential of chitosan-based and related nanocomposite systems in wound management: a review. Int. J. Mol. Sci. 2025; 26: 11748. doi: 10.3390/ijms262311748.
- Da Silva J., Leal E.C., Carvalho E., Silva E.A. Innovative functional biomaterials as therapeutic wound dressings for chronic diabetic foot ulcers. Int. J. Mol. Sci. 2023; 24: 9900. doi: 10.3390/ijms24129900.
- Han C., Singla R.K., Wang C. Application of biomaterials in diabetic wound healing: the recent advances and pathological aspects. Pharmaceutics. 2025; 17: 1295. doi: 10.3390/pharmaceutics17101295.
- He X., Wei Y., Xu K. Hydrogel-based treatment of diabetic wounds: from smart responsive to smart monitoring. Gels. 2025; 11: 647. doi: 10.3390/gels11080647.
- Lavery L.A., Reyes M.C., Najafi B., et al. The infected diabetic foot: incidence and risk factors for dehiscence after surgery for diabetic foot infections. Wound Repair Regen. 2025; 33: e13235. doi: 10.1111/wrr.13235.
- Liu Y., Ge L. Smart biomaterials in wound healing: advances, challenges, and future directions in intelligent dressing design. Bioengineering (Basel). 2025; 12: 1178. doi: 10.3390/bioengineering12111178.
- Neal L., Yates T., Shabnam S., et al. Frailty, diabetic foot ulceration and mortality in people diagnosed with type 2 diabetes: multistate analysis of primary care patients in the UK clinical practice research datalink. Diabetes Res. Clin. Pract. 2025; 113058. doi: 10.1016/j.diabres.2025.113058.
- Pauliukienė R., Šutienė K., Čemerkaitė A., Čeponis J. Predictors of unfavorable outcomes in diabetic foot ulcers. Diagnostics (Basel). 2025; 15: 3070. doi: 10.3390/diagnostics15233070.
- Sadeghi Moghaddam Bijari A., Alijanianzadeh M., Keshmiri Neghab H., et al. A mini-review on fibroblast-derived exosomes as wound healing stimulators. Int. J. Hematol. Oncol. Stem Cell Res. 2025; 19: 237-247. doi: 10.18502/ijhoscr.v19i3.19287.
- Zhang P., Lu J., Jing Y., et al. Global epidemiology of diabetic foot ulceration: a systematic review and meta-analysis. Ann. Med. 2017; 49: 106-116. doi: 10.1080/07853890.2016.1231932.