Генетичні й епігенетичні маркери при тиреоїдиті Хашімото
Переклала й адаптувала д-р мед. наук Лариса Стрільчук
Тиреоїдит Хашімото (ТХ) асоціюється із запаленням, що вражає щитоподібну залозу (ЩЗ) та може призвести до її недостатності. Ця хвороба належить до автоімунних, що вказує на складну взаємодію між генетичною схильністю, впливом чинників довкілля й імунною системою. За ТХ імунна система організму помилково сприймає тканину ЩЗ як чужорідний об’єкт і безперервно атакує її. Це призводить до патологічних змін у тканині залози, запалення тиреоцитів і, як наслідок, дуже повільної секреції гормонів ЩЗ. Клінічно симптоми ТХ подібні до проявів гіпотиреозу й охоплюють постійну втомлюваність, непереносимість холоду, збільшення маси тіла тощо. Діагноз установлюється на підставі результатів досліджень функції ЩЗ та серологічних маркерів.
Генетичні й епігенетичні чинники розвитку ТХ активно вивчаються, оскільки їх наукове розуміння може сприяти виявленню нових терапевтичних мішеней для ефективного та персоналізованого лікування. У цьому огляді узагальнено сучасні дані щодо генетичних і епігенетичних механізмів розвитку ТХ.
Визначення ТХ
ТХ є найпоширенішим автоімунним захворюванням ЩЗ та провідною причиною гіпотиреозу в регіонах з достатнім споживанням йоду. Розвиток ТХ зумовлений поєднанням генетичної схильності та впливу зовнішніх чинників, що призводить до втрати імунної толерантності. Це, своєю чергою, спричиняє автоімунну атаку на тканину ЩЗ та розвиток хвороби.
ТХ здатен зумовлювати розвиток гіпотиреозу навіть за умови достатнього надходження йоду. Хоча така ситуація найчастіше виявляється в жінок середнього віку, вона може виникати й у чоловіків, а також у людей похилого віку незалежно від статі. Описані вище ознаки ТХ мають вирішальне значення в діагностиці хвороби, яка ґрунтується на клінічній оцінці, аналізах функції ЩЗ та виявленні автоімунних маркерів, зокрема антитиреоїдних антитіл. Підходи до лікування спрямовані на досягнення нормального рівня секреції гормонів і підтримання цього стану за допомогою безперервної замісної терапії протягом усього життя. Незважаючи на хронічний перебіг хвороби та необхідність довготривалого медичного нагляду, пацієнти з ТХ можуть вести повноцінне життя й багато з них зберігають добрий стан здоров’я.
Генетичні й епігенетичні маркери ТХ
Генетичні маркери та їх взаємодія з довкіллям
Хоча на розвиток автоімунних процесів впливають і генетичні, й епігенетичні чинники, в більшості хвороб вирішальну роль відіграє спадковість, зокрема гени схильності до цих захворювань. Зокрема, одним з найпотужніших механізмів боротьби з інфекційними хворобами та водночас фактором схильності до автоімунних патологій є гени людського лейкоцитарного антигена (HLA), розташовані на шостій хромосомі. Також у патогенезі ТХ беруть участь гени протеїн-тирозин-фосфатази нерецепторного типу 22, інсуліну, цитотоксичного Т-лімфоцит-асоційованого антигена-4, фактора некрозу пухлини.
Важливе значення мають також чинники з боку довкілля, до яких відносять харчування, вплив токсинів і полютантів, хронічний стрес і психічне здоров’я, вплив сонячного світла, рівень фізичної активності. Взаємодія генетичних факторів і чинників довкілля формує тригери, які можуть підвищувати ризик розвитку автоімунних хвороб.
Епігенетичні маркери
До епігенетичних маркерів належать метилювання ДНК, модифікації гістонів і мікроРНК. Метилювання ДНК являє собою базовий механізм епігенетичної модифікації, що полягає в приєднанні метильної групи до цитозинової основи ДНК, головним чином у ділянках динуклеотидів цитозин-гуанін. У разі ТХ виявлено аномальне метилювання ДНК у генах, що відповідають за функції ЩЗ та регуляцію імунітету. Зокрема, гіперметилювання специфічних для ЩЗ генів рецептора тиреотропного гормону (ТТГ) та тиреопероксидази може бути передумовою виникнення гормональної недостатності в пацієнтів з ТХ.
Важливим елементом епігенетичного контролю експресії генів є модифікація гістонів – білків, що входять до складу нуклеосом (структурних одиниць ДНК). Аномальні зміни гістонів, зокрема ацетилювання й метилювання, можуть змінювати структуру хроматину та впливати на транскрипцію генів, що пов’язано з розвитком ТХ.
Своєю чергою, змінені рівні експресії мікроРНК здатні модулювати імунні реакції, а також проліферацію й апоптоз тиреоїдних клітин. Для визначення рівнів експресії мікроРНК у тканині ЩЗ використовується метод мікроматричного аналізу.
Значення й актуальність ТХ у контексті автоімунних захворювань
ТХ є одним з найпоширеніших автоімунних захворювань, що вражає тисячі людей, переважно жінок, у всьому світі. Цій хворобі часто властиве поєднання з іншими автоімунними захворюваннями: хворобою Ґрейвса, ревматоїдним артритом, цукровим діабетом 1-го типу, целіакією.
Найчастішими симптомами ТХ у дорослих є втомлюваність, млявість, непереносимість холоду, збільшення маси тіла, закрепи, зміни голосу та сухість шкіри, іноді когнітивні порушення.
Діагностика ТХ здебільшого ґрунтується на ультразвуковому дослідженні (УЗД), яке дає змогу виявити характерні ознаки хвороби. У процесі диференційної діагностики вузлів ЩЗ ефективним методом є тонкоголкова біопсія під контролем УЗД, яка допомагає відрізнити ТХ від інших патологій ЩЗ за гістологічними ознаками. Удосконалення скринінгових тестів для оцінювання функції ЩЗ та виявлення антитіл до її антигенів дає змогу виявляти ТХ вже на ранніх стадіях. Основним методом лікування, що полегшує симптоми та запобігає довгостроковим ускладненням, є замісна гормональна терапія левотироксином.
Патофізіологія ТХ
ТХ характеризується специфічним типом імунозалежного запалення, спрямованого проти тканини ЩЗ. У схильних до захворювання осіб відповідь імунної системи змінюється під впливом зовнішніх чинників (вірусних інфекцій, стресу тощо) й імунна система починає атакувати власні клітини ЩЗ. У ході цього процесу активуються автореактивні Т-лімфоцити, які проникають у тканину залози, розпізнають тиреоїдоспецифічні антигени, зокрема тиреоглобулін і тиреопероксидазу, та стимулюють В-лімфоцити до утворення антинуклеарних антитіл до цих антигенів. Ці автоантитіла, а також прозапальні цитокіни, що виділяються активованими імунними клітинами, спричиняють вторинне запалення в тканині залози. Через інфільтрацію лімфоцитів у тканині ЩЗ утворюються лімфоїдні фолікули, які ще більше посилюють запальну відповідь.
Хронічне запалення й автоагресія проти сполучної тканини ЩЗ призводять до поступового руйнування тиреоїдних фолікулів, унаслідок чого знижується здатність залози синтезувати тиреоїдні гормони.
У міру руйнування тиреоцитів тиреоглобулін і тирео‑пероксидаза потрапляють у кровотік, що зумовлює підвищення рівня відповідних автоантитіл у сироватці.
Дуже рідкісним ускладненням ТХ є енцефалопатія Хашімото, яка зазвичай виникає на тлі еутиреозу та являє собою виліковний, чутливий до стероїдів прогресивний або рецидивний тип енцефалопатії, який супроводжується підвищенням рівня тиреоїдоспецифічних автоантитіл.
Своєю чергою, орбітопатія, асоційована із ЩЗ, найчастіше трапляється при хворобі Ґрейвса з гіпертиреозом і лише іноді в пацієнтів з еутиреозом або гіпотиреозом. Оскільки більшість пацієнтів з еу- чи гіпотиреозом та орбітопатією мають позитивні титри антитіл до рецептора тиреотропіну, їм установлюють діагноз «еутиреоїдна/гіпотиреоїдна хвороба Ґрейвса». Якщо пацієнти з еу- чи гіпотиреозом та орбітопатією не мають цих антитіл, але мають ТХ, можливим діагнозом є офтальмопатія Хашімото.
Діагностика ТХ
Діагностика ТХ зазвичай ґрунтується на поєднанні клінічного обстеження, визначення рівня ТТГ і виявлення антитиреоїдних автоантитіл.
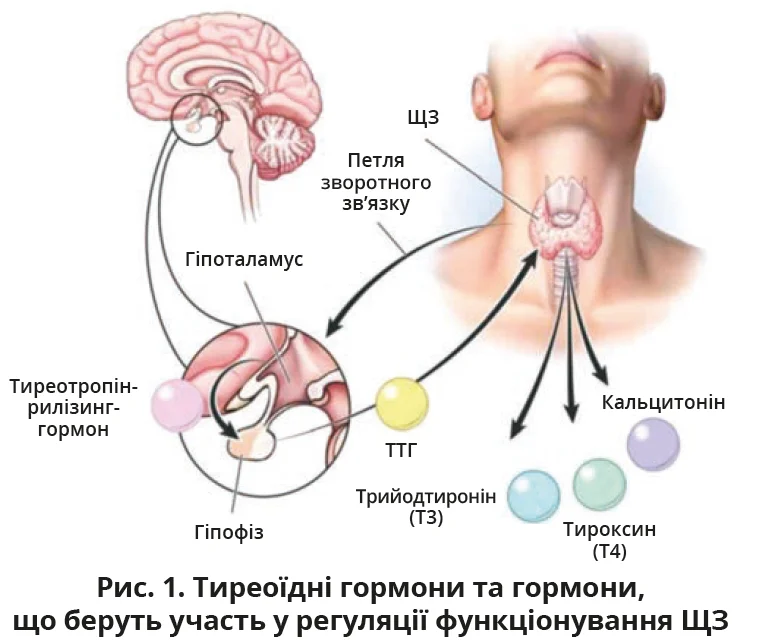
Найфундаментальнішим етапом діагностики є визначення функції ЩЗ шляхом оцінювання рівнів гормонів (рис. 1).
Зокрема, ТТГ вважається найбільш чутливим і специфічним показником функції ЩЗ порівняно з іншими доступними тестами. Вільний тироксин (вT4) відображає рівень тироксину – основного гормону, який секретується ЩЗ, і в разі ТХ зазвичай буває зниженим. Також можна визначати рівень трийодтироніну, однак у пацієнтів з гіпотиреозом він часто залишається в межах норми, особливо на ранніх стадіях.
Оцінювання наявності автоантитіл до ЩЗ допомагає виявити причини ТХ та виключити інші причини гіпотиреозу. Зазвичай визначають антитіла до тиреопероксидази (виявляються в >90% осіб з ТХ і є визначальними в діагностиці хвороби) та тиреоглобуліну. Також проводиться визначення імуноглобулінів, що стимулюють ЩЗ. Їх наявність допомагає розрізнити ТХ і хворобу Ґрейвса, яка також може проявлятися симптомами гіпотиреозу.
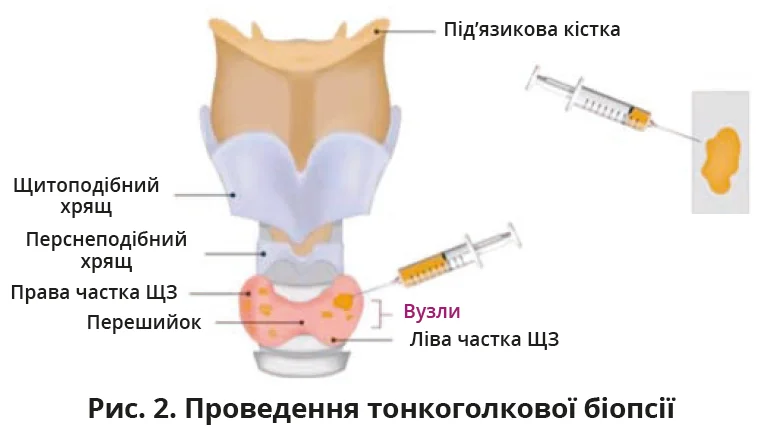
Для аналізу розмірів і форми ЩЗ виконується УЗД, яке за умови ТХ зазвичай виявляє дифузну чи неоднорідну ехогенність тканини залози, двобічне збільшення (зоб) або наявність вузлів. За потреби додатково проводиться тонкоголкова біопсія для підтвердження патологічного процесу (рис. 2).
Лікування ТХ
Ведення ТХ передбачає замісну гормональну терапію для контролю гіпотиреозу, зміни способу життя, ретельний регулярний моніторинг і відповідне симптоматичне лікування з метою поліпшення якості життя. Пацієнтам з ТХ потрібно надати повну інформацію про характер хвороби, важливість регулярного приймання медикаментів і необхідність тривалого спостереження.
Лікування гіпотиреозу, спричиненого ТХ, передбачає компенсацію нестачі гормонів ЩЗ за допомогою синтетичних препаратів, наприклад левотироксину. У більшості випадків левотироксин приймається перорально 1 раз на добу, вранці натще (для досягнення максимальної абсорбції). Доза препарату корегується індивідуально з урахуванням віку, маси тіла, тяжкості хвороби та наявності супутніх патологій. Для контролю ефективності терапії проводяться періодичні лабораторні дослідження з визначенням ТТГ, що дає змогу підтримувати рівні тиреоїдних гормонів у межах цільових показників. Контрольне відвідування ендокринолога рекомендується через 8-12 тижнів після початку терапії.
Пацієнтам з ТХ рекомендовано дотримуватися здорового способу життя, що охоплює збалансоване харчування, регулярну фізичну активність, контроль стресу та достатню кількість сну. Дієтичні фактори передбачають забезпечення адекватного споживання йоду (в разі його дефіциту), уникнення надмірної йодної суплементації, а також обмеження споживання зобогенних продуктів (наприклад, хрестоцвітих овочів). Важливим є припинення куріння, оскільки воно спричиняє загострення автоімунних тиреоїдитів.
Окрім замісної гормональної терапії, може виникнути потреба в симптоматичному лікуванні інших проявів хвороби. Зокрема, за наявності депресивних симптомів і порушень настрою рекомендується звертатися по допомогу до спеціалістів із психічного здоров’я.
У пацієнтів з ТХ варто оцінити ризик ускладнень і супутніх захворювань, пов’язаних з гіпотиреозом, зокрема гіперліпідемії, серцево-судинних захворювань і остеопорозу. Їх лікування може передбачати зменшення споживання жирів, корекцію серцево-судинних факторів ризику, а також приймання добавок кальцію та вітаміну D.
Висновки та перспективи майбутніх досліджень
Поєднання генетичних й епігенетичних даних може стати основою нових стратегій ведення пацієнтів – від діагностики та прогнозування до персоналізованого лікування. Проте необхідні подальші дослідження для підтвердження та поглиблення знань про вже виявлені генетичні й епігенетичні маркери, вивчення їхньої функціональної значущості та пошук нових терапевтичних підходів.
Література
Abdalrahman S.S., Smail H.O., Shallal A.F. Genetic and epigenetic markers in Hashimoto’s thyroiditis (review). International Journal of Epigenetics. 2025; 5 (1). doi: 10.3892/ije.2025.24.