Ендокринологія змінюється: короткий огляд ключових рекомендацій (2025)
Підготувала канд. мед. наук Тетяна Можина
У 2025 р. клінічна ендокринологія отримала одразу кілька нових міжнародних рекомендацій, які привернули значну увагу професійної спільноти. Серед них – оновлений консенсус Американської асоціації з клінічної ендокринології (ААСЕ) щодо алгоритму оцінювання та лікування ожиріння, нові настанови Європейського товариства ендокринології (ESE) з ведення жінок у перименопаузі та менопаузі, а також оновлені рекомендації Ендокринного товариства (ES) з діагностики й лікування первинного гіперальдостеронізму (ПГА). На перший погляд, ці документи стосуються різних клінічних проблем, але кожен з них пропонує переосмислити традиційні підходи до діагностики та лікування зазначених захворювань. У цьому матеріалі ми спробуємо визначити ключові акценти, які з’явилися в зазначених настановах.
ПГА: рекомендації ES
У липні 2025 р. на конгресі ENDO офіційно оприлюднили положення ES з ПГА. Якщо раніше ПГА розглядали переважно як рідкісну причину вторинної артеріальної гіпертензії (АГ), яку доцільно шукати лише в окремих клінічних ситуаціях (резистентна АГ, виражена гіпокаліємія, утворення надниркових залоз), то нині підхід суттєво змінився. У сучасних рекомендаціях цей стан дедалі частіше трактують як поширене та клінічно значуще захворювання, що може лежати в основі значної частини випадків АГ. Саме тому найразючіша зміна в новій настанові стосується підходу до скринінгу. Якщо раніше скринінг на ПГА рекомендували лише для окремих груп ризику, то нині експерти пропонують проводити його фактично всім пацієнтам з АГ [1].
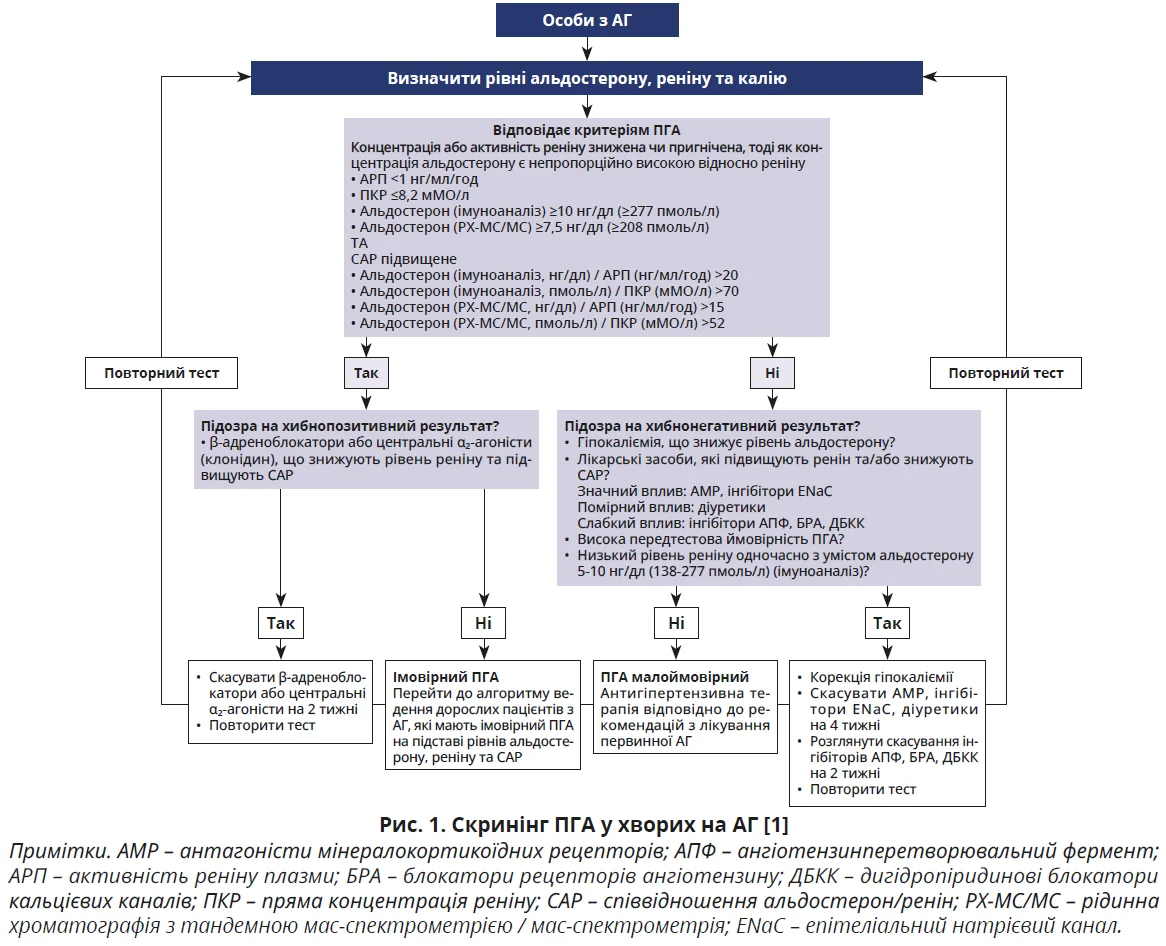
Ще одним важливим акцентом нової настанови є відмова від традиційної орієнтації на гіпокаліємію як ключовий клінічний маркер хвороби. У положеннях документа ES підкреслюється, що відсутність гіпокаліємії не виключає ПГА, а тому скринінг має ґрунтуватися на визначенні концентрації альдостерону та реніну з розрахунком їх співвідношення (рис. 1).
Дещо незвичним видається й гнучкіший підхід до проведення підтверджувальних тестів. Якщо раніше тести пригнічення альдостерону розглядали як обов’язковий етап діагностики, то тепер пропонується застосовувати їх вибірково: передусім у тих випадках, коли результати скринінгу не дають змоги однозначно визначити ймовірність латералізації ПГА (однобічної гіперсекреції альдостерону) та коли пацієнт потенційно може бути кандидатом для оперативного лікування.
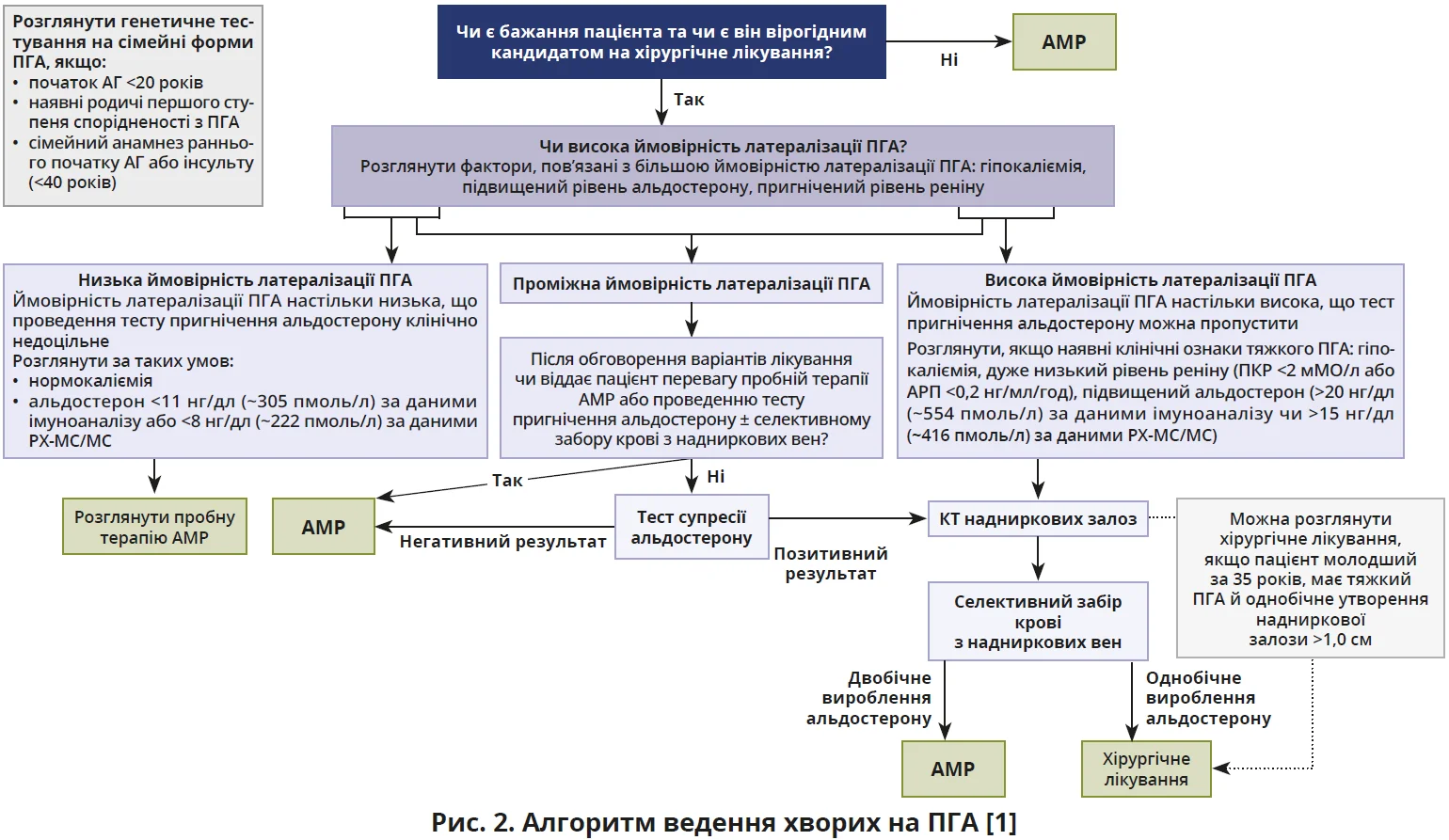
Значна увага приділяється й вибору лікувальної тактики. Рекомендації чітко підкреслюють, що пацієнти з ПГА мають отримувати специфічну терапію (медикаментозну/хірургічну), а не лише стандартну гіпотензивну терапію. При цьому рішення про оперативне втручання має ґрунтуватися на можливості доведення латералізації ПГА. Саме тому перед плануванням операції пропонується здійснювати комбіноване обстеження: комп’ютерну томографію (КТ) надниркових залоз разом із селективним забором крові з надниркових вен, що дає змогу точніше визначити джерело гормональної гіперсекреції (рис. 2).
Особливу увагу привертає новий підхід до оцінювання ефективності медикаментозного лікування. У рекомендаціях пропонується орієнтуватися не лише на рівень артеріального тиску (АТ), але й на підвищення вмісту реніну. Якщо ренін залишається пригніченим, а АГ контролюється недостатньо, рекомендується інтенсифікувати терапію антагоністами мінералокортикоїдних рецепторів (АМР).
Слід відзначити також ставлення експертів ES до вибору медикаментозної терапії. Попри появу нових препаратів, як основний засіб фармакотерапії рекомендується призначати спіронолактон, що пояснюється його доведеною ефективністю, широкою доступністю та низькою вартістю. Інгібітори епітеліального натрієвого каналу пропонується використовувати лише як альтернативу; тобто АМР залишаються терапією вибору [1].
Ожиріння: консенсус AACE
Наприкінці 2025 р. AACE представила оновлену практичну настанову з діагностики та лікування ожиріння, до якої було внесено суттєві зміни, починаючи з перегляду термінології та класифікації. Експерти ААСЕ запроваджують такі ключові поняття, як «хронічне захворювання, зумовлене адипозністю» (ХЗЗА) й «асоційовані з ожирінням ускладнення або захворювання» (АОУЗ) [3]. Ожиріння визначають як стан надлишкової адипозності з або без порушення розподілу чи функції жирової тканини.
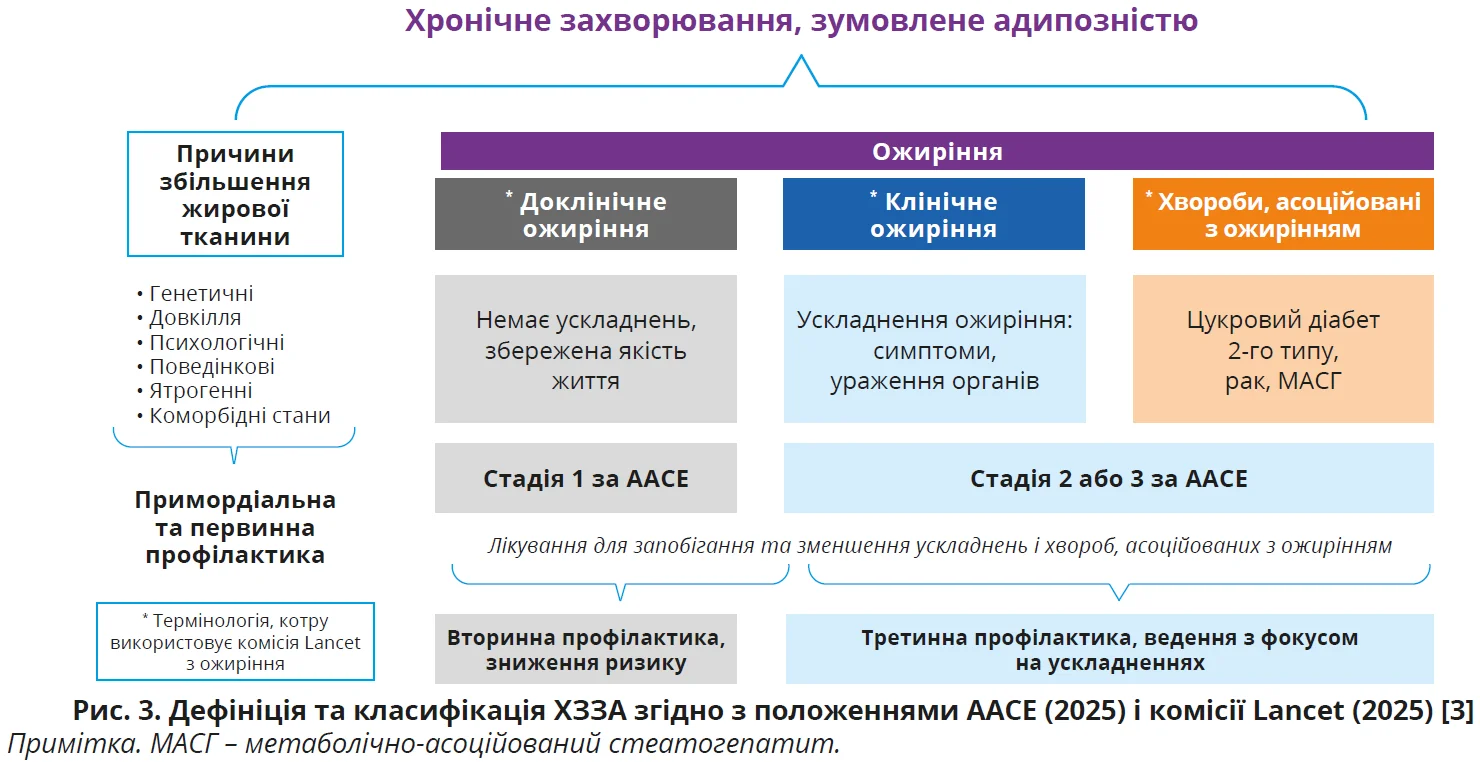
Концепція ХХЗА не є суто новою: вперше цей термін було запропоновано у 2017 р. з метою визначення ожиріння як хронічного захворювання та трактування цього стану не як «скільки важить пацієнт», а розуміння, що пацієнт є об’єктом лікування й навіщо це лікування потрібне. Нині ХХЗА розглядають як гетерогенне прогресивне хронічне захворювання, пов’язане з порушенням нейроендокринного контролю енергетичного балансу, що призводить до надлишкової/аномальної адипозності та може зумовлювати АОУЗ, погіршувати якість життя й підвищувати захворюваність/смертність [3]. АACE розглядає ХХЗА як узагальнювальний (парасольковий) термін, який охоплює всі аспекти хвороби: від факторів ризику, котрі потребують первинної профілактики ожиріння, до доклінічного та клінічного ожиріння, а також усіх АОУЗ (рис. 3).
Одним із принципових положень нового консенсусу ААСЕ є відхід від традиційної моделі оцінювання ожиріння, сфокусованої саме на визначенні індексу маси тіла (ІМТ). Нині підкреслюється, що ІМТ доцільно використовувати лише як інструмент первинного скринінгу. Водночас ІМТ не здатний точно відображати кількість і розподіл жирової тканини, особливо в осіб з розвиненою м’язовою масою, в літніх пацієнтів або при саркопенії [3]. Тому після первинного визначення ІМТ обов’язково слід оцінити розподіл жирової тканини. Для цього потрібно виміряти окружність талії та розрахувати співвідношення талія/зріст. Саме цей показник розглядають як простий і клінічно інформативний індикатор кардіометаболічного ризику, оскільки він краще відображає наявність вісцеральної жирової тканини. Значення співвідношення талія/зріст ≥0,5 вважається маркером підвищеного ризику метаболічних і серцево-судинних порушень [3].
Після визначення антропометричних показників експерти ААСЕ рекомендують визначити наявність і тяжкість АОУЗ. Із цією метою потрібно зібрати анамнез, провести фізичне обстеження, оцінити фактори ризику та результати лабораторних досліджень. З огляду на отримані дані визначають стадію хвороби (табл. 1).
До АОУЗ, які необхідно враховувати при визначенні стадії ХЗЗА, відносять АГ, дисліпідемію, порушення глікемії або цукровий діабет (ЦД) 2-го типу, обструктивне апное сну, атеросклеротичні серцево-судинні хвороби, серцеву недостатність, фібриляцію передсердь, хронічну хворобу нирок.
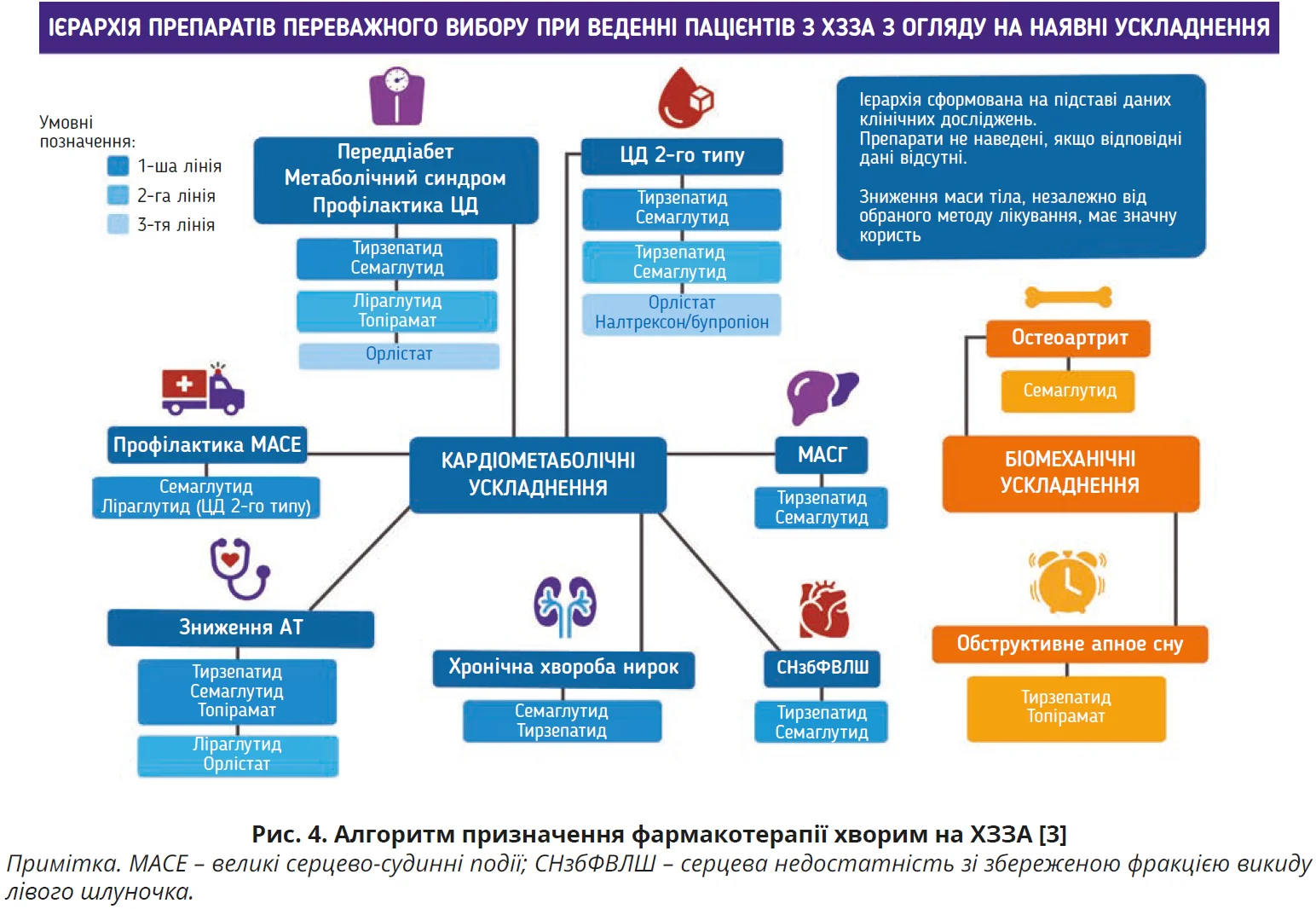
Практичну частину консенсусу ААСЕ представлено у вигляді 9 взаємопов’язаних алгоритмів, які послідовно розкривають нюанси ведення пацієнтів з ХЗЗА. Підхід до фармакотерапії ожиріння, запропонований ААСЕ, також ґрунтується на наявності АОУЗ (рис. 4).
Фармакотерапія підбирається з огляду на конкретні кардіометаболічні або біомеханічні ускладнення, а препарати розподіляються на 1-шу, 2-гу та 3-тю лінії терапії залежно від сили доказової бази й очікуваного клінічного ефекту. У більшості випадків провідне місце серед препаратів 1-ї лінії займають інкретинові агенти (семаглутид, тирзепатид). Саме вони найчастіше призначаються при високому кардіометаболічному ризику (переддіабет, метаболічний синдром, ЦД 2-го типу, МАСГ, хронічна хвороба нирок). Водночас алгоритм демонструє більш диференційований підхід до фармакотерапії інших типів ускладнень. Для біомеханічних проявів ожиріння (остеоартроз, обструктивне апное сну) також пропонується орієнтуватися на препарати з найбільшою доказовою базою щодо відповідних клінічних результатів (семаглутид, тирзепатид). Якщо ж препарати 1-ї лінії не можуть бути застосовані або виявляються недосить ефективними, рекомендації передбачають перехід до альтернативних варіантів фармакотерапії (ліраглутид, комбінація фентермін-топірамат або налтрексон-бупропіон, орлістат).
Перименопауза та менопауза: нові акценти в рекомендаціях ESE
Минулий 2025 р. змінив традиційне бачення менопаузи: в рекомендаціях ЕSЕ підкреслюється, що менопауза є не окремою подією, а безперервним спектром станів, який також охоплює перименопаузу та постменопаузу [2]. Експерти ЕSЕ намагаються змінити клінічне мислення й наполягають на ранньому розпізнаванні перименопаузальних змін, зокрема в жінок 40-45 років, коли нерегулярність циклу та вазомоторні симптоми вже можуть свідчити про початок гормональних змін.
Одним з найнеочікуваніших положень можна назвати рекомендацію щодо відмови від проведення рутинного гормонального тестування в жінок віком >45 років. Експерти пояснюють, що в більшості випадків діагноз перименопаузи або менопаузи має ґрунтуватися на клінічних симптомах і менструальному анамнезі, а не на лабораторному підтвердженні [2]. Біохімічні дослідження пропонується використовувати переважно в молодих жінок за появи ознак передчасної недостатності яєчників.
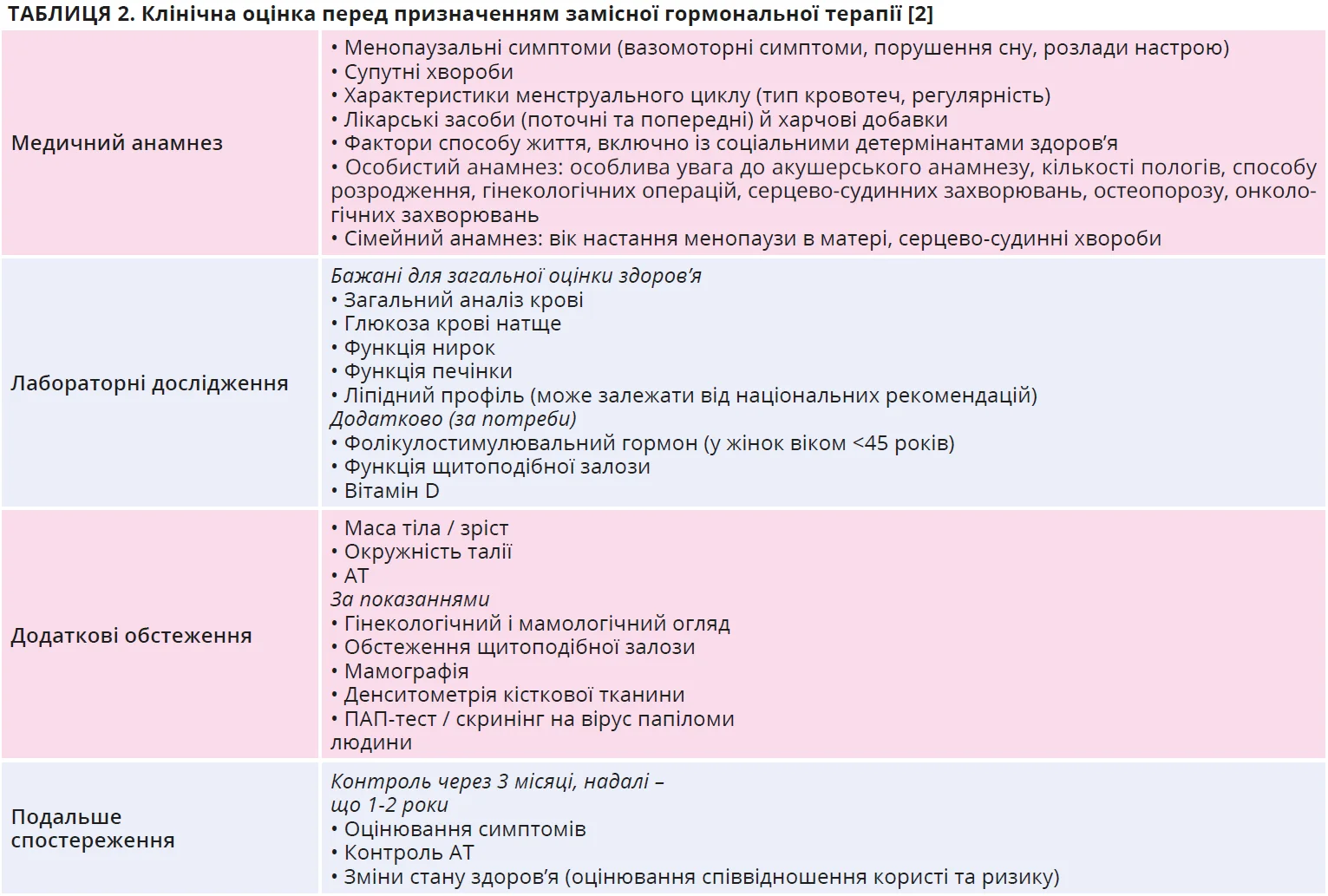
Іще одним важливим акцентом оновлених рекомендацій є зміна ставлення до ролі замісної гормональної терапії. У документі підкреслюється, що лікування не має зводитися лише до призначення гормонів: ведення жінок у перименопаузі та менопаузі має бути комплексним і враховувати загальний стан здоров’я, супутні хвороби й індивідуальні потреби. Перед призначенням гормональних препаратів рекомендується оцінити значну кількість параметрів (табл. 2). Водночас гормональну терапію розглядають як ефективний інструмент корекції симптомів і профілактики втрати кісткової маси, особливо якщо її розпочато в межах так званого вікна можливостей (протягом перших 10 років після менопаузи або у віці до 60 років).
Оновлені рекомендації пропонують індивідуалізованіший підхід до призначення гормональної терапії в жінок із супутніми хворобами. Нині добре контрольований ЦД або АГ не розглядаються як абсолютні протипоказання для застосування гормональної замісної терапії [2]. Експерти віддають перевагу трансдермальним формам доставлення естрогену, особливо при венозній тромбоемболії в анамнезі, мігрені з аурою, діабеті, контрольованій АГ. Такі положення радять не відмовлятися від терапії повністю, а шукати безпечніший шлях її призначення. Разом з тим документ чітко окреслює межі застосування гормональної терапії: її не рекомендується призначати для профілактики серцево-судинних подій, інсульту, деменції або як засіб лікування депресії [2].
Висновки
Нові рекомендації ES, AACE, ESE підкреслюють перехід до більш раннього виявлення ендокринної патології, комплексного оцінювання ризику й індивідуалізованого підбору терапії, наголошуючи на важливості не лише контролю клінічних симптомів, а й довгострокового збереження здоров’я.
Література
- Adler G.K., Stowasser M., Correa R.R., et al. Primary aldosteronism: an Endocrine Society clinical practice guideline. Journal of Clinical Endocrinology and Metabolism. 2025; 110 (9): 2453-2495. doi: 10.1210/clinem/dgaf284.
- Lumsden M.A., Dekkers O.M., Faubion S.S., et al. European Society of Endocrinology clinical practice guideline for evaluation and management of menopause and the perimenopause. European Journal of Endocrinology. 2025; 193 (4): G49-G81. doi: 10.1093/ejendo/lvaf206.
- Nadolsky K., Garvey W.T., Agarwal M., et al. American Association of Clinical Endocrinology consensus statement: algorithm for the evaluation and treatment of adults with obesity/adiposity-based chronic disease – 2025 update. Endocrine Practice. 2025; 31 (11): 1351-1394. doi: 10.1016/j.eprac.2025.07.017.