Цукровий діабет 2 типу й сепсис: сучасний стан проблеми та доказів
Переклала й адаптувала канд. мед. наук Ольга Королюк
Сепсис – це загрозлива для життя дисфункція органів, спричинена порушеннями реакції макроорганізму на інфекцію. Лише 2017 р. у світі зареєстровано майже 50 мільйонів випадків сепсису та 11 мільйонів смертей, тобто п’ята частина від загальної кількості смертей.
Збільшення чисельності людей похилого віку, яким притаманні поліморбідність, фізіологічна слабкість та імунне старіння, дає змогу прогнозувати подальше підвищення рівня смертності від сепсису. Захворюваність на цукровий діабет (ЦД) 2 типу також невпинно зростає, а його поширеність невдовзі перевищить 700 мільйонів. Ускладнення, пов’язані з ЦД, є основною причиною госпіталізації, інвалідності та смертності. У пацієнтів із діабетом вищі ризик інфікування, показники колонізації резистентними збудниками, зокрема метицилінорезистентним золотистим стафілококом, у 2-6 разів вищий ризик виникнення сепсису порівняно із зіставними за віком групами без ЦД та вищий рівень смертності від сепсису. Отже, ЦД – поширена супутня хвороба серед пацієнтів із септичними станами. Дослідження тривалістю 25 років (1979-2003 рр.) вказує на 12,5 мільйонів випадків сепсису та 930 мільйонів невідкладних госпіталізацій, серед яких 17% пацієнтів мали ЦД. Хворі на ЦД становлять найбільшу популяцію, яка страждає від ускладнень сепсису, включно зі смертю. Незважаючи на сучасні вдосконалення діагностики й лікування, ЦД та сепсис залишаються поширеними станами в усьому світі з високою летальністю й вартістю лікування.
Взаємодія між ЦД 2 типу та сепсисом
Для ЦД 2 типу характерна стійка гіперглікемія, зумовлена зниженням секреції інсуліну та чутливості до нього тканин. Реакцію макроорганізму на інфекцію порушує низка метаболічних розладів, зокрема інсулінорезистентність і запалення, спричинені хронічною або стресовою гіперглікемією, а також супутніми ожирінням і дисліпідемією. Крім того, сепсис несприятливо впливає на імунну систему, порушуючи тривалість життя, генерацію та функцію адаптивних і вроджених імунних клітин, що порушує імунний гомеостаз. На рисунку узагальнено сучасні знання про механізми впливу сепсису й наслідків хронічної гіперглікемії на імунну систему та несприятливі клінічні результати.
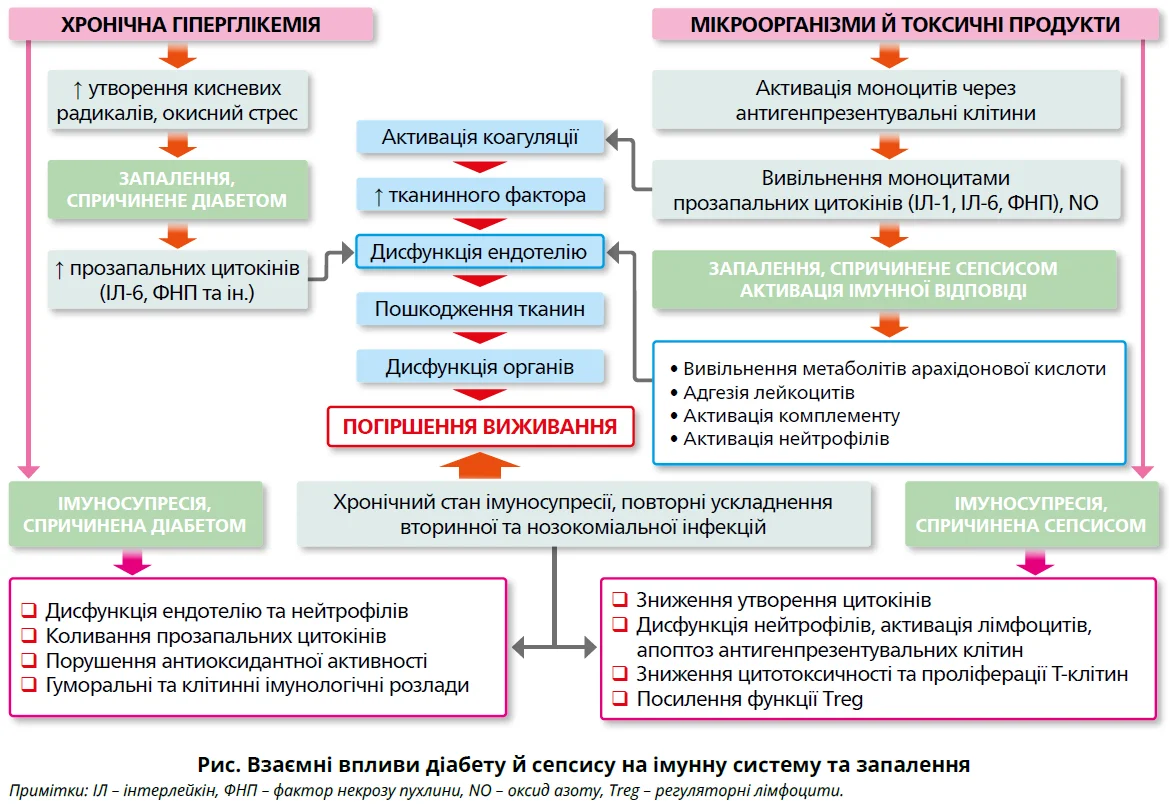
Преморбідні модифікаториризику сепсису
Тривалий контроль глікемії та ризик сепсису
Глікований гемоглобін (HbA1c) відображає процес повільного неферментативного приєднання глюкози до гемоглобіну за умови хронічної гіперглікемії. Цей показник є маркером довготривалої регуляції глюкози та показником ризику ускладнень ЦД. У разі сепсису HbA1c дає змогу відрізнити осіб без діабету зі стресовою гіперглікемією від пацієнтів із невстановленим ЦД. Порівнюючи фактичні значення глюкози в крові з рівнями HbA1c до госпіталізації, можна також ідентифікувати стресове погіршення глікемії в пацієнтів зі встановленим ЦД.
Нещодавній огляд високоякісних популяційних епідеміологічних досліджень вказує, що рівень HbA1c >7-8% асоціюється з підвищеним у 1,5-3,5 рази ризиком інфекції у хворих на ЦД. Ретроспективне когортне дослідження за участю понад 150 тисяч пацієнтів, серед яких майже 85 тисяч із ЦД переважно 2 типу, підтвердило потужний зв’язок між поганим контролем глікемії та високим ризиком розвитку серйозних інфекцій, зокрема сепсису. Потреба госпіталізації з приводу інфекцій у пацієнтів із ЦД вища, ніж у пацієнтів без ЦД, незалежно від глікемічного контролю. Частота сепсису вища навіть серед пацієнтів із рівнями HbA1c <6%. Проте ризик госпіталізації в пацієнтів із поганим метаболічним контролем діабету втричі вищий. Загалом зафіксовано 15,7% пов’язаних з інфекцією смертей, 16,5% пов’язаних з інфекцією госпіталізацій і 20% випадків сепсису в пацієнтів зі значенням HbA1c поза межами 6-7%. Коефіцієнт захворюваності на сепсис коливався від 1,2 для HbA1c ≥7% до 3,64 для HbA1c ≥11%. Навіть жорсткий метаболічний контроль із рівнем HbA1c <6% асоціювався з підвищеним ризиком розвитку інфекцій в осіб похилого віку.
Отже, хоча є докази зниження ризику інфекцій за умови кращого контролю глікемії, потрібні подальші дослідження за участю пацієнтів похилого віку, осіб із поганим метаболічним контролем і значними інфекційними хворобами в анамнезі.
Вплив інсуліну й інших протидіабетичних засобів (ПДЗ) на захворюваність і смертність від сепсису
Імуномодулювальна дія інсуліну та неінсулінових ПДЗ відома. Є припущення про їхній сприятливий вплив на пацієнтів із ЦД та сепсисом. Інсулін може захищати від надмірної активації імунної системи, запобігати несприятливому впливу гіперглікемії на імунні функції, мати пряму та непряму протизапальну дію. Проте два великі обсерваційні дослідження не виявили різниці в смертності залежно від інсулінотерапії. Перше дослідження включало тяжкохворих осіб (серед них 7% із ЦД на інсулінотерапії). Встановлено, що хворі на ЦД, які отримували інсулін, хворіли тяжче, але рівень смертності в них не був вищим. У проспективному обсерваційному дослідженні за участю пацієнтів ізсепсисом у відділенні інтенсивної терапії (ВІТ) прогресування хвороби та смертність від сепсису в пацієнтів із ЦД не залежали від застосування інсуліну.
Доклінічні дослідження вказують на можливість імуномодулювального впливу інших ПДЗ. Зокрема, важливими плейотропними ефектами метформіну можуть бути регуляція метаболізму лактату, активація АМФ-активованої протеїнкінази, протизапальна, антиендотоксемічна, вазоактивна та протимікробна дії. Тіазолідиндіони (ТЗД) збільшують міграцію нейтрофілів, що свідчить про потенційні переваги стосовно модуляції запальної відповіді та клінічних результатів у пацієнтів із септичними станами. Показано протизапальну дію й імовірний імуномодулювальний вплив інкретинових гормонів, які беруть участь у запальній відповіді. Доклінічні моделі сепсису продемонстрували, що терапія на основі інкретину знижує активацію імунних клітин, пригнічує вивільнення прозапальних цитокінів, зменшує дисфункцію органів і смертність. Хоча терапія на основі інкретину ще не перевірена в клінічних дослідженнях сепсису, є ймовірність позитивного плейотропного ефекту інкретиноміметиків та інгібіторів дипептидилпептидази-4 (ДПП-4) на запалення й імуномодуляцію. Щодо секретогенів інсуліну, то доклінічні дослідження демонструють можливість погіршення імунної відповіді на патогенні мікроорганізми внаслідок пригнічення чутливого до аденозинтрифосфату калієвого каналу β-клітин.
Результати великого дослідження «випадок – контроль», в якому аналізували вплив поточного лікування неінсуліновими препаратами на частоту сепсису, вказують на тривалі переваги метформіну щодо частоти госпіталізації з приводу сепсису. На відміну від меглітиніду, застосування ТЗД мало зворотний зв’язок із виникненням сепсису. Лікування похідними сульфонілсечовини й інгібіторами ДПП-4 не змінювало частоти сепсису. Нещодавній метааналіз вказує на зниження смертності у хворих на ЦД із сепсисом за умови застосування метформіну. Проте надійність цього висновку обмежена відносно невеликим розміром вибірки. Більш пізнє та масштабне популяційне когортне дослідження свідчить, що лікування метформіном суттєво не пов’язане ані з ризиком сепсису, ані з 30-денною смертністю в пацієнтів із ЦД. Невеликі клінічні дослідження за участю пацієнтів у критичному стані показали потенційні переваги інфузії інкретину щодо контролю глікемії. Проте ці дослідження включали змішані групи пацієнтів і мали обмежену силу доказовості.
Відповідно, зв’язок між попереднім застосуванням ПДЗ та ризиком і клінічними наслідками сепсису залишається суперечливим. Ризик і смертність від сепсису радше залежать від ступеня глікемічного контролю, а не протидіабетичної терапії. Невелике обсерваційне дослідження вказує, що HbA1c є незалежним прогностичним чинником госпітальної смертності та тривалості госпіталізації для септичних пацієнтів із ЦД, а також на відсутність різниці впливу попереднього лікування ПДЗ на клінічні результати. Для встановлення потенційних переваг ПДЗ у септичних когортах потрібні подальші клінічні дослідження.
Оптимальний контроль глікемії під час сепсису
Під час сепсису змінюються циркулювальні рівні інсуліну та кортизолу, що призводить до значних коливань рівня глюкози, пошкодження органів і активації імунної системи. Крім стресової гіперглікемії, внаслідок патологічної реакції на стрес можлива гіпоглікемія. Гіпоглікемія зазвичай асоціюється із сепсисом і вважається епіфеноменом серйозної дисфункції органів, що передує смерті. Хоча механізми та взаємозв’язки між гіпоглікемією й тяжкістю перебігу сепсису не цілком зрозумілі, вказують на роль запальних цитокінів. У критичних ситуаціях порушення глікемічного контролю асоціюється з тяжчим перебігом і гіршим прогнозом. Утім, ЦД може модулювати зв’язок між дисглікемією та смертністю при сепсисі. Ризик пов’язаної з гіперглікемією смертності у хворих на ЦД нижчий, аніж в інших пацієнтів; на ризик не впливають варіабельність глікемії та гіпоглікемія.
Незважаючи на сильні рекомендації щодо раннього введення інсуліну, питання контролю та лікування стресової гіперглікемії залишаються дискусійними. Декілька великих досліджень вивчали оптимальний контроль гострої гіперглікемії в критичних пацієнтів, зокрема й септичних. Лише невеликі дослідження включали винятково пацієнтів із сепсисом. Жодне з них не було спрямоване на когорту ЦД. В одному з досліджень пацієнтів, госпіталізованих до ВІТ, рандомізували до груп інтенсивної інсулінотерапії з цільовим рівнем глікемії 80-110 мг/дл або традиційної терапії з цільовими показниками 180-200 мг/дл. Попри відсутність інформації про число пацієнтів із септичними станами на початковому етапі інтенсивна інсулінотерапія сприяла зменшенню кількості епізодів внутрішньолікарняної септицемії майже на 46%, а також частки пацієнтів, які потребували тривалої антибіотикотерапії.
Жорсткий контроль глікемії (<110 мг/дл) асоціювався з нижчими рівнями захворюваності та відносним зниженням ризику смертності у ВІТ на 43%. Проте позитивний результат стосувався насамперед підгрупи, що перебувала у ВІТ понад 5 днів, а також кардіохірургічних пацієнтів, які раніше отримували інфузії глюкози з метою харчування. У пізнішому дослідженні показано, що жорсткий контроль глікемії запобігав захворюваності в усіх пацієнтів ВІТ, але знижував смертність лише в тих, хто перебував у ВІТ ≥3 дні. Поза тим у цій підгрупі відзначено високий рівень гіпоглікемічних явищ (більш як ушестеро вищий, аніж у попередньому дослідженні). Аналіз post hoc об’єднаних даних двох досліджень також підтвердив, що жорсткий контроль глікемії посилює ризик гіпоглікемії: 11,3 проти 1,8% у групі звичайної інсулінотерапії (p<0,0001). Гіпоглікемія не була пов’язана з ранньою смертю та/або неврологічними наслідками, але підвищувала ризик смерті. Жорсткий контроль значно знижував захворюваність і смертність пацієнтів ВІТ (особливо за умови перебування понад 3 дні) в усіх підгрупах, зокрема із сепсисом. Утім, позитивного впливу на виживання не було
у хворих на ЦД. Подальші дослідження не підтвердили переваг жорсткого контролю, хоча відмінності в дизайні досліджень, відборі пацієнтів, підтримці харчування, вимірюванні глікемії та цільових діапазонах ускладнюють порівняння. Ще одне дослідження за участю пацієнтів із тяжким сепсисом не лише не продемонструвало переваги жорсткого контролю щодо смертності в пацієнтів із ЦД та без нього, але й було припинено завчасно з міркувань безпеки через збільшення частоти тяжких гіпоглікемій.
У широкомасштабних дослідженнях Glucontrol і NICE-SUGAR за участю змішаних популяцій медичних і хірургічних пацієнтів повідомлялося про вищу частоту гіпоглікемій у групі жорсткого контролю. Перше дослідження припинене достроково через високий рівень ненавмисних порушень протоколу. Відмінностей у смертності в підгрупі жорсткого контролю не виявлено. Інше дослідження показало, що менш суворий контроль глікемії призводить до зниження рівня смертності, незалежно від ЦД. Нещодавній метааналіз підтвердив відсутність клінічних переваг суворого глікемічного контролю щодо смертності. У групі жорсткого контролю відзначено вищу частоту гіпоглікемій у пацієнтів із ЦД та без нього порівняно з групами з цільовими рівнями глікемії 140-180 і 180-220 мг/дл.
Взаємозв’язок між контролем глікемії та смертністю U-подібний: гірші клінічні наслідки в пацієнтів із низьким і високим рівнями глікемії порівняно з пацієнтами з еуглікемією або помірною гіперглікемією. Проте питання, чи цей ефект зумовлений саме глікемією чи іншими чинниками, залишається відкритим. Окрім того, зв’язок між тривалішим часом у діапазоні глікемії від 70 до 140 мг/дл і нижчим рівнем смертності чітко простежується в пацієнтів без ЦД, але відсутній у хворих на діабет. Сучасні настанови рекомендують критичним пацієнтам цільові значення глікемії в межах 140-180 мг/дл, незалежно від наявності ЦД. Обговорюється потреба вивчення конкретних цільових рівнів глікемічного контролю в пацієнтів із ЦД.
Припускають, що менш суворий контроль глікемії на рівні 180-250 мг/дл може бути сприятливим у критичних пацієнтів із преморбідною хронічною гіперглікемією (HbA1c >7%, або >53 ммоль/моль). Однак у критичних пацієнтів із ЦД запропоновані рівні можуть підвищити ризик інфекції, глюкозурії та полінейропатії. Тому запропоновано прийняти єдиний цільовий рівень глюкози в крові для пацієнтів із ЦД та без нього ≤180 мг/дл. Триває рандомізоване контрольоване дослідження (РКД) LUCID (Liberal Glucose Control in Critically Ill Patients with Preexisting Type 2 Diabetes), яке вивчає переваги та ризики більш ліберальних стратегій контролю глікемії. Для уникнення гіпоглікемії під час інсулінотерапії та контролю підвищених рівнів циркулювальних цитокінів у хворих на ЦД із тяжким сепсисом
і септичним шоком запропоновано замкнуті системи контролю глюкози та варіанти імуномодулювальної терапії.
Гостра органна дисфункція під час сепсису
Частоту виникнення дисфункції органів у хворих на ЦД із сепсисом уперше оцінено в дослідженні, котре включало 12,5 мільйонів людей, госпіталізованих із приводу сепсису в період 1979-2003 рр., з яких понад 2 мільйони мали ЦД. Встановлено, що у хворих на ЦД рідше виникала гостра дихальна недостатність (9 проти 14% у пацієнтів без ЦД, p<0,05), незалежно від джерела інфекції, але частіше виникала гостра ниркова недостатність (13 проти 7%, p<0,05). Частота дисфункції інших органів істотно не відрізнялася.
Як при сепсисі, так і при хронічній гіперглікемії пошкодження глікокаліксу внаслідок утворення активних форм кисню й медіаторів запалення впливає на мікроциркуляцію та призводить до ураження органів. Поєднання тяжкого сепсису з ЦД погіршує пластичність еритроцитів і мікроциркуляцію, прискорюючи дисфункцію органів. Нещодавнє ретроспективне обсерваційне дослідження підтверджує зв’язок між преморбідною хронічною гіперглікемією та виникненням дисфункції органів у пацієнтів із сепсисом. У пацієнтів, госпіталізованих у ВІТ із септичними станами, значення HbA1c ≥6,5 незалежно асоціювалися з прогресуванням печінкової та ниркової недостатності впродовж 72 годин і смертністю у ВІТ. Повідомлялося про позитивну тенденцію щодо прогресування легеневої та серцевої дисфункцій і порушень зсідання крові. Велике загальнонаціональне ретроспективне дослідження та нещодавній метааналіз підтвердили менший ризик гострої респіраторної дисфункції, але вищий ризик гострого ураження нирок у хворих на ЦД.
Гостра дихальна недостатність
Гостре пошкодження легень (ГПЛ) і гострий респіраторний дистрес-синдром (ГРДС) – поширені загрозливі для життя стани в критичних пацієнтів. Захисна роль ЦД щодо виникнення ГПЛ/ГРДС описана в різних когортах пацієнтів із сепсисом і критично хворих осіб. Потенційні механізми такого захисного ефекту досі не з’ясовані, а нещодавній метааналіз поставив під сумнів цей факт, продемонструвавши подібну частоту дихальної дисфункції у хворих на сепсис із ЦД та без нього.
Серед можливих механізмів розглядають порушення функції нейтрофілів та їх взаємодії з ендотелієм, опосередковані гіперглікемією імуномодулювальні ефекти, що призводять до зміни реакції на пошкодження ендотоксинами, а також метаболічні впливи ожиріння та дисліпідемії. Потенційні захисні ефекти можуть бути пов’язані з наданням ранньої всебічної медичної допомоги та протизапальними властивостями ПДЗ (інсуліну, ТЗД, метформіну). Досі незрозуміло, чи діабет спричиняє збільшення частоти дисфункції інших органів у разі сепсису та як саме це відбувається.
Гостре пошкодження нирок (ГПН)
У чверті пацієнтів із сепсисом і в половини пацієнтів із бактеріємією або шоком виникає ГПН. За даними обсерваційних досліджень, у пацієнтів із ЦД частота ГПН коливається від 27 до 73%. Хоча ЦД посилює ризик як ГПН, так і сепсису та вважається незалежним чинником ризику стійкої ниркової дисфункції в пацієнтів ВІТ із септичними станами, його вплив на підвищення ризику ГПН залишається дискусійним.
В одноцентровому проспективному дослідженні у ВІТ підвищення рівня креатиніну в сироватці крові в першу добу асоціювалося з виникненням ГПН у пацієнтів із тяжким сепсисом, але не в пацієнтів із ЦД. У пізнішому великому багатоцентровому перехресному дослідженні за участю пацієнтів із тяжким сепсисом або септичним шоком ЦД не асоціювався з виникненням ГПН або потребою замісної ниркової терапії. Незважаючи на ці висновки та значну гетерогенність даних, пов’язаних із захворюваністю на ГПН у пацієнтів із ЦД та сепсисом, метааналіз підтвердив, що захворюваність на ГПН у хворих на ЦД однозначно вища (понад 50%) порівняно з пацієнтами без ЦД.
Смертність від сепсису
На підвищену сприйнятливість до інфекції та сепсису при ЦД вказує багато літературних джерел, але неоднозначні результати епідеміологічних досліджень викликають сумніви щодо зв’язку між ЦД і вищим ризиком захворюваності та смертності, пов’язаної з інфекцією. Вивчали різні популяції, зокрема з відсутністю поділу на ЦД 1 та 2 типів, різним корегуванням коморбідності, різною етіологією сепсису, тяжкості хвороби, схемами введення ПДЗ та методами вимірювання результатів. Масштабне обсерваційне дослідження вказує на підвищену смертність від інфекцій у пацієнтів із ЦД навіть після корегування супутніх захворювань і вдвічі вищий ризик смертності від сепсису порівняно із загальною популяцією. Два великі ретроспективні когортні дослідження виявили вищий рівень смертності, пов’язаної з інфекціями, у хворих на ЦД порівняно з пацієнтами без ЦД, тоді як сім досліджень не підтвердили такої асоціації. Одне дослідження повідомило про краще виживання хворих на ЦД. Два обсерваційні дослідження вивчали зв’язок між преморбідним глікемічним станом і наслідками сепсису. Встановлено, що рівень HbA1c на момент госпіталізації прямо пов’язаний із госпітальною смертністю пацієнтів із ЦД та сепсисом. Це підтвердив метааналіз, який продемонстрував відсутність зв’язку ЦД із несприятливими наслідками в пацієнтів із сепсисом. Деякі дослідження свідчать про зв’язок між гіперглікемією та підвищеною смертністю в пацієнтів без ЦД, на відміну від пацієнтів із ЦД. Цей факт дає змогу припускати різні патофізіологічні ефекти гострої гіперглікемії в пацієнтів із ЦД та без нього. Треба з’ясувати, чи зв’язок між гіперглікемією та смертністю у хворих без ЦД зумовлений токсичним впливом гіперглікемії, чи є ознакою тяжкості захворювання. Серед потенційних механізмів захисного впливу ЦД обговорюються посилення імунної адаптації внаслідок попередньої гіперглікемії, роль запалення, рівні цитокінів, прокоагулянтна реакція. До інших можливих механізмів віднесено сприятливий ефект уведення інсуліну, запобігання ГПЛ, адаптацію до попереднього окисного стресу та споживання нутрієнтів у пацієнтів з ожирінням і ЦД.
Висновки
Сепсис спричиняє значний відсоток загальної смертності, його поширеність у світі зростає. Частим коморбідним станом у септичних пацієнтів є ЦД. Незважаючи на високий ризик інфікування у хворих на ЦД, вплив діабету на клінічні наслідки сепсису та їхні патогенетичні механізми досі не з’ясовані. Критичні питання, котрі потребують з’ясування, включають вплив діабету й сепсису на імунну систему, роль контролю глікемії та потенційну захисну роль ПДЗ у виникненні сепсису та його наслідків, включаючи ризик гострого ураження нирок і легень. Рекомендації щодо цільових показників глікемії під час сепсису не мають переконливих доказів. Їх з’ясування потребує масштабних проспективних РКД за участю пацієнтів із сепсисом і ЦД. Важливими є питання відношення ризику та користі більш ліберального контролю гострої гіперглікемії, а також варіанти лікування з імуномодулювальним впливом на патогенетичні механізми сепсису та ЦД 2 типу, які забезпечили би покращення клінічних результатів.
Література
Costantini E., Carlin M., Porta M., Brizzi M.F. Type 2 diabetes mellitus and sepsis: state of the art, certainties and missing evidence. Acta Diabetol. 2021; 58 (9): 1139-1151. doi: 10.1007/s00592-021-01728-4.
