Чи може інтервальне голодування застосовуватися у лікуванні цукрового діабету?
Переклала та адаптувала канд. мед. наук Лариса Стрільчук
Цукровий діабет (ЦД) 2 типу є поширеним метаболічним захворюванням, що характеризується гіперглікемією, спричиненою низкою факторів: порушенням секреції інсуліну, інсулінорезистентністю (ІР), зниженою утилізацією глюкози, надмірним виробленням глюкози у печінці та системним запаленням низького рівня [1]. Відповідно до статистичних даних Центрів з контролю та профілактики захворювань США, на діабет хворіють 34,2 млн жителів США (10,5% загальної популяції) [2]. ЦД спричиняє численні віддалені ускладнення, які сприяють підвищенню захворюваності та смертності. Так, діабет є провідною причиною ниркової недостатності, сліпоти та нетравматичної ампутації нижніх кінцівок у США [3].
Ускладнення ЦД можуть мати судинну і несудинну природу. Судинні ускладнення включають ретинопатію, набряк макули, моно- та полінейропатію, автономну дисфункцію, нефропатію, ішемічну хворобу серця, хвороби периферичних судин та інсульт, а несудинні — розлади з боку травної системи (гастропарез), зміни кольору шкіри, підвищений ризик інфекції, катаракту, глаукому, пародонтоз, втрату слуху [3]. На сьогодні завданнями лікування ЦД 2 типу є профілактика або відтермінування ускладнень і збереження якості життя пацієнта [4].
Пацієнтів із ЦД 2 типу слід заохочувати до зміни способу життя, у тому числі підвищення фізичної активності та зниження маси тіла. Для досягнення контролю рівня глюкози крові більшість пацієнтів потребують застосування лікарських препаратів [5]. Хоча добре відомо, що в основі ЦД 2 типу лежить ІР, значна кількість методів фармакотерапії цієї хвороби ґрунтується на забезпеченні більшої кількості інсуліну у пацієнта. Наприклад, такі препарати, як похідні сульфонілсечовини, агоністи глюкагоноподібного пептиду‑1, інгібітори дипептидилпептидази‑4 та інсуліни, діють або шляхом підвищення ендогенного вироблення інсуліну, або збільшення надходження екзогенного інсуліну. Таке лікування дозволяє зменшити гіперглікемію у цих пацієнтів. Однак концепція лікування хвороби, в основі якої лежить ІР, за допомогою збільшення вмісту інсуліну, може бути контрпродуктивною, оскільки з часом потреба у фармакотерапії зростає. Henry та співавт. [6] показали: інтенсивна інсулінотерапія із досягненням суворого контролю глікемії в осіб з ЦД 2 типу призвела до того, що через 6 місяців лікування у всіх пацієнтів розвинулася значна гіперінсулінемія та зросла маса тіла.
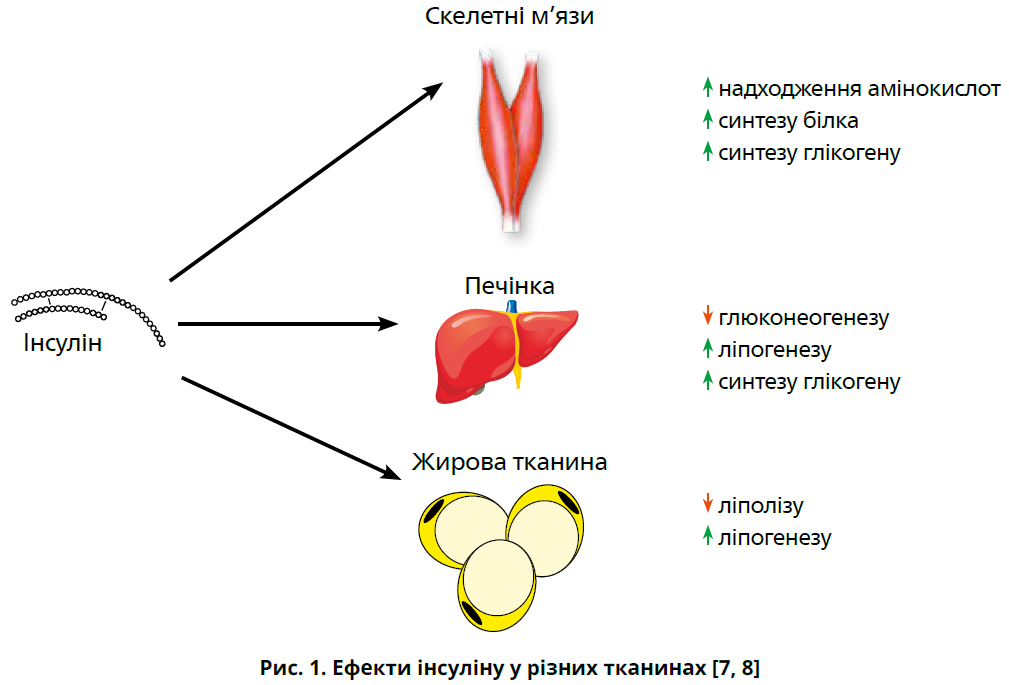
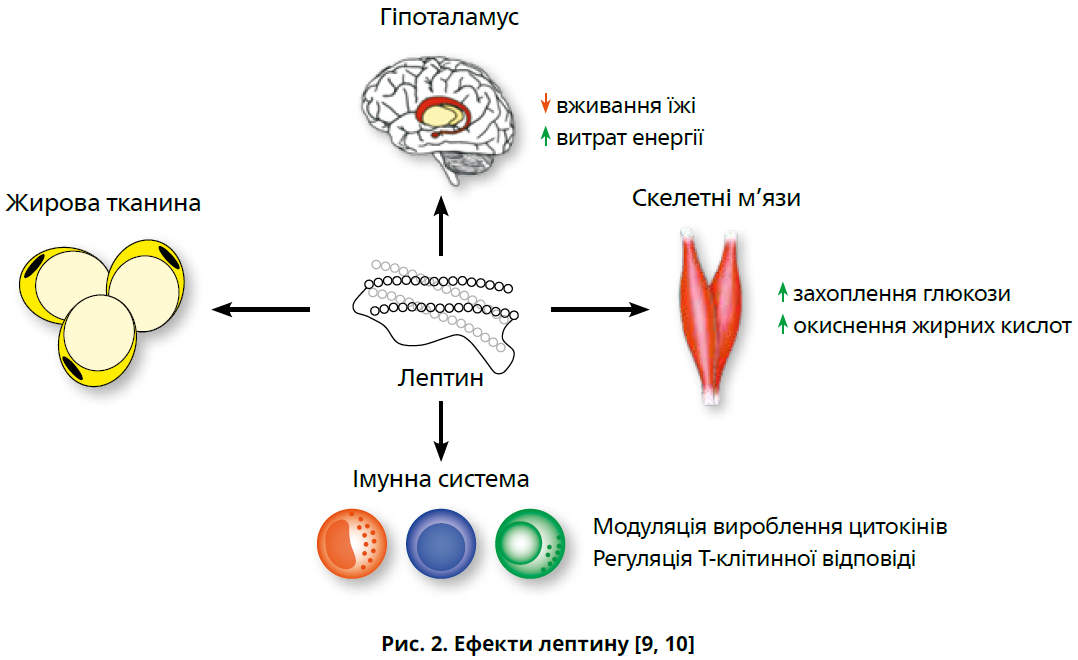
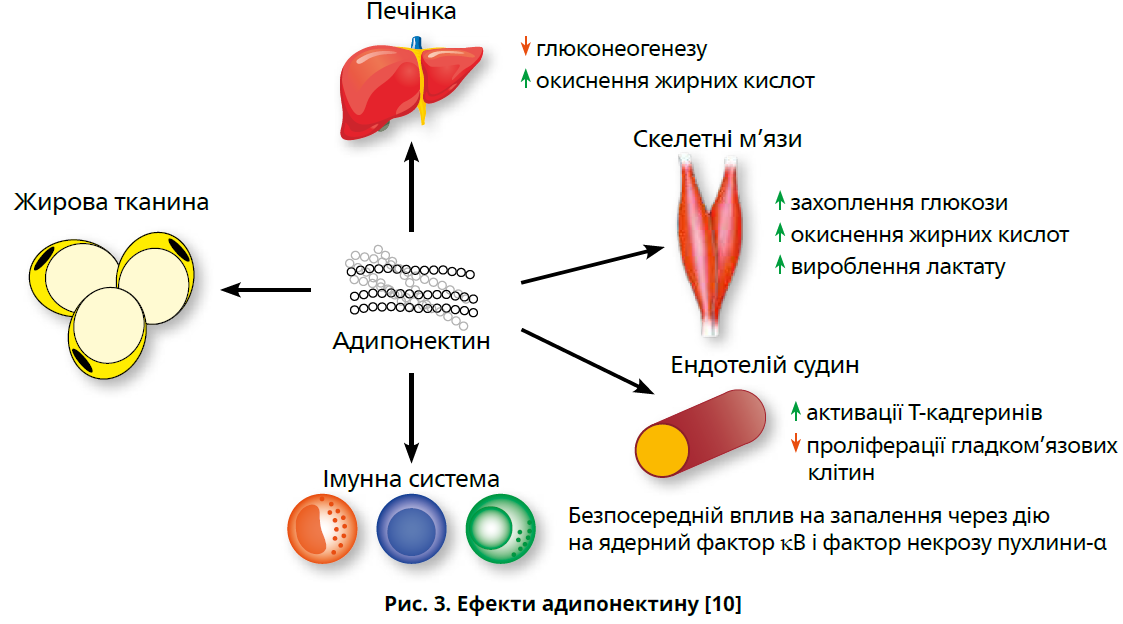
Метою цього огляду є ретельний розгляд інтервального голодування (ІГ) як опції немедикаментозного лікування ЦД 2 типу за рахунок покращення чутливості до інсуліну. Аналізуючи лікувальну роль ІГ у пацієнтів з діабетом, слід звернути увагу на три гормони, які, імовірно, відіграють важливу роль у процесах контролю маси тіла, а саме — на інсулін та адипокіни лептин і адипонектин (рис. 1-3). Цей огляд має на меті пояснити вплив зазначених гормонів на розвиток ІР та ЦД 2 типу, а також сприятливі ефекти ІГ стосовно цих метаболічних маркерів.
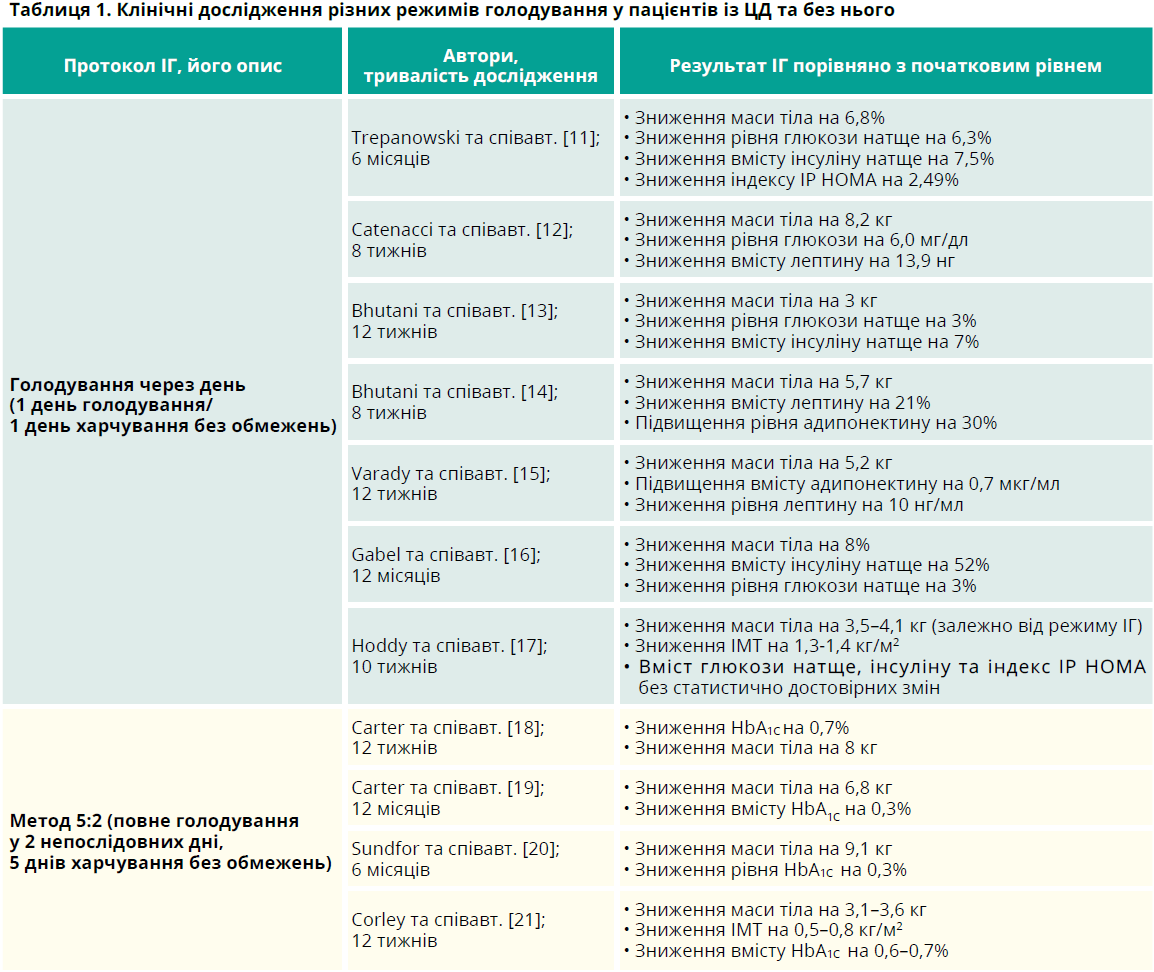
Було виконано огляд матеріалів баз даних PubMed, Google Scholar та Ovid MEDLINE за 1990–2020 рр., а також сайтів відповідних фахових організацій (Американська асоціація діабету, Європейська асоціація з вивчення діабету). В огляд були включені дослідження, присвячені трьом найбільш поширеним видам ІГ (повне голодування через день, періодичне голодування, обмеження часового проміжку прийому їжі), які передбачали визначення глюкози натще, глікозильованого гемоглобіну (HbA1C), інсуліну натще, лептину чи адипонектину. При первинному пошуку було знайдено 6852 дослідження, 17 із яких було включено до детального огляду (табл. 1 та 2).
Що таке ІГ?
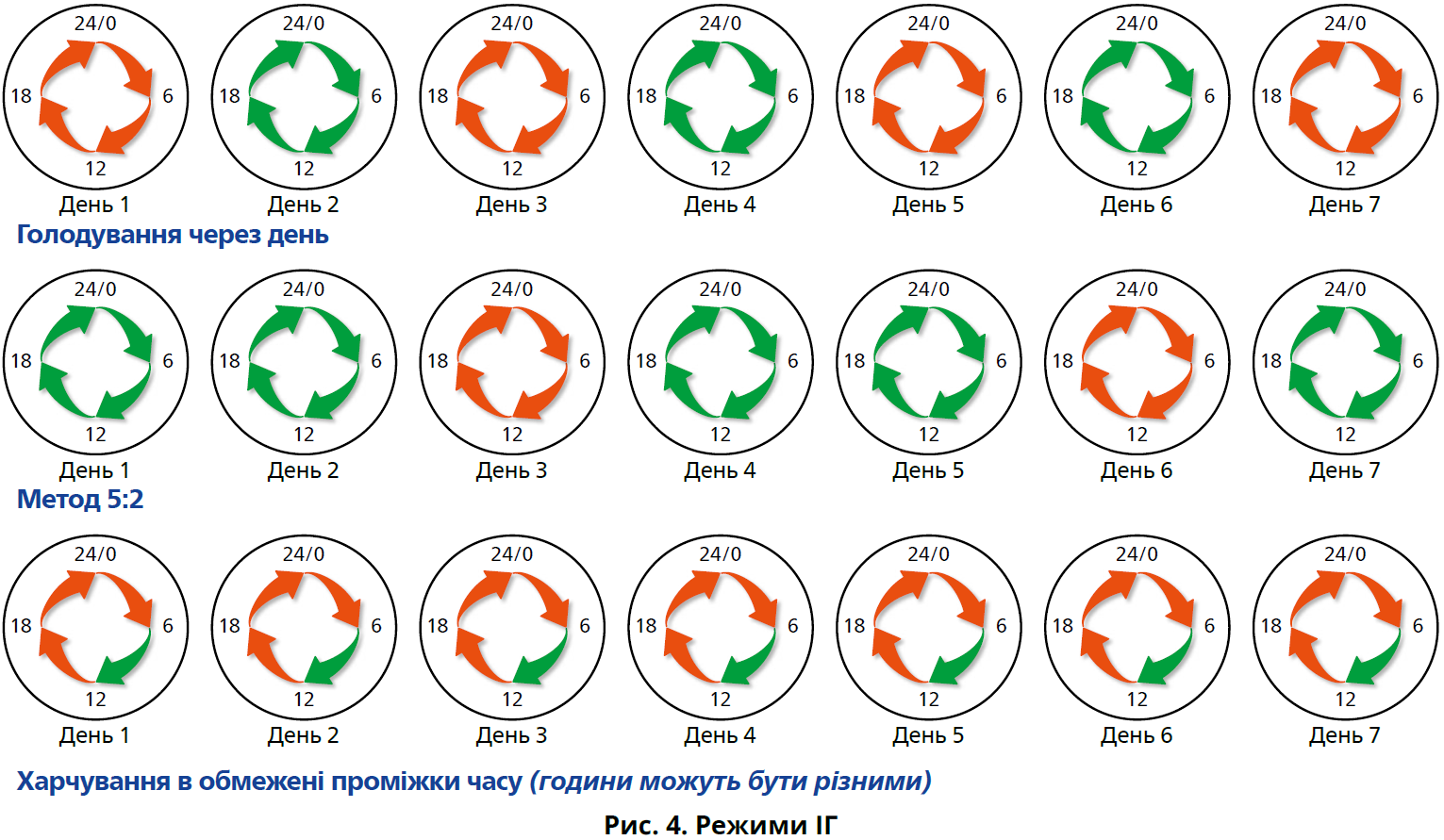
Протягом останнього часу ІГ стало популярним методом покращення якісного складу тіла та метаболічного здоров’я [28, 29]. Поняття «інтервальне голодування» стосується патернів харчування, побудованих на принципі відмови від їжі або споживання дуже малої кількості калорій протягом від 12 год до кількох днів на регулярній основі [28]. Виділяють кілька різних режимів ІГ. Одним із таких режимів є голодування через день, при якому дні голодування чергуються з днями споживання їжі без жодних обмежень [29]. Іншим методом є періодичне голодування, при якому слід голодувати протягом 1–2 днів на тиждень (в літературі часто називають голодуванням 5:2 або 6:1) [29]. Найбільш поширеним методом є харчування, обмежене у часі: вживання їжі дозволено лише у певний час доби (харчове вікно), який, зазвичай, становить 4–8 год [29]. Схеми найбільш вивчених режимів ІГ представлені на рисунку 4.
ІГ, зниження маси тіла та контроль апетиту
Ожиріння є значущим фактором ризику розвитку ЦД 2 типу. Наявні кілька механізмів розвитку ІР в осіб з ожирінням, які включають хронічне системне запалення й ектопічне накопичення ліпідів [7, 9, 30, 31].
Вісцеральна жирова тканина функціонує як паракринний та ендокринний орган, секретуючи адипокіни [10]. Ці адипокіни є або прозапальними агентами, які спричиняють хронічне запалення низького рівня, як-от лептин, або протизапальними молекулами, як-от адипонектин [10]. Відомо, що лептин відіграє роль у регуляції маси тіла за рахунок активації сигнальних шляхів у гіпоталамусі та інших ділянках мозку із пригніченням вживання їжі та збільшенням витрат енергії [9]. Прозапальні ефекти лептину, імовірно, опосередковані його роллю у виробленні інтерлейкіну‑6, який індукує синтез C‑реактивного білка у печінці та збільшення експресії прозапального фактора некрозу пухлини-α [10]. Примітно, що у пацієнтів із високим ІМТ та ІР часто спостерігають підвищений рівень лептину. Це може свідчити про те, що в осіб з ожирінням та ІР розвивається і лептинорезистентність [10].
Адипонектину, навпаки, притаманні антидіабетичний і протизапальний ефекти. Адипонектин діє на численні рецептори, спричиняючи посилене окиснення жирних кислот у скелетних м’язах і печінці, зменшуючи глюконеогенез у печінці та підвищуючи захоплення глюкози [10]. Цей гормон також чинить протизапальний ефект за рахунок безпосереднього впливу на запальні клітини, ядерний фактор kB та фактор некрозу пухлини-α [10]. У міру накопичення вісцерального жиру рівень адипонектину знижується [10]. López-Jaramillo та співавт. виконали огляд літератури з метою визначення рівнів лептину й адипонектину у пацієнтів із метаболічним синдромом. Було з’ясовано, що у пацієнтів з метаболічним синдромом, який включає ожиріння та ІР, дисбаланс рівнів лептину й адипонектину сприяє метаболічним змінам та підвищує ризик розвитку ЦД 2 типу [10]. Примітно, що у кількох дослідженнях продемонстровано, що ІГ, навіть за відсутності втрати жирової маси, призводило до зниження рівня лептину та підвищення рівня адипонектину, внаслідок чого зростала чутливість до інсуліну [32].
Давно відомо, що обмеження калорійності раціону може зменшувати масу тіла та покращувати метаболічне здоров’я [33]. Larson-Meyer та співавт. [34] продемонстрували, що зменшення спожитих калорій на 25% за допомогою дієти або поєднання дієти із фізичним навантаженням сприяє підвищенню інсуліночутливості в осіб з надлишковою масою тіла та нормальною толерантністю до глюкози. Однак у дослідженні за участю осіб з тяжким ожирінням встановлено, що людям дуже складно дотримуватися щоденного обмеження калорій протягом тривалого часу [28]. Показано, що ІГ здатне зменшувати вираженість метаболічних факторів ризику, покращувати якісний склад тіла та сприяти зменшенню маси тіла в осіб з ожирінням [28, 35, 36]. Ці сприятливі ефекти частково зумовлені зсувом метаболізму з утилізації глюкози до утилізації жирних кислот і кетонів. Унаслідок цієї метаболічної перебудови організм переходить від синтезу та накопичення ліпідів до їх мобілізації [28]. Помірний енергодефіцит, який має місце при ІГ, сприяє зменшенню вмісту жирової тканини в цілому та вісцерального жиру зокрема [12, 17]. Таке зменшення зумовлює нормалізацію рівнів лептину та адипонектину, збільшення чутливості до гормональних впливів, покращення контролю апетиту та зниження рівня хронічного запалення, одночасно впливаючи на кілька факторів ризику розвитку ЦД 2 типу.
ІГ та чутливість до інсуліну
Інсулін відіграє роль у гомеостазі глюкози завдяки впливу на накопичення й утилізацію глюкози. Однак ефекти інсуліну не обмежуються контролем гомеостазу глюкози. Крім цього, інсулін бере участь у стимуляції синтезу ДНК і РНК, рості та диференціації клітин, надходженні у клітину амінокислот, синтезі білків і пригніченні їх руйнування, стимуляції ліпогенезу та пригніченні ліполізу [8].
При ІР для досягнення глюкозознижувальної відповіді необхідний вищий рівень інсуліну у циркулюючій крові, ніж при нормальній чутливості до цього гормону. У зв’язку з цим ІР є основною патогенетичною ланкою ЦД 2 типу [7]. Регулюючи гомеостаз глюкози, інсулін діє передусім на рецептори скелетних м’язів, печінки та білої жирової тканини [7]. Основними ланками патогенезу ІР є підвищений вміст жиру й асоційоване із цим хронічне запалення [7].
Як було описано раніше, ІГ може знижувати вміст жирової тканини та, відповідно, ступінь ІР за рахунок зменшення кількості спожитих калорій і метаболічного перепрограмування. Крім того, зниження надходження енергії та нутрієнтів, яке досягається шляхом зменшення кількості спожитих калорій, сприяє більш здоровому старінню та зменшенню тягаря хронічних хвороб через посилення активації АМФ‑активованої протеїнкінази (ААПК) [37]. Підвищений рівень інсуліну внаслідок збільшеного надходження енергії або ІР призводить до активації медіаторів, які, навпаки, пригнічують ААПК. Роль ААПК у підвищенні чутливості до інсуліну найкраще відображають ефекти метформіну, який сприяє активації ААПК та знижує рівень глюкози при ЦД 2 типу [37]. Таким чином, зменшення надходження калорій при ІГ призводить до тривалого зниження продукції інсуліну та збільшення рівня ААПК,
що забезпечує покращення чутливості до інсуліну та нормалізацію гомеостазу глюкози.
ІГ як метод лікування ЦД 2 типу
У дослідженнях продемонстровано, що ІГ може стати потенційним методом лікування діабету (табл. 1 та 2). Дані систематичного огляду й метааналізу Cho та співавт. [32], що включав пацієнтів із предіабетом і нормальною толерантністю до глюкози, засвідчили, що через 4–24 тижні ІГ ІМТ учасників знизився на 0,75 кг/м2 порівняно з таким у контрольній групі. У групі ІГ також виявлено достовірне зниження рівня лептину та глюкози натще [32]. Furmli та співавт. спостерігали за трьома пацієнтами з ЦД 2 типу протягом кількох місяців ІГ у режимі трьох 24-годинних голодувань на тиждень. Упродовж цих місяців у всіх пацієнтів виявлено достовірне зниження рівня HbA1C та маси тіла; усім їм вдалося припинити лікування інсуліном [26]. Carter та співавт. [19] порівняли два режими ІГ (вживання 500–600 ккал/добу 2 дні на тиждень + звичайне харчування в інші дні та постійне вживання зменшеної кількості калорій на рівні 1200–1500 ккал/добу) у 137 дорослих із ЦД 2 типу. Через 12 місяців ІГ у обох групах спостерігали однакове зниження вмісту HbA1C, однак більш виражене зниження маси тіла супроводжувало перший режим. У схожому дослідженні Gabel та співавт. [16] порівнювали режим інтермітуючого ІГ (чергування вживання 25% калорій, необхідних для задоволення енергетичних потреб, із вживанням 125% калорій) та постійне обмеження надходження енергії (75% калорій, необхідних для задоволення енергетичних потреб, щоденно). Через 12 місяців зміни маси тіла, ІМТ та маси жирової тканини у цих групах були однаковими, але достовірне зниження рівня інсуліну натще (на 44%; р<0,05) та індексу ІР HOMA (на 53%; p<0,05) мало місце лише у групі обмеження калорійності через день [16].
Призначення ІГ в умовах клінічної практики
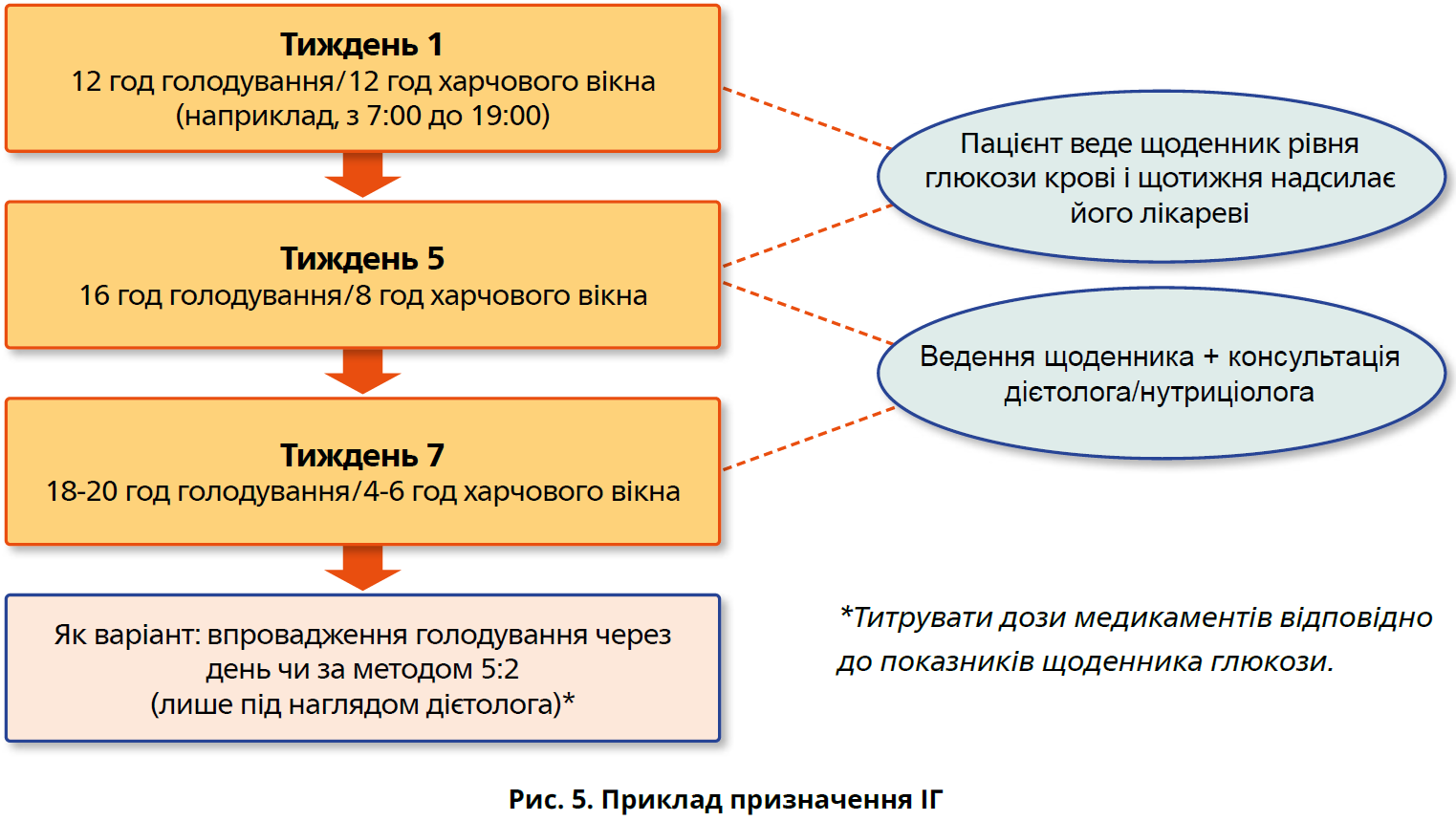
Хоча голодування через день та періодичне голодування продемонстрували високу ефективність у покращенні метаболічних факторів ризику, переконати пацієнта на 24 год відмовитися від їжі або різко зменшити сумарну калорійність раціону може бути складно. Значна частина людей їдять основні страви тричі на день та часто перекушують. Крім того, більшість соціальних заходів також передбачають вживання їжі. Тривале уникнення соціальних заходів з метою дотримання режиму харчування може стати тягарем для пацієнтів і негативно вплинути на їхню прихильність до лікування. У пацієнтів, які переходять на ІГ, на початку можуть спостерігатися такі симптоми, як голод і дратівливість, хоча ці симптоми зазвичай зникають впродовж перших 30 днів нового режиму харчування [38]. Таким чином, доцільно впроваджувати ІГ поступово, у формі обмеження часового проміжку, під час якого можна вживати їжу. Наприклад, клініцисти можуть рекомендувати пацієнтам відмовлятися від вживання їжі протягом 12 год на добу, зазвичай уночі, як-от з 19:00 до 7:00. Коли пацієнт адаптується до такого режиму харчування, можна збільшити обмеження, призначивши 16-годинне голодування та 8-годинне харчове вікно або 20-годинне голодування та 4-годинне харчове вікно. Пацієнт може сам обирати час доби, у який він зможе споживати їжу, що збільшує прихильність до ІГ. Зрештою, після адаптації до такого режиму можна переходити до повного голодування через день (рис. 5).
Розглядаючи застосування голодування в осіб з діабетом, слід врахувати кілька нюансів. По-перше, необхідно обговорити з пацієнтом потенційні ризики та питання безпеки. Пацієнти, які лікуються інсуліном або препаратами сульфонілсечовини, мають постійно перебувати під контролем лікуючого лікаря з метою профілактики гіпоглікемії [39]. За даними досліджень, дотримання протоколів ІГ супроводжується зниженням потреби в інсуліні, тому лікар має суворо контролювати рівень глюкози крові та пристосовувати дози препаратів до нового режиму харчування. Контроль може здійснюватися за допомогою щотижневої або щодвотижневої перевірки щоденників маси тіла та рівня глюкози, які пацієнт веде в електронному форматі та надсилає лікареві. Необхідно також моніторувати потенційний дефіцит вітамінів і мінералів та білка, хоча ці розлади є малоймовірними [39], та за потреби призначати відповідні добавки. Потрібно пояснити пацієнтам важливість належного вживання води, оскільки частина рідини надходить в організм з їжею, а при зменшенні кількості їжі може розвинутися зневоднення.
Голодування не рекомендоване вагітним і жінкам, які годують груддю, особам похилого віку, пацієнтам з імунодефіцитом, гіпоглікемією й особам з розладами харчової поведінки [39].
Висновки
Лише у США на ЦД 2 типу хворіють 34,2 млн осіб. Ця патологія асоційована зі значною захворюваністю та смертністю [1]. Хоча наріжним каменем діабету є ІР, більшість фармакопрепаратів для лікування цього захворювання сприяють підвищенню рівня інсуліну з метою досягнення кращого контролю глікемії. Це спричиняє такі несприятливі наслідки, як збільшення маси тіла, наростання ІР, підвищення рівня лептину та зниження рівня адипонектину.
Популярність ІГ як дієтологічного методу покращення якісного складу тіла та метаболічного здоров’я продовжує зростати [28, 29]. ІГ також є багатообіцяючим методом лікування ЦД 2 типу. Ефективність ІГ у цьому випадку може бути опосередкована його здатністю знижувати масу тіла, зменшувати ІР та чинити сприятливий вплив на концентрацію лептину й адипонектину [32]. Лікарі мають бути обізнані з перевагами ІГ у лікуванні ЦД 2 типу, що дозволить їм допомогти своїм пацієнтам у боротьбі з прогресуванням цієї хвороби.
Література
- Albosta M., Bakke J. Intermittent fasting: is there a role in the treatment of diabetes? A review of the literature and guide for primary care physicians. Clin Diabetes Endocrinol. 2021; 7, 3. https://doi.org/10.1186/s40842-020-00116-1.
Коментар фахівця
 Анастасія Соколова лікар-ендокринолог першої категорії, лікар-дієтолог, Національний медичний університет імені О.О. Богомольця, м. Київ
Анастасія Соколова лікар-ендокринолог першої категорії, лікар-дієтолог, Національний медичний університет імені О.О. Богомольця, м. Київ
Цукровий діабет 2 типу — неінфекційна епідемія сучасного світу, тому дуже важливим є пошук ефективних методів компенсації та лікування цього захворювання. Одним із базових принципів лікування є застосування немедикаментозних заходів, яке включає правильне харчування. Правильне харчування людей з ЦД 2 типу впливає не тільки на показники глікемії, а й на масу тіла. Одним з ефективних сучасних методів нормалізації маси тіла є ІГ.
ІГ — це узагальнене поняття режиму харчування. В основі ІГ лежить принцип чергування періодів прийому їжі з періодами голодування. Як і у всіх принципах і схемах харчування, ІГ має низку безумовних переваг і недоліків. Основною безумовною перевагою цього методу, на мою думку, є вироблення правильних харчових звичок. Адже ІГ — це не тільки про їжу, а й про самоорганізацію та дисципліну, що є важливим кроком у компенсації ЦД 2 типу. Якщо говорити про ефективність ІГ з медичної точки зору, то є дані про його позитивний вплив на масу тіла, рівень глікозильованого гемоглобіну, показники глюкози, рівень лептину. При ІГ людина переходить на субкалорійне харчування (через обмеження часу для вживання їжі), що зумовлює ефективну нормалізацію маси тіла, підвищення чутливості до інсуліну та нормалізацію глікемічної кривої. Крім того, вживання їжі в конкретно визначений час і періоди голодування підвищують чутливість до лептину, тим самим покращується функція центру голоду та насичення у ядрах гіпоталамуса. Якщо говорити про недоліки методу, то слід відмітити труднощі, з якими стикається пацієнт під час ІГ. По-перше, це збалансованість раціону під час такого режиму. Адже коли є часове обмеження вживання їжі, то потрібно більш ретельно слідкувати за вітамінним та мікроелементним складом тарілки на кожний прийом їжі. Зменшення обсягу, калорійності їжі та кількості прийомів їжі не має впливати на якісний склад раціону. По-друге, дуже поширена думка, що у «неголодні» дні вживання їжі не має обмежень. Але це не зовсім так. Переїдання, одночасне вживання великої кількості продуктів, що містять швидкі вуглеводи, впливатимуть на показники глікемії і сприятимуть декомпенсації захворювання. Крім того, правильне збалансоване харчування осіб із ЦД 2 типу є обов’язковою складовою лікування. На жаль, не завжди ІГ є комфортним режимом харчування на всі випадки життя. По-третє, є група пацієнтів з ЦД 2 типу, яким не рекомендоване дотримання «голодних» днів з ендокринологічної точки зору. Вкрай важливим є щоденне споживання їжі для тих, хто перебуває на інсулінотерапії або терапії препаратами сульфонілсечовини. Адже голод підвищує ризик розвитку тяжкої гіпоглікемії, яка є небезпечним загрозливим станом для хворого на ЦД. Оскільки ЦД 2 типу є хронічним захворюванням, то і компенсацію потрібно підтримувати постійно. Бажано обирати саме той режим харчування, якого пацієнт зможе дотримуватися весь час. Якщо цим режимом харчування стане ІГ, то краще перебувати під ретельним наглядом ендокринолога-дієтолога, який при необхідності допоможе скоригувати раціон чи терапію.
Освітньо-практичний журнал Ендо Practise №1 2022