Case challenge «Пацієнт із метаболічно-асоційованим стеатогепатитом. Роль ендокринолога та гастроентеролога в лікуванні»
Підготувала канд. мед. наук Тетяна Можина
Вітчизняні лікарі активно застосовують сучасні можливості навчання, користуючись спеціалізованими платформами, які пропонують різноманітні онлайн- та офлайн-заходи. Нещодавно у медичному тренінг-центрі Школа Іноваційної Медицини (SIM) відбувся розбір клінічного випадку «Пацієнт із метаболічно-асоційованим стеатогепатитом. Роль ендокринолога та гастроентеролога в лікуванні», який представили одразу дві спікерки: завідувачка гастроентерологічного відділення, наукова співробітниця відділу діагностики та лікування метаболічних захворювань ДНУ «Центр інноваційних медичних технологій НАН України» Олена Бака та завідувачка відділу діабетології ДУ «Інститут ендокринології та обміну речовин ім. В.П. Комісаренка НАМН України», докторка медичних наук Любов Соколова.
Розпочала презентацію гастроентеролог Олена Бака, яка навела коротку історичну довідку щодо виникнення термінів «неалкогольна жирова хвороба печінки» (НАЖХП) та «неалкогольний стеатогепатит» (НАСГ). Вона нагадала, що у 2020 р. група міжнародних експертів порушила питання доцільності оновлення номенклатури та заміни терміна НАЖХП на «метаболічно-асоційована жирова хвороба печінки» (МАЖХП). Експерти вважали, що діагноз МАЖХП має ґрунтуватися на наявності метаболічної дисфункції, а не на відсутності інших станів. Міжнародна експертна група Європейської асоціації з вивчення печінки (EASL) підкреслювала можливість співіснування МАЖХП з іншими захворюваннями печінки та недоцільність включення посилання на вживання алкоголю в акронім.
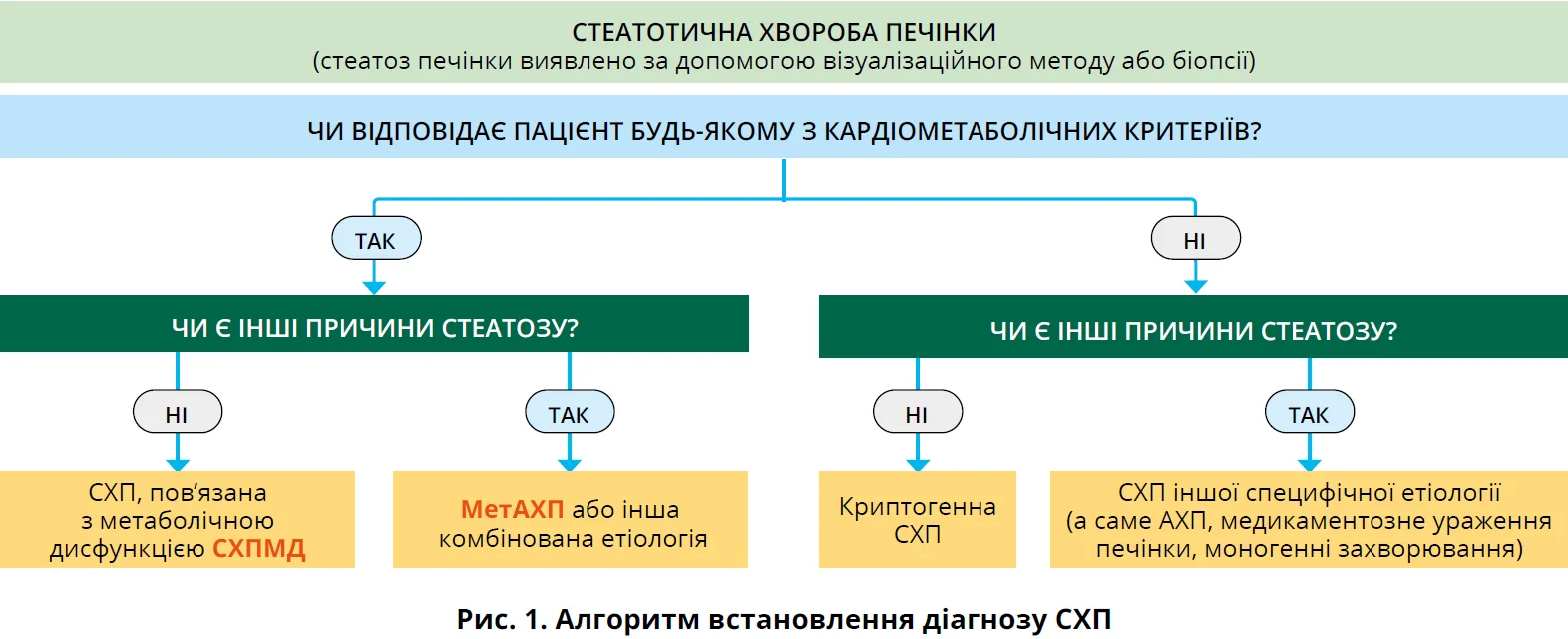
Ця класифікація використовувалася протягом неповних трьох років, тому що вже у 2023 р. три провідні міжнародні гепатологічні організації – EASL, Американська асоціація з вивчення захворювань печінки (AASLD), Латиноамериканська асоціація з вивчення печінки (ALEH) – презентували оновлену номенклатуру, згідно з якою лікарі в усьому світі мають діагностувати стеатотичну хворобу печінки (СХП) при виявленні ознак стеатозу печінки за допомогою візуалізаційних методів дослідження (рис. 1).
Відповідно до оновленої класифікації розрізняють СХП, пов’язану з метаболічною дисфункцією (СХПМД), СХП із підвищеним вживанням алкоголю (МетАХП), алкоголь-асоційовану хворобу печінки (АХП), СХП специфічної етіології і криптогенну СХП.
Діагностували СХП можна за наявності щонайменше одного з таких п’яти кардіометаболічних критеріїв:
- індекс маси тіла (ІМТ) ≥25 кг/м2 (для осіб азійського походження – 23 кг/м2), або окружність талії ≥94 см у чоловіків і ≥80 см у жінок, або етнічна приналежність;
- рівень глюкози натще ≥5,6 ммоль/л (100 мг/дл) або через 2 години після навантаження глюкозою ≥7,8 ммоль/л (≥140 мг/дл), або рівень глікозильованого гемоглобіну (HbA1c) ≥5,7% (39 ммоль/л), або наявність цукрового діабету (ЦД) 2-го типу в анамнезі, або лікування ЦД 2-го типу;
- артеріальний тиск ≥130/85 мм рт. ст. або специфічне лікування артеріальної гіпертензії (АГ);
- тригліцериди ≥1,70 ммоль/л (150 мг/дл) або специфічне лікування, спрямоване на зниження вмісту ліпідів;
- ліпопротеїни високої щільності ≤1,0 ммоль/л (40 мг/дл) у чоловіків та ≤1,3 ммоль/л (50 мг/дл) у жінок або специфічне лікування, спрямоване на зниження концентрації ліпідів.
Олена Бака представила клінічний кейс: пацієнт Р., 1957 р. н., який перебуває під наглядом гастроентеролога з 2013 р. з діагнозом НАСГ із вираженою активністю, має ожиріння 2-го ступеня (ІМТ – 37,9 кг/м2), ЦД 2-го типу (середній ступінь тяжкості, стадія субкомпенсації), гіпертонічну хворобу ІІ ст. На момент звернення в пацієнта виявили високу активність цитолітичного синдрому (АЛТ – 239 Од/л, АСТ – 98 Од/л), що стало підставою для виключення інфікованості вірусними гепатитами (HBcorAg – негативний результат, сумарні антитіла до HCV не виявлено) й автоімунної патології (ANA – негативний результат).
Протягом періоду спостереження, що триває з 2013 р., відзначали описану нижче динаміку основних показників. На тлі корекції дієти, збільшення фізичної активності спостерігали добру тенденцію до нормалізування ІМТ: він знизився з 37,9 кг/м2 (2013) до 35,5 (2017) та 32,4 (2018), але після оголошення пандемії коронавірусної хвороби (COVID-19), карантину та значного обмеження рухового режиму відзначалося поступове зростання ІМТ до 37,9 кг/м2 у 2023 р.
Призначена фармакотерапія сприяла значному зниженню активності цитолітичного синдрому: максимальний рівень АЛТ (239 Од/л), який зафіксували під час ініціального звернення, поступово зменшувався протягом періоду спостереження: через 3 місяці після початку терапії цей показник майже нормалізувався (74 Од/л), але протягом 2015-2020 рр. уміст АЛТ коливався в діапазоні 103-176 Од/л, протягом 2022-2023 рр. його рівень був значно менше – 59-78 Од/л. Аналіз динаміки вмісту АСТ віддзеркалював швидшу нормалізацію: найвища концентрація (98 Од/л) відзначалася у 2013 р., через 3 місяці після початку лікування вона нормалізувалася (34 Од/л), але потім, подібно до змін АЛТ, зросла та перевищувала нормативні показники (41-86 Од/л) з остаточною нормалізацією лише у 2022 р.: відтоді рівень АСТ становив 24-34 Од/л. На момент вихідного обстеження виявили ознаки внутрішньопечінкового холестазу: концентрація гамма-глутамілтранспептидази (ГГТП) перевищувала нормативні значення та становила 164 Од/л (2013), через 3 місяці після початку лікування вона нормалізувалася (42 Од/л), але у 2017 р. досягла максимальних значень – 196 Од/л із поступовим зменшенням (74-118 Од/л) протягом 2018-2021 рр. і досягненням у 2023 р. рівня 70 Од/л.
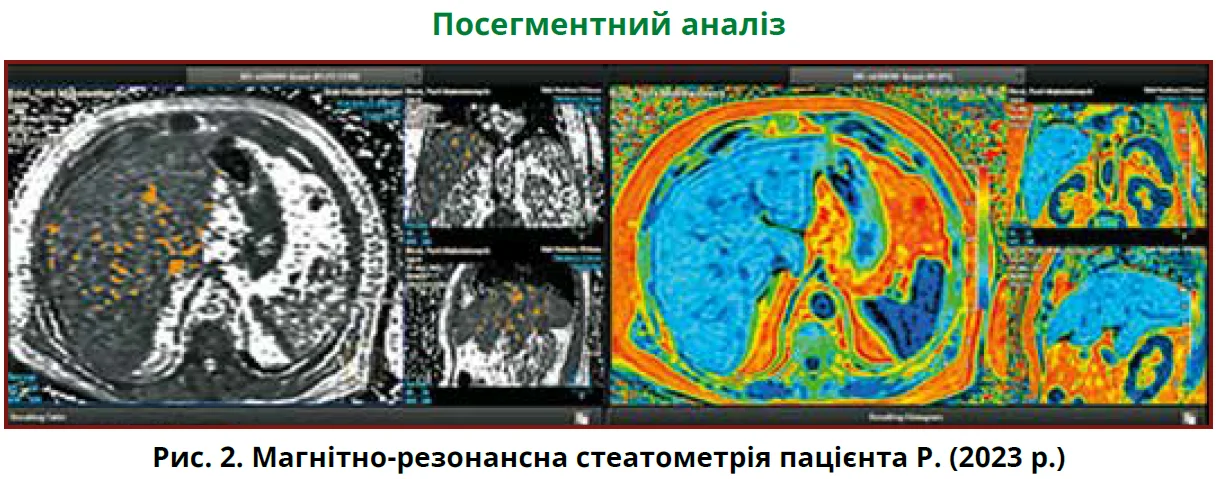
Останнє ультразвукове дослідження, виконане у 2023 р., виявило дифузні зміни печінки за типом жирового гепатозу, ознаки хронічного безкам’яного холециститу, хронічного панкреатиту. Виконано стеатоеластометрію, діагностовано стеатоз S3, фіброз печінки F3 за шкалою METAVIR. Також було проведено магнітно-резонансну стеатометрію, при якій виявлено: при загальному об’ємі печінки 2747 см3 насичення жиром 20,1-24,9% (залежно від використаної розрахункової формули), що значно перевищувало нормативні показники (рис. 2).
Спікерка Любов Соколова, аналізуючи вищенаведені дані, підкреслила, що пацієнт має всі фактори ризику прогресування захворювання: високий ІМТ, похилий вік, високий індекс АСТ/АЛТ, підвищений рівень АЛТ, він страждає на ЦД 2-го типу, АГ та має підвищені значення глікемії натще, HbA1c, тригліцеридів. Лекторка наголосила, що згідно із сучасними доказовими даними фіброз печінки є найважливішим показником смертності при СХПМД. Переконливо доведено, що хворі на СХПМД мають високий ризик смерті від різних причин, а також від причин, пов’язаних саме із захворюванням печінки. Цей ризик прогресивно збільшується зі зростанням стадії фіброзу печінки від F0 до F4. Крім того, наявність НАСГ також підвищує ризик смерті, асоційований із захворюванням печінки. Тобто пацієнт Р. має підвищений ризик смерті, з метою зниження котрого слід запобігти прогресуванню фіброзу печінки. Ендокринолог звернула увагу на високий рівень глікемії натще у 2024 р. 9,15 ммоль/л, що свідчить про активність хронічного запального процесу, який відбувається на тлі ожиріння. Нормативні значення С-пептиду 3,07 нг/мл свідчать про збережену функціональну здатність ендокринної частини підшлункової залози. У 2013 р. рівень HbA1c був дещо підвищеним – 7,29%, але в грудні 2017 р. відзначили значне погіршення стану компенсації вуглеводного обміну та зростання HbA1c до 9,03%; після корекції
цукрознижувальної терапії протягом 2021-2022 рр. цей показник зменшився до 8,06-8,19%, а у 2023 р. досяг позначки 7,56%. Ці коливання збігаються з активацією запального процесу в печінці. Запроваджена нова номенклатура СХП підкреслює новий підхід до лікування, що полягає в одночасній корекції декількох патологічних процесів: метаболічних порушень, ушкодження печінки, компенсації ЦД 2-го типу, ожиріння / надлишкової ваги.
Олена Бака наголосила на необхідності корегування основного патологічного процесу – дисметаболічних порушень; цей захід мають рекомендувати лікарі різних спеціальностей (кардіологи, ендокринологи, гастроентерологи, нефрологи) та заохочувати пацієнтів мінімізувати прояви метаболічного синдрому з метою захисту органів-мішеней (рис. 3).
Доповідачка зауважила, що СХПМД передує та сприяє розвитку ЦД 2-го типу, який, своєю чергою, створює умови для виникнення НАСГ і збільшує ризик розвитку цирозу печінки, гепатоцелюлярної карциноми. Доведено, що на тлі ЦД ризик розвитку СХПМД зростає у 2,2 раза; з іншого боку, СХПМД зумовлює зростання інсулінорезистентності, ускладнює перебіг ЦД й утруднює досягнення його компенсації, збільшує ризик атерогенної дисліпідемії та виникнення серцево-судинних захворювань (ССЗ). Окрім системного впливу СХПМД погіршує прогноз саме для печінки, спричиняючи зростання ризику фіброзу печінки у 2-6 разів.
Любов Соколова розкрила декілька патогенетичних шляхів поліпшення стану хворих на СХП, зазначивши, що зменшення центрального ожиріння, особливо вісцеральної жирової тканини, може сприяти покращенню гістологічної картини при НАСГ. Саме тому основною рекомендацією для пацієнтів із СХПМД є корекція маси тіла.
Із цією метою рекомендують змінити спосіб життя, відмовитися від малорухливості та збільшити щоденну активність. Наступним кроком є раціоналізація харчового раціону завдяки зниженню вживання насичених жирів, крохмалю та доданих цукрів, мінімізуванням або повною відмовою від споживання алкогольних напоїв (особливо при прогресивному фіброзі печінки F3-F4).
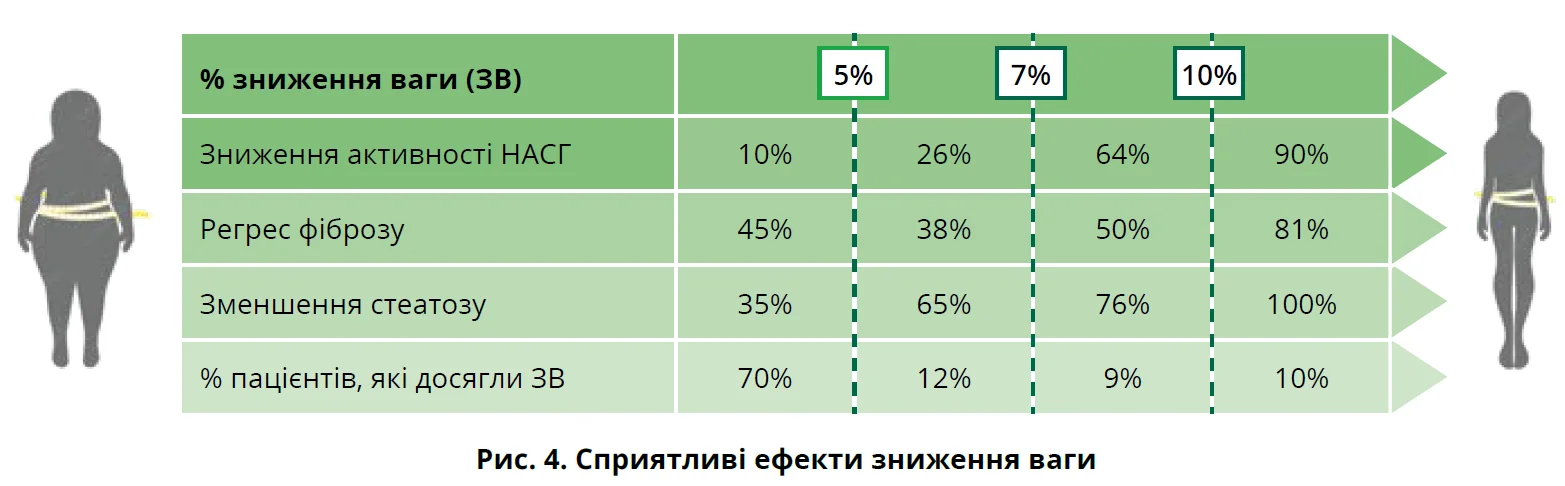
Фізичні навантаження лежать в основі покращення кардіометаболічного здоров’я, зниження ризику саркопенії: найефективнішими визнано аеробні вправи тривалістю 30-60 хвилин одночасно з 20-30-хвилинними силовими тренуваннями. Якщо перелічені заходи недосить ефективні, передбачають спеціалізований менеджмент ожиріння з використанням структурованих програм, фармакотерапії і баріатричної хірургії. Доведено, що втрата жирової тканини внутрішньочеревної та внутрішньопечінкової локалізації сприяє зниженню кардіометаболічного ризику та покращенню гістологічного стану печінки (рис. 4), що підкреслюється в різноманітних практичних настановах. Спікерка навела короткий огляд положень рекомендацій AASLD, Американської діабетологічної асоціації (ADA), які наполягають на необхідності зниження маси тіла >10%, збільшення фізичного навантаження, призначення агоністів рецепторів глюкагоноподібного пептиду-1 (ГПП-1) і проведення баріатричних втручань.
Експерти EASL і Американської гастроентерологічної асоціації (AGA) рекомендують знижувати масу тіла в межах 7-10% завдяки переважно фізичним вправам.
Доповідачка розглянула основні положення лікування ЦД при СХПМД. Мета фармакотерапії ЦД полягає в оптимізації контролю глюкози за допомогою засобів, здатних забезпечити регрес стеатогепатиту. За наявності супутніх ССЗ призначають агоністи рецепторів ГПП-1 та інгібітори натрійзалежного котранспортера глюкози 2-го типу (іНЗКТГ-2), у разі хронічного захворювання нирок та/або сердцевої недостатності перевагу мають іНЗКТГ-2. Хворим на СХПМД з низьким і середнім ризиком виникнення фіброзу можна призначати метформін, інгібітори дипептидилпептидази-4, акарбозу й інсулін, але їхня користь визнана обмеженою через мінімальну здатність впливати на гістологічний стан печінки. Обов’язковою також є корекція АГ.
Спікерка Олена Бака підкреслила, що в березні цього року Управління США з контролю продовольства та медикаментів (FDA) схвалило перший препарат для лікування дорослих із НАСГ. Препарат має назву ресметіром, він призначений для пацієнтів із помірним і тяжким ступенем хвороби. Сучасна медикаментозна терапія СХМПД/НАСГ ґрунтується на визначенні ризику розвитку фіброзу печінки на підставі розрахунку індексу FIB-4 або проведення еластометрії. Серед ліків, які здатні потенційно впливати на перебіг СХПМД, є вітамін Е, піоглітазон, ліраглутид, семаглутид, іНЗКТГ-2.
Крім цих препаратів можуть бути використані засоби, які сприяють відновленню функціональної здатності гепатоцитів, – S-аденозил-L-метіонін (SAMe), оригінальний препарат якого представлений в Україні під торговою назвою Гептрал®. Доведено, що SAMe забезпечує розвиток антиоксидантного ефекту, бере участь у синтезі глутатіону та фосфатидилхоліну, відновлює структуру й функцію гепатоцитів, покращує ліпідний і вуглеводний обмін, посилює елімінацію тригліцеридів разом із ліпопротеїнами дуже низької щільності, знижуючи кількість жиру в печінці та регулюючи печінковий глюконеогенез. Застосування Гептрал® дає змогу зменшити фіброзування, активність синтезу колагену; SAMe зменшує запалення та сприяє імуномодуляції завдяки балансу цитокінів.
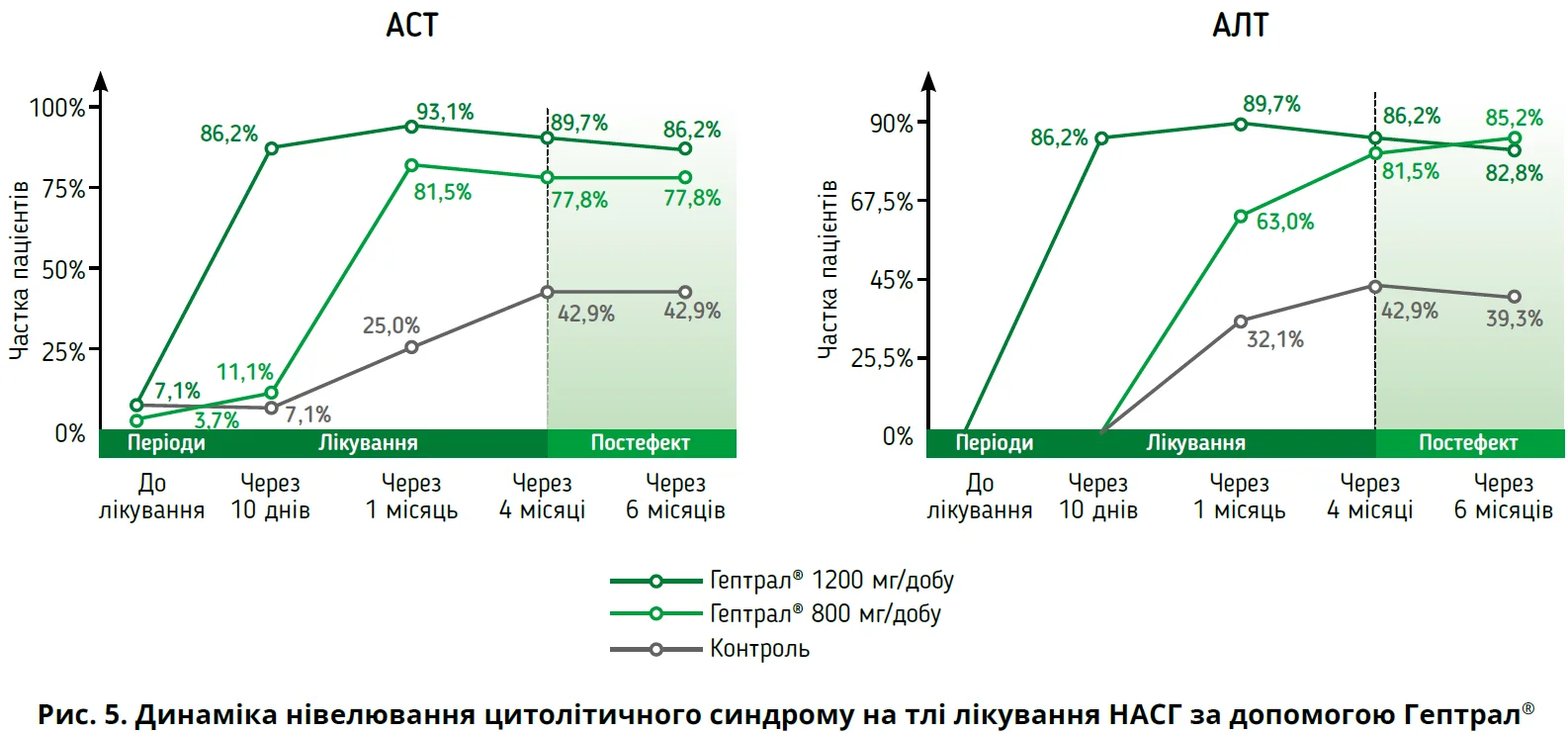
У клінічному дослідженні, проведеному під керівництвом А. Барановського, доведено, що призначення Гептрал® хворим на НАСГ сприяє нормалізації рівнів АЛТ, АСТ уже на 10-ту добу терапії (рис. 5).
У цьому дослідженні зафіксовано дозозалежний ефект Гептрал®: швидшу нормалізацію АЛТ, АСТ спостерігали на тлі прийому 1200 мг SAMe порівняно з 800 мг, контрольною групою. Автори описали постефект від прийому Гептрал® у вигляді збереження АЛТ, АСТ у межах норми протягом 2 місяців після припинення прийому препарату (рис. 5). Отже, терапія Гептрал® протягом 7-14 днів сприяє поліпшенню біохімічних показників (АЛТ, АСТ, ГГТП, лужної фосфатази) та зниженню гепатогенної втоми, що є одним із симптомів внутрішньопечінкового холестазу; застосування Гептрал® протягом 1 місяця забезпечує поліпшення показників ліпідограми, тривале застосування протягом 2 місяців сприяє покращенню ультразвукової картини печінки, застосування протягом 3 місяців дає змогу зберігати досягнуті результати до 3 місяців після припинення терапії (постефект).
Ведення пацієнтів із метаболічно-асоційованим стеатогепатитом є своєрідним викликом для лікарів різних спеціальностей. Першочерговими завданнями мультидисциплінарної команди лікарів є нівелювання дисметаболічних змін і сповільнення прогресування фіброзу печінки.
SAMe (Гептрал®) може застосовуватися в таких хворих із метою швидкого нормалізування функціонального стану печінки, покращення показників ліпідограми й ультразвукової картини печінки.
Переглянути запис вебінару Ви можете за посиланням https://youtu.be/IdT4O6wUXzk?si=bbCJ5j5MRcVbSowh
Згідно з інструкцією для медичного застосування лікарського засобу Гептрал® показанням до застосування є ВПХ у дорослих, у тому числі у хворих на хронічний гепатит різної етіології та цироз печінки, а також ВПХ у вагітних.