Метаболічно-асоційована стеатотична хвороба печінки, саркопенія та клінічне харчування: виклики, докази й перспективи. Підсумки конгресу ESPEN 2025
 Автор: Олена Олександрівна ПОГРЕБНЯК, терапевтка, дієтологиня, лікарка УЗД Regional Klaudian Hospital (м. Млада-Болеслав, Чехія), кандидатка медичних наук, асистентка кафедри загальної практики – сімейної медицини Національного медичного університету ім. О.О. Богомольця (м. Київ, Україна), експертка ГО «Асоціація превентивної та антиейджинг медицини», член Європейської асоціації з вивчення печінки, Європейської асоціації ендокринологів, Чеської асоціації обезитологів, Британської асоціації дієтологів, Асоціації дієтологів України
Автор: Олена Олександрівна ПОГРЕБНЯК, терапевтка, дієтологиня, лікарка УЗД Regional Klaudian Hospital (м. Млада-Болеслав, Чехія), кандидатка медичних наук, асистентка кафедри загальної практики – сімейної медицини Національного медичного університету ім. О.О. Богомольця (м. Київ, Україна), експертка ГО «Асоціація превентивної та антиейджинг медицини», член Європейської асоціації з вивчення печінки, Європейської асоціації ендокринологів, Чеської асоціації обезитологів, Британської асоціації дієтологів, Асоціації дієтологів України
Ключовою метою сучасної медицини є збільшення тривалості життя людини та збереження її функціональної активності. Нині переважну більшість пацієнтів у стаціонарах становлять особи похилого та старечого віку, які часто мають численні супутні хвороби, що поєднуються з віковими змінами периферичних тканин. Одним з найпоширеніших таких станів є саркопенія, котра характеризується прогресивною генералізованою втратою маси, сили й функції скелетних м’язів.
На тлі глобального старіння населення значущість цієї проблеми постійно зростає. Очікується, що чисельність людей віком ≥65 років у світі збільшиться приблизно у 2,2 раза та досягне 1,664 млрд, тому саркопенію дедалі частіше розглядають як одну з ключових медичних і соціальних проблем сучасності. Водночас вона поширена не лише серед осіб старшого віку: ознаки саркопенії виявляють навіть у 40-річних пацієнтів з метаболічним синдромом. Доведено, що цей стан значно погіршує прогноз, підвищуючи ризик смерті та знижуючи якість життя.
З огляду на зазначені тенденції проблема саркопенії привертає дедалі більшу увагу міжнародної наукової спільноти. Саме тому вона стала одним з помітних акцентів конгресу ESPEN 2025 – одного з провідних світових форумів у галузі клінічного харчування та метаболічної медицини. У межах конгресу активно обговорювали роль саркопенії у формуванні кардіометаболічних порушень, а також її взаємозв’язок з метаболічно-асоційованою стеатотичною хворобою печінки (МАСХП) та ожирінням, що підкреслює актуальність цієї проблеми для сучасної клінічної практики.
Саркопенія: дефініція та клінічні фенотипи
Саркопенію визначають як синдром, що характеризується прогресивною генералізованою втратою маси, сили та функції скелетних м’язів і асоціюється з підвищеним ризиком несприятливих клінічних наслідків. Формування цього стану пов’язане з дисрегуляцією кількох молекулярних механізмів, зокрема порушенням білкового обміну, інсулінорезистентністю (ІР), мітохондріальною дисфункцією та хронічним системним низькоградієнтним запаленням. У міру прогресування цих процесів деградація м’язового білка починає переважати над його синтезом, що призводить до поступового зменшення м’язової маси, сили та функціональної здатності м’язів.
Залежно від етіології виділяють два основні типи саркопенії. Первинна саркопенія пов’язана переважно з віковими змінами організму. Вторинна саркопенія розвивається під впливом інших чинників, серед яких велике значення мають недостатнє споживання білка/енергії, тривала нерухомість, застосування деяких лікарських засобів, а також хронічні хвороби, зокрема цукровий діабет (ЦД) 2-го типу, ожиріння та МАСХП.
Окрему увагу привертає такий фенотип, як саркопенічне ожиріння: цей стан характеризується поєднанням зменшення м’язової маси та сили зі збільшенням жирової тканини. У таких пацієнтів одночасно відбуваються процеси втрати м’язової маси та накопичення жиру, що зумовлює формування складних метаболічних порушень. Таке поєднання розглядають як один з несприятливих фенотипів кардіометаболічного ризику, оскільки саркопенія й ожиріння взаємно посилюють одне одного, формуючи замкнене коло.
Патофізіологічна вісь «печінка – жирова тканина – м’язи» при МАСХП
Саркопенія, ожиріння та МАСХП формують єдину взаємопов’язану метаболічну вісь. У межах цієї осі порушення енергетичного й білкового обміну, ІР і хронічне системне запалення призводять до змін як у жировій тканині, так і в печінці та скелетних м’язах.
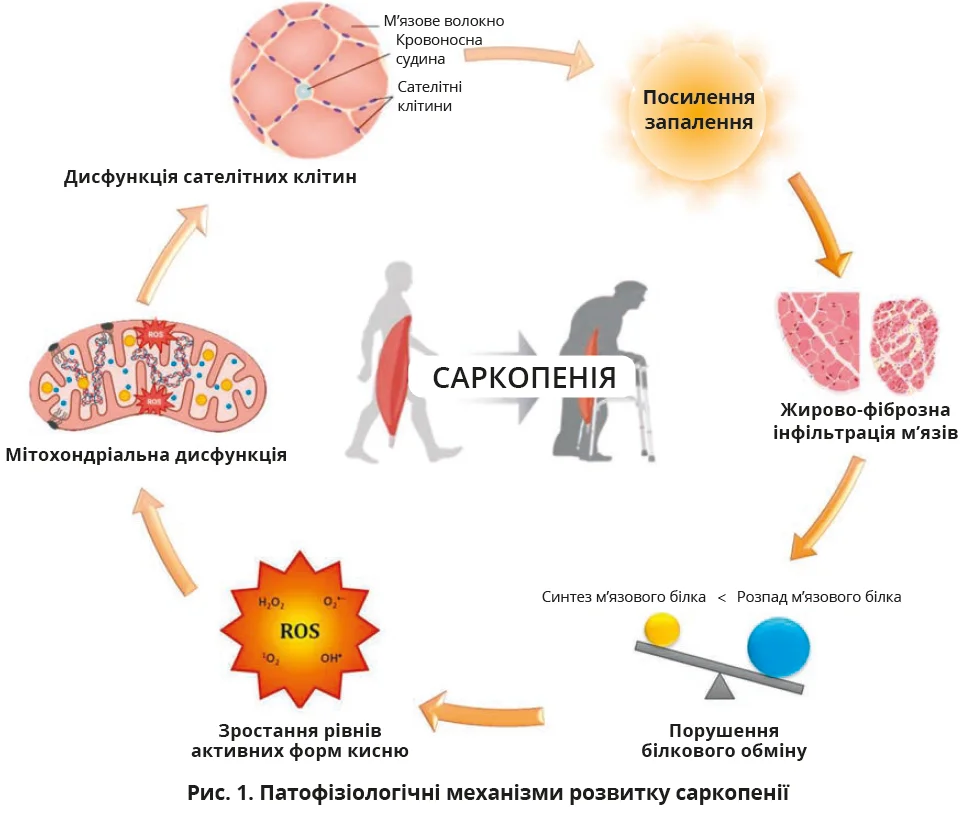
Надлишок жирової тканини зумовлює розвиток хронічного запалення з підвищеним вивільненням прозапальних цитокінів (фактора некрозу пухлин-α – ФНП-α, інтерлейкіну-6 – ІЛ-6), а також лептину, вміст якого асоціюється з ІР і тяжкістю ураження печінки (рис. 1). Накопичення ліпідів у печінці спричиняє ліпотоксичність, змінює сигнальні шляхи, пов’язані з mTORC1, знижує синтез м’язового білка. У межах цього метаболічного континууму МАСХП може прогресувати до метаболічно-асоційованого стеатогепатиту (МАСГ), що супроводжується посиленням системного запалення та м’язової дисфункції.
Додатковим чинником прогресування ураження печінки є внутрішньопечінковий холестаз (ВПХ). Накопичення токсичних жовчних кислот ушкоджує гепатоцити, активує запальні й фібротичні процеси та спричиняє розвиток фіброзу. У цьому контексті активацію рецептора FXR розглядають як один з механізмів, здатних зменшувати запалення та покращувати жовчовиділення.
Водночас надлишкове ліпідне навантаження на скелетні м’язи спричиняє розвиток міостеатозу. Накопичення керамідів і діацилгліцеринів порушує інсулінову сигналізацію та зумовлює зростання ІР. Збільшення внутрішньом’язового жиру супроводжується зниженням синтезу білка, хронічним запаленням і поступовою втратою функції м’язів.
Важливу роль у цій метаболічній осі відіграють гепатокіни, зокрема фетуїн А, гепасоцин, LECT2 та фолістатин, рівні яких корелюють з ІР, МАСХП і прогресуванням до МАСГ. Окрім того, гіперамоніємія може посилювати саркопенію й запалення печінки, формуючи замкнене коло печінкової та м’язової дисфункцій, що клінічно проявляється м’язовою слабкістю, втомою та зниженням функціональної активності.
Отже, саркопенія, ожиріння й ураження печінки формують єдину взаємопов’язану патофізіологічну систему, в межах якої кожен компонент здатний посилювати прогресування інших.
Саркопенічне ожиріння та МАСХП: прогностичне значення
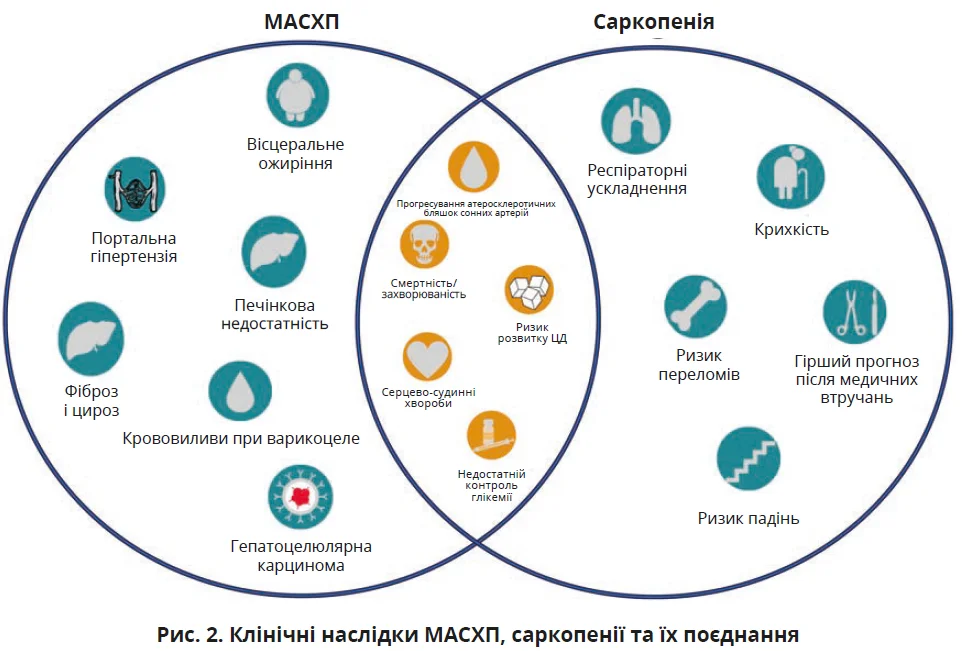
Саркопенічне ожиріння на тлі МАСХП і МАСГ спричиняє посилення ІР і системного запалення, що може погіршувати перебіг хвороби. Доведено, що наявність саркопенії й ожиріння у хворих на МАСХП асоціюється з гіршим прогнозом: у когорті таких пацієнтів фіксують значно вищий ризик виникнення ускладнень, розвитку серцево-судинних подій, прогресування фіброзу печінки та загальної смертності (рис. 2) порівняно з особами, які мають лише один з перелічених станів.
Водночас вплив ожиріння на прогноз може бути неоднозначним. У літніх пацієнтів із цирозом описано так званий парадокс ожиріння, коли надлишкова маса тіла асоціюється з певним захисним ефектом. Однак у разі поєднання ожиріння із саркопенією цей ефект зникає.
Сучасні критерії діагностики та класифікації
Сучасна діагностика саркопенії ґрунтується на рекомендаціях Європейської робочої групи з питань саркопенії в людей похилого віку (EWGSOP2). Для оцінювання цього стану потрібно визначити три ключові параметри: м’язову масу та силу, фізичні функції. М’язову масу визначають за допомогою комп’ютерної томографії (КТ), магнітно-резонансної томографії, двохенергетичної рентгенівської абсорбціометрії (ДРА), ультразвукового дослідження (УЗД) або біоімпедансного аналізу (БІА). М’язову силу найчастіше оцінюють за допомогою динамометрії, тоді як фізичну функцію визначають з використанням тестів швидкості ходьби чи підведення зі стільця.
На підставі вимірювання цих показників виділяють три стадії саркопенії. Передсаркопенія (І стадія) характеризується зниженням м’язової маси без втрати сили або функції. Саркопенію (ІІ стадія) діагностують у разі одночасного зменшення м’язової маси та м’язової сили або функціональної здатності. Тяжку саркопенію (ІІІ стадія) встановлюють за наявності одночасного зниження м’язової маси, сили та фізичної функції.
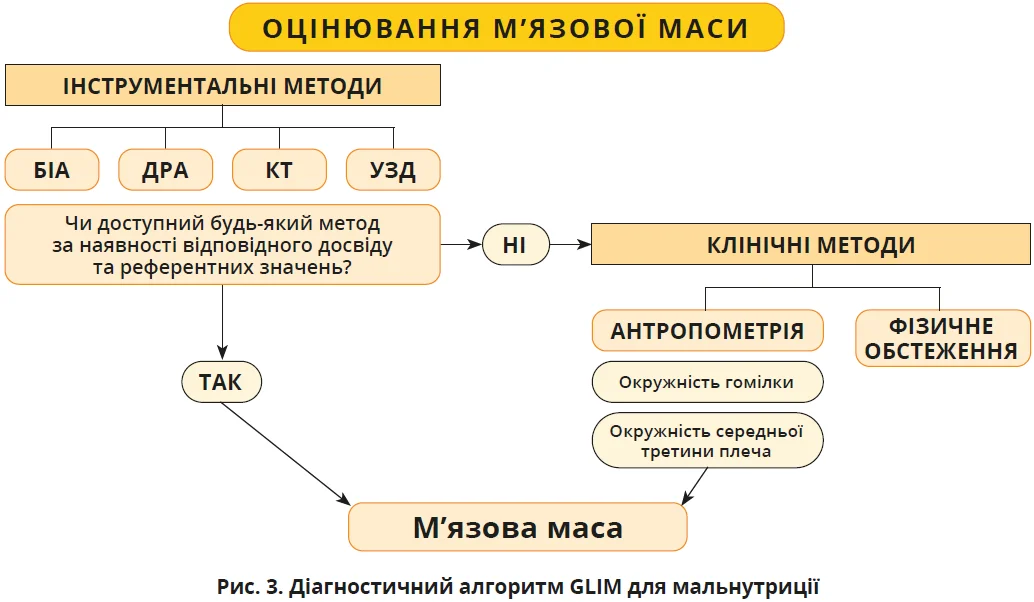
У клінічній практиці оцінювання м’язової маси також є важливою складовою діагностики мальнутриції. Оскільки саркопенія часто поєднується з мальнутрицією, визначення м’язової маси та функції розглядають не лише як інструмент діагностики саркопенії, а і як важливий компонент оцінювання нутритивного статусу пацієнта. Для цього застосовують консенсусні критерії Global Leadership Initiative on Malnutrition (GLIM), які передбачають поєднання фенотипових ознак (втрата маси тіла, низький індекс маси тіла чи зменшення м’язової маси) з етіологічними чинниками, як-от недостатнє споживання їжі або наявність запалення. У межах цього алгоритму інструментальне оцінювання м’язової маси може доповнюватися клінічними методами, зокрема антропометрією та фізикальним обстеженням (рис. 3).
Терапевтична стратегія при саркопенії: рекомендації ESPEN
Роль харчування та фізичної активності
На конгресі ESPEN 2025 було представлено сучасні підходи до профілактики й лікування мальнутриції та саркопенічного ожиріння. Підкреслюється, що терапевтична стратегія в осіб із саркопенією має бути спрямована на покращення складу тіла: зменшення жирової маси при одночасному збереженні/збільшенні м’язової маси, підвищенні м’язової сили та покращенні якості м’язової тканини. Важливу роль у цьому процесі відіграють зменшення жирової інфільтрації м’язів і відновлення мітохондріальної функції.
Основою немедикаментозного лікування є модифікація способу життя, котра включає корекцію харчування та регулярну фізичну активність. У пацієнтів похилого віку рекомендується уникати надмірно жорсткого обмеження калорійності раціону, оскільки це може негативно впливати на масу скелетних м’язів, нутритивний статус і мінеральну щільність кісткової тканини. Орієнтовна енергетична потреба для таких пацієнтів становить 25-30 ккал/кг/добу.
Дієтотерапія передбачає достатнє споживання високоякісного білка. Зазвичай рекомендують 1-1,2 г/кг/добу при первинній саркопенії, близько 1 г/кг ідеальної маси тіла при саркопенічному ожирінні та до 1,0-1,7 г/кг/добу в пацієнтів з МАСХП і саркопенією. Перевагу віддають джерелам білка, що містять лейцин. Якщо адекватне споживання білка з їжею неможливе, можуть застосовуватися пероральні білкові добавки. Важливим також є своєчасне усунення дефіцитів вітамінів і мінералів, а також потенційне застосування антиоксидантів, довголанцюгових жирних кислот, вітаміну D, креатину й амінокислот з розгалуженим ланцюгом.
Регулярні фізичні навантаження є ще одним ключовим компонентом терапії. Вони сприяють мітохондріальному біогенезу, зменшують хронічне низькоградієнтне запалення та покращують чутливість до інсуліну. Скелетні м’язи при цьому виступають метаболічно активною тканиною, що бере участь у регуляції енергетичного обміну, а в умовах саркопенії можуть також відігравати роль у детоксикації аміаку. Підтримання та відновлення м’язової маси значною мірою залежать від поєднання адекватного білкового забезпечення з регулярною фізичною активністю.
Фармакотерапія
Попри значний прогрес у вивченні саркопенії, на сьогодні не існує схвалених фармакологічних препаратів, спеціально розроблених для лікування саркопенії при МАСХП. Вивчаються потенційні підходи, серед яких корекція дефіциту вітаміну D, застосування сучасних препаратів проти ожиріння, гормональної терапії, селективних модуляторів андрогенних рецепторів, метформіну, агоністів греліну та препаратів, що впливають на сигнальні шляхи міостатину. Додатковим методом лікування тяжкого ожиріння залишається баріатрична хірургія, однак її вплив на перебіг саркопенії потребує подальшого вивчення.
Гепатогенна втома: бич хворих із саркопенією та МАСХП
За відсутності ефективної фармакотерапії ключове значення у веденні пацієнтів з МАСХП мають зміни способу життя. Проте їх реалізацію часто ускладнює гепатогенна втома. Однією з особливостей клінічного перебігу МАСХП є те, що захворювання може тривалий час залишатися безсимптомним, а серед небагатьох неспецифічних проявів іноді відзначають патологічну втому, не пов’язану з фізичним навантаженням і таку, яка не зникає після відпочинку. Вона може супроводжуватися загальною слабкістю й абдомінальним дискомфортом, а іноді клінічні прояви стають помітними вже на стадії прогресування хвороби до цирозу або гепатоцелюлярної карциноми.
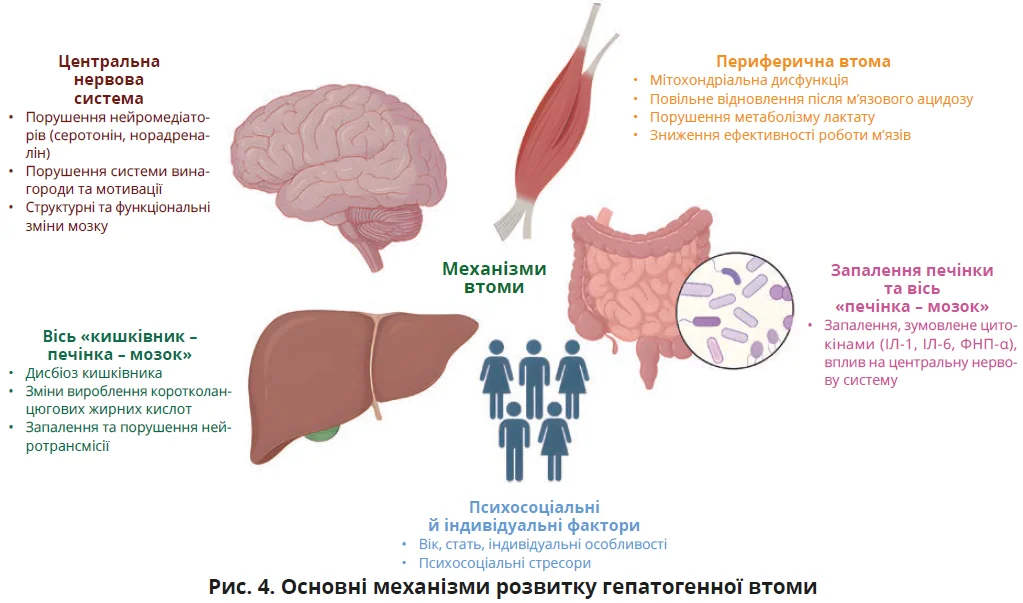
Порушення функції печінки, зокрема цитоліз і ВПХ, можуть впливати на центральну нервову систему через зниження синтезу нейромедіаторів, як-от серотонін і дофамін, а також через порушення нейротрансмісії в головному мозку, що пов’язують з розвитком патологічної втоми. Водночас формування втоми може бути зумовлене й периферичними механізмами, пов’язаними з порушенням функції скелетних м’язів (рис. 4). До них належать мітохондріальна дисфункція, уповільнене відновлення після м’язового ацидозу, порушення метаболізму лактату та зниження ефективності м’язової роботи.
S-аденозилметіонін для корекції гепатогенної втоми
Одним з метаболічних механізмів, що може бути залучений у формування гепатогенної втоми при хронічних захворюваннях печінки (ХЗП) та внутрішньопечінковому холестазі (ВПХ), є порушення обміну S-аденозилметіоніну (SAMe). Перебіг ХЗП та ВПХ часто супроводжується дефіцитом цієї сполуки, що призводить до порушення низки біохімічних реакцій. SAMe є універсальним донором метильних і сульфатних груп і відіграє центральну роль у клітинному метаболізмі. Він бере участь у реакціях метилювання ДНК, РНК, білків і фосфоліпідів клітинних мембран, а також у синтезі гормонів і нейромедіаторів, зокрема дофаміну, серотоніну та мелатоніну. SAMe залучений у процеси транссульфурування й амінопропілювання, котрі забезпечують синтез глутатіону, таурину та поліамінів.
Зниження рівня SAMe при ХЗП призводить до порушення цих метаболічних шляхів і може супроводжуватися зменшенням синтезу фосфоліпідів клітинних мембран, зниженням антиоксидантного захисту через дефіцит глутатіону, мітохондріальну дисфункцію та накопичення ліпідів у печінці.
У доклінічних і клінічних дослідженнях доведено, що SAMe сприяє відновленню функціональної активності гепатоцитів через вплив на кілька ключових метаболічних механізмів. Зокрема, його дія пов’язана з посиленням синтезу глутатіону й антиоксидантного захисту, участю в синтезі фосфатидилхоліну клітинних мембран і покращенням ліпідного та вуглеводного обміну, що сприяє зменшенню накопичення жиру в печінці. Крім того, SAMe може зменшувати процеси фіброзоутворення, а також чинити протизапальні, імуномодулювальні та нейропротекторні ефекти, пов’язані з участю в синтезі нейромедіаторів.
Клінічну ефективність адеметіоніну в зменшенні проявів астенічного синдрому в пацієнтів з неалкогольним стеатогепатитом (НАСГ) яскраво продемонстровано в рандомізованому плацебо-контрольованому клінічному дослідженні. Пацієнтів з НАСГ (n=84) рандомізували для 4-місячного приймання SAMe у дозах 1200 або 800 мг/добу чи плацебо з подальшим 2-місячним періодом спостереження.
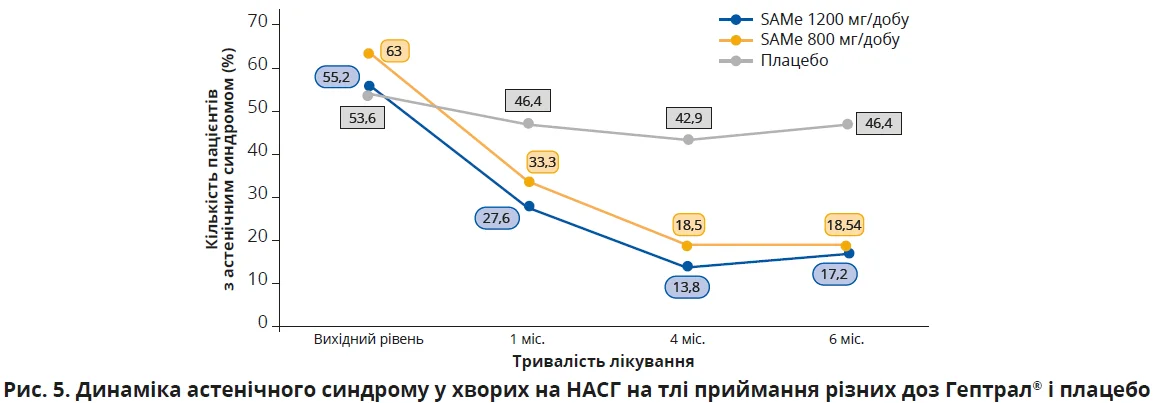
Терапія SAMe супроводжувалася зменшенням активності цитолітичного та холестатичного синдромів. На цьому тлі відзначали й істотне зниження вираженості астенічного синдрому. У групах приймання SAMe частка пацієнтів з астенією поступово зменшувалася протягом лікування та подальшого спостереження, тоді як у групі плацебо істотної динаміки не спостерігали (рис. 5). Найвираженіше зниження астенічних проявів відзначали при застосуванні адеметіоніну в дозі 1200 мг/добу.
Отримані результати свідчать: застосування SAMe може сприяти зменшенню вираженості патологічної втоми в пацієнтів з НАСГ та ВПХ, що має важливе клінічне значення, оскільки астенічний синдром часто ускладнює дотримання рекомендацій щодо фізичної активності та змін способу життя.
Треба зазначити, що ефективність SAMe значною мірою залежить від стабільності та якості активної речовини. Однією з важливих характеристик SAMe-вмісних препаратів є їхній ізомерний склад. SAMe являє собою рацемічну суміш S- та R-ізомерів, але клінічну активність пов’язують саме з S-ізомером, частка якого має переважати в препараті. У разі нестабільності активної форми можливе перетворення S-ізомерів на неактивні R-ізомери з подальшим розпадом молекули та втратою фармакологічної активності. Саме тому навіть незначну кількість продуктів деградації розглядають як небажану.
Зважаючи на зазначені особливості, значну увагу привертає технологія виробництва SAMe-вмісних препаратів. Зокрема, оригінальний препарат адеметіоніну Гептрал® виробляється за запатентованою технологією у вигляді стабільної солі SAMe, що забезпечує високий уміст активного S-ізомеру – не менш ніж 80-85% в активній речовині на момент виробництва. Важливо, що активна речовина виготовляється відповідно до швейцарських стандартів якості, тоді як виробництво готового лікарського засобу здійснюється на фармацевтичних підприємствах у Франції й Італії.
Висновки
Саркопенія є поширеним патологічним станом серед хворих на МАСХП, її недооцінювання може суттєво знижувати ефективність лікування. Поєднання з ожирінням формує фенотип саркопенічного ожиріння, що асоціюється з несприятливішим прогнозом і потребує міждисциплінарного підходу до діагностики та терапії. Лікування саркопенії залишається складним завданням, оскільки ефективність дієтотерапії та фізичної активності може варіюватися, а їх реалізація в частини пацієнтів ускладнюється гепатогенною втомою, котра часто супроводжує ХЗП і може посилюватися за наявності ВПХ. В осіб з МАСХП, саркопенічним ожирінням і ВПХ доцільним може бути застосування SAMe (Гептрал®), який впливає на ключові метаболічні процеси в печінці та м’язовій тканині, сприяє зменшенню гепатогенної втоми й потенційно полегшує реалізацію змін способу життя.
Література
- Abenavoli L., Statsenko M., Scarlata G.G.M., et al. Sarcopenia and metabolic dysfunction-associated steatotic liver disease: a narrative review. Livers. 2024; 4 (4): 495-506. doi: 10.3390/livers4040035.
- Altamirano-Barrera A., Barranco-Fragoso B., Méndez-Sanchez N. Management strategies for liver fibrosis. Annals of Hepatology. 2017; 16 (1): 48-56.
- Anstee Q.M., et al. S-adenosylmethionine (SAMe) therapy in liver disease: a review of current evidence and clinical utility. Journal of Hepatology. 2012; 57: 1097-1106.
- Baranovsky A.Y., et al. Clinical perspectives in gastroenterology and hepatology. 2010; 1: 3-11.
- Bertolini A. Bile acids and their receptors: modulators and therapeutic targets in liver inflammation. 2022; 44: 547-564.
- Crişan D. Sarcopenia in MASLD — Eat to Beat Steatosis, Move to Prove Strength. 2025.
- Francque S.M., Marchesini G., Kautz A., et al. Non-alcoholic fatty liver disease: a patient guideline. JHEP Reports. 2021 Sep 17; 3 (5): 100322. doi: 10.1016/j.jhepr.2021.100322.
- He N. Relationship between sarcopenia and cardiovascular diseases in the elderly: an overview. Frontiers in Cardiovascular Medicine. 2021.
- Isley S., Johnson E., Swain M.G., et al. Fatigue in cholestatic liver disease: a review of mechanisms and non-pharmacological management. Curr. Hepatology Rep. 2025; 24 (31).
- Luque-Urbano M.R., Fernández-Ramos D., Lopitz-Otsoa F., et al. S-adenosylmethionine deficit disrupts very low-density lipoprotein metabolism promoting liver lipid accumulation in mice. Journal of Lipid Research. 2025.
- Mao H., et al. Hepatoprotective effect of S-ademetionine in the treatment of intrahepatic cholestasis through farnesoid X receptor mechanism in rats. Journal of Biomolecular Research & Therapeutics. 2019; 8: 176.
- Mato J.M., Martinez-Chantar M.L., Lu S.C. S-adenosylmethionine metabolism and liver disease. Annals of Hepatology. 2013; 12 (2): 183-189.
- Mirzai S. Sarcopenic obesity and cardiovascular disease: an overlooked but high-risk syndrome. Current Obesity Reports. 2024.
- Swain M.G. Fatigue in chronic liver disease: new insights and therapeutic approaches. Liver International. 2018.
- Dayal U. MAFLD: exploring the systemic effects beyond liver. Journal of Community Hospital Internal Medicine Perspectives. 2025.
- Xing Z., Tu B.P. Mechanisms and rationales of SAMe homeostasis. Trends in Biochemical Sciences. 2025.
- Li Z. Methionine metabolism in chronic liver diseases: an update on molecular mechanism and therapeutic implication. Signal Transduction and Targeted Therapy. 2020.
- Анохіна Г.А., Харченко В.В., Динник О.Б. Роль запалення та метаболічних порушень у прогресуванні хронічних захворювань печінки: профілактика та лікування. Здоров’я України. 2018; 15-16: 60-62.
- Губергриц Н.Б. «Роковая цепочка» и адеметионин. Сучасна гастроентерологія. 2014; 4: 106-120.
- Погребняк О.О. Стовпи сучасного немедикаментозного лікування метаболічно-асоційованої стеатотичної хвороби печінки: дієта та фізична активність. Освітньо-практичний журнал Gastro Practice. 2024; 4: 18-23.