Стан кісток за патології паращитоподібних залоз: перегляд доказів щодо епідеміології, хірургічного та медикаментозного лікування. Частина 1
Переклала й адаптувала канд. мед. наук Ольга Королюк
Порушення, пов’язані з паратгормоном (ПТГ), мають значущий вплив на кістковий метаболізм через ключову роль ПТГ у гомеостазі мінералів і ремоделюванні кісток. У цьому огляді розглядатимуться скелетні зміни при гіперпаратиреозі, гіпопаратиреозі (гіпоПТ) та рідкісних спадкових синдромах, а також наявні докази щодо ефективності різних методів лікування вказаних розладів.
Більшість порушень паращитоподібних залоз (ПЩЗ) діагностуються випадково на ранніх стадіях скелетних змін. Найпоширенішим є первинний гіперпаратиреоз (ПГПТ) – стан автономного гіпервироблення ПТГ здебільшого через аденому ПЩЗ, що призводить до значних скелетних змін. Класичним і найтяжчим проявом ПГПТ є фіброзно-кістозний остеїт (osteitis fibrosa cystica). При вторинному гіперпаратиреозі (ВГПТ) надмір ПТГ є наслідком дефектів гомеостазу кальцію, які зумовлюють гіпокальціємію.
ГіпоПТ характеризується відсутнім або надто низьким рівнем ПТГ за наявності гіпокальціємії. Зазвичай гіпоПТ ускладнює операції на шиї. Дефіцит ПТГ призводить до зниження кісткового обміну та підвищення мінеральної щільності кісткової тканини (МЩКТ). Проте навіть за таких умов можливе ураження кісток через надмірну мінералізацію та зміни мікроархітектури.
Роль ПТГ у кістковому та мінеральному обміні
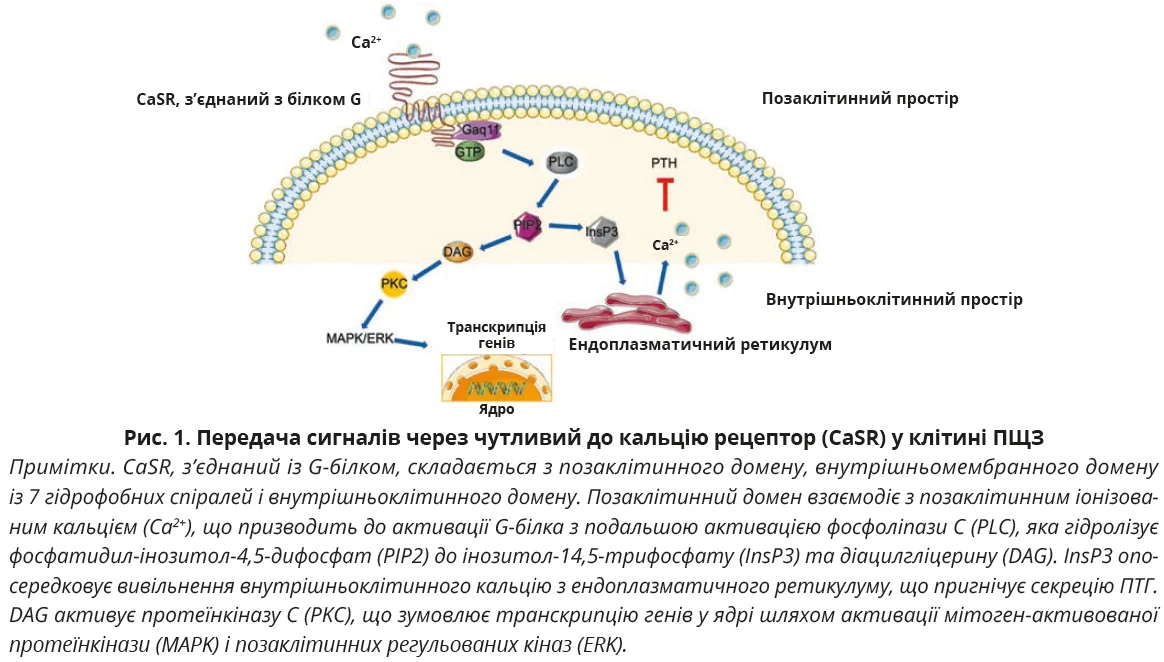
ПЩЗ синтезують неактивний попередник ПТГ, який після розщеплення депонується у вигляді біоактивної молекули (ПТГ 1-84). Клітини ПЩЗ вловлюють найменші коливання позаклітинного кальцію через чутливий до кальцію рецептор (CaSR), з’єднаний із G-білком. Його сигнали передаються шляхом активації фосфоліпази С з подальшим утворенням діацилгліцерину й інозитолтрифосфату. Внаслідок активації сигнального шляху збільшується вміст внутрішньоклітинного кальцію та пригнічується вивільнення ПТГ (рис. 1).
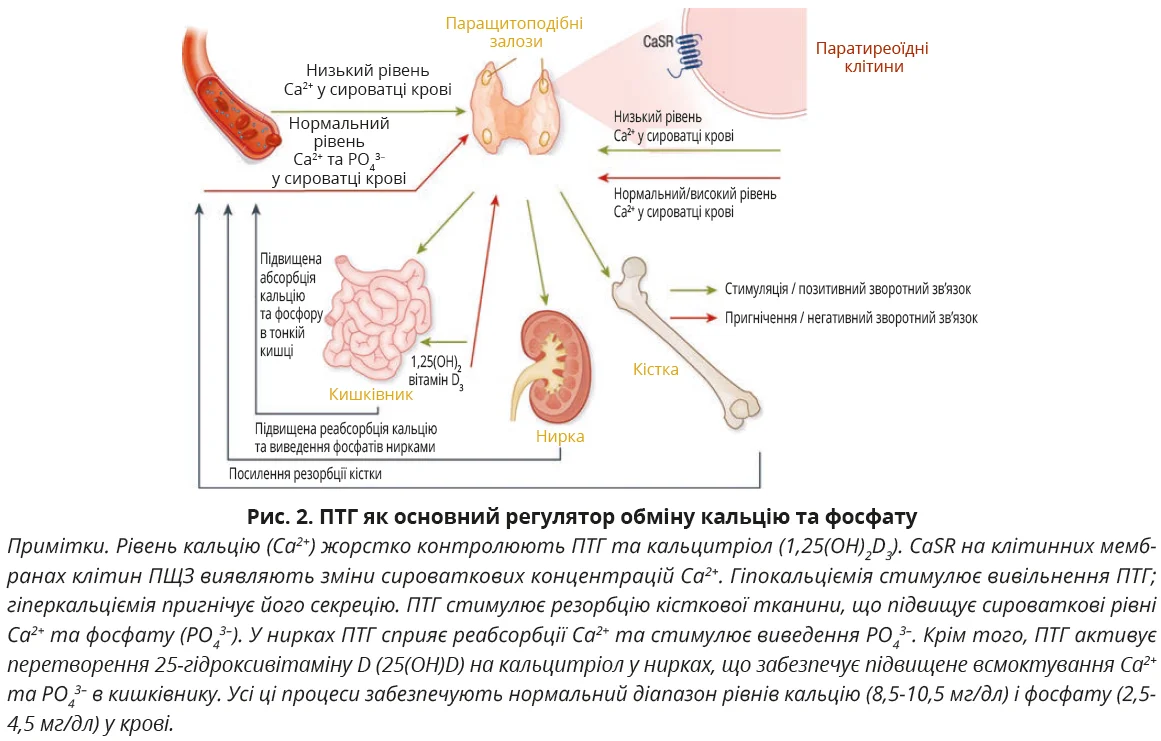
Вивільнення ПТГ відбувається у відповідь на низькі сироваткові рівні іонізованого кальцію (Ca2+). Підвищення Ca2+ пригнічує транскрипцію та стабільність генів ПТГ. Хронічна гіпокальціємія спричиняє реплікацію клітин, наслідком чого є гіперплазія ПЩЗ. Дія ПТГ спрямована на відновлення рівня кальцію в сироватці крові, що безпосередньо впливає на мінеральний обмін у кістках і нирках, а також має непрямий вплив на всмоктування мінералів у кишківнику (рис. 2). Вказані взаємодії суворо підтримують рівні Ca2+ у вузькому діапазоні 1,1-1,3 ммоль/л. Збалансований гомеостаз Ca2+ необхідний не тільки для метаболізму кісток, але й для багатьох інших фізіологічних процесів, зокрема передачі внутрішньоклітинних сигналів, функції нервів і м’язів.
Основною циркулювальною біоактивною формою ПТГ є пептид, що містить 84 амінокислотні залишки. Проте майже вся біологічна активність гормону міститься в межах аміно(NH2)-термінального домену; тому синтетичний пептид, який складається з перших 34 амінокислот N-кінця (ПТГ 1-34, терипаратид), має біологічну активність усієї молекули.
Дія ПТГ реалізується через рецептор, з’єднаний із G-білком, ПТГ1Р – рецептор-1 ПТГ та білка, спорідненого з ПТГ (ПТГсБ). Здатність обох молекул (ПТГ та ПТГсБ) впливати на аналогічний рецептор пояснюється структурною схожістю NH2-термінального домену, що дає їм змогу утворювати подібні вторинні та третинні структури, пов’язані з рецептором. Утім, біологічні ефекти вказаних молекул не є ідентичними. Імовірно, біологічна активність ПТГсБ реалізується через домени за межами N-кінця, але ці впливи мало вивчені. Зв’язування ПТГ або ПТГсБ з ПТГ1Р призводить до активації G-білків (зокрема Gas) і аденілілциклази з утворенням вторинного месенджера циклічного аденозинмонофосфату (цАМФ). Сигнальний каскад зумовлює активацію протеїнкінази А (ПKA), яка транслокується до ядра та фосфорилює цАМФ-чутливі елементи ДНК, призводячи до транскрипції цільових генів. Передавання сигналу контролюється кількома внутрішньоклітинними механізмами: деградація цAMФ фосфодіестеразами, селективна активація ПКА, пригнічення активності ПКА інгібіторним пептидом. Цікаво, що нижча біодоступність ПТГсБ для ПТГ1Р зумовлює його меншу ефективність порівняно з пептидами ПТГ, котрі використовувалися як остеоанаболічні засоби.
Вплив ПТГ на кістку може бути катаболічним або анаболічним. Резорбцію кісток ПТГ стимулює через шлях OPG-RANKL-RANK (остеопротегерин [OPG] – ліганд рецептора-активатора ядерного фактора κВ [RANKL] – рецептор активатора ядерного фактора κВ [RANK]). Зокрема, ПТГ модулює експресію RANKL і OPG на мезенхімальних стовбурових клітинах (попередники остеобластів) та остеоцитах; зв’язується з RANK на поверхні остеокластів та їхніх гемопоетичних попередників, сприяючи диференціації, виживанню й активності цих клітин; зв’язується з RANKL, пригнічуючи взаємодію RANK-RANKL. Баланс цих впливів визначає остеокластогенез. Основним джерелом RANKL є остеоцити. Безперервна інфузія ПТГ гризунам збільшувала кодування мРНК для RANKL, зменшуючи кодування мРНК для OPG, що підвищувало співвідношення RANKL/OPG та сприяло остеокластогенезу й резорбції кісток. Імовірно, в людини ПТГ так само регулює шлях OPG-RANKL-RANK. У пацієнтів з ПГПТ рівні RANKL, OPG та RANKL/OPG були вищими, ніж у здорових осіб групи контролю; високі рівні RANKL позитивно корелювали з показниками резорбції кісток і частотою втрати загальної кісткової маси стегнової кістки. Через 1 рік після паратиреоїдектомії співвідношення RANKL/OPG знижувалося. Іншим потенційним посередником ПТГ-залежної резорбції кісток є моноцитарний хемоатрактант-1 (MCP-1) – хемокін моноцитів і макрофагів. Дослідження in vitro й in vivo показують, що MCP-1 є хемоатрактантом для попередників остеокластів і стимулює остеокластогенез, зумовлений RANKL, посилюючи резорбцію кісток. Лікування ПТГ посилювало експресію MCP-1 у щурів. Рівні MCP-1 прямо корелювали з рівнями ПТГ у пацієнтів з ПГПТ і помітно та швидко знижувалися після паратиреоїдектомії. Резорбція кісток, опосередкована ПТГ, особливо впливає на компактну (кортикальну) кістку. Тривалий вплив надлишку ПТГ сприяє ремоделюванню та демінералізації скелета, зменшує МЩКТ і підвищує ризик остеопоротичних переломів.
Дослідження на мишах підтвердили важливу анаболічну роль ПТГ у формуванні кісток плода та загоєнні переломів. На відміну від постійного ендогенного впливу, інтермітивне введення екзогенного ПТГ стимулює кісткоутворення. Впровадження в клінічну практику агоністів ПТГ1Р (терипаратиду, абалопаратиду) сприяло їх схваленню як остеоанаболічних засобів для лікування остеопорозу. Інтермітивне введення ПТГ активує «анаболічне вікно» – період, коли стимулюється утворення кістки без її резорбції. ПТГ забезпечує диференціацію остеобластів і пригнічує їх апоптоз через сигнальні шляхи цAМФ/ПКА. Анаболічна дія реалізується через активацію генів, пов’язаних з формуванням кістки (Runx2, остеокальцин, лужна фосфатаза – ЛФ), і сигнальні шляхи кісткового морфогенетичного білка. ПТГ пригнічує експресію склеростину – глікопротеїну, що блокує формування кістки. У пацієнтів з ПГПТ виявлено нижчі рівні склеростину та їх підвищення після паратиреоїдектомії. Іншим інгібітором кісткоутворення є Dickkopf1 (DKK-1); проте його реакція на ПТГ недосить вивчена.
Баланс між утворенням і резорбцією кістки визначає загальний ефект ПТГ. При зниженні рівня кальцію (Ca2+) в позаклітинному просторі ПТГ швидко активує резорбцію кістки для підтримання нормокальціємії. Дефіцит ПТГ знижує кісткове ремоделювання, що може підвищувати МЩКТ, але вплив на ризик переломів не з’ясований (табл. 1). Загалом ПТГ є ключовим регулятором ремоделювання кісток.
Гіперпаратиреоз
Первинний гіперпаратиреоз
ПГПТ – це надмірна та неадекватна секреція ендогенного ПТГ однією або кількома ПЩЗ, що призводить до гіперкальціємії через порушення зворотного контролю за рівнем кальцію. Частота ПГПТ становить 34-120 випадків на 100 000; більшість пацієнтів – це жінки після менопаузи. Імовірно, естроген пригнічує резорбцію кістки, а його дефіцит після менопаузи дає ПТГ змогу повністю реалізувати свій ефект, спричиняючи гіперкальціємію. Підтвердженням цієї теорії є позитивні впливи естрогену та ралоксифену на кістковий обмін і біохімічні показники при ПГПТ.
Серед амбулаторних пацієнтів ПГПТ є основною причиною гіперкальціємії. 75-85% випадків спорадичного ПГПТ зумовлені одиничною доброякісною аденомою, 15-25% – мультигландулярною аденомою або гіперплазією ПЩЗ, зрідка (<1%) – раком ПЩЗ. Близько 5-10% випадків мають спадкову або синдромну природу: синдром множинної ендокринної неоплазії (MEN1 – найчастіше); MEN2A; MEN4; ізольований сімейний гіперпаратиреоз; синдром HPT-JT («гіперпаратиреоз – щелепна пухлина»).
Стосовно діагностики, передусім слід виключити ВГПТ, спричинений нирковою недостатністю, дефіцитом вітаміну D або діуретичною терапією. Для підтвердження ПГПТ потрібний біохімічний аналіз крові, хоча спектр показників може бути різним. Наприклад, у разі класичного ПГПТ визначаються гіперкальціємія та неадекватно високий ПТГ. Близько 20% випадків становить нормогормональний ПГПТ, коли гіперкальціємія поєднується з нормальними значеннями ПТГ. Нарешті, нормокальціємічний ПГПТ (нкПГПТ) – це стійке підвищення ПТГ з нормальним рівнем кальцію в сироватці крові за відсутності вторинних причин; із часом цей тип може перейти в класичну форму. Вкрай важливо диференціювати ПГПТ та сімейну гіпокальціуричну гіперкальціємію (СГГ), бо, попри схожі біохімічні показники, лікування цих станів різне: при ПГПТ показана паратиреоїдектомія, тоді як у разі СГГ операція протипоказана через відсутність впливу на гіперкальціємію. Для диференціації використовують коефіцієнт кліренсу кальцію/креатиніну: значення >0,02 характерне для ПГПТ; показники <0,01 вказують на СГГ. Однак у 40% людей з будь-яким станом можливі значення в межах 0,01-0,02.
За останні 50 років клінічна картина ПГПТ змінилася. Раніше діагноз установлювали за наявності тяжких уражень кісток, патологічних переломів або ниркових каменів чи кальцифікатів. Нині ПГПТ частіше діагностують випадково, виявляючи гіперкальціємію при біохімічному скринінгу. Відповідно, частка безсимптомного ПГПТ (бсПГПТ) та нкПГПТ суттєво зросла. На відміну від класичного ПГПТ, вказані варіанти не мають системних ускладнень, але кісткова тканина залишається основною мішенню. ПГПТ спричиняє втрату МЩКТ у специфічних ділянках і підвищує ризик патологічних переломів. Усім пацієнтам рекомендовано вимірювати МЩКТ у ділянках кульшового суглоба, поперекового відділу хребта та дистальної частини променевої кістки, бо затримка діагностики призводить до тяжких ускладнень: фіброзно-кістозного остеїту, повторних переломів або затримки їх зрощення. Після підтвердження діагнозу визначають тактику лікування. Єдиним радикальним методом є оперативне видалення ПЩЗ. Візуалізація (ультразвукове дослідження + сцинтиграфія з технецієм Tc-99m) допомагає локалізувати уражену залозу та виявити супутню патологію щитоподібної залози. У складних випадках, за підозри на множинне ураження або ектопічну паращитоподібну тканину, застосовують КТ-4D, магнітно-резонансну томографію, однофотонну емісійну комп’ютерну томографію або ПЕТ/КТ з холіном. Показання до паратиреоїдектомії узагальнено в таблиці 2.
Ураження кісток за спорадичного ПГПТ
Вплив ПГПТ на ремоделювання, МЩКТ, якість кісток і ризик переломів
Надлишок ПТГ прискорює ремоделювання кісток, зміщуючи баланс у бік резорбції. Це супроводжується підвищенням рівнів OPG і RANKL у сироватці крові та зниженням співвідношення OPG/RANKL, а також підвищенням біохімічних маркерів кісткового обміну. Встановлено позитивну кореляцію між рівнем ПТГ й остеокальцином і ЛФ. ПТГ спричиняє витончення губчастої, ендо- й інтракортикальної поверхонь, розширення мозкової порожнини, пористість і утворення кортикальних залишків, схожих на трабекули. Денситометрія та гістоморфометрія показали, що найбільше уражується компактна (кортикальна) кістка, тоді як губчаста (трабекулярна) зберігається, що підтверджено даними біопсії клубової кістки. Проте вивчення сегментації трабекул виявило знижену осьову організацію та зв’язність трабекулярної мережі, зменшення співвідношення пластинчастих і стрижневих трабекул. Імпакт-мікроіндентація in vivo показала зниження індексу міцності кісткового матеріалу в пацієнтів з ПГПТ (особливо в осіб із частими переломами) порівняно зі здоровими людьми.
Зниження МЩКТ відображає катаболічну дію ПТГ. Тому МЩКТ слід вимірювати методом двохенергетичної рентгенівської абсорбціометрії (DXA) не тільки в поперековому відділі хребта, кульшовому суглобі та шийці стегнової кістки, а й у дистальній третині променевої кістки – ділянці з переважно компактною структурою, що насамперед уражається внаслідок надлишку ПТГ. Зважаючи на те що ПГПТ змінює мікроархітектуру кістки, МЩКТ не є єдиним предиктором ризику переломів. Для оцінювання мікроархітектури, залучення губчастих кісток і ризику переломів корисні: оцінка хребцевих переломів (VFA), індекс трабекулярної кістки (TBS) та високороздільна периферична кількісна комп’ютерна томографія (HRpQCT). Раніше зафіксована висока трабекулярна щільність пояснюється хибним урахуванням кортикальних залишків, які не відрізняються від справжніх трабекул під час візуалізації. Метааналіз показав значне зниження МЩКТ в усіх ділянках у пацієнтів з ПГПТ порівняно з контролем. TBS – показник текстури губчастої кістки, що визначається під час DXA, корелює з ризиком переломів і деформацією хребта незалежно від МЩКТ, віку, статі й індексу маси тіла. Індекс перевантаження кістки – новий якісний показник, який можна визначити під час DXA, порушується в пацієнтів з ПГПТ порівняно з контролем.
На клінічні прояви ПГПТ впливають стать і місце проживання: жінки до менопаузи та чоловіки мають вищий ризик нефролітіазу, але однакові показники T-score поперекового відділу хребта й кульшового суглоба; жінки після менопаузи частіше страждають від остеопорозу. При порівнянні жінок європейського походження зі США й Італії вищу МЩКТ виявлено в пацієнток зі США.
У пацієнтів з ПГПТ вищий ризик переломів будь-якої локалізації – відносний ризик 1,71 порівняно зі здоровими людьми. Найуразливішими є губчасті кістки: хребці (відношення шансів 2,57), ребра, дистальна третина кісток передпліччя (відношення шансів 2,36). Додатковими факторами ризику є старший вік, тривалість менопаузи, знижена МЩКТ у дистальній третині променевої кістки та поперековому відділі хребта.
Отже, ПГПТ знижує МЩКТ, насамперед у жінок після менопаузи. Зниження якості кісток підвищує ризик переломів.
Фіброзно-кістозний остеїт
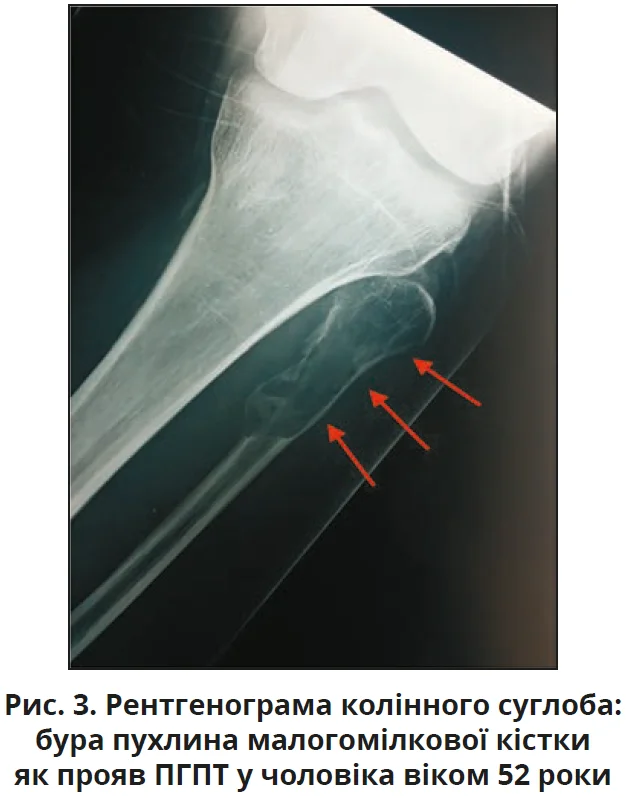
На сьогодні класичні кісткові прояви фіброзно-кістозного остеїту є рідкісними (<2%). Частіше це ускладнення трапляється при вторинному або третинному гіперпаратиреозі внаслідок хронічної ниркової недостатності. Основними симптомами є слабкість, біль у кістках, патологічні переломи; можливі неспецифічні симптоми (закрепи, нейропсихічні симптоми, нефролітіаз). Радіологічні ознаки: «сіль/перець» або «матове скло» в черепі (демінералізація); резорбція дистального кінця ключиці та фаланг; кісткові кісти, бурі пухлини, остеокластоми, дифузна остеопенія. Бурі пухлини – неонкологічні утворення, що складаються з остеокластів, грануляційної, фіброзної та судинної тканин з відкладенням гемосидерину й не повністю мінералізованої кістки внаслідок надмірної активності остеокластів; типова локалізація: щелепи, череп, таз, ключиця, ребра, стегна, хребет. Пухлини можуть бути одиничними або множинними (рис. 3), при візуалізації часто імітують доброякісні (кісти, фіброзна дисплазія) або злоякісні ураження, але біль за них менш інтенсивний, супроводжується типовими ознаками ПГПТ. Значно знижена МЩКТ відновлюється після успішної операції. При тяжкому ПГПТ значно підвищені рівні кальцію та ПТГ у сироватці крові. Через те що ПГПТ характеризується посиленням ремоделювання кісток, підвищуються біохімічні маркери як остеосинтезу (ЛФ, остеокальцин), так і резорбції кісток (N-термінальний телопептид [NTX], C-телопептид [CTX]).
Ураження кісток за нормокальціємічного ПГПТ
Стан з нормальними рівнями загального й іонізованого кальцію, але підвищеним рівнем інтактного ПТГ у ≥2 вимірюваннях протягом 3-6 місяців за відсутності причин ВГПТ визначають як нкПГПТ. Серед пацієнтів, яким проводили DXA, поширеність нкПГПТ становила 0,18%.
В одній когорті виявлено, що кістковий фенотип нкПГПТ подібний до такого в групі контролю: нормальне ремоделювання кісток, відсутність значних змін МЩКТ, текстури кістки та ризику переломів. Інші дослідження виявили остеопороз хребта та стегна в 57% пацієнтів із частотою переломів 11%; дистальний відділ променевої кістки уражався рідше. Порівняння з гіперкальціємічним ПГПТ показало, що пацієнти з нкПГПТ можуть бути резистентними до дії ПТГ на кістки та нирки; не виявлено також значних відхилень за індексом перевантаження кістки. Дослідження WHO MONICA не виявило підвищеного ризику переломів у пацієнтів з нкПГПТ впродовж 17 років спостереження.
Отже, дані щодо нкПГПТ суперечливі: частина досліджень не виявляє його впливу на кістки, інші фіксують зниження МЩКТ, але менш виражене та без кортикальної локалізації, типової для класичного ПГПТ. Ризик переломів здебільшого не перевищує показники в групі контролю. Виникає питання, чи є нкПГПТ справжнім клінічним станом, чи лише біохімічним варіантом поза межами норми загальної популяції.
Ураження кісток за безсимптомного ПГПТ
Спостережні дослідження показали, що в більшості пацієнтів без нефролітіазу, фіброзно-кістозного остеїту, класичних симптомів, гіперкальціємії >3,00 ммоль/л і азотемії протягом 10 років не відбувається значного прогресування біохімічних показників чи змін МЩКТ. Утім, можливе зниження якості життя. В одному дослідженні спостерігалося прогресування хвороби у 25% пацієнтів цієї когорти, причому в осіб до 50 років виявлено втричі вищий ризик виникнення ≥1 нового показання для паратиреоїдектомії.
Нові методи оцінювання (TBS, HRpQCT) виявили вираженіші ураження кісток, аніж вважалося раніше. Загальний ризик переломів у пацієнтів з бсПГПТ у 1,5 раза вищий. Надлишок ПТГ змінює геометрію кістки: посилює ендостальну резорбцію та періостальну аппозицію, що збільшує переважно внутрішній діаметр довгих кісток при збереженні механічних властивостей компактних кісток. Уражаються губчасті та компактні кістки, але в кістках, які несуть вагу (наприклад, великогомілковій), ефект менш виражений, аніж у променевій. Спостерігається зменшення товщини кортикального шару шийки стегнової кістки, що збільшує осьове навантаження, підвищуючи ризик переломів.
Відповідно, пацієнти з бсПГПТ зазвичай залишаються стабільними, але можуть мати поступове погіршення біохімічних показників, щільності та мікроархітектури кістки, що збільшує ризик переломів губчастих і компактних кісток.
Ураження кісток за синдромних варіантів ПГПТ
l ПГПТ за синдрому множинної ендокринної неоплазії (MEN)
MEN-синдроми (MEN1, MEN2A, MEN2B, MEN4) – спадкові автосомно-домінантні ендокринні хвороби – становлять 5-10% усіх випадків ПГПТ та часто супроводжуються множинними пухлинами ПЩЗ. Генетичне тестування переконливо рекомендується пацієнтам з ПГПТ віком до 30 років за підозри на синдромний ПГПТ (підозра на ураження кількох ендокринних залоз за даними анамнезу або візуалізації, виявлення інших ендокринних пухлин, атипової аденоми чи карциноми ПЩЗ, сімейний анамнез гіперкальціємії або синдромів MEN1, MEN2A, MEN4, HPT-JT).
Найпоширенішим є MEN1, спричинений мутаціями гена MEN1, який кодує білок-супресор пухлини менін. Характеризується пухлинами ПЩЗ, аденогіпофіза й острівців підшлункової залози. У 95% пацієнтів першим проявом хвороби є ПГПТ (середній вік – 20-25 років). У структурі ПГПТ поширеність MEN1 становить 2-4%. У більшості випадків гіперкальціємія виникає у віці до 50 років. Щодо впливу на кістки, то зниження МЩКТ подібне до спорадичного ПГПТ, але починається раніше (30-40 років). У різних дослідженнях зниження МЩКТ виявлено у 86% пацієнтів; 18% пацієнтів мали остеопороз; у 50% пацієнтів до 35 років спостерігалася значна остеопенія. Найчастіше уражаються шийка стегнової кістки та поперекові хребці. За даними DXA в пацієнтів з MEN1 нижча МЩКТ, ніж у разі спорадичного ПГПТ, але HRpQCT не виявила різниці в геометрії чи мікроархітектурі між двома когортами. Загалом кісткове ураження за MEN1 тяжче, ніж у разі спорадичного ПГПТ, тоді як ураження нирок подібне. TBS може бути чутливим показником для виявлення порушень мікроархітектури губчастих кісток.
Можна виокремити такі особливості ПГПТ, спричиненого синдромом МЕN1: а) вік <50 років; б) відсутність типового зворотного зв’язку між рівнем ПТГ і МЩКТ, притаманного для спорадичних випадків; в) наявність інших ендокринних порушень (гіперпролактинемія, гіперкортицизм, гіпогонадизм, дефіцит гормону росту), що зумовлюють втрату кісткової маси; г) є дані про прямий вплив гена MEN1 на кісткову фізіологію: в мишей з дефіцитом меніну остеобласти демонстрували порушену мінералізацію та знижену чутливість; менін безпосередньо пригнічував міогенну диференціацію мезенхімальних клітин, одночасно прискорюючи ріст остеобластів.
Існує три клінічні варіанти MEN2: MEN2A, MEN2B та медулярний рак щитоподібної залози (MРЩЗ). Причинами MEN2A та MEN2B є мутації протоонкогена RET, який кодує рецептор тирозинкінази. Найпоширенішим є MEN2A, для котрого характерні MРЩЗ, пухлини ПЩЗ (20-30%) і феохромоцитома (50%); перебіг ПГПТ зазвичай безсимптомний і легший, аніж у разі синдрому MEN1. Основними характеристиками MEN2B є МРЩЗ та феохромоцитома; супутні ознаки охоплюють марфаноїдний фенотип, мієлінізовані нервові волокна рогівки, невроми слизових оболонок і дисфункцію кишкових вегетативних гангліїв. Кістковими проявами є сколіоз, деформації стоп, порушення метаболізму кістки та підвищений ризик переломів. У дослідженні 48 пацієнтів з MEN2B віком 5-36 років частота переломів була значно вищою, ніж у загальній популяції (38 проти 19%), переважно в ділянках епіфіза головки стегнової кістки, хребців і довгих кісток нижніх кінцівок.
Причиною MEN4 є мутації інгібітора циклічно-залежної кінази. Клінічні прояви охоплюють множинні пухлини ПЩЗ (80%), пухлини аденогіпофіза (40%) та інші пухлини – феохромоцитоми, пухлини шлунка. Даних про ураження кісток мало через рідкісність хвороби.
Отже, MEN1 характеризується тяжчим ураженням кісток через поєднання ПГПТ з іншими ендокринопатіями. У разі MEN2 прояви ПГПТ легші (MEN2A) чи майже відсутні (MEN2B). При MEN4 даних про кісткову патологію недостатньо.
l Синдром «гіперпаратиреоз – щелепна пухлина»
Синдром HPT-JT спричинений інактивувальними мутаціями гена супресора пухлини HRPT2/CDC73; проявляється осифікувальними фібромами верхньої або нижньої щелепи, аденоматозними поліпами матки, пухлинами нирок і підвищеним ризиком карциноми ПЩЗ. У більшості випадків виникає ПГПТ; подальше ураження кісток характеризується остеопорозом та/або остеопенією, осифікувальними фібромами верхньої та нижньої щелеп, фіброзно-кістозним остеїтом.
l Сімейна гіпокальціурична гіперкальціємія
СГГ – автосомно-домінантна хвороба внаслідок інактивувальних мутацій у сигнальному каскаді CaSR. Існує три форми хвороби: СГГ1 – мутації гена CaSR (хр. 3q21.1; описано >300 варіантів CaSR, переважно місенс-мутації перших 350 амінокислот у позаклітинному домені рецептора), поширеність становить 1×1000-5000; СГГ2 – мутації GNA11 (хр. 19p13.3; описано лише 4 варіанти гена GNA11 зі втратою функції – T54M, L135Q, I200del, F220S), дуже рідкісна; СГГ3 – мутації AP2S1 (хр. 19q13.32, мутації зі втратою функції, які найчастіше впливають на залишок R15, – Arg15Cys, Arg15His і Arg15Leu), поширеність становить 1×13 000.
Зазвичай СГГ1 безсимптомна зі стабільною легкою гіперкальціємією впродовж життя, ПТГ нормальний/підвищений, рівні фосфатів у межах низької норми, екскреція кальцію із сечею низька. При СГГ3 рівні кальцію вищі, ніж у разі СГГ1. Загалом біохімічні зміни при СГГ схожі на спорадичний ПГПТ, за винятком зниження співвідношення кліренсу кальцію до креатиніну <0,01 у певної частки пацієнтів. Тому, щоб уникнути непотрібної операції, важливі сімейний анамнез і генетичне тестування.
Щодо кісткових змін, то для СГГ1 характерні нормальна площинна МЩКТ на всіх ділянках, вища МЩКТ у стегновій кістці та кістках передпліччя порівняно з ПГПТ, нижчі рівні маркерів кісткового ремоделювання (ЛФ, відношення NTX/креатинін у сечі). Частота переломів, за даними різних досліджень, становить 5-14% випадків, частіше трапляється хондрокальциноз (22%). При СГГ3 у частини пацієнтів виявлено низьку МЩКТ у поперекових хребцях і шийці стегнової кістки.
Тож міцність кісток у разі СГГ (особливо СГГ1) не порушена. Для диференціації з ПГПТ потрібно провести генетичне тестування. За високого ризику переломів можливе застосування антирезорбтивних препаратів, хоча доказів поки недостатньо.
Література
Roumpou A., Palermo A., Tournis S., et al. Bone in parathyroid diseases revisited: evidence from epidemiological, surgical and new drug outcomes. Endocr. Rev. 2025 Jul 15; 46 (4): 576-620. doi: 10.1210/endrev/bnaf010.