Хронобіологія гормонотерапії: коли приймати ліки?
Підготувала канд. мед. наук Ірина Жакун
Центральною ланкою взаємодії ендокринної та нервової систем організму людини є гіпоталамус, у передній частині якого розташовані супрахіазматичні ядра (СХЯ). Цей «головний годинник» організму, основними елементами якого є гени CLOCK1 і BMAL2, контролює ритми секреції гормонів. Торік італійські науковці E. Colonnello, A. Graziani, R. Rossetti та співавт. провели аналіз досліджень і підготували огляд, який висвітлює циркадну регуляцію гормональних систем і наслідки порушень біоритмів організму людини [1].
Система «гіпоталамус – гіпофіз – щитоподібна залоза (ЩЗ)» підпорядковується циркадному ритму, який задають СХЯ. Рівень тиреотропного гормону (ТТГ) гіпофіза зростає ввечері, досягає піку вночі та знижується вранці. Рівні тироксину (Т4) та трийодтироніну (Т3) максимальні зранку й мінімальні ввечері, Т3 підвищується за 90 хвилин після виділення в кров ТТГ. Існують також ультрадіанні ритми, що залежать від сну, пори року й особливостей харчування. Нестача сну підвищує ранковий ТТГ, а зменшення його тривалості знижує ТТГ та рівень Т4. Улітку ТТГ нижчий, аніж узимку, через реакцію на холод. Порушення сну, змінна робота та джетлаг порушують ритми й підвищують ризик виникнення хвороб ЩЗ.
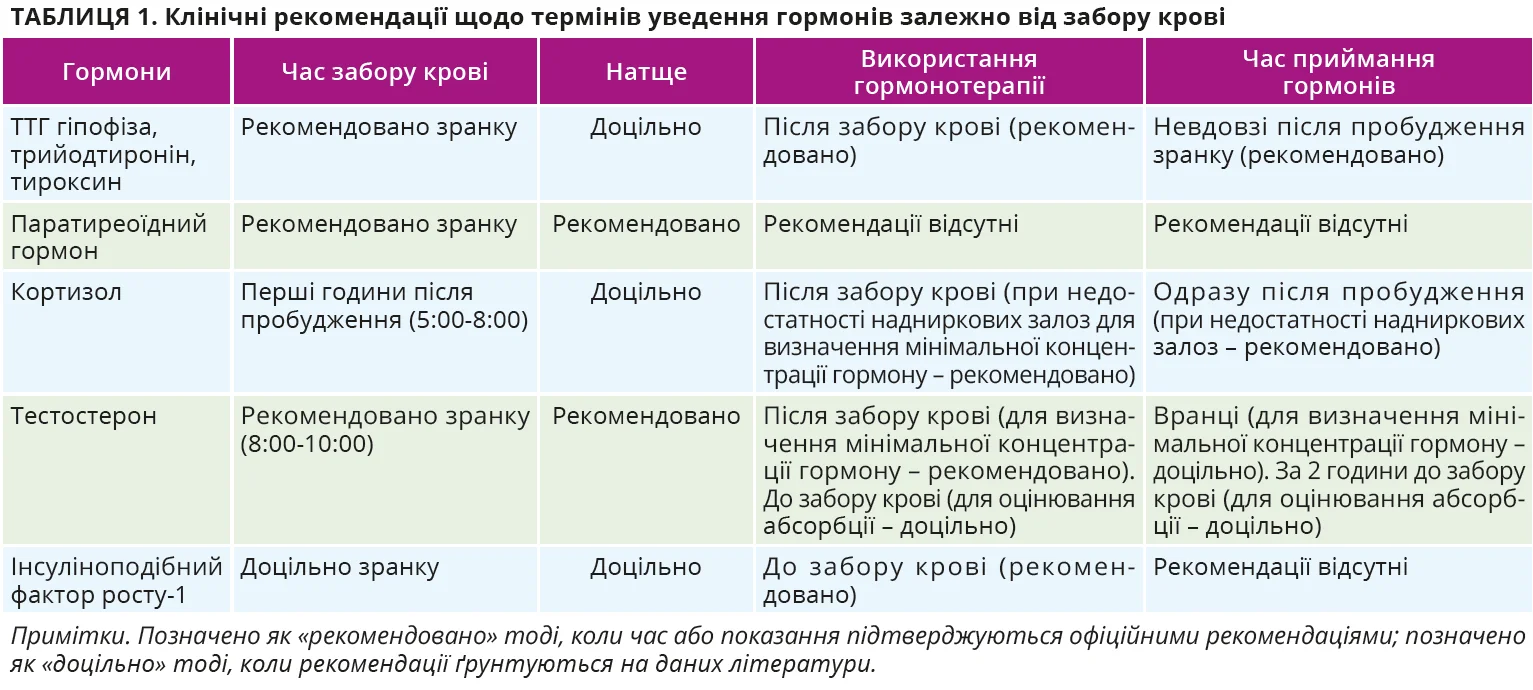
Циркадний ритм ТТГ зберігається в пацієнтів, які приймають препарати Т4 або Т3, але найкращий час для застосування гормонів ЩЗ точно не визначено. Препарати Т4 та Т3 рекомендовано приймати натще. Рівень вільного Т4 підвищується приблизно за 2 години від застосування. Американська тиреоїдна асоціація радить приймати левотироксин за годину до сніданку або перед сном (понад 3 години після вечері). Метааналіз показав, що ефективність приймання перед сном така сама, як і перед сніданком, хоча рівень вільного Т4 ввечері може бути незначно вищим. Вечірній час може бути зручнішим, коли вечеря не надто пізня. На всмоктування левотироксину впливають продукти харчування та ліки: соя, клітковина, кава, кальцій, препарати заліза, сукральфат, жовчні кислоти, орлістат, антациди, інгібітори протонної помпи. Потрібно уникати одночасного призначення цих медикаментів і левотироксину. Оскільки ендогенний Т4 має ранковий пік, а застосування препаратів Т4 зміщує його пік приблизно на 9 годин, ранкове приймання є оптимальним, оскільки є фізіологічнішим. Якщо пацієнту ранковий і вечірній варіанти однаково зручні, бажано обрати ранок. Хоча єдиної думки щодо належного часу забору зразків крові для визначення рівнів гормонів ЩЗ немає, рекомендовано проводити забір крові вранці натще, до початку гормонотерапії (табл. 1).
Паратиреоїдний гормон (ПТГ) також має чіткий циркадний ритм: піки його рівнів реєструються зранку та ввечері. Для забору крові на ПТГ рекомендовано ранкові години, бажано натще. Голодування призводить до зниження концентрації ПТГ та робить його добовий ритм менш виразним. Окрім того, рівні ПТГ змінюються сезонно: найнижчі значення реєструються влітку. Секреція ПТГ відбувається імпульсоподібно – близько 6-7 разів на годину. Такий ритм секреції стимулює кісткоутворення, на відміну від тривалого підвищення рівня ПТГ. У пацієнтів з первинним гіперпаратиреозом циркадний ритм ПТГ зникає.
У лікуванні хворих на гіпопаратиреоз використовують рекомбінантні форми ПТГ. Інтермітивний ритм уведення цих препаратів забезпечує анаболічний ефект. Терипаратид (синтетичний аналог фрагмента ПТГ) застосовують 1 раз на добу для лікування остеопорозу. При хронічному гіпопаратиреозі частіші ін’єкції (2-4 рази на день) краще відтворюють фізіологічну секрецію та потребують менших добових доз. З огляду на циркадний ритм ПТГ й обмежені клінічні дані, введення препаратів ПТГ зранку є оптимальним (табл. 1).
Добові коливання глюкокортикоїдів (ГК) мають чіткий циркадний ритм, який задають СХЯ. Самі гормони кори наднирковиків також синхронізують «периферичні годинники». Кортизол у нормі підвищується близько 3-4-ї ранку та досягає піку після пробудження, його мінімум спостерігається опівночі. Через це рівень кортизолу рекомендують вимірювати рано-вранці натще. Порушення циркадного ритму кортизолу пов’язують з підвищеним ризиком виникнення метаболічних і серцево-судинних хвороб. Дослідження показали, що зміщення піку кортизолу до вечора погіршує толерантність до глюкози, підвищення його рівня вночі частіше виявляється у хворих на артеріальну гіпертензію, метаболічний синдром, ожиріння та цукровий діабет. У хворих на синдром Кушинга втрата добового ритму є ключовим фактором розвитку метаболічних ускладнень.
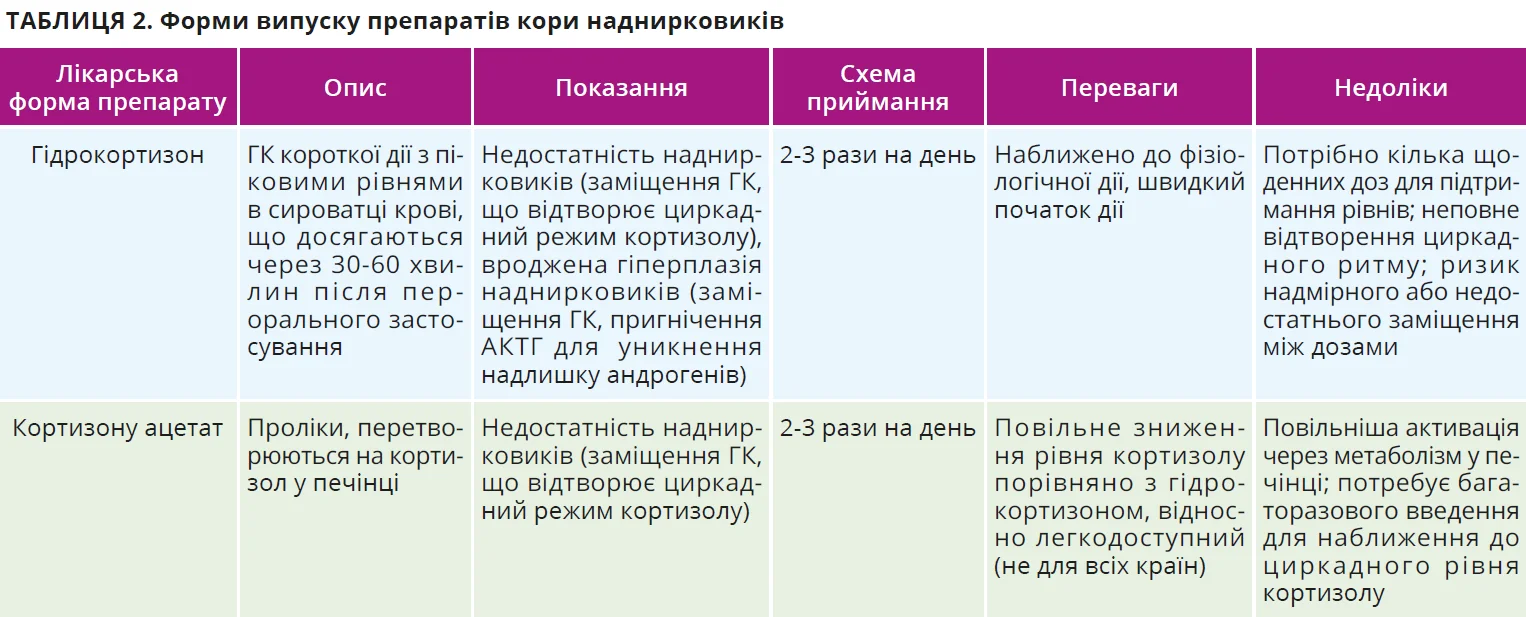
Пацієнтам, які мають наднирковозалозну недостатність, потрібна замісна терапія, що максимально імітує природний ритм. Гідрокортизон або кортизону ацетат призначають у 2-3 прийоми з найбільшою дозою зранку, але ця схема лише частково відтворює фізіологічний профіль. Нові форми гідрокортизону з подвійним вивільненням забезпечують ранковий пік і поступове зниження впродовж дня, що покращує метаболічні показники та самопочуття хворих. Метою терапії пацієнтів з уродженою гіперплазією наднирковиків є нормалізація не лише вмісту кортизолу, а й надлишкового адренокортикотропного гормону (АКТГ) й андрогенів. Тому інколи використовують потужніші ГК (преднізолон, дексаметазон), але ризик побічних ефектів цих препаратів високий. Нові форми гідрокортизону з поступовим вивільненням дають змогу краще контролювати нічний підйом АКТГ та знизити загальну добову дозу ГК (табл. 2).
Вироблення тестостерону також має виразний циркадний ритм. Максимальні значення визначаються близько 8-ї години ранку, після чого його рівень поступово знижується до вечора. Нічне підвищення пов’язане зі стадіями сну. У чоловіків, які хворіють на гіпогонадизм, коливання рівнів тестостерону не виразні. У нормі рівень тестостерону контролюється гонадотропін-рилізинг-гормоном гіпоталамуса та лютеїнізувальним гормоном (ЛГ) гіпофіза, а також циклічними змінами чутливості яєчок до ЛГ. Хоча ритм виділення гормонів найбільше залежить від циклу «сон – неспання», ЛГ має власні циркадні коливання, тому вночі відзначаються нижча частота та вища амплітуда імпульсів його вироблення.
З віком добовий ритм тестостерону змінюється через зміни секреції ЛГ, зниження чутливості яєчок і порушення роботи стероїдопродукувальних клітин. У людей, які працюють уночі, частіше виникають симптоми гіпогонадизму й еректильна дисфункція. Порушення ритму та зниження рівня тестостерону асоціюються зі зменшенням чутливості до інсуліну, метаболічним синдромом і збільшенням вісцерального жиру. Оскільки натще рівень тестостерону вищий, сучасні рекомендації радять визначати його зранку натще.
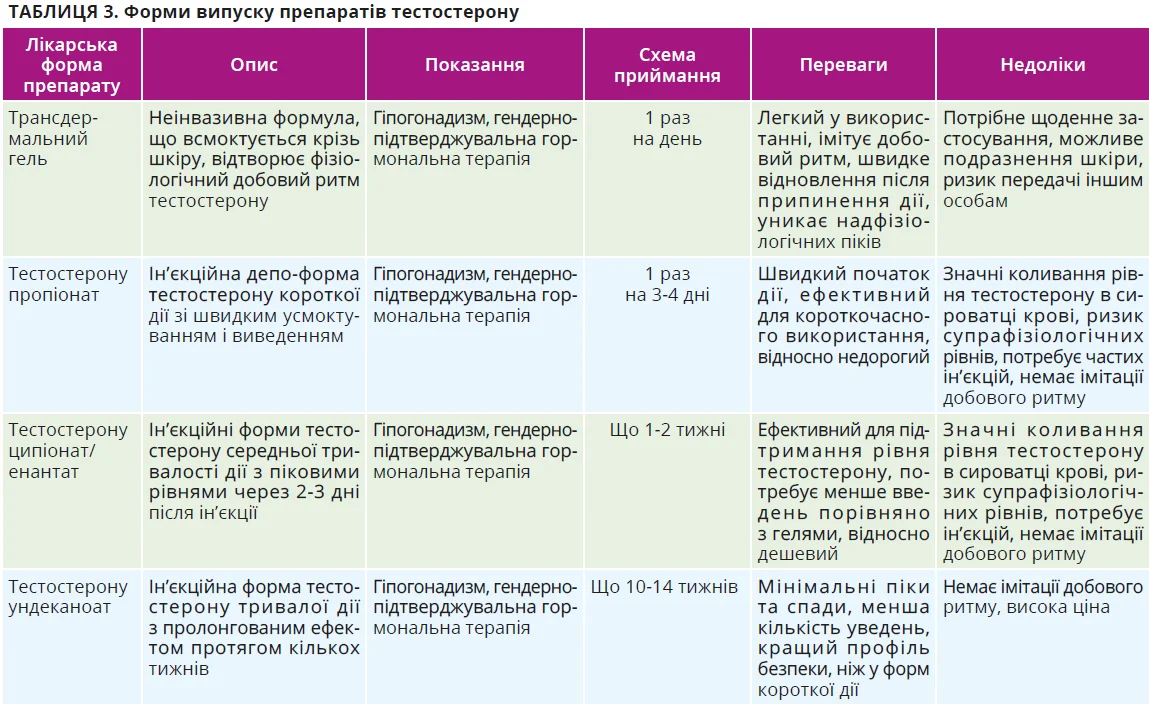
На сьогодні широко використовується замісна терапія тестостероном, розроблено різні форми введення препаратів. Трансдермальні форми (гель, розчини, пластирі) забезпечують усмоктування з піком через 2-4 години та поступове зниження, що відповідає природному ритму. Внутрішньом’язово вводять депо-препарати тестостерону (енантат, ципіонат, пропіонат, ундеканоат). Препарати короткої дії дають різкі піки та значні коливання тестостерону, що підвищує ризик побічних ефектів. Натомість тестостерону ундеканоат, який діє тривало, забезпечує стабільні фізіологічні рівні та не потребує частих ін’єкцій. Теоретично доцільнішим є введення трансдермальних препаратів зранку, оскільки це краще імітує фізіологічний добовий ритм тестостерону. Проте введення препарату перед сном може сприяти дотриманню пацієнтами режиму лікування. Препарати тривалої дії з депо-формою мають значну перевагу двомісячного або щоквартального введення, але їм бракує здатності адаптуватися до добових ритмів (табл. 3).
Естрогени тісно пов’язані із циркадною системою. Вільний естрадіол має складний добовий ритм, тоді як прогестерон секретується як цілодобово, так і ультрадіанно, досягаючи максимуму приблизно о 18-й годині. Характер ритмів змінюється залежно від фази циклу: під час фолікулярної фази спостерігаються добові коливання естрадіолу та прогестерону, тоді як у лютеїновій фазі цей патерн втрачається. Ранковий пік естрадіолу зміщується залежно від фази циклу. Порушення циркадних ритмів яєчників пов’язують з розвитком андрогенії, синдрому полікістозних яєчників (СПКЯ) та дисфункцією системи «гіпоталамус – гіпофіз – яєчники». Жінки, які працюють у нічні зміни, частіше хворіють на СПКЯ. У хворих на СПКЯ виявляють знижену експресію CLOCK і BMAL1, порушення стероїдогенезу та розлади сну.
Естрогени використовують для замісної терапії в період менопаузи або при гіпогонадизмі, для контрацепції та корекції менструальних порушень. Існують різні шляхи введення (пероральний, трансдермальний, вагінальний), які мають різну ефективність. Трансдермальний естрадіол найкраще імітує фізіологічні рівні, уникає печінкового «проходження» та має нижчий ризик тромбозів і метаболічних змін порівняно з пероральними формами. Пероральні форми прогестинів метаболізуються в печінці, що знижує їхні рівні. У жінок з інтактною маткою естрогенозамісна терапія має включати прогестин для профілактики гіперплазії ендометрія, а після гістеректомії призначають лише естроген.
Секреція інсуліну має виражений циркадний ритм: найнижчі рівні – вночі, найвищі – від опівдня до вечора. Дослідження показали, що чутливість β-клітин змінюється впродовж доби незалежно від сну чи харчування. У «біологічний вечір» толерантність до глюкози гірша через те, що слабшає раннє вивільнення інсуліну. Це пояснює кращий глікемічний контроль зранку. Секреція інсуліну також має ультрадіанні ритми, які регулюються «локальним панкреатичним годинником» за участю CLOCK і BMAL1. Порушення роботи цих генів погіршує секрецію інсуліну, знижує периферичне засвоєння глюкози та підвищує ризик розвитку цукрового діабету 2-го типу (ЦД2). Інсулін також регулює циркадні гени в жировій тканині: після їди він змінює їх експресію та є зовнішнім сигналом для периферичних тканин, який синхронізує внутрішній біологічний годинник організму з довкіллям.
Це підкреслює важливість часу приймання їжі, оскільки його зміна може спричиняти ожиріння й ЦД2.
Різні види інсуліну – швидкої, короткої, проміжної та тривалої дій – імітують природну секрецію гормону. Час уведення інсулінів тривалої дії залежить від глікемії, харчування, фізичної активності та типу препарату. Гларгін проявляє свою активність залежно від часу ін’єкції: при введенні інсуліну вранці він сильніше діє впродовж 12 годин, а при вечірньому – в другій половині доби. Тобто різниця активності визначається не типом інсуліну, а циркадними змінами чутливості тканин до нього. Пацієнтам із ЦД2, які не приймають ГК, частіше рекомендують вечірнє введення інсуліну. Якщо ж ГК приймають зранку та глюкоза підіймається вдень, інсулін тривалої дії доцільніше вводити вранці.
Лептин має чіткий 24-годинний ритм: його рівень підвищується на початку відпочинку та досягає максимуму під час нічного сну, а мінімуму – в другій половині дня. Зміщення сну на пізніший час зміщує й пік лептину, але зменшує його добові коливання. Ритм лептину тісно пов’язаний із циркадною регуляцією метаболізму, температурою тіла, рівнями глюкози й інсуліну. Лептин має власний циркадний ритм транспорту через гематоенцефалічний бар’єр, що впливає на апетит. Адипоцити також мають «внутрішній годинник», робота якого змінюється при дефіциті лептину.
Метрелептин застосовується при вродженому дефіциті лептину та деяких формах ліподистрофій. Його вводять підшкірно 1 раз на добу, бажано в один і той самий час для того, щоб підтримувати стабільний рівень гормону.
Функції глюкагоноподібного пептиду-1 (ГПП-1) в організмі людини полягають у зменшенні секреції глюкагону, стимуляції вивільнення інсуліну після їди та зменшенні апетиту. ГПП-1 виділяється згідно з добовим ритмом. У здорових чоловіків його рівень найвищий удень, з піком у післяобідній час, і найнижчий уночі. Секреція ГПП-1 контролюється внутрішнім циркадним механізмом і залежить від гена BMAL1, який узгоджує ритм роботи клітин, метаболізм і сон.
Час уведення агоністів рецептора ГПП-1 може впливати на їхню ефективність при ожирінні та діабеті. Препарат для лікування ЦД2 й ожиріння ліраглутид працює як аналог людського гормону ГПП-1, стимулює секрецію інсуліну та знижує апетит, сприяє зниженню ваги та контролю цукру крові. Його рекомендують уводити щодня в один і той самий час. Часто це роблять до сніданку, щоби краще пригнічувати апетит. Семаглутид потрібно приймати вранці натще, після нічного голодування. Після застосування слід зачекати щонайменше 30 хвилин перед їдою чи прийманням інших ліків.
Отже, оптимізація часу введення ліків відповідно до гормональних циркадних ритмів організму й індивідуального хронотипу є ефективною стратегією лікування ендокринної патології.
1 CLOCK – абревіатура Circadian Locomotor Output Cycles Kaput – фактор, що регулює циркадні ритми. 2 BMAL – абревіатура Brain and Muscle ARNT- Like – ключовий елемент циркадного годинника.
Література
Colonnello E., Graziani A., Rossetti R., et al. The chronobiology of hormone administration: “Doctor, what time should I take my medication?”. Endocrine Reviews. 2025; 46 (5): 670-689. doi: 10.1210/endrev/bnaf013.