Удосконалення лікування ожиріння: огляд терапевтичних утручань
Переклала й адаптувала д-р мед. наук Лариса Стрільчук
Ожиріння визначають як надмірне або аномальне накопичення жирової тканини в організмі центрально та підшкірно, що супроводжується ризиками для здоров’я. Протягом минулих декад поширеність ожиріння зростала з величезною швидкістю, чинячи навантаження на світову економіку. Історично ожиріння визначали як підвищення маси тіла щонайменше на 20% від ідеальної маси тіла. У сучасному світі ожиріння діагностується та класифікується лише на підставі визначення індексу маси тіла (ІМТ), що розраховують як масу тіла в кілограмах, поділену на зріст у метрах, піднесений до квадрату. Отже, маса тіла вважається нормальною при ІМТ 18,5-24,9 кг/м2, надлишкова маса тіла (НМТ) діагностується при ІМТ у межах 25-29,9 кг/м2, а ожиріння – при ІМТ ≥30 кг/м2. За даними Всесвітньої організації охорони здоров’я, у 2017 р. налічувалося майже 2 млрд дорослих з НМТ, понад 600 млн з яких мали ожиріння. В Америці поширеність ожиріння зросла з 6,8% у 1980 р. до 22,4% у 2019 р., а в Європі – з 8,4% у 1980 р. до 20% у 2019 р.
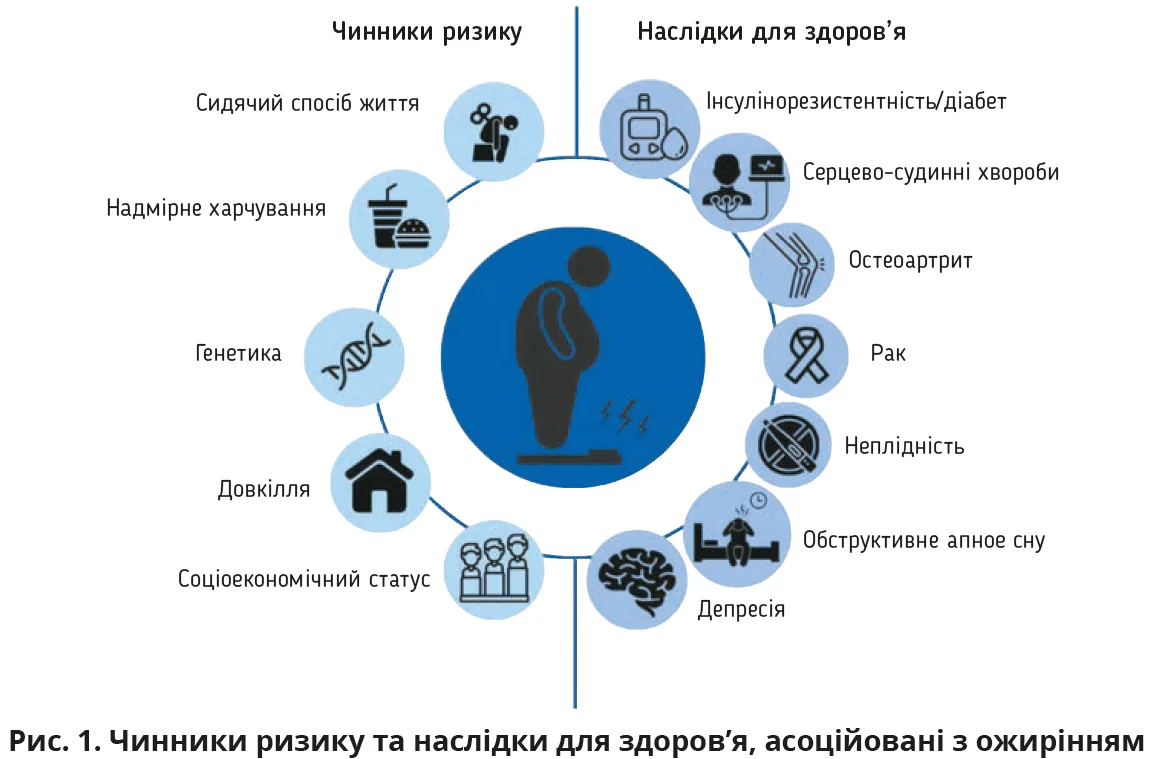
Ожиріння являє собою багатофакторну хворобу, спричинену комплексом генетичних і поведінкових чинників і факторів довкілля (рис. 1). Взаємодія між цими чинниками зумовлює складність ожиріння й утруднює його лікування через складний взаємозв’язок між різними генами й іншими факторами ризику: наприклад, способом життя та чинниками довкілля. Хоча особисте генетичне тло людини є одним із ключових факторів, котрі визначають як причину ожиріння, основа цієї хвороби полягає не в генетиці. Доказова база свідчить, що для впливу на масу тіла відповідні гени мають супроводжуватися впливом факторів способу життя та поведінки. Отже, подальше розуміння поширених причин ожиріння й набору ваги є дуже важливим. Нещодавно було ідентифіковано кілька генетичних факторів, які зумовлюють формування схильності до ожиріння, а також кілька генів, які регулюють масу тіла та метаболізм. Наприклад, ген, асоційований з масою жирової тканини й ожирінням, і ген рецептора меланокортину-4 асоціюються з підвищеною масою тіла та призводять до ожиріння; проте слід зауважити, що ожиріння неспроможна спричинити виключно генетика.
З іншого боку, в глобальній перспективі одними з причин ожиріння є смартфони, відеоігри, комп’ютери, телевізори та сидячий спосіб життя, поєднаний з нездоровим харчуванням і низьким рівнем фізичної активності. Діти та молоді дорослі, які постійно користуються ґаджетами, зазвичай ведуть неактивний спосіб життя та можуть споживати менше енергії, що порушує сигнальні системи їхнього апетиту й може призводити до переїдання.
Ожиріння підвищує ризик розвитку хронічних хвороб, зокрема цукрового діабету (ЦД) та серцево-судинних захворювань, знижує загальну якість життя, підвищує ймовірність виникнення раку. Наведені факти зумовлюють потребу пошуку ефективного лікування та профілактичних заходів для осіб з НМТ й ожирінням (табл.).
Наразі першою лінією заходів є модифікація способу життя, тобто підвищення фізичної активності та зміна харчування. Деякі пацієнти також можуть потребувати поведінкової терапії. Однак ефективність модифікації способу життя є незначною, крім того, більшість пацієнтів повторно набирають вагу після припинення змін способу життя. Фармакотерапія може застосовуватися сама чи на додачу до модифікації способу життя, але ефективність ліків усе одно є меншою за показники баріатричної хірургії.
Автори цього матеріалу провели систематичний огляд літератури в базах даних PubMed, EMBASE, MEDLINE, Scopus, Cochrane Library (CENTRAL) і Web of Science. Результат огляду представлено в цьому матеріалі.
Орлістат
Орлістат пригнічує шлункову й панкреатичну ліпази та знижує прандіальне всмоктування жирів, блокуючи гідроліз тригліцеридів. Відповідно, неперетравлені жири виділяються з фекаліями, що сприяє зниженню споживання калорій і зменшенню маси тіла.
Орлістату притаманна доведена, проте невисока ефективність. Дослідження продемонстрували здатність цього препарату зменшувати інсулінорезистентність, покращувати ліпідний профіль і антропометричні показники. Крім того, орлістат здатен дещо знижувати артеріальний тиск і запобігати розвитку ЦД 2-го типу.
Рекомендована доза орлістату становить 120 мг до 3 разів на добу; препарат треба приймати з їжею. Найпоширенішими побічними ефектами орлістату є світлий колір калових мас, діарея та здуття живота. Існують також дані, що орлістат здатен спричиняти дефіцит жиророзчинних вітамінів.
Ліраглутид
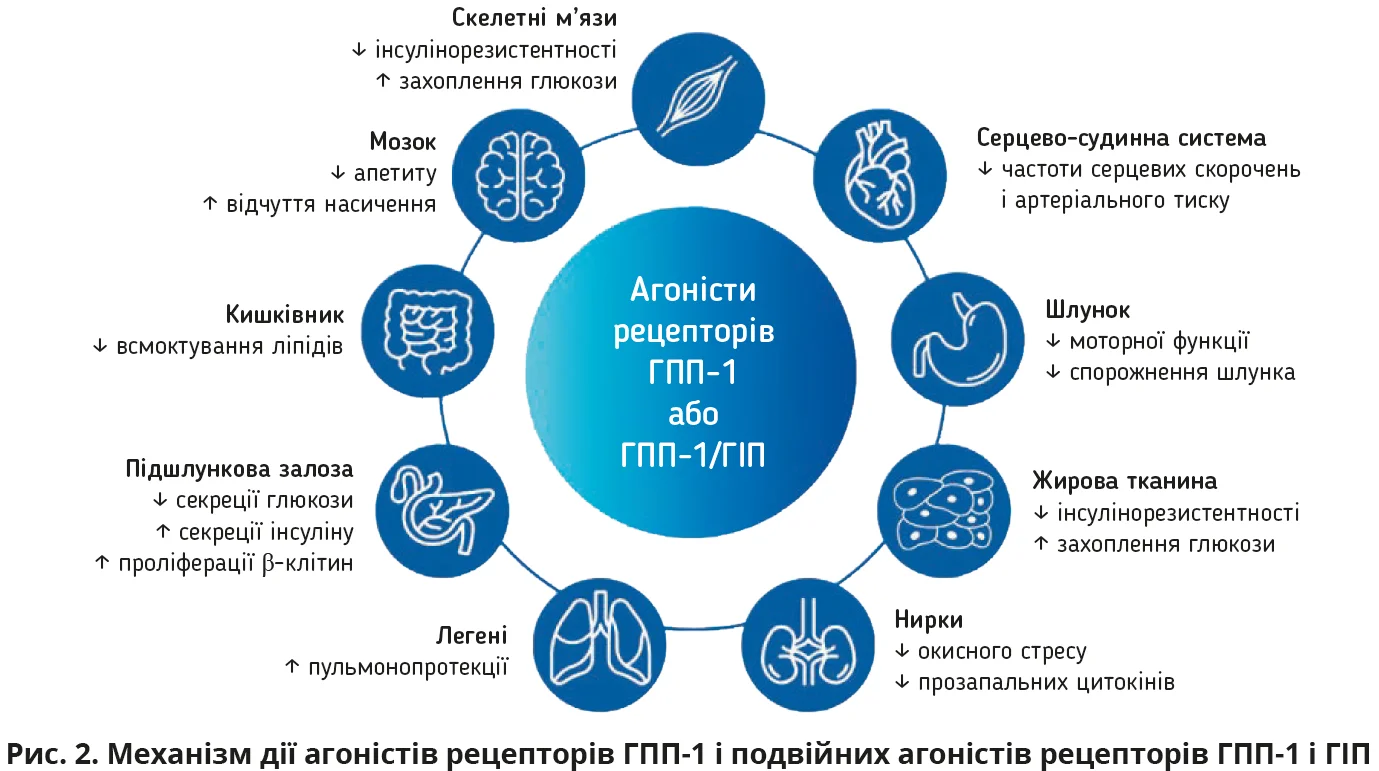
Ліраглутид застосовується для лікування ЦД 2-го типу й ожиріння. Механізм дії цього препарату імітує ефекти природного гормону – глюкагоноподібного пептиду-1 (ГПП-1), який вивільняється в кишківнику у відповідь на вживання їжі. ГПП-1 підсилює глюкозозалежну секрецію інсуліну та пригнічує секрецію глюкагону, модулюючи активність β- й α-клітин підшлункової залози відповідно. Крім того, ліраглутид посилює відчуття насичення та сповільнює спорожнення шлунка (рис. 2). За даними дослідження SCALE, застосування ліраглутиду (3 мг підшкірно 1 раз на тиждень протягом 56 тижнів) сприяло зниженню маси тіла щонайменше на 5% від стартового рівня в 63,2% учасників.
У групі плацебо цей показник становив 27,1%. Зниження маси тіла щонайменше на 10% досягли 33,1% пацієнтів групи ліраглутиду та лише 10,6% групи плацебо.
Тирзепатид
Тирзепатид є подвійним агоністом рецепторів ГПП-1 і глюкозозалежного інсулінотропного поліпептиду (ГІП). Завдяки подвійному механізму дії тирзепатид забезпечує кращий глікемічний контроль і більший потенціал зниження маси тіла, ніж агоністи рецепторів ГПП-1 (рис. 2). Препарат уводиться 1 раз на тиждень підшкірно. У серії досліджень SURPASS різні дози тирзепатиду (5, 10 і 15 мг) забезпечували достовірне зниження маси тіла в пацієнтів з ожирінням і ЦД 2-го типу порівняно з плацебо, семаглутидом (1 мг), інсуліном деглюдек, інсуліном гларгін і комбінацією плацебо + інсулін гларгін. У середньому зниження ваги становило 7,6; 10,7 та 12,9 кг для тирзепатиду в дозі 5, 10 і 15 мг відповідно.
Семаглутид
Семаглутид належить до агоністів рецепторів ГПП-1 і застосовується в лікуванні ожиріння та ЦД. Його застосовують 1 раз на тиждень. Програма досліджень STEP сформувала доказову базу використання семаглутиду (2,4 мг 1 раз на тиждень) у осіб з ожирінням або НМТ з асоційованими з надлишком ваги ускладненнями. За даними цих досліджень, через 68 тижнів досягається середнє зниження маси тіла на 14,9-17,4% від вихідного рівня. Зниження ваги щонайменше на 10% спостерігалося в 69-79% учасників. Дослідження STEP також продемонстрували покращення таких показників, як обвід талії, ліпідний профіль, артеріальний тиск і C-реактивний білок.
Рекомендації Національного інституту здоров’я та вдосконалення медичної допомоги Великої Британії (NICE, 2023) радять застосовувати семаглутид упродовж максимум 2 років у осіб з НМТ/ожирінням, які мають щонайменше один асоційований з надлишковою вагою коморбідний стан та індекс маси тіла ≥35 кг/м2. Пацієнтів з ІМТ у межах 30-34,9 кг/м2 варто скеровувати до спеціалізованих центрів контролю ваги, де семаглутид призначають лікарі мультидисциплінарної команди.
Препарати минулого
Фентермін/топірамат
Цю комбінацію було схвалено Управлінням США з контролю продовольства та медикаментів (FDA) у 2012 р. як допоміжний засіб для доповнення модифікації способу життя з метою контролю ваги в осіб з НМТ й ожирінням. Фентермін підвищує вивільнення норадреналіну, пригнічуючи апетит, а також допаміну та серотоніну – нейротрансмітерів, що регулюють апетит і настрій. Своєю чергою, топірамат зменшує відчуття винагороди при отриманні їжі, що сприяє зменшенню її споживання.
У низці досліджень комбінація фентермін/топірамат продемонструвала здатність знижувати масу тіла, однак це супроводжувалося підвищеною частотою серцебиття, перепадами настрою, розладами сну та порушенням травлення. У зв’язку з цим у багатьох країнах ця комбінація не отримала дозволу на вихід на фармацевтичний ринок.
Налтрексон/бупропіон
Налтрексон здатний зменшувати споживання їжі та ймовірність неконтрольованого переїдання, однак як монотерапія він не дієвий. Своєю чергою, бупропіон є антидепресантом, побічним ефектом якого є зниження маси тіла. У дослідженні CONTRAVE комбінація налтрексон/бупропіон продемонструвала зіставне зниження ваги порівняно з плацебо, а в дослідженні COR-BMOD додавання цієї комбінації до програми модифікації поведінки забезпечувало достовірно кращий порівняно з плацебо результат (зниження ваги становило 11,5 та 7,3% вихідного рівня відповідно).
Сетмеланотид
Сетмеланотид є анорексигенним препаратом, що діє як агоніст рецепторів меланокортину-4.
У 2020 р. FDA схвалило цей засіб для лікування генетично зумовленого ожиріння. Сетмеланотид сприяє відновленню контролю над апетитом, але не корегує проблеми, які спричинили ожиріння. Він показаний особам зі спадковими дефектами гена проопіомеланокортину, рецепторів лептину та пропротеїнової конвертази субтилізину / кексину типу 1.
Метрелептин
Цей препарат є аналогом лептину, який було схвалено FDA у 2014 р. як замісний засіб для пацієнтів з гіполептинемією та ліподистрофією. Метрелептин призначається 1 раз на добу підшкірно. Засіб має сприятливий вплив на чутливість до інсуліну та зменшує вираженість стеатозу печінки, проте за його застосування можуть виникати антитіла до лептину, які нейтралізують дію препарату.
Сибутрамін
Сибутрамін виступає супресантом апетиту та часто використовується як додаток до модифікації способу життя. Його механізм дії полягає в блокуванні зворотного захоплення нейротрансмітерів (серотоніну, допаміну та норадреналіну), що сприяє зниженню апетиту. Незважаючи на ефективність, повідомлено, що застосування сибутраміну може асоціюватися зі значним серцево-судинним ризиком і потенціалом розвитку інсультів. У зв’язку з цим препарат було відкликано з фармацевтичного ринку.
Римонабант
Римонабант являє собою селективний блокатор канабіноїдних рецепторів 1-го типу, які відіграють ключову роль у регуляції апетиту, енергетичного балансу та метаболізму. Продемонстровано, що римонабант знижував уміст аланінамінотрансферази та сприяв зниженню ваги в жінок з ожирінням і синдромом полікістозних яєчників. Проте застосування цього препарату асоціюється з депресивними розладами, коливаннями настрою та суїцидальними намірами. У зв’язку з цим римонабант не застосовують для лікування ожиріння.
Лоркасерин
Цей препарат було схвалено для лікування ожиріння або НМТ (за наявності ЦД, дисліпідемії чи артеріальної гіпертензії). Лоркасерин активує серотонінові рецептори гіпоталамуса, пригнічуючи апетит і сприяючи зниженню ваги на 3-5%. У зв’язку з потенційною асоціацією з раковими пухлинами його було відкликано з ринку у 2020 р.
Препарати майбутнього
Нині досліджуються кілька багатонадійних препаратів центральної та периферичної дії: наприклад, селективний подвійний агоніст рецепторів глюкагону та ГПП-1 сурводутид; потрійний агоніст ГІП, ГПП-1 і рецепторів глюкагону ретатрутид; пероральний непептидний агоніст рецепторів ГПП-1 орфогліпрон; подвійний агоніст ГПП-1 і глюкагону пемвідутид.
Хірургічні втручання
Баріатрична хірургія застосовується для осіб з ІМТ >40 кг/м2 та осіб з ІМТ >35 кг/м2 з асоційованими з надлишковою вагою коморбідними станами. Найчастішою процедурою є шунтування шлунка Roux-en-Y. Також застосовуються рукавна гастроектомія та біліопанкреатична диверсія з дуоденальним вимикачем. Баріатричні втручання не лише знижують вагу, а й сприяють ремісії ЦД, однак їхніми недоліками є хірургічні ускладнення та нутритивні дефіцити.
Висновки
Методи лікування, що ґрунтуються на застосуванні агоністів рецепторів ГПП-1, швидко розвиваються, хоча спочатку зниження ваги було вторинним наслідком застосування цих препаратів у лікуванні ЦД 2-го типу. І лікування агоністами рецепторів ГПП-1, і баріатрична хірургія забезпечують покращення глікемічного контролю й ліпідного профілю та зниження маси тіла, хоча баріатрична хірургія зазвичай має перевагу над фармакотерапією. Слід, однак, зауважити, що баріатрична хірургія являє собою інвазивну процедуру, яка підходить лише певній групі пацієнтів, тому багатонадійним підходом є поєднання фармакотерапевтичних і хірургічних методів, особливо у випадку пацієнтів, які повторно набрали вагу після хірургічного втручання.
Література
Roomy M.A., Hussain K., Behbehani H.M., et al. Therapeutic advances in obesity management: an overview of the therapeutic interventions. Front. Endocrinol. (Lausanne). 2024; 15: 1364503. doi: 10.3389/fendo.2024.1364503.