Субклінічний гіпотиреоз у пацієнтів з ожирінням і метаболічним синдромом
Переклала й адаптувала д-р мед. наук Лариса Стрільчук
Субклінічний гіпотиреоз (СГіпо) являє собою початкову стадію дефіциту тиреоїдних гормонів, за якої рівень вільного тироксину (вТ4) перебуває на нижній межі нормального референтного діапазону, а рівень тиреотропного гормону (ТТГ) перевищує межі норми. СГіпо розвивається в 4-20% дорослого населення й частіше трапляється в країнах із достатнім споживанням йоду. Близько 75% пацієнтів мають легку форму захворювання з умістом ТТГ у межах 4,5-6,9 мМО/л. У таких пацієнтів СГіпо може бути зворотним і не потребувати лікування в безсимптомних осіб без серцево-судинних чинників ризику та в невагітних жінок. Приблизно у 20% дорослих пацієнтів із СГіпо відзначається помірний дефіцит тиреоїдних гормонів, що характеризується рівнем ТТГ у межах 7,0-9,9 мМО/л, і лише 5% пацієнтів мають тяжку форму дисфункції зі значенням ТТГ ≥10 мМО/л. Помірний і тяжкий СГіпо асоціюються з підвищеним ризиком прогресування до маніфестного захворювання.
Своєю чергою, метаболічний синдром (МС) характеризується сукупністю серцево-судинних чинників ризику, серед яких абдомінальне ожиріння, артеріальна гіпертензія, підвищений рівень тригліцеридів, знижений рівень холестерину ліпопротеїнів високої щільності, інсулінорезистентність (ІР) або порушена толерантність до глюкози.
МС часто супроводжується протромботичним і прозапальним станами.
Зв’язок між СГіпо та МС
Тиреоїдні гормони регулюють споживання їжі шляхом впливу на апетит і термогенез, а також беруть участь у метаболізмі глюкози, ліпідів і адипогенезі. Опубліковано низку досліджень і метааналізів, які оцінюють зв’язок між СГіпо, МС та ожирінням, однак їхні результати є суперечливими. Зокрема, масштабний метааналіз (n=79 727) виявив значне зростання ризику МС у пацієнтів із СГіпо (відношення шансів 1,28; 95% довірчий інтервал (ДІ) 1,19-1,39; p<0,00001), але інший нещодавній метааналіз не отримав переконливих доказів взаємозв’язку між маніфестним гіпотиреозом або СГіпо та МС.
Зв’язок між СГіпо та частотою розвитку цукрового діабету 2-го типу
Регулюючи продукцію інсуліну й засвоєння глюкози в печінці, скелетних м’язах і жировій тканині, тиреоїдні гормони модулюють функцію β-клітин підшлункової залози. ІР у разі гіпотиреозу спричинена зниженими транспортуванням та утилізацією глюкози в периферичних тканинах. Гіпотиреоз також характеризується порушеним усмоктуванням глюкози, зниженими глюконеогенезом і глікогенолізом у печінці. Проспективні дослідження свідчать, що в пацієнтів з маніфестним гіпотиреозом підвищується ризик розвитку цукрового діабету (ЦД) 2-го типу (відношення ризиків (ВР) 1,26; 95% ДІ 1,05-1,52), проте дані щодо зв’язку між СГіпо та ЦД 2-го типу є суперечливими.
Зв’язок між ожирінням і СГіпо
Останніми роками спостерігається зростання поширеності МС та ожиріння. За даними Всесвітньої організації охорони здоров’я (2022), >60% населення Європи має надлишкову вагу або ожиріння, а відповідно до Національного дослідження здоров’я та харчування США (NHANES) 53,13% американців мають абдомінальне ожиріння. У період між 2001-2002 і 2017-2018 рр. поширеність ожиріння зросла для обох статей: із 33,09 до 41,36% для жінок і з 26,88 до 42,43% для чоловіків. Також зросла поширеність тяжкого ожиріння (індекс маси тіла (ІМТ) ≥40,0 кг/м2).
Порівняно з підшкірною жировою тканиною вісцеральна жирова тканина має нижчу ангіогенну здатність. Недостатня оксигенація адипоцитів, гіпоксія та посилений окисний стрес спричиняють фіброз і запалення жирової тканини, що асоціюється з високим кардіометаболічним ризиком.
Гіпотиреоз і ожиріння є тісно пов’язаними станами, оскільки гіпотиреоз супроводжується зниженням термогенезу та рівня енергетичних витрат у стані спокою. В осіб з ожирінням спостерігається підвищена поширеність СГіпо. Згідно з нещодавнім метааналізом сукупна поширеність СГіпо серед пацієнтів з ожирінням становить 14,6% (95% ДІ 9,2-20,9%).
Дисфункція щитоподібної залози (ЩЗ) може спричиняти зміни маси тіла, і раніше дефіцит тиреоїдних гормонів вважався основною причиною ожиріння. Для визначення можливої причини надмірної ваги або відсутності зниження маси тіла за гіпокалорійної дієти досі рутинно оцінюють функцію ЩЗ, однак гіпотиреоз асоціюється лише з незначним збільшенням ваги, яке переважно зумовлене змінами у складі тіла. Крім того, лікування гіпотиреозу сприяє лише помірному зниженню маси тіла (на <10%), що підтверджує: тяжке ожиріння зазвичай не є вторинним наслідком гіпотиреозу.
Зв’язок між ожирінням і функцією ЩЗ
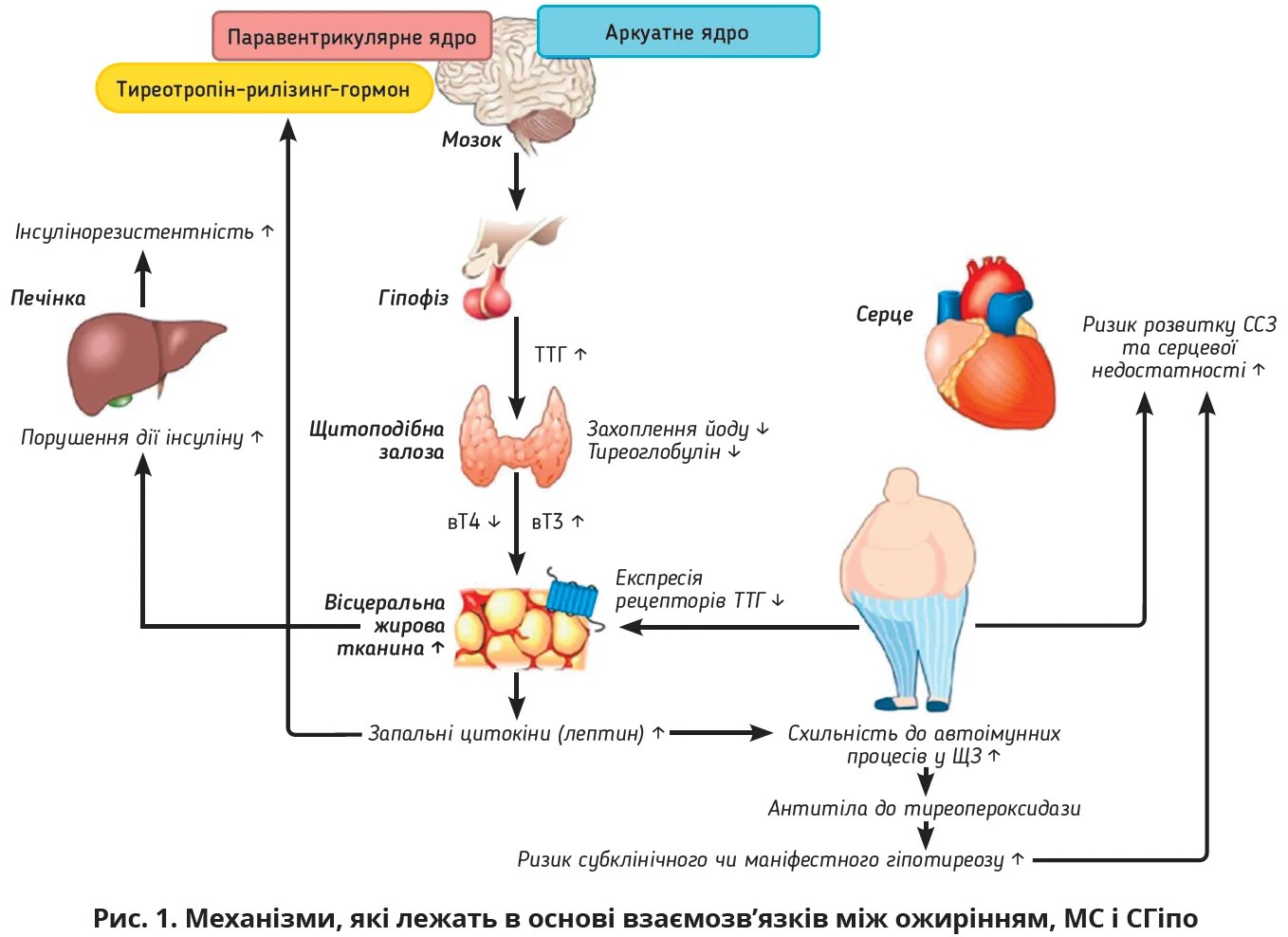
Навіть у еутиреоїдних осіб ожиріння пов’язане зі змінами показників функції ЩЗ. Зокрема, рівні ТТГ корелюють з ІМТ і часто вищі в людей з ожирінням, аніж у контрольній групі з нормальною масою тіла. Лептин контролює експресію тиреотропін-рилізинг-гормону в паравентрикулярному ядрі й аркуатному ядрі, він є ключовим нейроендокринним регулятором гіпоталамо-гіпофізарно-тиреоїдної осі. Гіперлептинемія, зумовлена надмірною масою тіла, активує гіпоталамо-гіпофізарно-тиреоїдну вісь, посилюючи секрецію ТТГ (рис. 1). Численні дослідження продемонстрували негативну кореляцію між вT4 й ІМТ, а також позитивну кореляцію між ТТГ та ІМТ. Раніше вважалося, що підвищення рівнів ТТГ і трийодтироніну (Т3), яке спостерігається в осіб з ожирінням, є фізіологічним механізмом підвищення енергетичних витрат для протидії набиранню ваги. Проте жодного зв’язку між рівнями ТТГ і Т3 й енергетичними витратами в еутиреоїдних осіб з ожирінням виявлено не було.
Нещодавні дослідження дали змогу припустити, що ожиріння впливає на функцію ЩЗ і спричиняє гіпертиреотропінемію, а зміни рівнів тиреоїдних гормонів є наслідком збільшення маси тіла, а не її причиною. Виявлено, що збільшення рівня ТТГ на 1 мМО/л пов’язане з набиранням ваги на 0,6 кг у жінок і 0,7 кг у чоловіків; це свідчить про те, що незначне підвищення рівня ТТГ може бути радше вторинним ефектом, а не основною причиною ожиріння.
Оскільки секреція лептину адипоцитами стимулюється зв’язуванням ТТГ з його рецепторами, між рівнями ТТГ та лептину існує позитивний зворотний зв’язок. Окрім того, лептин регулює активність дейодинази в адипоцитах, що стимулює внутрішньоклітинний синтез Т3, хоча місцевий вплив Т3 може бути порушений через зміни експресії рецепторів тиреоїдних гормонів на адипоцитах (рис. 1). Продемонстровано, що пацієнти з ожирінням мають вищі рівні циркулювального ТТГ і вT3 порівняно з контрольною групою, а після зменшення ІМТ на 33% ці зміни виявилися зворотними. Отже, адипоцити відіграють важливу роль у регуляції рівнів ТТГ і тиреоїдних гормонів, а ожиріння може спричинити розвиток центральної та периферичної резистентності до гормонів ЩЗ, що проявляється підвищеними рівнями ТТГ і вT3 у плазмі крові, проте ці зміни можуть бути зворотними за умови зниження ваги.
Зв’язок між ожирінням і автоімунними хворобами ЩЗ
Дослідження свідчать, що антитіла до тиреопероксидази (АТПО) частіше трапляються в пацієнтів з ожирінням, а рівень лептину може асоціюватися з тиреоїдитом Хашімото незалежно від антропометричних параметрів. У метааналізі 14 досліджень було зафіксовано причинно-наслідковий зв’язок між ожирінням і СГіпо. В осіб з ожирінням ризик СГіпо й тиреоїдиту Хашімото був підвищеним (ВР 1,70; 95% ДІ 1,42-2,03; p<0,001 та ВР 1,91; 95% ДІ 1,10-3,32; p=0,022 відповідно). Це доводить той факт, що надмірна маса тіла є чинником ризику для СГіпо та тиреоїдиту Хашімото.
За даними популяційного крос-секційного дослідження (n=12 531), за наявності АТПО та/або антитіл до тиреоглобуліну ймовірність виявлення високого ТТГ була у 2,201 раза більшою в групі з ожирінням і в 1,857 раза більшою в групі з надлишковою масою тіла порівняно з групою без антитиреоїдних антитіл. При стратифікації лише за ІМТ відмінностей за поширеністю гіпертиреотропінемії зафіксовано не було.
Вплив ожиріння на морфологію ЩЗ
Навіть за відсутності дисфункції ЩЗ чи автоімунних процесів у ній постійне запалення, пов’язане з ожирінням, може впливати на морфологію залози. У пацієнтів із морбідним ожирінням спостерігаються значні зміни, які можна виявити за допомогою ультразвукового дослідження (УЗД), зокрема збільшений об’єм і гіпоехогенна структура ЩЗ. Ці зміни є зворотними після зниження ваги за допомогою баріатричної хірургії. Вказані анатомічні зміни можуть бути пов’язані з індукованою адипокінами вазодилатацією та підвищеною проникністю кровоносних судин ЩЗ. В осіб з ожирінням відзначається також більша ймовірність розвитку вузлів ЩЗ. За підозри на вузол ЩЗ у пацієнтів з ожирінням доцільне проведення УЗД, оскільки пальпація шиї в таких осіб утруднена.
Діагностика СГіпо в пацієнтів з ожирінням
Оскільки симптоми СГіпо можуть бути схожими на симптоми ожиріння, а ожиріння здатне змінювати морфологію та функцію ЩЗ, діагностика СГіпо може бути складною. Крім того, деякі препарати, які часто застосовуються при ожирінні та МС (пероральні гіпоглікемічні засоби, ліраглутид), здатні впливати на рівень ТТГ у сироватці крові.
Згідно з європейськими настановами функція ЩЗ має визначатися в усіх пацієнтів з ожирінням. Окрім того, для всіх пацієнтів з екстремальним ожирінням перед баріатричною хірургією рекомендується скринінгове визначення ТТГ. Також слід визначати рівень вT4 за підозри на первинний гіпотиреоз або за підвищення рівня ТТГ. Оскільки перетворення T4 на T3 може інгібувати низка екстратиреоїдних факторів (включно з харчовим статусом і системним запаленням), інтерпретація рівнів вT3 у сироватці крові може бути складною.
Профіль антитіл до ЩЗ є корисним для діагностики автоімунного гіпотиреозу та виявлення пацієнтів з підвищеним ризиком маніфестного гіпотиреозу. Отже, визначення АТПО рекомендовано пацієнтам з ожирінням і підвищеним рівнем ТТГ. Рекомендація щодо визначення антитіл до тиреоглобуліну, особливо в контексті ожиріння, наразі є слабкою.
Існують різні думки щодо можливості підвищення захворюваності на диференційований рак ЩЗ у пацієнтів з ожирінням або ІР. Згідно з нещодавнім метааналізом пацієнтам з ожирінням властивий вищий ризик раку ЩЗ: кожне збільшення ІМТ на 5 кг/м2 асоціювалося зі зростанням ризику цього раку на 30%.
Незалежно від функції ЩЗ клінічні настанови рекомендують уникати використання рутинного УЗД ЩЗ у пацієнтів з ожирінням. Попри високий ризик утворення вузлів ЩЗ у цього контингенту систематичне УЗД ЩЗ вважається непотрібним і дорогим.
Лікування СГіпо в пацієнтів з ожирінням
У минулому препарати тиреоїдних гормонів широко використовували для лікування ожиріння, але таке призначення є неправильним. Більше того, в разі призначення еутиреоїдним пацієнтам із ожирінням ці засоби можуть зумовити несприятливі побічні ефекти через ятрогенний тиреотоксикоз. Після лікування левотироксином зниження ваги є малоймовірним, а в пацієнтів з ожирінням, які вже перебувають у групі ризику серцево-судинних захворювань (ССЗ), ятрогенний надлишок гормонів ЩЗ може прискорити розвиток аритмії, серцевої недостатності чи ішемічних подій. Згідно з рекомендаціями Європейського товариства ендокринологів і Американської тиреоїдної асоціації пацієнти з ожирінням і підвищеним ТТГ за нормального вT4 не мають отримувати левотироксин для зниження ваги.
Натомість лікування левотироксином слід розпочати тоді, коли в пацієнтів з ожирінням, особливо в молодих осіб і жінок репродуктивного віку, діагностується СГіпо, асоційований з автоімунним процесом, або за наявності інших причин первинного гіпотиреозу (попереднє лікування гіпертиреозу радіоактивним йодом, часткова тиреоїдектомія або анамнез деструктивного тиреоїдиту). Пероральна монотерапія левотироксином є ефективним методом лікування тяжкого СГіпо та маніфестного гіпотиреозу (рис. 2). Крім того, для зменшення ризику автоімунного гіпотиреозу в пацієнтів з ожирінням можуть бути доцільними зниження споживання тваринних жирів і білків, середземноморська дієта.
Деякі науковці вважають, що дози левотироксину для пацієнтів з ожирінням і гіпотиреозом мають бути вищими, ніж для осіб з нормальною вагою. Однак, за результатами великого когортного дослідження, корегована за вагою доза левотироксину зменшується зі збільшенням ІМТ, тому для підбору дози доцільно оцінювати безжирову масу тіла. Для розрахунку належної початкової дози левотироксину варто спиратися на показник 0,91 мг/кг/добу.
Для запобігання негативним наслідкам надмірного лікування цільове значення ТТГ у разі замісної терапії має бути скореговано за віком, а адекватність доз левотироксину слід регулярно оцінювати, особливо в пацієнтів похилого віку. За даними нещодавнього дослідження, доза, потрібна для досягнення еутиреозу, становила 1,76 мкг/кг для пацієнтів з ІМТ <25 кг/м2, 1,47 мкг/кг для осіб з ІМТ 26-30 кг/м2, 1,42 мкг/кг для осіб з ІМТ 31-35 кг/м2, 1,27 мкг/кг для осіб з ІМТ 35-40 кг/м2 та 1,28 мкг/кг для осіб з ІМТ >40 кг/м2.
Небажані наслідки поєднання СГіпо та МС
Пацієнтам із маніфестним гіпотиреозом і СГіпо властивий підвищений ризик розвитку ССЗ. В осіб із СГіпо відзначаються порушення релаксації судин, збільшена жорсткість артерій, артеріальна гіпертензія й ендотеліальна дисфункція. В осіб з помірно тяжким СГіпо, зокрема в пацієнтів з ІР, можуть виникати й метаболічні зміни. За даними Thyroid Studies Collaboration (>75 000 осіб), уміст ТТГ ≥10 мМО/л асоціювався з підвищеним ризиком серцевої недостатності, коронарних подій і смертності від ішемічної хвороби серця порівняно з нормальним умістом ТТГ. Крім того, підвищений ризик фатального інсульту та смерті від ішемічної хвороби серця був пов’язаний з концентрацією ТТГ у межах 7,0-9,9 мМО/л. Загалом що тяжчим є СГіпо, то вищим є серцево-судинний ризик, що зумовлює потребу в лікуванні помірного та тяжкого СГіпо (ТТГ – 7-10 мМО/л і >10 мМО/л). Для пацієнтів віком >70 років із легким СГіпо (ТТГ – 4,5-6,9 мМО/л) може бути доцільним ретельне спостереження.
У масштабному метааналізі (n=951 083) було виявлено кореляцію між МС і підвищеним ризиком ССЗ (ВР 2,35; 95% ДІ 2,02-2,73), смертності від ССЗ (ВР 2,40; 95% ДІ 1,87-3,08), загальної смертності (ВР 1,58; 95% ДІ 1,39-1,78), інфаркту міокарда (ВР 1,99; 95% ДІ 1,61-2,46) та інсульту (ВР 2,27; 95% ДІ 1,80-2,85). Особам, які не мали ЦД, але мали МС, теж був властивий підвищений серцево-судинний ризик.
В осіб із гіпотиреозом можуть спостерігатися зміни метаболізму ліпідів з накопиченням ліпотоксинів і розвитком ІР, що спричиняє розвиток неалкогольної жирової хвороби печінки (НАЖХП). Окрім того, кілька генів, експресія котрих змінюється при НАЖХП, також регулюються гормонами ЩЗ. Утім, дані щодо зв’язку між СГіпо та НАЖХП є суперечливими. Деякі автори вказують на позитивну асоціацію рівнів ТТГ і вT3 із ризиком стеатозу печінки в пацієнтів із морбідним ожирінням і користь низьких доз левотироксину для зменшення вмісту жиру в печінці навіть у еутиреоїдних пацієнтів із НАЖХП.
Продемонстровано також зв’язок між ожирінням і підвищеним ризиком розвитку або прогресування хронічної хвороби нирок. У разі ниркової недостатності СГіпо асоціюється з вищою смертністю порівняно з еутиреоїдними пацієнтами.
Подальші дослідження
Існує потреба у вивченні механізму несприятливого впливу комбінації МС і СГіпо на ризик ССЗ, НАЖХП та ниркової недостатності. Доцільно також вивчити лікування помірного й легкого СГіпо в осіб молодого віку та вплив замісної терапії тиреоїдними гормонами на зниження серцево-судинного й метаболічного ризику в пацієнтів із СГіпо, ожирінням і МС. Для доведення потенційних переваг лікування левотироксином за помірного та легкого СГіпо в поєднанні з МС потрібно більше доказів із клінічних випробувань. Також треба встановити, які порогові значення ТТГ слід застосовувати в людей з ожирінням під час гормонозамісної терапії. Для зменшення ризиків із покращення якості життя та зменшення симптомів пацієнтів із СГіпо, МС чи ожирінням потрібно сформулювати індивідуальні дозування левотироксину з урахуванням віку.
Література
Biondi B. Subclinical hypothyroidism in patients with obesity and metabolic syndrome: a narrative review. Nutrients. 2023; 16 (1): 87. doi: 10.3390/nu16010087.
Від редакції
L-Тироксин Берлін-Хемі (виробник – «Берлін-Хемі АГ», Німеччина) є одним із препаратів левотироксину натрію з більш ніж 30-річним досвідом застосування в Україні. Лікарський засіб представлений у формі таблеток з рискою для поділу на рівні дози в п’ятьох дозуваннях (50, 75, 100, 125 і 150 мкг) [1-4]. Завдяки особливій формі таблетки Snap-tab (глибока насічка з одного боку) її можна легко розділити, надавивши пальцем зверху в перпендикулярному напрямку [1-4]. Таблетки L-Тироксину Берлін-Хемі випускаються у фольгованому блістері, який забезпечує надійний захист від світла, вологи та кисню [5-7].
Нещодавно виробник змінив склад таблеток L-Тироксину Берлін-Хемі в частині допоміжних речовин для того, щоб іще більше поліпшити стабільність діючої речовини протягом усього терміну придатності лікарського засобу. Діюча речовина – левотироксин натрію, його дозування та спосіб застосування залишаються без змін. Лікарські засоби L-Тироксин 50/75/100/125/150 Берлін-Хемі зі зміненим складом будуть доступні з першого кварталу 2025 року. Нова рецептура таблеток L-Тироксину Берлін-Хемі захищена патентом Європейського патентного відомства з терміном дії до 02.02.2038 [8]. Зміна складу допоміжних речовин забезпечила високу стабільність таблеток L-Тироксину Берлін-Хемі в будь-якому кліматі [8]. У новій рецептурі препарату L-Тироксин Берлін-Хемі немає допоміжних речовин, які потребують спеціального маркування, а також компонентів тваринного походження [1-4, 9, 10]. Для того щоб візуально відрізнити препарат з новим складом від препарату з попереднім складом, було змінено упаковку та блістер.
Біоеквівалентність між попереднім і новим складами було продемонстровано дослідженнями з біодоступності. Однак у деяких пацієнтів усмоктування діючої речовини між цими складами може відрізнятися, тому згідно з вимогою регуляторних органів Європейського Союзу та Державного експертного центру МОЗ України рекомендовано ретельний моніторинг пацієнтів, які перейшли на новий склад таблеток L-Тироксину Берлін-Хемі, щоб пересвідчитися, що індивідуальна добова доза залишається відповідною для пацієнта й не потребує корегування. Дослідження концентрації ТТГ через 4 тижні є достовірною підставою такого підтвердження.
Список літератури – в редакції.