Діагностика й лікування надниркової недостатності, індукованої глюкокортикоїдами: реферативний огляд настанов Європейського товариства ендокринології та Ендокринного товариства (2024)
Підготувала канд. мед. наук Ольга Королюк
Глюкокортикоїди (ГК) широко використовуються в клінічній практиці як протизапальні й імуносупресивні засоби. Принаймні 1% населення постійно приймає ГК та має ризик розвитку надниркової недостатності, індукованої глюкокортикоїдами (ННІГ). Ризик залежить від дози, тривалості та сили ГК, шляху введення й індивідуальної чутливості. Виникнення ННІГ або підозра на неї потребують навчання пацієнтів і відповідного лікування.
Скасування ГК може бути складним, коли симптоми скасування поєднуються із симптомами ННІГ. Загалом швидше зниження дози ГК можливе в надфізіологічному діапазоні, тоді як застосування фізіологічних доз потребує повільнішого скасування. Ступінь і стійкість пригнічення гіпоталамо-гіпофізарно-наднирникової осі (ГГНО) після припинення терапії ГК залежать від загальної експозиції, а відновлення функції наднирників має значні індивідуальні коливання. Це перша клінічна настанова Європейського товариства ендокринології та Ендокринного товариства, що містить вказівки щодо ведення цього клінічно значущого стану. Формулювання «рекомендується» застосовується для сильних рекомендацій, «пропонується» – для слабких. Якість доказів класифікується як дуже низька ( ⊕⭘⭘⭘), низька ( ⊕⊕⭘⭘), помірна ( ⊕⊕⊕⭘) та сильна (⊕⊕⊕⊕ ). Рекомендації, що ґрунтуються на належній клінічній практиці та досвіді членів робочої групи, визнаються як «належна клінічна практика». Рекомендації, що не ґрунтуються на доказах або належній клінічній практиці, не оцінюються.
Визначення
Побічна дія тривалої терапії ГК
Навіть низькі дози ГК (преднізолон 2,5-7,5 мг/добу) підвищують ризик розвитку серцево-судинних захворювань, артеріальної гіпертензії, діабету, тяжких інфекцій, остеопорозу та переломів, а також рівень загальної смертності в осіб із цукровим діабетом 2-го типу. Вищі дози ГК та тривала терапія підвищують ризик розвитку діабету, остеопорозу, переломів, артеріальної гіпертензії, тромботичних подій, шлунково-кишкових ускладнень і смертності від усіх причин.
Патофізіологія ННІГ
Екзогенні ГК пригнічують утворення кортикотропін-рилізинг-гормону гіпоталамусом і адренокортикотропного гормону (АКТГ) гіпофізом. Тривала терапія надфізіологічними дозами ГК знижує загальну чутливість передньої частки гіпофіза, спричиняє апоптоз і деградацію білка в кортикотропних клітинах, що зрештою призводить до атрофії кори наднирників. Після скасування ГК стимуляція АКТГ кори наднирників поступово відновлюється й у більшості випадків виробляється достатній рівень кортизолу. Проте час до повного біохімічного та клінічного відновлення ГГНО дуже варіабельний. Будь-який шлях уведення та будь-яка доза ГК, що перевищує еквівалент фізіологічної добової дози, має потенціал пригнічення ГГНО, ступінь і тривалість якого залежать від загальної експозиції. Експозиція визначається силою ГК (табл. 2), дозою, тривалістю терапії та індивідуальною чутливістю.
Епідеміологія ННІГ і адреналової кризи
У Данії серед 286 680 осіб, які припиняли пероральну терапію ГК тривалістю ≥3 місяці, коефіцієнти частоти клінічних показників ННІГ були вищими, ніж до початку лікування: гіпотензія – 2,5; шлунково-кишкові симптоми – 1,7; гіпоглікемія – 2,2; гіпонатріємія – 1,5. У Європейському реєстрі надниркової недостатності лише 1 з 26 смертей була чітко пов’язана з адреналовою кризою в пацієнта з ННІГ.
У Сполученому Королівстві ретроспективне когортне дослідження за участю 70 638 пацієнтів на пероральних ГК виявило різке збільшення смертності протягом перших 2 місяців після скасування ГК, яке швидко знизилося після перших 3 місяців. Хоча надниркова недостатність була причиною смерті лише 13 пацієнтів, зв’язок із припиненням прийому ГК викликає підозру на недіагностовану адреналову кризу.
Клінічні запитання
- Яка частота відновлення функції ГГНО в пацієнтів із ННІГ?
Метааналіз 11 досліджень виявив зниження надниркової недостатності з 38,7% після скасування високодозової терапії ГК до 14,9% через 4 тижні; при скасуванні середньодозової терапії ГК тривалістю >1 рік –із 56,4 до 25,3% через 6 місяців. За даними невеликих досліджень із низькою якістю доказів, функція наднирників відновлюється в 10-60% пацієнтів упродовж 3-24 місяців, іноді до 4 років.
Ia. Які клінічні/біохімічні параметри передбачають відновлення ГГНО в пацієнтів із ННІГ?
Пацієнти з відновленням функції наднирників демонстрували більший приріст кортизолу під час першого тесту АКТГ(1-24), ніж пацієнти без відновлення (219 проти 99 нмоль/л, або 10,3 проти 6,7 мкг/дл).
В іншому дослідженні такі пацієнти мали вищі ранкові рівні кортизолу між повторним тестування за допомогою тесту АКТГ(1-24) в амбулаторних умовах (286 проти 186 нмоль/л, або 7,9 проти 3,6 мкг/дл).
- Яка оптимальна схема поступового зниження дози в пацієнтів, які більше не потребують тривалої терапії ГК для контролю основної хвороби?
Попри відносно невелику кількість пацієнтів і неоднорідність основної патології, результати 5 досліджень свідчать, що зазвичай різке припинення безпечне при короткочасному застосуванні високих доз ГК.
У разі тривалої терапії безпечною стратегією є швидше зниження доз за надфізіологічного дозування, але повільніше зменшення доз у фізіологічному діапазоні. Досліджень, які порівнювали б різні стратегії скасування ГК, не було.
III. Яка діагностична точність ранкового визначення кортизолу порівняно з тестом із 250 мкг АКТГ(1-24) у діагностиці ННІГ?
Визначені методом рідинної хроматографії-мас-спектрометрії рівні сироваткового кортизолу >327 нмоль/л (11,8 мкг/дл) виключають ННІГ (чутливість – 98%, негативне прогностичне значення – 99%); значення кортизолу <152 нмоль/л (5,5 мкг/дл) підтверджують ННІГ (специфічність – 98%, позитивне прогностичне значення – 99%) (помірна якість доказів).
Рекомендації
- Загальні рекомендації щодо ГК-терапії неендокринних захворювань і рекомендації щодо навчання пацієнтів.
Р 1.1. Загалом рекомендується, щоб пацієнти, які приймають ГК із приводу неендокринних захворювань або скасовують їх, не потребували огляду спеціаліста-ендокринолога.
Р 1.2. Клініцистам, які впроваджують лікування ГК, рекомендується інформувати пацієнтів про можливість різноманітних ендокринних наслідків терапії ГК (належна клінічна практика).
Р 1.3. Рекомендується, щоб пацієнти, які отримують терапію ГК, мали доступ до актуальної та відповідної інформації про різні ендокринні аспекти цієї терапії (належна клінічна практика).
Обґрунтування
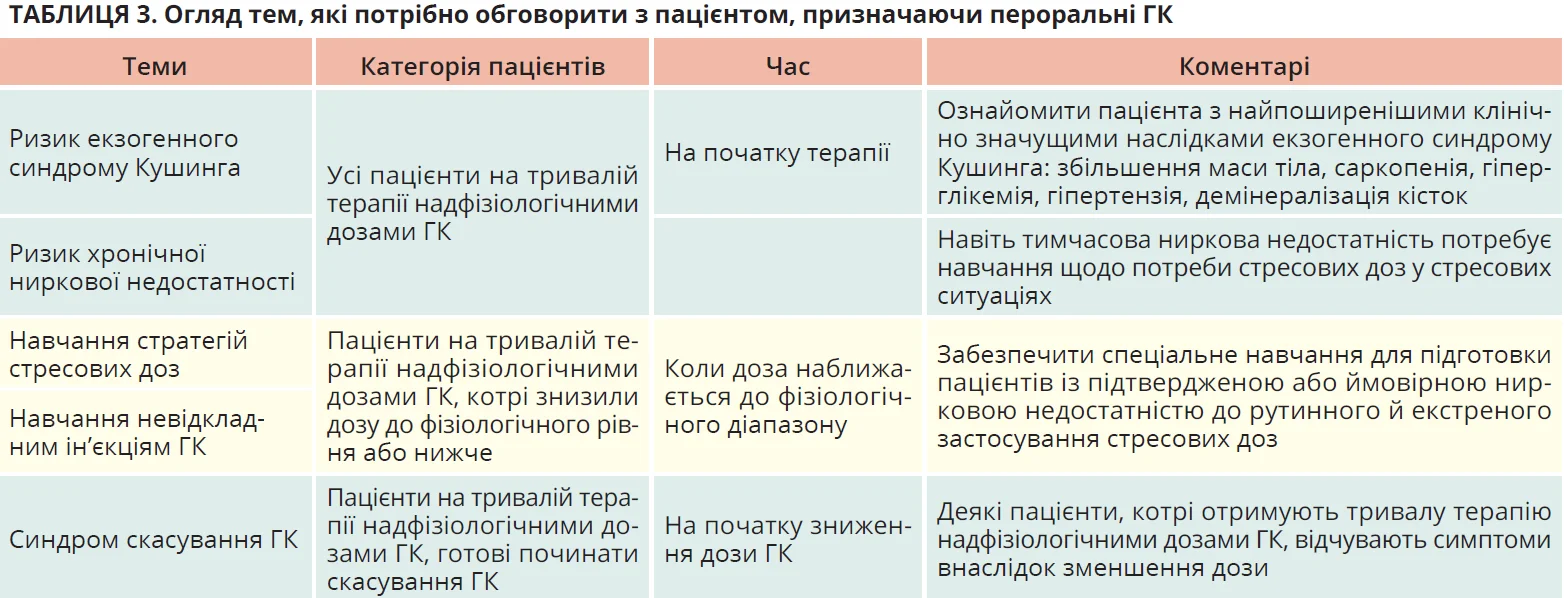
Хронічне застосування ГК асоціюється із синдромом Кушинга та ННІГ. Отже, клініцистам рекомендується застосовувати мінімально ефективні дози та тривалість терапії, розглядаючи можливість поступового скасування, коли ГК більше не потрібні для лікування основної патології. Важливо, щоб лікарі всіх спеціальностей були добре обізнані з клінічними наслідками тривалої супрафізіологічної терапії ГК, принципами профілактики, діагностики та лікування ННІГ. Керування терапією ГК – загальна медична навичка, якою має володіти кожен лікар. Кількість пацієнтів, які приймають ГК, занадто велика, щоби проводити консультації ендокринолога в кожному випадку зниження дози. Якщо клініцист вважає, що скасування ГК обґрунтоване, потрібно обговорити з пацієнтом низку важливих питань (табл. 3) у форматі, який відповідає віку, освітньому рівню та стилю навчання пацієнта. До навчальних занять рекомендується залучати членів сім’ї або основного опікуна.
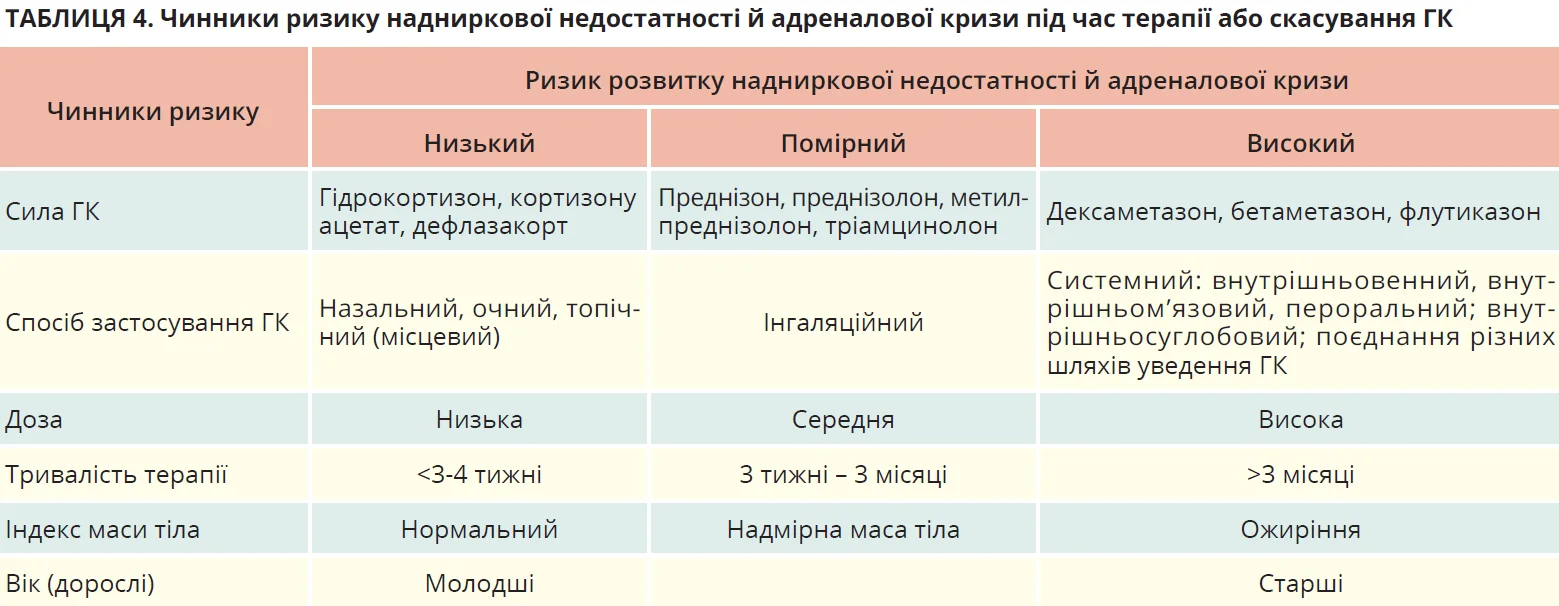
Можливість консультації ендокринолога слід розглядати в рідкісних випадках, як-от терапія надфізіологічними дозами ГК >1 рік, адреналова криза. Ризик розвитку ННІГ і адреналової кризи зростає зі збільшенням сукупної кількості чинників ризику (табл. 4).
- Рекомендації щодо зменшення дози та скасування системної терапії ГК за неендокринних станів; діагностика й підхід до ННІГ і синдрому скасування.
Р 2.1. Пропонується не зменшувати ГК у пацієнтів, які отримують короткочасну терапію ГК <3-4 тижні незалежно від дози. У таких випадках прийом ГК можна припинити без тестування через низьку занепокоєність щодо пригнічення ГГНО (⊕⭘⭙⭘).
Р 2.2. Зменшувати дозу ГК для пацієнтів, які отримують тривалу терапію, слід лише за умови досягнення контролю основної хвороби за відсутності потреби в подальшій терапії ГК. У таких випадках дозу ГК поступово зменшують до досягнення фізіологічного еквівалента добової дози (наприклад, 4-6 мг преднізолону) (належна клінічна практика).
Р 2.3. Рекомендується враховувати синдром скасування, що може виникнути під час зменшення доз ГК. За тяжких проявів синдрому скасування дозу ГК можна тимчасово збільшити до останньої переносимої дози, а також подовжити тривалість зниження доз ГК (належна клінічна практика).
Р 2.4. Рекомендується не проводити рутинні тести на ННІГ у пацієнтів, які отримують надфізіологічні дози ГК, або якщо основна хвороба потребує продовження терапії ГК (належна клінічна практика).
Р 2.5. Пропонується, щоб пацієнти, які приймають ГК тривалої дії (дексаметазон, бетаметазон), переводилися на ГК коротшої дії (гідрокортизон, преднізолон) за відсутності потреби в ГК тривалої дії (⊕⭘⭙⭘).
Р 2.6. Пацієнтам, які отримують еквівалент фізіологічної добової дози та мають намір припинити терапію ГК, пропонується один із таких варіантів:
- продовжувати поступове зниження дози ГК із клінічним моніторингом ознак і симптомів надниркової недостатності;
- визначити кортизол сироватки крові зранку (⊕⭘⭙⭘).
Р 2.7. Якщо потрібне підтвердження відновлення ГГНО, як перший тест рекомендується визначити сироватковий кортизол уранці. Показник цього тесту слід розглядати як континуум: вищі значення більше вказують на відновлення ГГНО (⊕⭘⭙⭘).
Як орієнтир:
1) припускається, що тест указує на відновлення ГГНО, якщо рівень кортизолу >300 нмоль/л (10 мкг/дл), ГК можна безпечно припинити;
2) якщо результат у межах від 150 нмоль/л (5 мкг/дл) до 300 нмоль/л (10 мкг/дл), пропонується продовжити фізіологічну дозу ГК та повторити тест через певний проміжок часу (зазвичай від тижнів до місяців);
3) якщо результат <150 нмоль/л (5 мкг/дл), пропонується продовжити фізіологічну дозу ГК та повторити тест через декілька місяців.
Р 2.8. Пропонується не проводити рутинно динамічний тест для діагностики надниркової недостатності в пацієнтів, які зменшують дозу або припиняють терапію ГК (⊕⭘⭙⭘).
Р 2.9. Пропонується пересторога щодо можливості ННІГ у таких категорій пацієнтів:
1) поточне чи нещодавнє застосування непероральних форм ГК за наявності ознак і симптомів, що вказують на надниркову недостатність, або
2) одночасне використання кількох форм ГК або
3) застосування високих доз інгаляційних чи місцевих ГК або
4) використання інгаляційних чи місцевих ГК >1 рік або
5) внутрішньосуглобові ін’єкції ГК протягом попередніх 2 місяців або
6) супутнє застосування потужних інгібіторів цитохрому P450 3A4.
Р 2.10. Пропонується, щоб пацієнти з поточним або попереднім лікуванням ГК з ознаками та симптомами екзогенного синдрому Кушинга вважалися такими, що мають ННІГ (належна клінічна практика).
Р 2.11. Пропонується, щоб пацієнти, які планують припинити прийом ГК, але не демонструють відновлення ГГНО протягом 1 року під час прийому еквівалента фізіологічної добової дози, консультувалися ендокринологом. Пропонується, щоб пацієнти, які приймають ГК та мали адреналову кризу в анамнезі, також пройшли обстеження в ендокринолога (належна клінічна практика).
Р 2.12. Не рекомендується використовувати флудрокортизон у пацієнтів із ННІГ.
Обґрунтування
Короткочасна терапія ГК зазвичай використовується при загостренні астми або хронічного обструктивного захворювання легень, запальних захворюваннях кишківника, шкірних алергіях і ревматоїдному артриті. Зокрема, при загостренні астми зазвичай використовують преднізолон у дозі 50 мг, яка зменшується до нуля протягом 5-7 або 10-14 днів. На сьогодні немає доказів, що такі короткі періоди терапії призводять до клінічно значущого пригнічення ГГНО. Хоча ННІГ малоймовірна після короткочасної терапії, клініцистам варто пам’ятати, що навіть у цьому випадку збільшується ризик сепсису, шлунково-кишкових кровотеч, тромбоемболії та переломів.
Загалом швидке зниження дози можливе при застосуванні високих добових доз ГК (>30 мг преднізону). За наявності ускладнень терапії ГК (неконтрольована гіпертензія або гіперглікемія, психоз, герпетичний кератит) можуть знадобитися швидші темпи зниження до фізіологічних доз. Коли добова доза ГК наближається до еквівалента фізіологічної добової дози (табл. 1), темпи зниження треба сповільнити (табл. 5).
Відновлення ГГНО можливе після зменшення ГК до фізіологічної добової дози (4-6 мг преднізолону). У цей час можна проводити скасування або оцінку відновлення ГГНО. Перед плануванням подальшого зниження дози варто враховувати ймовірність ННІГ, ризик загострення основної хвороби, супутню патологію або застосування інших ліків із потенційним впливом на метаболізм ГК, загальну експозицію ГК й індивідуальні особливості фармакодинаміки та фармакокінетики (наприклад, знижений кліренс ГК в осіб похилого віку).
Синдром скасування виникає в 40-67% осіб, що потребує інформування пацієнта з поясненням відмінностей від ННІГ і загострення основної хвороби (табл. 6). Для диференціації ННІГ і синдрому скасування важливо зважати на загальну добову дозу ГК. Наприклад, у пацієнта, який упродовж кількох місяців лікувався преднізолоном у дозі 20-40 мг, можливі симптоми скасування ГК, але спонтанні прояви ННІГ слід підозрювати лише тоді, коли доза досягає 5-7,5 мг/добу.
Повільне зниження дози ГК – єдиний відомий спосіб запобігання тяжким симптомам скасування.
За відсутності ефекту тимчасове підвищення дози ГК до попередньої зазвичай полегшує симптоми.
Відновлення ГГНО неможливе в умовах постійного застосування потужних ГК тривалої дії (табл. 2) через безперервний нециркадний ефект. Натомість ГК середньої-короткої дії (табл. 2) частіше сприятимуть відновленню ГГНО, за відсутності введення вночі. Тому, плануючи скасування, варто перейти з ГК тривалої дії на препарати короткої дії (табл. 2), щоби сприяти відновленню ГГНО. На пероральні ГК короткої дії доцільно також перейти за підозри на ННІГ у пацієнтів, які приймають непероральні ГК.
Надфізіологічні дози ГК однозначно спричиняють пригнічення ГГНО, тому перевіряти функцію наднирників немає сенсу. Тестування також непотрібне за неможливості скасування ГК (наприклад, після трансплантації органів); таких пацієнтів треба вчити правил лікування ННІГ. На початку зниження дози ГК рівні АКТГ і кортизолу залишаються пригніченими. Надалі гіпоталамус і гіпофіз починають відновлюватися, що збільшує утворення АКТГ, сприяє відновленню функції наднирників і підвищенню кортизолу (рис. 1).
Єдиного підходу до зниження дози ГК ще не встановлено. Триває рандомізоване контрольоване клінічне дослідження TOASST, яке порівнює раптове припинення та поступове зниження дози преднізону 7,5 мг. Після зниження дози ГК до фізіологічної замісної дози експертна група пропонує два можливі підходи до припинення терапії (рис. 2).
Біохімічне тестування є чутливим, але неспецифічним. Зважаючи на низьку поширеність клінічно значущої надниркової недостатності та значну поширеність біохімічної надниркової недостатності після зниження дози ГК, тестування дає змогу виявити осіб із меншим ризиком, але не є передумовою для продовження зниження дози.
Пацієнти з низьким рівнем кортизолу (<150 нмоль/л, або 5 мкг/дл) мають високу ймовірність стійкої надниркової недостатності; їм доцільно продовжити фізіологічні добові дози ГК; повторне тестування проводити через 1-6 місяців, залежно від дози ГК, тривалості терапії та попередніх значень кортизолу. У пацієнтів із рівнем кортизолу 150-300 нмоль/л (5-10 мкг/дл) відновлення ГГНО можливе; найпрактичніша стратегія – продовжити прийом фізіологічних доз ГК з контролем кортизолу що декілька тижнів до одужання. Значення >300 нмоль/л (10 мкг/дл) зазвичай указує на відновлення функції ГГНО при ННІГ.
Інтерпретація результатів ранкового кортизолу потребує врахування таких впливів: 1) хибнонизькі рівні в осіб із порушеним циркадним ритмом (робота в нічну зміну, безсоння); 2) можливе підвищення в осіб із високим рівнем кортизолозв’язувального глобуліну (вагітність, прийом пероральних естрогенів); 3) низький рівень в осіб із низькими рівнями альбуміну та кортизолозв’язувального глобуліну (прогресивний цироз, нефротичний синдром, недостатнє харчування, тривала критична хвороба); 4) точність методу визначення: імунологічний із використанням поліклональних антитіл < імунологічний із використанням моноклональних антитіл < рідинна хроматографія-мас-спектрометрія.
Якщо рівень кортизолу невизначений, можна розглянути динамічне тестування через ≥24 години після прийому ГК, а саме: 1) 250 мкг АКТГ(1-24) – оцінює пряму відповідь наднирників на надфізіологічну стимуляцію АКТГ; піковий рівень кортизолу <500 нмоль/л (<18,1 мкг/дл) через 30 або 60 хвилин є ознакою надниркової недостатності; тест менш надійний у разі короткотривалої терапії ГК; 2) нічний тест зі стимуляцією метирапоном і тест на толерантність до інсуліну більш трудомісткі, можливі значні побічні ефекти.
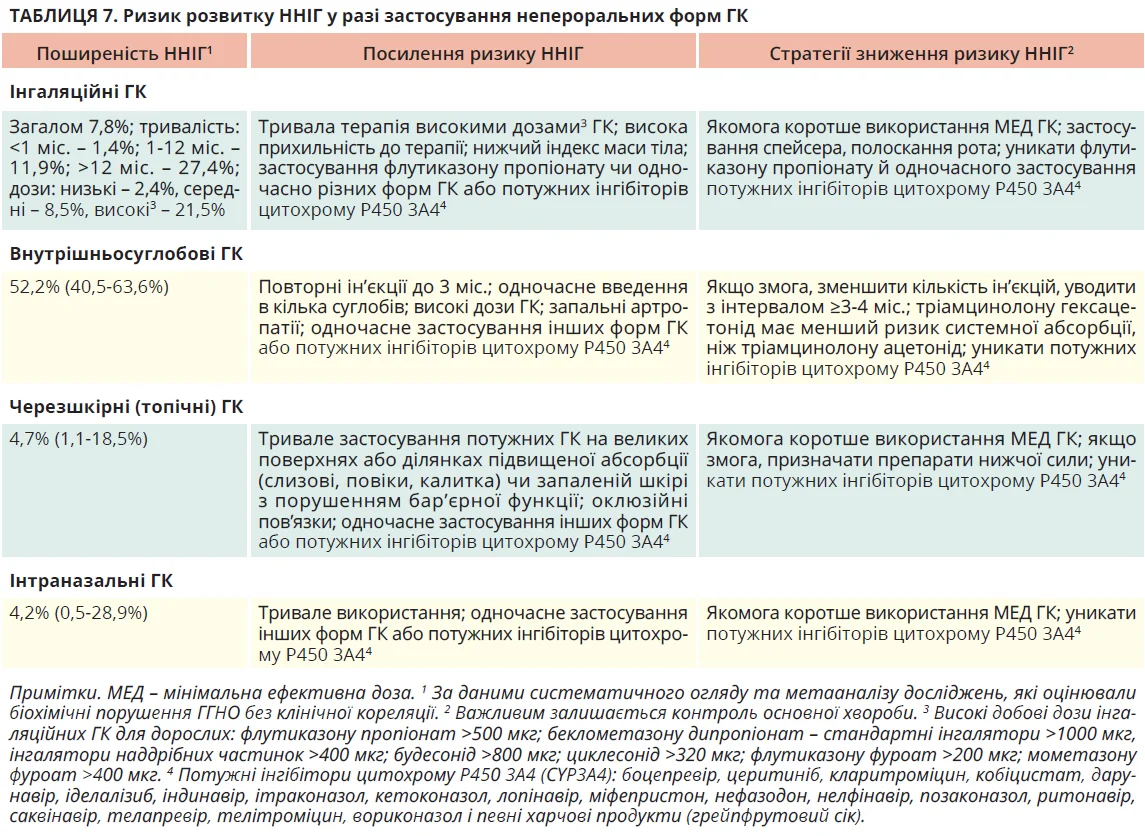
ННІГ може виникнути при застосуванні будь-якої форми ГК (табл. 7), встановленого безпечного рівня експозиції не існує.
Екзогенний синдром Кушинга (табл. 8) може виникнути при застосуванні будь-якої форми ГК; після зниження добової дози ГК до фізіологічного діапазону іноді потрібно декілька місяців до зникнення симптомів. Ранкове визначення кортизолу диференціює пацієнтів із наднирковою недостатністю (пригнічений рівень кортизолу) й ідентифікує пацієнтів із відновленням ГГНО, але збереженням кушингоїдних проявів.
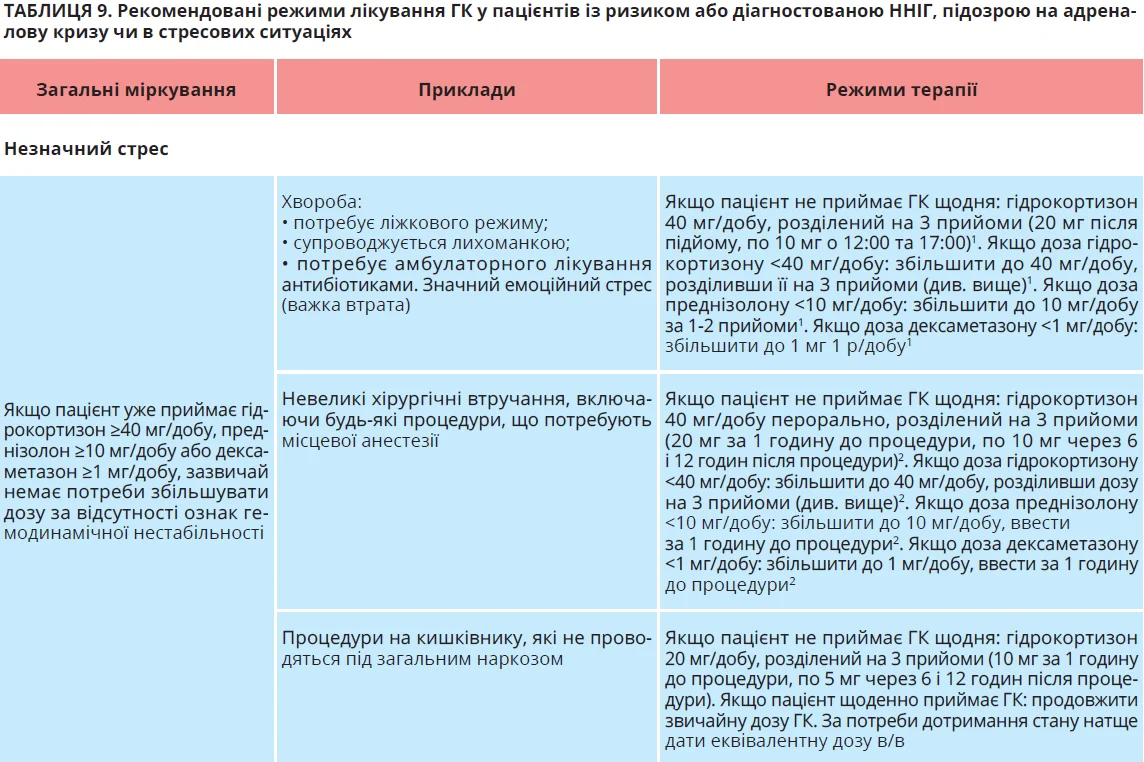
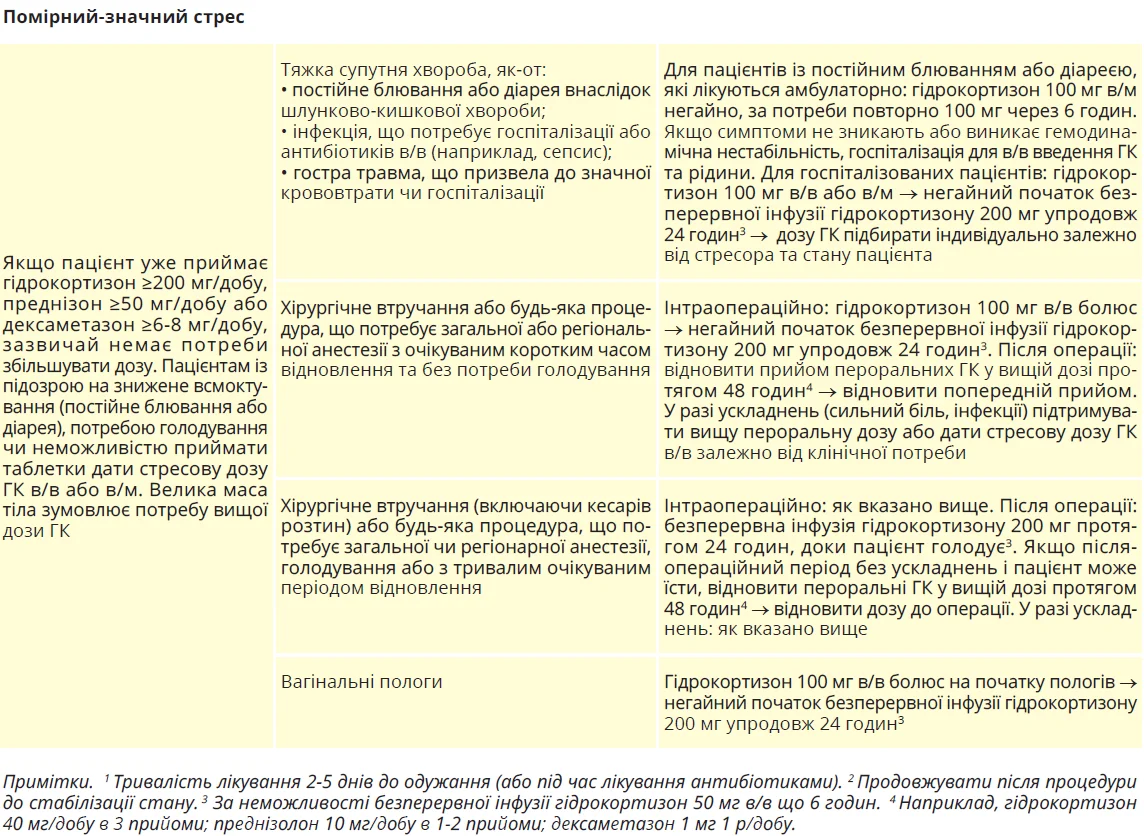
Іноді надниркова недостатність триває до 2-4 років після припинення прийому ГК. Стійке порушення секреції кортизолу >4 роки свідчить про малу ймовірність відновлення функції наднирників і потребує довгострокової замісної терапії ГК. Запропоновано, щоб такі пацієнти консультувалися ендокринологом для визначення можливої причини надниркової недостатності. Консультація ендокринолога показана також особам, які мали адреналову кризу під час прийому ГК. Пацієнти з наднирковою недостатністю >1 рік мають лікуватися стандартними замісними дозами гідрокортизону або преднізолону (табл. 2); їх потрібно навчити корегувати дозу замісної терапії ГК під час стресових ситуацій (табл. 9).
Секреція мінералокортикоїду альдостерону значною мірою регулюється ренін-ангіотензиновою системою та рівнями калію. Тож очікується, що мінералокортикоїдна функція при ННІГ й інших формах вторинної або третинної надниркової недостатності буде збережена та замісна терапія флудрокортизоном не показана.
- Рекомендації щодо діагностики та терапії адреналової кризи в пацієнтів із ННІГ
Р 3.1. Рекомендується, щоб пацієнти, які приймають або нещодавно приймали ГК, але не проходили біохімічних тестів для виключення ННІГ, отримували покриття стресовою дозою під час стресових станів (належна клінічна практика).
Р 3.1a. Пероральні ГК слід застосовувати в разі незначного стресу за відсутності ознак гемодинамічної нестабільності, тривалого блювання або діареї.
Р 3.1b. Парентеральні ГК слід застосовувати в разі помірного-значного стресу, процедур, які проводяться під загальною чи регіональною анестезією, або потребують тривалого голодування, або унеможливлюють пероральний прийом, або за наявності ознак гемодинамічної нестабільності, тривалого блювання чи діареї.
Р 3.2. Пропонується, щоб у пацієнтів, які приймають або нещодавно приймали ГК, але не проходили біохімічних тестів для виключення ННІГ і мають ознаки гемодинамічної нестабільності, блювання чи діарею, розглядався діагноз адреналової кризи незалежно від типу, способу введення та дози ГК; пацієнтів із підозрою на адреналову кризу слід лікувати парентеральними ГК та регідратацією (належна клінічна практика).
Обґрунтування
Щоб запобігти адреналовій кризі, слід користуватися алгоритмом (рис. 3) та навчити пацієнтів стресовому дозуванню ГК (табл. 9). Надниркову недостатність і потребу застосування стресової дози ГК слід розглядати навіть після припинення терапії ГК, особливо в пацієнтів, які не пройшли біохімічного тестування відновлення ГГНО.
Адреналова криза (гостра надниркова недостатність, аддісонівська криза) – загрозливий для життя стан, який потрібно негайно розпізнати та лікувати. Можлива в пацієнтів, які приймають надфізіологічні дози ГК, якщо доступність препарату раптово зменшується (наприклад, пропущені дози, гастроентерит). Характеризується нездатністю кори наднирників виробляти достатню кількість кортизолу, щоб належним чином реагувати на стресори (табл. 9). Патофізіологія складна й докладно не вивчена; обов’язкові характеристики: гіповолемія та вазоплегія, що призводять до гіпотензії, шоку та смерті за відсутності лікування. Важливо підкреслити, що це клінічний діагноз, який слід запідозрити в будь-якого пацієнта, котрий приймає або нещодавно приймав будь-яку форму ГК за наявності відповідних симптомів і ознак (табл. 10). Лабораторні або візуалізаційні дослідження не мають затримувати початок лікування.
Отже, навіть за підозри на адреналову кризу слід негайно зробити внутрішньовенну або внутрішньом’язову ін’єкцію гідрокортизону 100 мг із наступним швидким внутрішньовенним уведенням рідини. Надалі пацієнти з підтвердженою адреналовою кризою мають одержувати підтримувальні дози гідрокортизону до клінічного одужання та подальших рекомендацій ендокринолога. Для пацієнтів із дуже високою масою тіла можна розглянути вищі дози. Деякі центри використовують еквівалентні дози інших парентеральних ГК – метилпреднізолону, дексаметазону. Якщо змога, слід лікувати будь-які ідентифіковані тригери (табл. 10). Короткочасне введення парентеральних ГК у рекомендованих дозах є безпечним; отже, лікування слід розпочинати, навіть якщо діагноз адреналової кризи зрештою буде виключено.
Профілактика адреналової кризи полягає в навчанні пацієнтів вчасно розпізнавати стресори та прояви ускладнення, наголошуючи на важливості інформування медиків у разі тяжкого стану або непритомності (наприклад, стероїдна картка екстреної допомоги: ese-hormones.org). Порівняно з іншими причинами надниркової недостатності пацієнти з ННІГ менш обізнані щодо діагнозу, рідше беруть участь у профілактичних стратегіях (наявність екстреної ін’єкції гідрокортизону, носіння ідентифікаторів), а отже, мають більше затримок надання невідкладної допомоги та більше труднощів управління своїм станом загалом. Це підкреслює потребу впровадження стратегій профілактики й освіти як пацієнтів, так і медичних фахівців.
Література
Beuschlein F., Else T., Bancos I., Hahner S., Hamidi O., van Hulsteijn L., Husebye E.S., Karavitaki N., Prete A., Vaidya A., Yedinak C., Dekkers O.M. European Society of Endocrinology and Endocrine Society Joint Clinical Guideline: diagnosis and therapy of glucocorticoid-induced adrenal insufficiency. The Journal of Clinical Endocrinology & Metabolism. 2024 July; 109 (7): 1657-1683. doi: 10.1210/clinem/dgae250.