Гестаційний діабет: клінічне оновлення
Підготувала канд. мед. наук Ольга Королюк
Доказову базу для визначення ризику гестаційного цукрового діабету (ГЦД) забезпечило велике міжнародне проспективне обсерваційне дослідження HAPO (Hyperglycemia and Adverse Pregnancy Outcomes), результати якого опубліковано 2008 року.
Сучасні діагностичні критерії
Дослідники оцінювали взаємозв’язок між рівнями глікемії через 2 години після перорального застосування 75 г глюкози в понад 25 тис. жінок на 24-32-му тижні вагітності та первинними перинатальними результатами: маса тіла при народженні >90-го процентиля для гестаційного віку, первинний кесарів розтин, неонатальна гіпоглікемія та С-пептид сироватки пуповинної крові >90-го центиля. Результати показали безперервну позитивну лінійну залежність між ризиком первинного результату й материнськими рівнями глікемії натще, через 1 та 2 години після навантаження впродовж орального тесту на толерантність глюкози (ОГТТ), нижчими за рівні, запропоновані для діагностики діабету в загальній популяції.
Ґрунтуючись на цих висновках, підкріплених дослідженнями ACHOIS (Australian Carbohydrate Intolerance Study in Pregnant Women) і MFMU (Maternal-Fetal Medicine Units Network Trial), Міжнародна асоціація груп із вивчення діабету та вагітності (IADPSG) переглянула діагностичні критерії ГЦД, встановивши пороговими рівні глікемії, за яких шанси досягнення первинного результату були в 1,75 раза вищі від шансів за середніх рівнів глікемії в когорті дослідження HAPO. Крім того, консенсус IADPSG постановив, що для діагностики ГЦД достатньо підвищення принаймні одного показника глікемії впродовж ОГТТ. Отож основною метою зміни діагностичних критеріїв ГЦД було встановлення рівнів глікемії, пов’язаних із підвищеним ризиком перинатальних ускладнень. Проте різні організації пропонують різні підходи скринінгу та тестування для діагностики ГЦД (табл. 1).
Сучасна класифікація гіперглікемії під час вагітності
За визначенням Всесвітньої організації охорони здоров’я (ВООЗ) 1965 року, ГЦД – це гіперглікемія діабетичного рівня, що виникає під час вагітності. Отже, історично термін «ГЦД» охоплював увесь спектр материнської гіперглікемії під час вагітності – від прегестаційного діабету до гіперглікемії, вперше виявленої під час вагітності. У 1979 році Національна група даних про діабет США (NDDG) визначила ГЦД як «непереносимість глюкози, яка виникає або виявляється під час вагітності». Згодом, на ІІ Міжнародній конференції з гестаційного діабету (1985) визначення було сформульовано як «непереносимість вуглеводів, що призводить до гіперглікемії різного ступеня тяжкості з початком або першим розпізнаванням під час вагітності». Донедавна це визначення ГЦД використовували найчастіше. Сучасна номенклатура та діагностичні критерії чіткіше диференціюють жінок із прегестаційним діабетом і жінок із гіперглікемією, вперше виявленою під час вагітності (рис. 1). Прегестаційний діабет включає діабет 1 та 2 типів, а також інші типи діабету, як-от діабет, пов’язаний із кістозним фіброзом, моногенний діабет і діабет, індукований тероїдами/ліками. Гіперглікемія під час вагітності класифікується IADPSG на дві окремі категорії – ЦД під час вагітності (ЦДВ), або явний ЦД, та ГЦД.
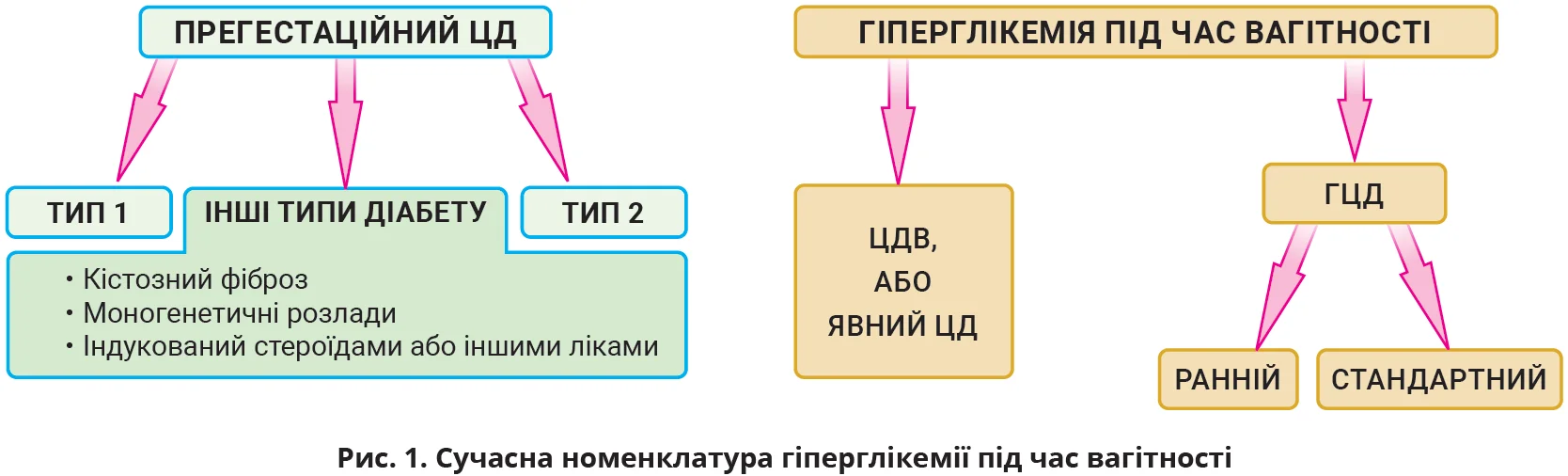
IADPSG рекомендує раннє тестування в жінок із високим ризиком для діагностики діабету на ранніх термінах вагітності, оскільки ЦДВ, діагностований за глікемічними діагностичним критеріями діабету для невагітних, має більший ризик. Зокрема, нещодавнє дослідження за участю майже 5 тис. жінок у Франції виявило, що ЦДВ асоціюється з у 3,5 раза більшим ризиком гіпертензивних розладів під час вагітності порівняно з жінками з нормальною толерантністю до глюкози. Рання гіперглікемія може спостерігатися ще під час зачаття.
З іншого боку, ЦДВ не тотожний попередньому діабету. Проведення ОГТТ австралійським жінкам із ЦДВ через 6-8 тижнів після пологів указує на діабет лише у 21% жінок, предіабетичні розлади виявлено у 38%, тоді як 41% жінок повернулися до категорії нормальної толерантності глюкози.
ГЦД принципово відрізняється від ЦДВ нижчими пороговими значеннями глікемії під час ОГТТ. За визначенням ADA, жінок, у яких діабет діагностовано під час І триместру вагітності, класифікують як таких, що мають (наявний раніше) діабет 2 типу. Натомість ГЦД визначають як діабет, діагностований на пізніх термінах вагітності, що не відповідає діагностичним критеріям діабету 2 типу. Сучасну міжнародну номенклатуру та діагностичні критерії гіперглікемії під час вагітності підсумовано в таблиці 1.

Ранній ГЦД
Критеріями раннього ГЦД вважаються рівні глікемії, нижчі за діабетичні показники, виявлені до 24 тижнів вагітності. За даними досліджень, від 27 до 66% ГЦД можна виявити на ранніх термінах вагітності залежно від популяції, критеріїв скринінгу та методів діагностики, які застосовуються. Нещодавні дослідження, що оцінювали взаємозв’язок між материнською глікемією та траєкторіями росту плода, підтверджують ранній вплив материнської глікемії на надлишковий ріст плода відносно терміну гестації й ожиріння. Наразі немає єдиного консенсусу щодо підходу до тестування та діагностичних рівнів глікемії для раннього ГЦД. Короткий огляд рекомендацій різних міжнародних організацій із відповідними критеріями підсумовано в таблиці 2.
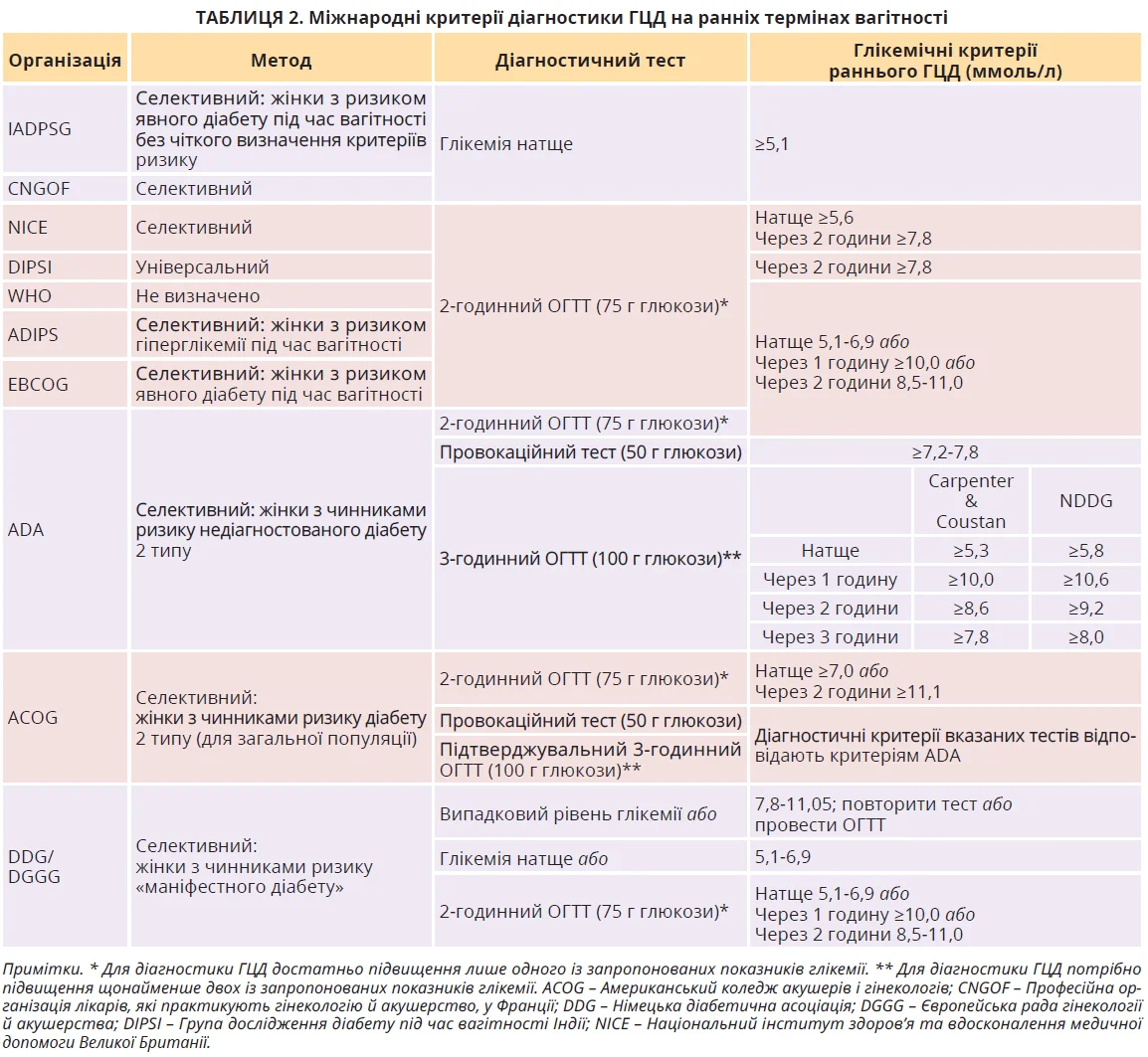
Незважаючи на відсутність чітких рекомендацій щодо діагностики раннього ГЦД, з’являється дедалі більше доказів про високий ризик у цій когорті. Перше велике ретроспективне когортне дослідження показало, що жінки з раннім ГЦД у І триместрі мали тяжчу інсулінорезистентність і значно вищий ризик акушерських і неонатальних ускладнень порівняно з жінками, яким ГЦД діагностували після 24 тижнів вагітності. Низка інших досліджень не лише підтверджує ці дані, а й указує на вищий ризик перинатальної смертності та вроджених аномалій у немовлят. Зокрема, в 5% таких жінок виявляли аномальні результати ехокардіографії плода. Нещодавній метааналіз 13 когортних досліджень показав більшу перинатальну смертність серед жінок із раннім ГЦД порівняно з пізнім ГЦД, незважаючи на лікування. Оцінка патофізіологічних характеристик жінок із ГЦД, встановленим у середньому на 16-му тижні вагітності за діагностичними критеріями IADPSG, показала нижчу чутливість до інсуліну, ніж у жінок із ГЦД, діагностованим на 24-му тижні вагітності. Інше дослідження вказує на порушення функції β-клітин підшлункової залози при обох типах ГЦД. Ці дані підкреслюють фенотипові відмінності ГЦД за часом встановлення діагнозу та ступенем гіперглікемії.
Поки що бракує високоякісних доказів того, що діагностика та лікування раннього ГЦД покращує клінічні наслідки. Нещодавнє рандомізоване контрольоване дослідження (РКД), проведене в США за участю 962 жінок з ожирінням, оцінювало підгрупи раннього тестування ГЦД 2-кроковою стратегією (n=69; 15,0%) та стандартного тестування (n=56; 12,1%). Середній гестаційний вік у підгрупах був подібним (24,3±5,2 та 27,1±1,7 тижня відповідно), проте первинний комплексний перинатальний результат (макросомія, первинний кесарів розтин, гестаційна гіпертензія, прееклампсія, гіпербілірубінемія, дистоція плечиків і неонатальна гіпоглікемія) був дещо вищим у групі раннього скринінгу (56,9% проти 50,8%; P=0,06). Крім того, в жінок із раннім ГЦД потреба в інсулінотерапії була майже вчетверо вищою, а термін вагітності на момент пологів був істотно нижчим (36,7 проти 38,7 тижня; P=0,001). Триває дослідження Treatment of Booking Gestational Diabetes Mellitus, що має на меті визначити, чи є користь від лікування раннього ГЦД.
Захворюваність і поширеність ГЦД
ГЦД – одне з найпоширеніших медичних ускладнень вагітності. За підрахунками Міжнародної федерації діабету (IDF), 2019 року це ускладнення мав 1 із 6 живонароджених у світі. Понад 90% випадків гіперглікемії під час вагітності трапляються в країнах із низьким і середнім рівнями доходу. Поширеність ГЦД значно варіює залежно від популяції, методу скринінгу та діагностичних критеріїв, які застосовуються. Проведений 2012 року систематичний огляд діагностичних критеріїв ЦД вказує, що глобальна поширеність ГЦД становить 2-24,5% за критеріями ВООЗ, 3,6-38% – за критеріями Carpenter & Coustan, 1,4-50% – за критеріями NDDG та 2-19% – за критеріями IADPSG.
Поширеність ГЦД у світі продовжує зростати внаслідок збільшення фонових показників діабету 2 типу, поширеності ожиріння серед жінок дітородного віку та збільшення віку вагітних. Упровадження оновлених діагностичних критеріїв IADPSG значно збільшило частку жінок із ГЦД. Захворюваність на ГЦД у початковій когорті дослідження HAPO із застосуванням діагностичних критеріїв IADPSG коливалася від 9,3 до 25,5% залежно від місця дослідження. Останні дані також демонструють значну варіабельність частоти ГЦД у світі – від 6,6% у Японії та Непалі до 45,3% вагітностей в Об’єднаних Арабських Еміратах.
Чинники ризику ГЦД
Визначено декілька модифікованих і немодифікованих чинників ризику ГЦД (табл. 3). Серед них найсильнішим є ГЦД під час попередньої вагітності з частотою рецидивів до 84%, особливо в етнічних групах із високим ризиком діабету 2 типу (вихідці з Південної та Східної Азії, латиноамериканці, чорношкірі й корінні американці, аборигени й жителі островів Торресової протоки та жителі Близького Сходу). Крім того, жінки з ГЦД мають вищий ризик діабету 2 типу в майбутньому. Іншими вагомими чинниками ризику ГЦД є сімейний анамнез діабету 2 типу в родичів першого ступеня спорідненості (батьків, братів, сестер) і вік під час вагітності понад 35 років. Велике проспективне дослідження, що оцінювало ризик у І-ІІ триместрах, продемонструвало безперервний позитивний зв’язок між збільшенням віку матері та ризиком несприятливих наслідків вагітності, включно з ГЦД (скореговане відношення шансів у вікових групах 35-39 років і ≥40 років становило 1,8 та 2,4 відповідно).
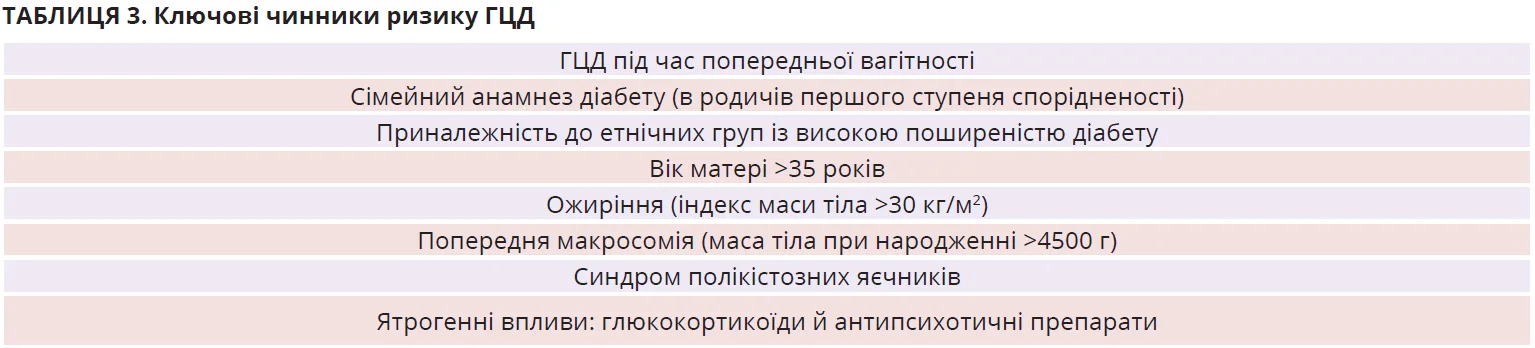
Поширеними чинниками ризику ГЦД є надмір маси тіла й ожиріння матері до вагітності. Порівняно з жінками з індексом маси тіла (ІМТ) <30 кг/м2 ризик ГЦД майже втричі вищий у жінок з ожирінням I класу (ІМТ – 30-34,99 кг/м2) і вчетверо вищий у жінок з ожирінням ІІ класу (ІМТ – 35-39,99 кг/м2). Збільшення маси тіла під час вагітності, особливо в І триместрі, також асоціюється з вищим ризиком ГЦД. Імовірність аномальної толерантності глюкози в жінок з ожирінням і значним приростом маси під час вагітності в 3-4 рази вища, ніж у жінок із приростом маси під час вагітності в межах рекомендацій Інституту медицини 1990 року. Збільшення маси тіла між вагітностями підвищує ризик розвитку ГЦД і перинатальних ускладнень під час наступної вагітності.
Існує зв’язок між синдромом полікістозних яєчників і ГЦД, що значно послаблюється після корегування ІМТ матері. До інших чинників ризику ГЦД відносять: багатоплідність, вагітність двійнею, попередню макросомію плода, перинатальні ускладнення в анамнезі, наявність у матері LGA (велика для гестаційного віку) або SGA (мала для гестаційного віку), низьку фізичну активність, уживання продуктів із високим глікемічним індексом і низьким умістом клітковини, низьке споживання вуглеводів і значної кількості харчових жирів, застосування глюкокортикоїдів й антипсихотичних засобів.
Гіпертензія матері до та на ранніх термінах вагітності також асоціюється з вищим ризиком ГЦД.
Загалом найсильнішими чинниками ризику ГЦД є сімейний анамнез діабету та ГЦД під час попередньої вагітності. До сильних чинників ризику відносять етнічну приналежність, старший вік матері й ІМТ.
Патофізіологія ГЦД
Нормальна вагітність асоціюється з помітними змінами фізіології глікемії з прогресивним підвищенням резистентності до інсуліну внаслідок збільшення циркулювальних плацентарних гормонів – гормона росту, кортикотропін-рилізинг-гормона, людського плацентарного лактогена, пролактину, естрогена та прогестерону. Надмір жирової клітковини в матері, особливо на ранніх термінах вагітності, посилює резистентність до інсуліну та ліполіз на пізніх термінах вагітності. Як наслідок, підвищується рівень вільних жирних кислот (ВЖК) у матері, що посилює резистентність до інсуліну шляхом пригнічення поглинання глюкози та посилення глюконеогенезу в печінці. На пізніх термінах вагітності в 40-80% жінок знижується чутливість до глюкози. Підвищена резистентність матері до інсуліну призводить до вищих постпрандіальних рівнів глюкози та ВЖК, посилення полегшеної дифузії через плаценту, що збільшує доступність глюкози для росту плода. Прогресивне посилення інсулінорезистентності матері в ІІ-ІІІ триместрах вагітності лежить в основі підходу відстроченого тестування ГЦД, спрямованого на максимізацію його виявлення. Крім інсулінорезистентності та підвищення постпрандіальних рівнів глікемії, адаптація під час нормальної вагітності включає посилену секрецію інсуліну. Еуглікемія під час вагітності забезпечується збільшенням секреції інсуліну на 200-250%, особливо на ранніх термінах. До основних регуляторів гіперсекреції інсуліну β-клітинами матері та проліферації під час вагітності відносять плацентарний лактоген, пролактин і гормон росту.
Для ГЦД характерний відносний дефіцит секреції інсуліну, коли рівень секреції інсуліну β-клітинами матері не в змозі компенсувати прогресивну інсулінорезистентність. Це призводить до зниження поглинання глюкози, посилення глюконеогенезу в печінці та гіперглікемії в матері, ймовірно, внаслідок недостатнього збільшення маси β-клітин. Ліпотоксичне ураження β-клітин може зумовити гіперліпідемія (гіпертригліцеридемія), що ще більше порушує секрецію інсуліну. Відповідно, патогенез ГЦД схожий на патогенез діабету 2 типу, що характеризується як підвищеною резистентністю до інсуліну, так і відносним дефіцитом інсуліну внаслідок зниження функції та маси β-клітин. Оцінка секреторної відповіді інсуліну в жінок із ГЦД свідчить про те, що аномальна реакція виникає ще до вагітності та посилюється на ранніх термінах, випереджуючи порушення чутливості до інсуліну. Отже, в багатьох жінок із ГЦД можлива хронічна дисфункція β-клітин, опосередкована циркулювальними гормонами, зокрема лептином.
Генетика ГЦД
Генетичні аспекти метаболізму глюкози під час вагітності вивчені недостатньо. Більшість досліджень зосереджувалися на варіантах, пов’язаних із діабетом 2 типу, та продемонстрували подібність до ГЦД. Метааналіз 28 досліджень типу «випадок – контроль» (n=23 425) виявив 6 генетичних поліморфізмів у локусах, пов’язаних із секрецією інсуліну (IGF2BP2, MTNR1B, TCF7L2), резистентністю до інсуліну (IRS1, PPARG) та запаленням (TNF-α) при діабеті 2 типу. Серед них лише три (MTNR1B, TCF7L2, IRS1) були значущо пов’язані з ГЦД. Аналіз підгруп показав, що алелі ризику TCF7L2 та PPARG були значущими лише в азійських популяціях, а зв’язок ризику ГЦД з IRS1 та TCF7L2 змінювався залежно від діагностичних критеріїв і методології генотипу.
Два загальногеномні дослідження асоціацій (GWAS) оцінювали генетичні асоціації ГЦД. Перше дослідження включало корейських жінок та ідентифікувало два локуси, значущо пов’язані з ГЦД, – CDKAL1 та MTNR1B. Локус CDKAL1 асоціювався зі зниженням концентрації інсуліну натще й індексу HOMA (оцінка моделі гомеостазу функції β-клітин) у жінок із ГЦД, тобто вказував на порушення компенсації β-клітин. Локус MTNR1B асоціювався зі зниженням концентрації інсуліну натще в жінок із ГЦД та збільшенням рівнів глікемії натще в жінок із та без ГЦД. Інші дослідження вказують на зв’язок варіантів CDKAL1 та MTNR1B із ризиком діабету 2 типу.
Інше дослідження GWAS за участю європейських, тайських, афрокарибських і латиноамериканських жінок оцінювало метаболічні особливості вагітних. Виявлено 5 варіантів, які асоціювалися з рівнями глюкози та С-пептиду під час вагітності, хоча сила асоціацій була різною в різних когортах. Із глікемією натще були пов’язані GCKR, G6PC2, PCSK1, PPP1R3B та MTNR1B; із рівнями C-пептиду натще – GCKR та PPP1R3B; із глікемією через 1 годину після навантаження – MTNR1B. За даними інших досліджень, ці локуси асоціювалися з метаболізмом ліпідів (GCKR і PPP1R3B), глікогену (PPP1R3B) й ожирінням (PCSK1).
Нещодавно ідентифіковано ще два локуси, актуальні під час вагітності: HKDC1 асоціювався з глікемією через 2 години після навантаження, BACE2 – з рівнем С-пептиду натще.
Загалом дослідження підтверджують, що генетичні детермінанти рівня глюкози й інсуліну натще, секреції інсуліну та чутливості до інсуліну, про які повідомляється поза вагітністю, впливають на ризик ГЦД. Відомі на сьогодні гени, пов’язані з ГЦД, підсумовано в таблиці 4.
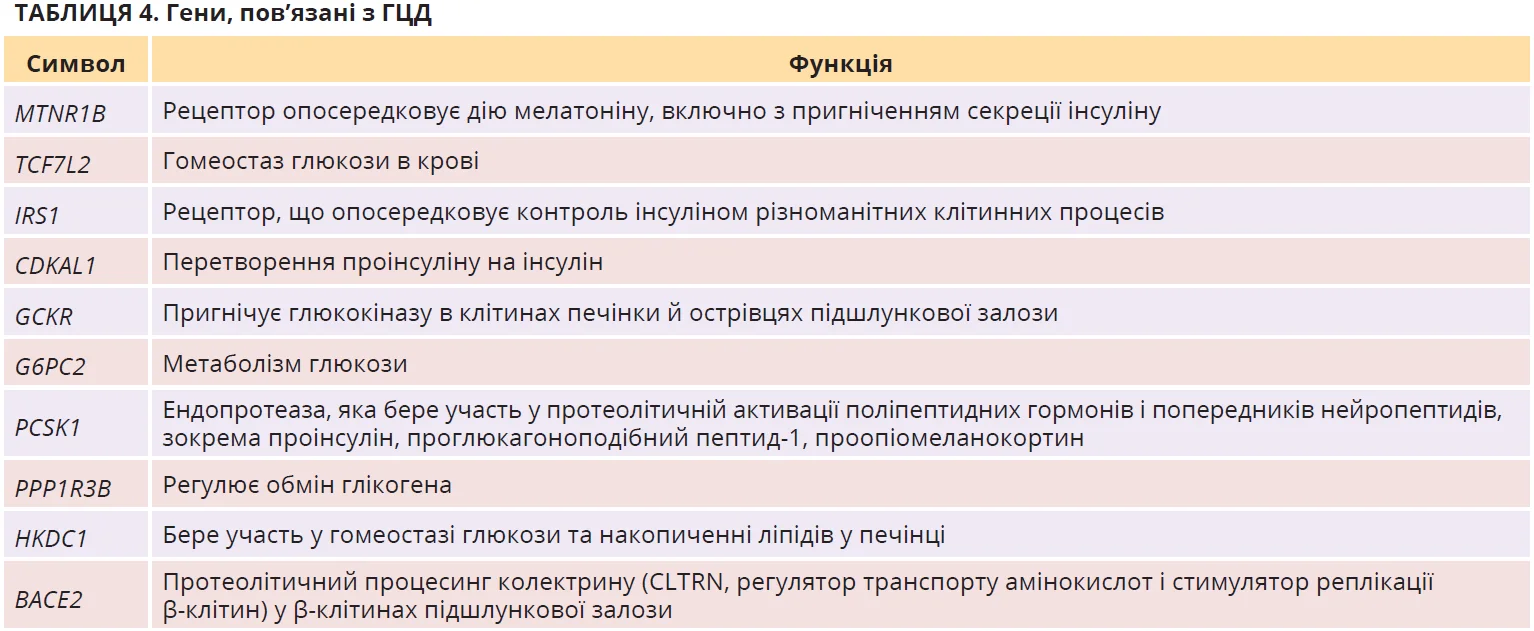
MODY-діабет
ЦД дорослого типу в молодих, або MODY-діабет (maturity-onset diabetes of the young), – це найпоширеніша форма моногенного діабету, тобто спадкових форм діабету з дефектами окремих генів, які регулюють розвиток і функцію β-клітин. MODY-діабет включає декілька автосомно-домінантних форм і становить до 2% усіх діагнозів діабету.
Для встановлення діагнозу потрібне підтверджувальне молекулярно-генетичне тестування. Тому MODY-діабет часто неправильно діагностують як попередній діабет або ГЦД. За підрахунками поширеність таких помилок у період вагітності може становити до 5% «випадків» ГЦД.
MODY-діабет також неоднорідний. У вагітних найчастіше виявляють глюкокіназний підтип (GCK-MODY, до 1% усіх «випадків» ГЦД), спричинений мутаціями в гені глюкокінази. Клінічно GCK-MODY характеризується легкою стабільною гіперглікемією та низькою частотою мікро- й макросудинних ускладнень. Цей тип слід запідозрити в осіб із позитивним сімейним анамнезом легкої гіперглікемії або діабету, ІМТ <25 кг/м2, гіперглікемією натще в межах 98-150 мг/дл (5,4-8,3 ммоль/л) і приростом глікемії впродовж 2-годинного ОГТТ із навантаженням 75 г глюкози <4,6 ммоль/л. Що стосується лікування, то інсулінотерапія матері показана лише за наявності мутації GCK-MODY в плода, критерієм якої є збільшення черевної порожнини плода >75-го центиля на серійних УЗД-знімках після
26 тижнів вагітності.
Наслідки ГЦД
ГЦД пов’язаний із надмірною короткостроковою та довгостроковою захворюваністю матерів і новонароджених (табл. 5).
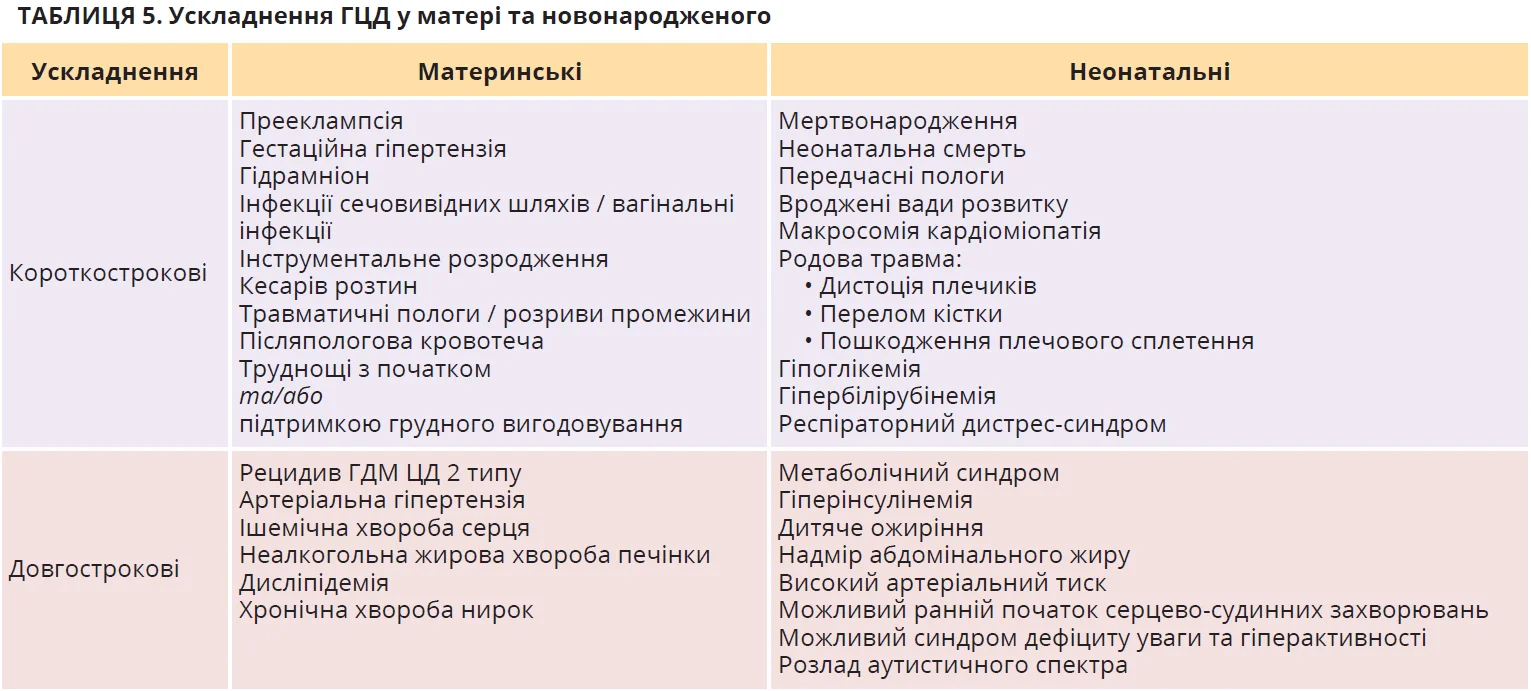
Неонатальні ускладнення
Ранні
Патофізіологію перинатальних ускладнень описує гіпотеза Педерсена (рис. 2). Гіперглікемія матері призводить до гіперглікемії плода через полегшену дифузію глюкози транспортером глюкози-1 (GLUT1). Як наслідок, виникає гіперінсулінемія плода, що посилює анаболізм і відкладання жиру, прискорює ріст плода, спричиняючи макросомію та LGA. Гіперліпідемія матері також зумовлює надмірний ріст плода. Макросомія та LGA підвищують ризик кесаревого розтину, родової травми й перинатальних ускладнень, включаючи дистоцію плечиків, переломи, пошкодження плечового сплетення та перинатальну асфіксію. Вищий ризик перинатальної асфіксії пов’язаний із внутрішньоутробною загибеллю плода, поліцитемією та гіпербілірубінемією. Фетальна гіперінсулінемія також може збільшити ризик метаболічних аномалій, включаючи неонатальну гіпоглікемію, гіпербілірубінемію та респіраторний дистрес-синдром після пологів. Неонатальні ризики вищі серед жінок із тяжкою гіперглікемією. ГЦД також асоціюється з підвищеним ризиком передчасних пологів, родової травми, неонатального респіраторного дистрес-синдрому та гіпертрофічної кардіоміопатії. В окремих когортах відзначено вищий ризик вад серця та перинатальної смертності після 37 тижнів вагітності. Ризик родових травм і гіпоглікемії плода значно зростав за умови поєднання ГЦД та макросомії плода (маса тіла ≥4000 г).
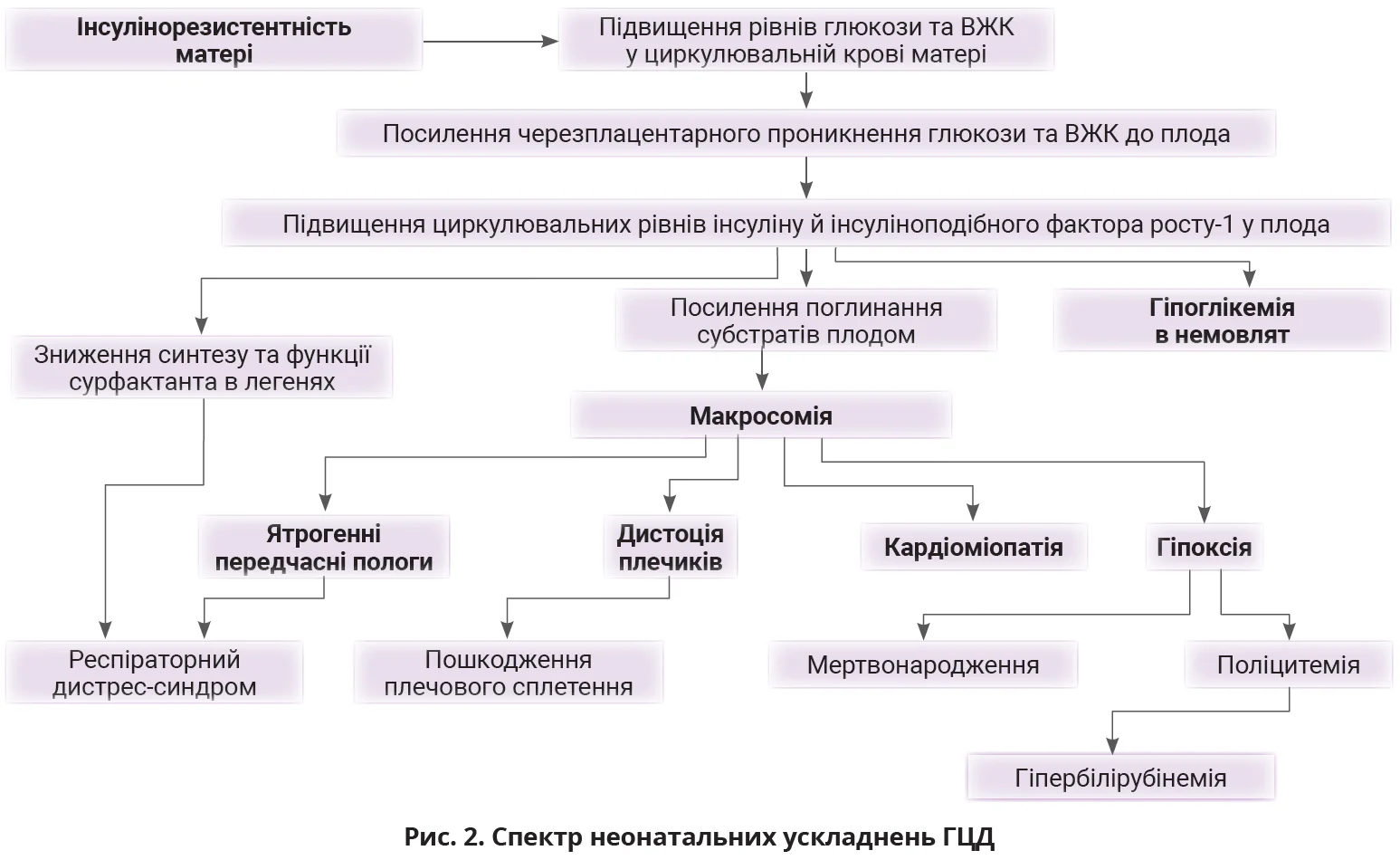
Проте слід підкреслити, що ГЦД підвищує ризик розвитку багатьох перинатальних ускладнень незалежно від маси тіла при народженні. У жінок із недіагностованим ГЦД встановлено вчетверо вищий ризик мертвонародження після 28-го тижня гестації, чого не спостерігалося в дослідженні за участю жінок ізвстановленим ГЦД. Отже, діагностика та лікування ГЦД істотно знижують ризик мертвонародження.
Пізні
Нещодавні епідеміологічні дослідження вказують на підвищений ризик віддалених несприятливих кардіометаболічних наслідків у нащадків жінок із ГЦД (на 19% вищий ризик виникнення у віці до 40 років серцево-судинних захворювань – ССЗ), адже ГЦД асоціюється зі структурно-функціональними змінами серця плода, систолічною та діастолічною дисфункцією в дитинстві. Дослідження HAPO-FUS за участю 4832 дітей віком 10-14 років, чиї матері були учасницями HAPO, продемонструвало значний вплив материнської глікемії на метаболізм глюкози в потомків у довгостроковій перспективі. У нащадків встановлено прямий зв’язок між ГЦД та порушенням толерантності глюкози й обернений зв’язок між ГЦД та чутливістю до інсуліну. Вищі рівні гіперглікемії матері впродовж ОГТТ асоціювалися з вищою частотою ожиріння в дітей. Нещодавно встановлено підвищену активацію гіпоталамуса в дітей 7-11 років, які зазнали внутрішньоутробного впливу ГЦД й ожиріння матері. Активація гіпоталамуса була предиктором вищих показників ІМТ у дітей та є одним із можливих пояснень ризику виникнення ожиріння в дітей.
Материнські ускладнення
Короткостроковий ризик
Жінки з ГЦД мають вищий ризик акушерських втручань (індукція пологів, кесарів розтин) і пов’язаних із пологами ускладнень (розриви промежини та матки). Насамперед це пов’язано з макросомією плода й багатоводдям. Низка досліджень указує на вищий ризик гестаційної гіпертензії та прееклампсії. Аномалії метаболізму глюкози впливають на інвазію трофобласта, що порушує плацентацію та підвищує ризик прееклампсії. Механізм, імовірно, пов’язаний з інсулінорезистентністю й активацією запального шляху. Дослідження in vitro продемонстрували, що підвищені концентрації глюкози пригнічують інвазивність трофобласта шляхом впливу на активність активатора плазміногена в матці.
Довгостроковий ризик
Жінки з ГЦД мають вищий ризик рецидивів під час майбутніх вагітностей (частота рецидивів – 30-84%), а також ризик діабету 2 типу – у 20 разів упродовж життя та в 10 разів упродовж перших 5 років після ГЦД. Через 14 років більш як половина учасниць дослідження HAPO-FUS мали предіабет.
Встановлено також зв’язок ГЦД із такими серцево-судинними чинниками ризику, як ожиріння, гіпертензія та дисліпідемія. Ризик розвитку ССЗ упродовж життя підвищується в 1,5 раза, а за умови виникнення діабету 2 типу – майже втричі. Порівняно з жінками без ГЦД перенесений ГЦД збільшує ризик артеріальної гіпертензії на 26%, інфаркту міокарда чи інсульту – на 43%.
Менеджмент ГЦД
Позитивні впливи на перинатальні результати
Сучасні зміни методів виявлення та лікування ГЦД асоціюються з досягненням результатів маси тіла й параметрів ожиріння новонароджених, які практично зіставні із загальною популяцією вагітностей у розвинених країнах. Першим великим РКД, яке оцінювало, чи лікування ГЦД знижує ризик перинатальних ускладнень, було дослідження ACHOIS (n=1000). Встановлено, що поєднання дієтичних порад, самоконтролю глікемії матері й інсулінотерапії (за потреби) з досягненням цільових рівнів глікемії натще в межах 3,5-5,5 ммоль/л (63-99 мг/дл), глікемії перед прийомом їжі ≤5,5 ммоль/л (99 мг/дл), глікемії через 2 години після їди ≤7,0 ммоль/л (126 мг/дл) знижує сукупну частоту перинатальних ускладнень (комбінація смерті, дистоції плечиків, переломів, паралічу нервів) учетверо (1% проти 4% у групі звичайного догляду; P=0,01). Втручання також сприяло зниженню ризику макросомії (10% проти 21%; P<0,001), прееклампсії (12% проти 18%; P=0,02) та покращенню пов’язаної зі здоров’ям якості життя матері.
Схожі результати продемонструвало дослідження MFMU (n=958). Лікування ГЦД включало дієтичне втручання, самоконтроль глікемії в матері й інсулінотерапію (за потреби) й асоціювалося з покращенням наслідків порівняно зі звичайним доглядом за умови досягненням цільових рівнів глікемії натще <5,3 ммоль/л (95 мг/дл) і глікемії через 2 години після прийому їжі <6,7 ммоль/л (121 мг/дл). Зокрема, зниження частоти макросомії (5,9% проти 14,3%; P<0,001), LGA (7,1% проти 14,5%; P<0,001), дистоції плечиків (1,5% проти 4,0%; P=0,02), кесаревого розтину (26,9% проти 33,8%; P=0,02), а також прееклампсії та гестаційної гіпертензії (8,6% проти 13,6%; P=0,01). Проте втручання не забезпечило суттєвої різниці в первинному сукупному результаті, яке включало мертвонародження, перинатальну смерть і неонатальні ускладнення (гіпербілірубінемію, гіпоглікемію, гіперінсулінемію, пологову травму).
Нещодавній кокранівський огляд (8 РКД; n=1418) дійшов висновку, що лікування ГЦД шляхом дієтичного втручання й інсулінотерапії зменшило сукупний результат перинатальної захворюваності (смерть, дистоція плечиків, переломи кісток і параліч нервів) на 68% порівняно зі звичайним антенатальним доглядом. Лікування також асоціювалося зі зменшенням макросомії, LGA та прееклампсії, але збільшенням потреби в індукції пологів та госпіталізації новонароджених у відділення інтенсивної терапії.
Втручання в спосіб життя
Основна мета лікування ГЦД – досягнення та підтримка нормоглікемії в матері, що запобігає надмірному росту плода. Підхід насамперед включає лікувальне харчування. Вуглеводи – визначальний чинник остпрандіальної глікемії, тому сучасна дієтична практика спрямована на зміну якості вуглеводів (глікемічного індексу) та їх розподілу. Оригінальний харчовий підхід у разі ГЦД запропонував зниження споживання вуглеводів до 33-40% від загального споживання енергії (EI), що асоціювалося зі зниженням постпрандіальної глікемії та надмірного росту плода. Більше споживання вуглеводів (60-70% EI) з низьким глікемічним індексом також обмежує гіперглікемію в матері. Проте доказових даних щодо дієтичних втручань у разі ГЦД недостатньо.
Нещодавній метааналіз (18 РКД; n=1151) показав, що збільшення якості харчування після діагностики ГЦД покращує материнські рівні глікемії натще та після їди, знижує потребу фармакотерапії, зменшує масу тіла при народженні та ризик макросомії незалежно від типу дієтичного втручання. Тому міжнародні настанови поки що рекомендують споживати вуглеводи від 33 до 55% EI. Дослідження вказують на покращення наслідків вагітності при ГЦД у разі застосування як низького (42% EІ), так і високого (55% EІ) вмісту вуглеводів. Настанови IOM рекомендують під час вагітності споживання вуглеводів не менш як 175 г/день із добовим споживанням калорій у межах 2000-2500 ккал. ACOG рекомендує дієту з низьким умістом вуглеводів (33-40% EІ). Проте настанови ADA (2005) висловлюють занепокоєння щодо вищого споживання жиру матір’ю за умови обмеження вуглеводів і впливу ліпідів на плід, скасовуючи спеціальні дієтичні рекомендації для ГЦД. Оскільки материнська глюкоза насамперед підтримує ріст плода та розвиток мозку, зменшення вуглеводів у раціоні матері може порушувати градієнт глюкози між матір’ю та плодом. Обмеження загального ЕІ матері асоціюється зі зниженням росту плода. Нещодавній систематичний огляд також показав, що низьке споживання вуглеводів корелює з меншою масою тіла при народженні та більшою частотою SGA; мінімальний уміст вуглеводів, що асоціюється з належним ростом плода, становить 47% EI.
Отже, порогові значення вуглеводів у разі ГЦД чітко не встановлені. Проблеми безпеки, пов’язані з низьковуглеводними дієтами, включають потенційний ризик впливу підвищених рівнів материнських кетонів на плід і дефіцит мікроелементів. Дослідження in vitro показали, що кетони пригнічують поглинання глюкози трофобластом, порушуючи перенесення глюкози через плаценту. Проспективне когортне дослідження в США за участю жінок із встановленим діабетом, ГЦД та нормальною толерантністю глюкози продемонструвало зворотну кореляцію між вищим умістом β-гідроксибутирату та ВЖК у матері впродовж ІІІ триместру й нижчими показниками інтелектуального розвитку дітей у віці 2-5 років.
Гестаційний приріст маси тіла (ГПМТ)
Настанови IOM містять рекомендації щодо ГПМТ відповідно до ІМТ до вагітності, проте конкретних рекомендацій для жінок із ГЦД не існує. За даними досліджень у жінок із надмірною масою тіла чи ожирінням, зменшення або збільшення маси тіла ≤5 кг підвищувало ризик SGA. Нещодавній систематичний огляд (n≈740 000) продемонстрував, що ГПМТ 5-9 кг у жінок з ожирінням I класу, 1-5 кг у жінок з ожирінням II класу й 0 кг у жінок з ожирінням III класу мінімізували комбінований ризик LGA, SGA та кесаревого розтину. Метааналіз (n=88 599), який оцінював зв’язок між ГПМТ і результатами вагітності при ГЦД, показав, що ГПМТ, вищий за рекомендації IOM, асоціюється з підвищеним ризиком фармакотерапії, гіпертензивних розладів вагітності, кесаревого розтину, LGA та макросомії. ГПМТ, нижчий за рекомендації IOM, знижував ризик LGA та макросомії. Відповідно, цілі ГПМТ у разі ГЦД можуть бути нижчими, ніж рекомендовані для нормальної вагітності. Проте з практичного погляду лише 30% жінок набирають менше, ніж рекомендовані цілі IOM.
Цільові рівні глікемії в матері
Жінкам із ГЦД рекомендовано вимірювати рівень глікемії натще та через 1 або 2 години після прийому їжі. Піковий рівень глюкози через 1 годину після прийому їжі корелює з рівнем інсуліну в амніотичній рідині, що відображає гіперінсулінізм плода, а в жінок із діабетом 1 типу – і з окружністю живота плода. Встановлено, що титрування інсулінотерапії на підставі рівня глікемії через 1 годину після їди асоціювалося з покращенням контролю глікемії в матері та зменшувало ризик неонатальних ускладнень, пов’язаних із гіперінсулінемією плода. Цільові рівні глікемії в матері також варіабельні (табл. 6).
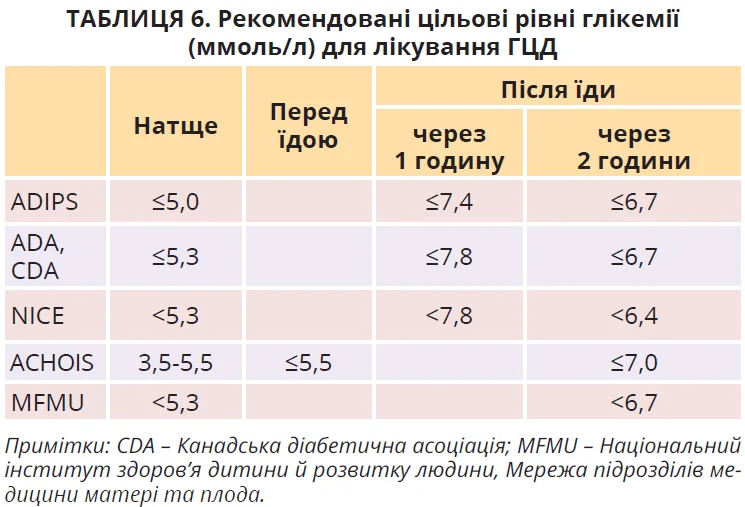
Імовірно, нижчі цільові рівні глікемії можуть покращити результати вагітності при ГЦД, але це потрібно перевірити в РКД достатньої потужності. І навпаки, нижчі цілі глікемії можуть асоціюватися з вищим ризиком SGA, гіпоглікемії матері та плода.
Інсулінотерапія
Традиційно, якщо рівень глікемії в матері залишається підвищеним на тлі лікувального харчування, застосовують інсулін. Для підтримки еуглікемії цей вид терапії застосовує приблизно половина жінок із ГЦД. У жінок із високим рівнем глікемії натще застосовують вечірнє введення інсуліну середньотривалої дії; за показаннями додають інсулін швидкої дії під час їди. Додаткова денна доза інсуліну середньотривалої дії може знадобитися для контролю гіперглікемії перед обідом.
У ІІІ триместрі може виникнути потреба зменшити дози інсуліну внаслідок фізіологічного підвищення чутливості матері до інсуліну, притаманного цій стадії вагітності. Потреба значного зниження дози інсуліну, повторна гіпоглікемія в матері, уповільнення росту плода чи прееклампсія вказують на патофізіологічну плацентарну недостатність, що впливає на термін пологів та інтенсивність акушерського моніторингу.
Нещодавнє дослідження вказує такі незалежні предиктори інсулінотерапії: вік матері >30 років, сімейний анамнез діабету, ожиріння до вагітності, попередній ГЦД, раннє виявлення ГЦД, рівень глікемії натще ≥5,3 ммоль/л (96 мг/дл) і рівень HbA1c ≥5,5% (37 ммоль/моль) на момент встановлення діагнозу.
Пероральна фармакотерапія
Порівняно з інсуліном пероральна фармакотерапія асоціюється з кращими прихильністю, прийнятністю й економічною ефективністю. Найчастіше застосовують глібурид і метформін. Однак існують проблеми щодо ефективності та безпеки, особливо в довгостроковій перспективі. Тому інсуліну зазвичай віддають перевагу як фармакотерапії І лінії після втручання в спосіб життя.
Глібурид зазвичай призначають як терапію І лінії ГЦД у США. У ранньому дослідженні за участю 404 жінок із ГЦД порівнювали ефективність глібуриду з інсулінотерапією. Відмінностей у рівнях материнської глікемії та неонатальних результатах між групами не виявлено. Проте подальші дослідження показують, що ≈20% жінок потребують додавання інсуліну для досягнення адекватної глікемії. Велике ретроспективне дослідження в США за участю ≈111 тис. жінок із ГЦД (4982 отримували глібурид, 4191 – інсулін) показує, що глібурид асоціювався з вищим ризиком неонатальних ускладнень (госпіталізація новонароджених у відділення інтенсивної терапії, респіраторні захворювання, дистрес-синдром, гіпоглікемія, пологова травма та LGA). Трансплацентарний перехід глібуриду може досягати 50-70% концентрації в плазмі крові матері, викликаючи пряму стимуляцію утворення інсуліну в плода.
Дедалі частіше під час вагітності застосовують метформін, але доцільність його призначення залишається суперечливою через занепокоєння щодо ефектів довгострокового метаболічного програмування та трансплацентарного проникнення до плода, оскільки деякі дослідження свідчать про однакові концентрації метформіну в плазмі крові матері та плода. Нещодавній систематичний огляд із метааналізом 28 досліджень (n=3976), які оцінювали ріст потомства жінок із ГЦД, показали, що новонароджені, чиї матері отримували метформін, мали меншу масу тіла при народженні (середня різниця -107,7 г), нижчий ризик LGA й макросомії та нижчі пондеральні індекси порівняно з новонародженими, чиї матері отримували інсулін.
У нащадків жінок із ГЦД, які отримували метформін, виявлено прискорений постнатальний ріст у віці від 18 до 24 місяців (два дослідження, n=411; середня різниця в масі тіла – 440 г) і вищі показники ІМТ у віці 5-9 років (три дослідження, n=520; середня різниця ІМТ – 0,78 кг/м2). У дослідженні The Metformin in Gestational Diabetes 751 жінку рандомізували до терапії метформіном або інсуліном і не виявили суттєвої різниці в сукупному неонатальному результаті (неонатальна гіпоглікемія, респіраторний дистрес-синдром, гіпербілірубінемія, низькі бали за шкалою Апгар, пологова травма та передчасні пологи). У групі метформіну спостерігалася тенденція до збільшення передчасних пологів і зниження ГПМТ у матері; тяжка неонатальна гіпоглікемія була вищою в групі інсуліну. Майже 50% жінок, які отримували метформін, потребували додаткової інсулінотерапії. Інші дослідження показали, що 14,0-55,8% жінок на метформіні потребують додавання інсуліну для досягнення оптимального контролю глікемії. Декілька досліджень віддалених результатів у дітей, чиї матері під час вагітності приймали метформін, указують на вищі показники ІМТ і частоту надмірної маси тіла й ожиріння в дітей у віці 4-9 років.
Нещодавній кокранівський огляд (8 РКД; n=1487), що оцінював використання метформіну, глібуриду й акарбози в жінок із ГЦД, показує, що переваги та потенційна шкода цих методів лікування порівняно одне з одним неясні. Інші метааналізи, які порівнювали глібурид, метформін та інсулін, показали, що метформін асоціювався з меншим ГПМТ, нижчою постпрандіальною глікемією та нижчою частотою гестаційної гіпертензії порівняно з глібуридом або інсуліном. Проте ризик передчасних пологів у разі застосування метформіну був вищим порівняно з інсулінотерапією. Глібурид асоціювався з вищим ризиком збільшення маси при народженні, LGA, макросомії, неонатальної гіпоглікемії та вищим ГПМТ порівняно з метформіном.
Акушерський менеджмент
Нещодавній кокранівський огляд (три невеликі РКД, n=524) повідомив про недостатність доказів щодо використання біометрії плода для визначення тактики медичного менеджменту ГЦД. Проте серійне ультразвукове дослідження (УЗД) росту плода, зокрема оцінка окружності живота, є потенційно корисним для визначення інтенсивності цільового рівня глікемії матері й інсулінотерапії. За даними досліджень, у новонароджених із розрахованою масою плода ≥75-го процентиля за даними УЗД на початку ІІІ триместру вдесятеро більша ймовірність LGA порівняно з тими, в кого цей показник становив <75-го процентиля. Виміряна окружність живота плода <90-го процентиля під час двох УЗД з інтервалом 3-4 тижні також показала високу надійність виключення ризику LGA. Ці результати свідчать про потенційну корисність біометрії плода для виявлення вагітності з високим ризиком.
Оптимальні терміни пологів у разі ГЦД остаточно не встановлені та визначаються за чинниками матері, плода й материнським контролем глікемії. Поточні настанови рекомендують пологи до терміну вагітності 40+6 тижнів у жінок із низьким ризиком і ГЦД, який лікується лише дієтою, та від 39+0 до 39+6 тижнів вагітності для жінок із ГЦД, добре контрольованим за допомогою терапії. Популяційне когортне дослідження в Канаді впродовж 10 років вивчало тижневі ризики тяжких ускладнень вагітності (138 917 жінок із ГЦД та 2 553 243 жінки без діабету). У жінок із ГЦД не було суттєвої різниці в гестаційній віковій смертності або захворюваності, що включала ≥1 подію в перинатальному періоді (акушерська емболія, акушерський шок, післяпологова кровотеча з гістеректомією або іншими процедурами для контролю кровотечі, сепсис, тромбоемболія чи розрив матки) між ятрогенними пологами та вичікувальною тактикою. Проте ятрогенні пологи асоціювалися з підвищеним ризиком неонатальної смертності та захворюваності (родова чи фетальна асфіксія, внутрішньошлуночкова кровотеча 3-4 ступеня, неонатальні судоми, інші порушення церебрального статусу новонароджених, респіраторний дистрес-синдром, родова травма, дистоція плечиків, мертвонародження або неонатальна смерть) на 36-37-му тижні вагітності, але нижчим ризиком неонатальної захворюваності та смертності на 38-40-му тижні вагітності порівняно з вичікувальною тактикою. Отже, пологи на 38-му, 39-му або 40-му тижні вагітності можуть забезпечити найкращі неонатальні результати в жінок із ГЦД.
Довгостроковий менеджмент жінок після ГЦД
За результатами післяпологового тестування, через 6-12 тижнів до третини жінок із ГЦД мають діабетичні або предіабетичні рівні глікемії.
Відповідно, тестування доцільно проводити вже через 6-12 тижнів після пологів методом ОГТТ або глікемії натще. Лише близько 25% жінок проходять тестування в цей період, загалом після пологів тестують 23-58% жінок.
У жінок із ГЦД та надмірною масою тіла чи ожирінням зменшення ІМТ між вагітностями ≥2,0 кг/м2 знижує ризик наступного ГЦД на 74%. У довгостроковій перспективі жінкам показана регулярна оцінка кардіометаболічного здоров’я й оптимізація способу життя для зменшення ризику діабету 2 типу та ССЗ. Серед жінок із ГЦД діабет 2 типу виникає в майже 74% з ожирінням і <25% жінок, які досягли нормальних показників ІМТ після пологів. У 50% жінок діабет 2 типу виникає впродовж 5-10 років після ГЦД. Програма профілактики діабету продемонструвала, що зміни способу життя й терапія метформіном покращують чутливість до інсуліну та зберігають функцію β-клітин у жінок із ГЦД. Отже, рання профілактика діабету 2 типу після ГЦД є важливим компонентом сучасної парадигми виявлення та лікування ГЦД.
Лікування ГЦД та віддалені наслідки для потомства
Важливо, що попри зниження ризику макросомії при народженні дослідження ACHOIS і MFMU не продемонстрували сприятливого впливу на дитяче ожиріння та толерантність глюкози у віці 5-10 років серед дітей, народжених жінками, які отримували лікування гіперглікемії. Інші проспективні когортні дослідження вказують на вищий ризик ожиріння, діабету 2 типу, метаболічного синдрому та ССЗ у ранньому дитинстві й підлітковому віці серед дітей народжених від жінок із ГЦД. Отже, поточний підхід до глікемічного контролю при ГЦД не обов’язково пом’якшує його вплив на довгострокове здоров’я немовлят. У таблиці 7 представлено практичні поради щодо ведення жінок із ГЦД.

Висновки
- ГЦД – одне з найчастіших медичних ускладнень вагітності, поширеність якого зростає в усьому світі.
- ГЦД асоціюється з акушерськими й неонатальними ускладненнями, здебільшого через збільшення маси тіла при народженні, та є основним чинником майбутнього ризику ЦД 2 типу, ожиріння та ССЗ у матері й дитини.
- Виявлення ГЦД вкрай важливе, оскільки лікування значно знижує перинатальні ускладнення та ризик мертвонародження.
- Точний медичний підхід до ГЦД із розпізнаванням тяжкості та початку материнської гіперглікемії, а також генетичних і фізіологічних підтипів може вирішити поточні діагностичні суперечливі моменти шляхом точної стратифікації ризику й індивідуальних стратегій лікування, що сприятиме покращенню моделей клінічної допомоги та наслідків.
- Традиційне фокусування на нормалізації акушерських і неонатальних результатів, досягнутих за допомогою короткотривалого антенатального контролю рівня глікемії матері, має змінитися стратегією ранньої постнатальної профілактики для зменшення трансформації ГЦД у діабет 2 типу та вирішення довгострокового метаболічного ризику матері й дитини, зважаючи на глобальну епідемію діабету, ожиріння та ССЗ.
Література
Sweeting A., Wong J., Murphy H.R., Ross G.P. A clinical update on gestational diabetes mellitus. Endocr. Rev. 2022 Sep 26; 43 (5): 763-793. https://doi.org/10.1210/endrev/bnac003.
