Крок перший – метформін, які кроки наступні? Глімепірид учора чи сьогодні?
Переклала й адаптувала канд. мед. наук Лариса Стрільчук
Відомо, що суворий глікемічний контроль зменшує кількість асоційованих із цукровим діабетом (ЦД) ускладнень і покращує якість життя пацієнтів. Відповідно до результатів британського дослідження UKPDS, кожне зниження рівня глікованого гемоглобіну (HbA1c) на 1% асоціюється зі зменшенням ризику опосередкованої діабетом захворюваності та смертності на 12-43% [52].
Прогресивна природа ЦД 2 типу з поступовим зменшенням кількості функціональних β-клітин із часом призводить до зменшення глюкозознижувальної ефективності пероральних глюкозознижувальних препаратів (ПГЗП) [40]. Доказова база свідчить, що раннє призначення комбінованої терапії як захід інтенсивного глікемічного контролю може бути ефективним методом збереження функції β-клітин, який дасть змогу швидко досягти глікемічних цілей і зменшити кількість і тяжкість діабетичних ускладнень [2, 14, 19, 26, 27, 44].
Раннє впровадження комбінованої терапії також зменшує кількість побічних ефектів, асоційованих із підвищенням дози препарату для монотерапії. І навпаки, відтермінування інтенсифікації лікування призводить до тривалих періодів гіперглікемії та зростання ризику макро- й мікроваскулярних ускладнень [17]. Покрокове додавання укрознижувальних препаратів до метформіну дає змогу не лише досягти та підтримувати цільовий рівень HbA1с, а й чітко побачити сприятливі та несприятливі ефекти доданих препаратів, водночас знижуючи витрати на лікування й кількість потенційних побічних явищ. У разі перевищення цільового показника HbA1c на 1,5-2,0% слід розглянути початок лікування з комбінованої терапії [21].
Не слід відтерміновувати інтенсифікацію лікування в пацієнтів, які не досягли цільових показників HbA1c. Вибір препарату для інтенсифікації має ґрунтуватися на клінічних характеристиках пацієнта та його вподобаннях. Вагомими клінічними характеристиками в цьому випадку є наявність атеросклеротичного серцево-судинного захворювання (АСССЗ) або ознак його високого ризику, серцева недостатність (СН), хронічна хвороба нирок (ХХН), ожиріння, неалкогольна жирова хвороба печінки, неалкогольний стеатогепатит, ризик розвитку певних побічних ефектів. Потрібно також зважати на безпечність, переносимість і вартість препарату. Результати порівняльних метааналізів свідчать, що кожен новий клас неінсулінових засобів, який додається до стартової терапії метформіном, знижує HbA1c приблизно на 0,7-1,0% [9, 37].
Наявні рекомендації щодо інтенсифікації лікування
Міжнародні та локальні фахові організації одностайно погоджуються, що препаратом першої лінії в лікуванні ЦД 2 типу є метформін, а оптимальним другим кроком – додавання іншого ПГЗП. Оскільки наявні рекомендації є досить гнучкими щодо вибору другого препарату після метформіну, питання оптимальної комбінації постає перед лікарем.
Рекомендації робочої групи Міжнародної федерації діабету (IDF) вказують, що в разі невдачі монотерапії метформіном варто додати до лікування інший ПГЗП, віддаючи перевагу препаратам сульфонілсечовини (ПСС), окрім глібенкламіду, інгібіторам α-глюкозидази чи дипептидилпептидази-4 (іДПП-4) [6, 29].
Консенсусний документ Американської асоціації діабету / Європейської асоціації з вивчення діабету (ADA/EASD, 2018, 2020) стверджує, що оптимальною стартовою терапією є метформін, а вибір другого препарату для комбінованої терапії ґрунтується на індивідуальних характеристиках пацієнта, причому якщо для пацієнта велике значення має вартість лікування, то рекомендовано додавати ПСС [13, 16].
Відповідно до рекомендацій Всесвітньої організації охорони здоров’я щодо інтенсифікації лікування ЦД 2 типу пацієнтам, які не досягли глікемічного контролю на тлі монотерапії метформіном або мають протипоказання до метформіну, доцільно призначити ПСС [47].
Отже, для більшості пацієнтів без АСССЗ, ХХН та/або СН ПСС останніх поколінь можуть вважатися найбільш економічно доцільними засобами навіть у найбільш економічно розвинених країнах. ПСС можуть застосовуватися в усьому спектрі можливостей лікування ЦД 2 типу, починаючи від ранніх стадій (як монотерапія на додачу до модифікації способу життя) та закінчуючи пізніми (як один із пероральних складників комплексної схеми лікування на основі базального інсуліну). Потенційні можливості застосування ПСС представлено на рисунку 1. Безперечно, вибір препарату має бути персоналізованим і залежати від клінічного профілю й уподобань пацієнта [51].
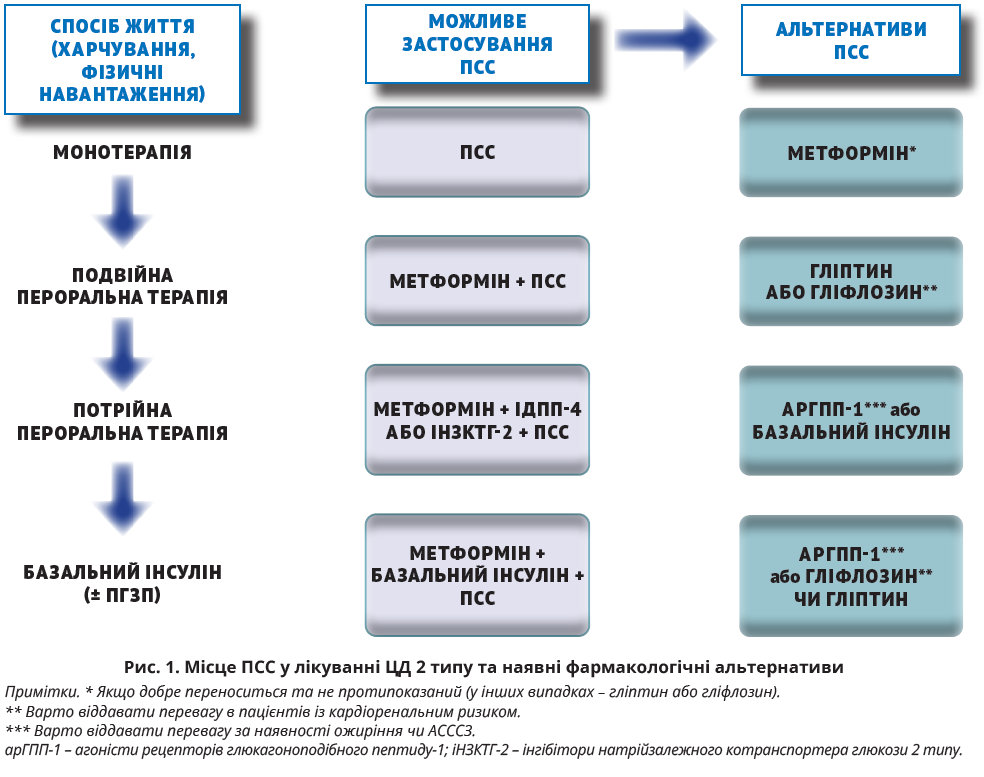
Особливості препаратів сульфонілсечовини
ПСС, які вийшли на фармацевтичний ринок наприкінці 1950-х рр., були першим класом ПГЗП у світі. Механізм дії ПСС полягає в стимуляції секреції інсуліну через закриття калієвих каналів β-клітин острівців Лангерганса, а вагомими перевагами цього класу є низька вартість і великий клінічний досвід застосування [24, 36].
Протягом тривалого часу ПСС були єдиною альтернативою метформіну або ідеальним його доповненням у разі невдачі монотерапії. Поява нових ПГЗП із низкою переваг змістило ПСС із цього п’єдесталу, проте їх дотепер продовжують активно призначати [51].
Хоча, на думку деяких авторів, ПСС значно поступаються новим протидіабетичним препаратам, інші науковці вважають, що ПСС дотепер є вагомим інструментом у терапевтичному арсеналі [1, 33, 54], особливо в країнах з обмеженими ресурсами [41].
Слід пам’ятати, що побічні ефекти ПСС не стосуються всього цього класу препаратів однаковою мірою. Сучасним ПСС (глімепірид, гліклазид) притаманний набагато кращий профіль безпеки, ніж старим поколінням цих засобів. Індивідуалізоване лікування, застосування ПСС у комбінації з іншими медикаментами, ретельний моніторинг і освіта пацієнтів дають можливість досягти максимальних переваг із мінімальними побічними ефектами [31, 32].
Консенсусні рекомендації міжнародної робочої групи щодо застосування ПСС та їхніх комбінацій
Міжнародна робоча група дає такі рекомендації щодо застосування ПСС [31]:
- Сучасні ПСС (глімепірид і гліклазид модифікованого вивільнення) є ефективними та безпечними препаратами другої лінії, які застосовують у пацієнтів, що не досягли попередньо визначених глікемічних цілей за допомогою монотерапії метформіном.
- Сучасні ПСС є ефективними й безпечними як стартова терапія в разі поєднання з модифікацією способу життя та застосуванням метформіну в пацієнтів із вихідним рівнем HbA1c ≥7,5%.
- ПСС можуть застосовуватися в комбінації з усіма класами ПГЗП, окрім глінідів.
- Якщо вони не були призначені раніше, сучасним ПСС можна віддавати перевагу як засобам третьої лінії для лікування ЦД 2 типу, що не вдається контролювати за допомогою подвійної терапії.
- Фіксовані комбінації, які містять ПСС, знижують вартість і поліпшують зручність лікування, підвищують прихильність пацієнтів до терапії.
Автори консенсусного документа також подають кілька тверджень стосовно ПСС у поєднанні з метформіном і порівняння цих засобів з іншими ПГЗП (табл.).
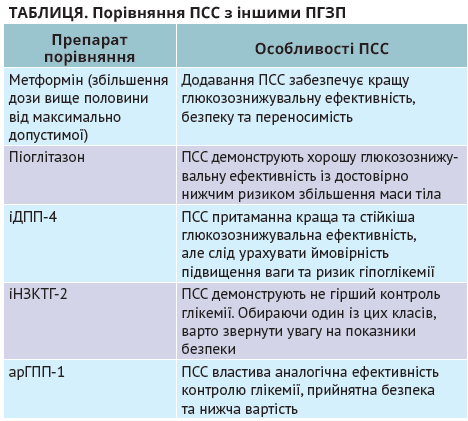
Сучасні ПСС можуть застосовуватися в осіб похилого віку, оскільки вони асоціюються з низьким ризиком гіпоглікемії. Також наразі недостатньо доказів того, що ПСС останніх поколінь підвищують кардіоваскулярний ризик.
Механізм дії ПСС і переваги їх поєднання з метформіном
Метформін діє завдяки інсуліносенсибілізувальним властивостям, тобто сприяє захопленню інсуліну периферичними тканинами, посилюючи утилізацію глюкози в жировій тканині та кишківнику. Отже, оскільки метформін чинить свою антигіперглікемічну дію, не впливаючи на секрецію інсуліну, в комбінованій терапії доцільним є поєднання метформіну з секретагогічним препаратом на кшталт ПСС [31].
Механізм дії ПСС полягає в стимуляції панкреатичних β-клітин до секреції інсуліну. Прикріплюючись до відповідних рецепторів на мембрані β-клітин, ПСС блокують калієві канали, що сприяє припливу іонів Ca2+ до клітини, а це, своєю чергою, забезпечує деполяризацію клітини з посиленням екзоцитозу інсуліну [30].
Важливо, що сучасним ПСС властиві також плейотропні ефекти: підвищення чутливості тканин до інсуліну, пригнічення секреції глюкагону острівцевими клітинами, стимуляція синтезу глікогену в печінці, антиоксидантний ефект, покращення стану судин [18, 30, 46]. Слід зауважити, що, враховуючи клітинноопосередкований, а не глюкозоопосередкований механізм дії, ПСС є найефективнішими на ранніх стадіях ЦД 2 типу, коли функціональна здатність β-клітин є найвищою [40, 50].
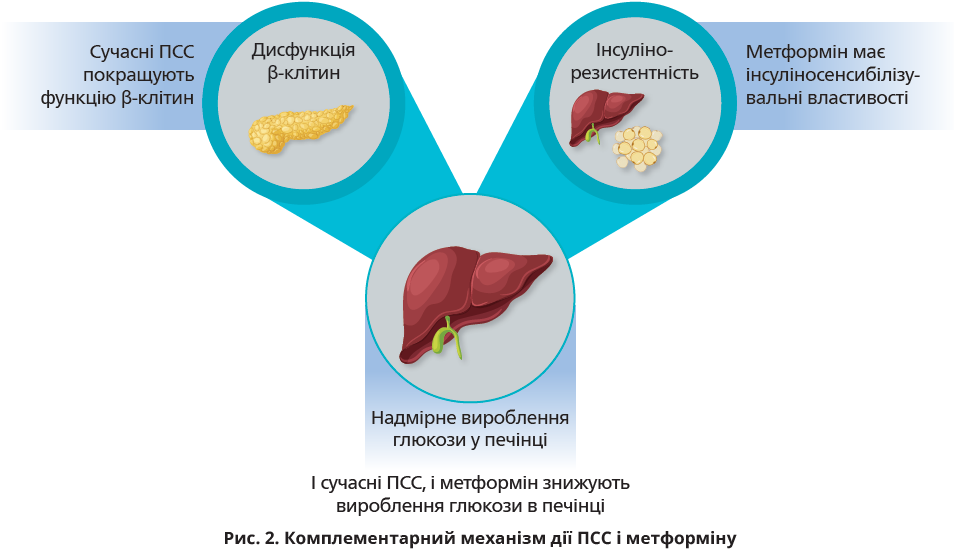
Комбінація двох препаратів із комплементарним механізмом дії здатна впливати на кілька етіологічних чинників гіперглікемії в осіб із ЦД 2 типу (рис. 2) [30]. Серед усіх ПГЗП, які можна додавати до метформіну, сучасні ПСС можна вважати ідеальним варіантом у зв’язку з високою ефективністю, відносною кардіоваскулярною безпекою й низькою вартістю. Потенційні ризики гіпоглікемії та збільшення маси тіла можна мінімізувати шляхом застосування сучасних ПСС – глімепіриду та гліклазиду модифікованого вивільнення [31].
Безпека ПСС
Найпоширенішим занепокоєнням у разі застосування ПСС є ризик гіпоглікемій, але гіпоглікемічний потенціал цих засобів є різним і залежить від фармакокінетичних і фармакодинамічних особливостей кожного окремого препарату. Доказова база свідчить, що сучасні ПСС асоціюються з меншим ризиком гіпоглікемії порівняно зі старшими поколіннями засобів цього класу [5, 8, 15, 20].
Обговорюється також набір ваги, асоційований із ПСС. Аналогічно ситуації з гіпоглікеміями, все залежить від препарату: сучасним ПСС (глімепірид, гліклазид модифікованого вивільнення) притаманна відсутність впливу на масу тіла або навіть здатність її знижувати [30]. Наявні докази свідчать, що глімепірид найменше серед усіх ПСС спричиняє набір ваги. Крім того, варто зауважити, що збільшення маси тіла, пов’язане із застосуванням ПСС, може бути наслідком покращеної утилізації спожитої глюкози з відповідним зниженням глюкозурії та зменшенням загального глюкотоксичного впливу на організм [23, 38].
Старим ПСС був притаманний певний несприятливий вплив на серце та судини, але нещодавнє дослідження CAROLINA не виявило відмінностей у поширеності значущих несприятливих кардіоваскулярних подій між групами глімепіриду (ПСС останнього покоління) та лінагліптину, для котрого було доведено серцево-судинну безпеку порівняно з плацебо [48]. Метааналіз D.V. Rados і співавт. (2018) також показав, що ПСС не асоціювалися з підвищенням смертності від усіх причин і кардіоваскулярної смертності. Під час аналізу окремих препаратів з’ясувалося, що ризик підвищення смертності був найменшим для глімепіриду [45]. Імовірно, така відмінність між старими та новими ПСС зумовлена більшою панкреатоселективністю останніх [31].
Інший метааналіз 301 клінічного дослідження з вивчення таких ПГЗП, як метформін, ПСС, іДПП-4, інгібітори α-глюкозидази, іНЗКТГ-2, арГПП-1, меглітиніди й інсулін у вигляді монотерапії чи в комбінації, не виявив жодних значущих відмінностей у показниках смертності на тлі прийому будь-яких із цих препаратів [43].
Низка досліджень продемонструвала, що глімепірид не має несприятливого впливу на функцію серця та майже не впливає на його електричну активність [7, 42]. Глімепіриду також притаманна нижча частота виникнення гіпоглікемій і зростання ваги порівняно зі старішими ПСС у зв’язку з нижчою у 2-3 рази зв’язувальною афінністю та швидкими процесами асоціації/дисоціації з білками рецепторів до ПСС [12, 28, 35]. Дослідження Veterans Affairs Diabetes Trial виявило, що режим інтенсивної терапії ЦД 2 типу на основі глімепіриду асоціювався зі зниженням відносного ризику кардіоваскулярних подій на 17% [26].
Комбінація метформін/ПСС у клінічних дослідженнях:акцент на глімепірид
Крос-секційне дослідження виявило, що поєднання метформін/ПСС забезпечує зниження HbA1c, аналогічне поєднанню метформін/інсулін (на 1,04±0,96 та 1,02±1,03% відповідно). Пацієнти, які отримували метформін і ПСС, у 4,3 раза частіше досягали цільового показника HbA1c, ніж учасники групи метформіну й інсуліну. Крім того, в групі додавання інсуліну спостерігався вищий сумарний ризик кардіоваскулярних подій (40,5 проти 34,0%) [22].
У рандомізованому відкритому багатоцентровому дослідженні H. Kim і співавт. (2014) узяли участь 209 пацієнтів із ЦД 2 типу з HbA1c 7,0-10,0%, які приймали метформін у дозі 500-1000 мг/добу. Для інтенсифікації лікування цих пацієнтів переводили на фіксовану комбінацію (ФК) глімепірид/метформін або збільшували дозу метформіну. Через 24 тижні ФК глімепірид/метформін забезпечувала достовірно вираженіше зниження HbA1c порівняно зі збільшенням дози метформіну (на 1,2 проти 0,8%, р<0,0001) і глюкози плазми крові натще (на 35,7 проти 18,6 мг/дл, р<0,0001). Наприкінці дослідження цільового рівня HbA1c (<7%) досягла достовірна більша частка пацієнтів групи ФК: 74,7 проти 46,6% у групі монотерапії метформіном у високій дозі. У групі ФК спостерігалася більша частота гіпоглікемій, але жодного випадку тяжкої гіпоглікемії зафіксовано не було [34].
Метааналіз 15 рандомізованих контрольованих досліджень показав, що в усіх включених дослідженнях глюкозознижувальна ефективність комбінації метформіну та ПСС була вищою за показник монотерапії метформіном [11]. Плацебо-контрольоване дослідження B. Ahren і співавт. (2014), яке тривало 104 тижні, зіставило лікування метформіном (>1500 мг/добу) із застосуванням комбінації метформіну (≥1500 мг/добу) та глімепіриду (до 4 мг/добу), виявивши міжгрупову різницю в HbA1c на 0,63% на користь групи комбінації [3].
У пацієнтів із неконтрольованою глікемією на тлі метформіну додавання глімепіриду забезпечує швидше зниження HbA1c при оцінці на 6-й, 12-й і 20-й тиждень лікування порівняно з піоглітазоном. Цільового показника HbA1c ≤7% учасники групи глімепіриду досягали за 80-90 днів, а учасники групи піоглітазону – за 140-150 днів [53].
Відповідно до результатів систематичного огляду й метааналізу глімепірид асоціювався з більшим на 12% зниженням HbA1c порівняно з іДПП-4 [4].
Фармакоекономічна доцільність застосування ПСС
Вартість терапії відіграє важливу роль у веденні будь-яких хвороб, оскільки впливає на використання призначених препаратів і прихильність пацієнтів до лікування. Особи, які не мають медичного страхування, та соціально незахищені категорії людей не мають можливості застосовувати дороговартісні засоби для лікування ЦД 2 типу [31].
Показано, що ПСС асоціюються з достовірно меншими витратами на рік життя з поправкою на його якість і з найдовшим серед ПГЗП часом до досягнення інсулінозалежності [55].
Оскільки прихильність до лікування безпосередньо пов’язана з вартістю й доступністю препаратів, режимом їх застосування та кількістю й тяжкістю пов’язаних із лікуванням ускладнень [10, 39, 49], ФК дають змогу підвищити прихильність, зменшуючи частоту вживання препарату та витрати на лікування [31].
Висновки
Проактивний підхід до інтенсифікації лікування діабету – ключова засада досягнення глікемічних цілей. ПСС є важливим компонентом фармакологічного арсеналу лікаря при веденні хворих на ЦД 2 типу та протягом кількох декад виступають золотим стандартом препаратів другої лінії [25].
У зв’язку з добре вивченим профілем ефективності та безпеки ПСС доцільно додавати до метформіну в разі недостатнього результату монотерапії. Враховуючи відмінності у фармакокінетиці та фармакодинаміці різних ПСС, слід бути обережними у виборі препарату, особливо в пацієнтів високого ризику, та віддавати перевагу сучасним ПСС.
Висока глюкозознижувальна ефективність і хороша переносимість на тлі низької вартості лікування й відмінних показників прихильності забезпечують ПСС провідні позиції в комплексній терапії ЦД 2 типу, а комплементарний метформіну механізм дії надає комбінації метформін + ПСС додаткового впливу на глікемію завдяки подоланню й інсулінодефіциту, й інсулінорезистентності [31, 34].
* Повний список джерел – у редакції.
