Рекомендації щодо амбулаторного контролю глікемії у хворих на рак
Переклала й адаптувала Олена Зотова
Пацієнти із цукровим діабетом (ЦД) мають вищий ризик розвитку кількох видів раку, ймовірно, через наявність деяких спільних для цих захворювань чинників ризику [1]. Згідно з оцінками, приблизно 20% пацієнтів зі злоякісними новоутвореннями одночасно мають ЦД 2 типу; при цьому рак на сьогодні є однією з провідних причин смертності в популяції осіб із ЦД [3]. Для пацієнтів зі злоякісними новоутвореннями характерний підвищений ризик дебюту ЦД або гіперглікемії, а також погіршення контролю глікемії при вже наявному ЦД [4].
Узагальнений огляд даних метааналізів обсерваційних досліджень засвідчив підвищений ризик розвитку раку в пацієнтів із ЦД порівняно з особами без діабету [5]. Було продемонстровано, що отримані докази є найпоказовішими для раку молочної залози, внутрішньопечінкової холангіокарциноми, колоректального раку та раку ендометрія. З’являються також дані про те, що гіперглікемія може бути пов’язана з гіршою загальною виживаністю та підвищеним ризиком рецидиву онкологічного захворювання при низці підтипів раку, включаючи як солідні злоякісні новоутворення, так і гемобластози [4, 6-15]. Один із найбільших оглядів 12 ретроспективних досліджень, у яких узяли участь 9872 пацієнти з раком і без відомого діабету, виявив, що особи з гіперглікемією мали значно гіршу безрецидивну виживаність (відношення ризику [ВР] 1,98; 95% довірчий інтервал [ДІ] 1,20-3,27) порівняно з особами з нормоглікемією, а також гіршу загальну виживаність (ВР 2,05; 95% ДІ 1,67-2,551) [16]. Окрім того, на підставі даних низки доклінічних досліджень було висловлено припущення про те, що гіперглікемія може специфічно знижувати ефективність хіміотерапії в пацієнтів із раком (із діабетом або без нього) [17]; можливо, це частково пояснює гірші результати. Проте на сьогодні не було проведено рандомізованих контрольованих досліджень, які підтверджували би припущення про те, що кращий контроль глікемії може поліпшувати результати лікування раку.
Відомо, що деякі протипухлинні засоби збільшують ризик розвитку гіперглікемії навіть у осіб без діагностованого ЦД (табл. 1).
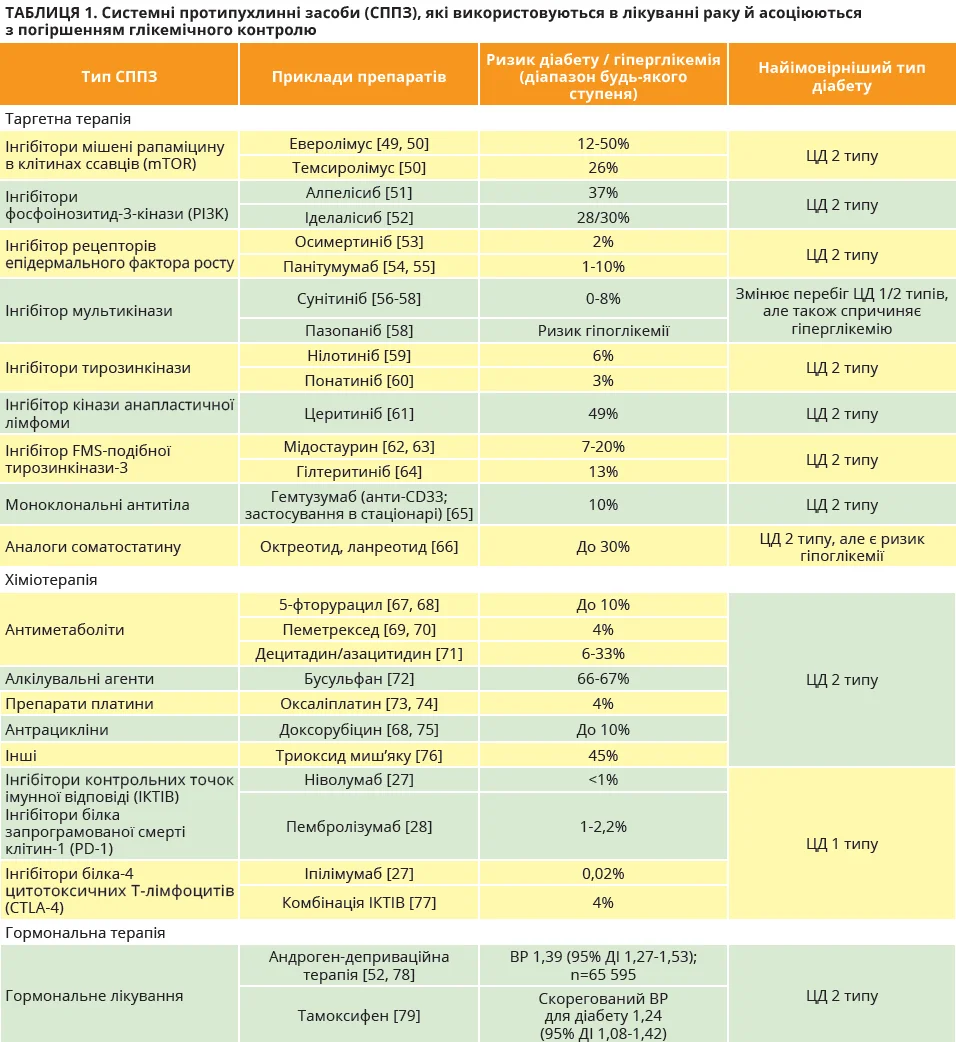
Під час хіміотерапії приблизно в 10-30% хворих на рак може виникати гіперглікемія [18-20].
Низка обсерваційних досліджень показала, що незадовільний глікемічний контроль може збільшити ризик інфекцій і госпіталізації, особливо в осіб із метастатичним або прогресивним раком, які отримують хіміотерапію [21, 22]. Це, своєю чергою, може призвести до перерв у лікуванні та зменшення доз протипухлинних препаратів, а також до значного збільшення показників захворюваності та навіть зростання смертності [23]. Огляд усіх випадків госпіталізацій у спеціалізованій онкологічній лікарні в Лондоні показав, що 11% стаціонарних пацієнтів мали ЦД або гіперглікемію [24], а в осіб із гіперглікемією частота невідкладних госпіталізацій під час проведення протипухлинної терапії була вищою, ніж у пацієнтів без неї [25]. Для цих осіб раннє втручання, спрямоване на покращення глікемічного контролю, найімовірніше, буде корисним [26].
КТІВ, як-от інгібітори CTLA-4 та PD-1, можуть індукувати розвиток діабету de novo, хоча це відбувається з низькою частотою (<1%) [27].
Встановлено, що застосування інгібіторів PD-1, інгібіторів PD-L1 та комбінованої терапії інгібіторами CTLA-4/PD-1 прискорює розвиток діабету частіше, ніж монотерапія інгібіторами CTLA-4. Дефіцит інсуліну, індукований застосуванням ІКТІВ, може проявлятися у вигляді як дебюту інсулінозалежного діабету, так і погіршення перебігу вже наявного ЦД 2 типу; проте механізм, що лежить в основі цього явища, вважається подібним до механізму розвитку ЦД 1 типу [28].
Застосування глюкокортикоїдів (ГК) у високих дозах є поширеною практикою при раку на пізніх стадіях. ГК є основою багатьох схем лікування гемобластозів і часто використовуються для контролю симптомів під час надання паліативної допомоги [29]. Вони часто використовуються разом із системним лікуванням із метою зменшення нудоти та блювання, є основними засобами лікування проявів токсичності імунотерапії (табл. 2).

ГК чинять прямий гіперглікемічний ефект, який розвивається дуже швидко після прийому [29, 30].
Зазвичай вони спричиняють підвищення рівнів глюкози в крові через 4-8 годин після перорального прийому, що призводить до досягнення максимального рівня глікемії між обідом і вечерею [30, 31].
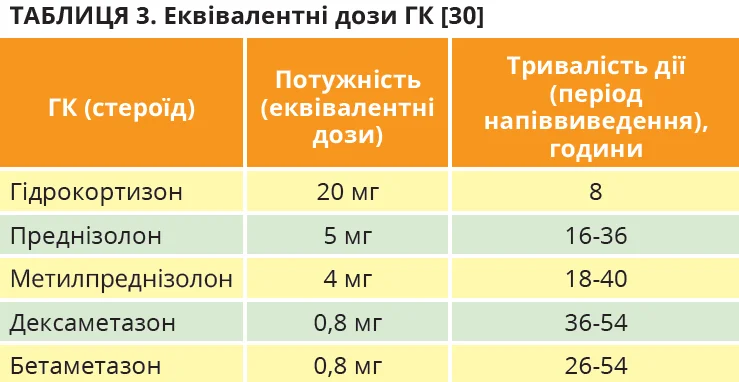
ГК-індукований діабет розвивається в 1 людини з 10, які раніше не страждали на ЦД [32]; при цьому діабетогенний ефект ГК залежить від дози [33]. Супрафізіологічні дози ГК наближаються до дози преднізолону понад 5 мг на добу або еквівалентної дози альтернативного синтетичного ГК (табл. 3). Після скасування ГК індукована ними гіперглікемія може зникнути чи зберегтися.
Для кращого розуміння важливості контролю глікемії в людей, хворих на рак, потрібні додаткові докази високого рівня, проте цілком зрозуміло, що ці пацієнти потребують активного виявлення гіперглікемії та ЦД і потенційно складнішого лікування діабету [24]. Настанов щодо ведення таких пацієнтів дуже мало.
Тому нещодавно міждисциплінарною робочою групою експертів від імені Ради з хіміо-терапії Великої Британії (UKCB) та Об’єднаного британського діабетичного товариства зі стаціонарного лікування (JBDS), до складу якої увійшли представники медичних, діабетичних, фармацевтичних і дієтологічних груп Об’єднаного Королівства Великої Британії та Північної Ірландії, було розроблено мультидисциплінарні рекомендації та запропоновано принципи ведення пацієнтів із раком і ЦД.
В Об’єднаному Королівстві UKCB є провідним органом, який забезпечує керівництво, нагляд і підтримку для постійного розвитку хіміотерапії (системної протипухлинної терапії). Групу JBDS було створено 2008 року для «надання набору рекомендацій щодо стаціонарного лікування діабету та пропонування стандартів медичної допомоги в організаціях вторинної медичної допомоги» із загальною метою покращення стаціонарного лікування ЦД шляхом розроблення та використання високоякісних, заснованих на фактичних даних настанов.
Ці рекомендації призначені для амбулаторного ведення пацієнтів з онкологічними захворюваннями (зокрема, в умовах онкологічної/онкогематологічної клініки), а також для надання консультацій пацієнтам удома, але за потреби вони можуть застосовуватися також для стаціонарних пацієнтів.
РЕКОМЕНДАЦІЇ
Перед початком протипухлинної терапії в усіх хворих на рак потрібно перевірити вихідний рівень HbA1c і рівень глюкози в плазмі крові в умовах амбулаторної клініки.
Пацієнти мають бути забезпечені глюкометром для вимірювання рівня глюкози в капілярній крові й тест-смужками для визначення рівня глюкози, якщо вони мають високий ризик ГК-індукованого діабету (табл. 4) або початковий рівень глюкози в плазмі крові становить ≥12 ммоль/л.

Ті пацієнти, в яких виявлено підвищений вихідний рівень HbA1c (>6,5%), мають бути направлені до закладів первинної медичної допомоги для призначення відповідного лікування; проте не слід відкладати початок системної протипухлинної терапії, особливо якщо це клінічно терміново.
На початку застосування СППЗ/ГК пацієнти мають бути проінформовані про ризик розвитку гіперглікемії/діабету та можливі очікувані симптоми (поліурію, ніктурію, втомлюваність, спрагу, затуманення зору, головний біль, сплутаність свідомості, зниження маси тіла).
Пацієнти без попереднього діагнозу ЦД
Початок терапії ГК/СППЗ (без застосування ІКТІВ) (алгоритм 1)
Алгоритм 1 описує схему лікування пацієнтів із раком, які починають терапію СППЗ або ГК та не мають попередньо діагностованого ЦД.
- Під час кожного амбулаторного візиту слід перевіряти рівень глюкози в плазмі крові. Якщо результати визначення рівня глюкози в плазмі або капілярній крові стабільно становлять <10 ммоль/л, розгляньте питання про припинення тестування (доти, доки не буде розпочата нова протипухлинна терапія / здійснені зміни в терапії або не буде призначено лікування ІКТІВ).
- Якщо рівень глюкози в плазмі крові становить ≥12 ммоль/л у двох випадках вимірювання в амбулаторних умовах, варто провести скринінг на симптоми гіперглікемії (наприклад, спраги й поліурії) та перевірити наявність кетонурії/кетонів у крові, щоб виключити кетоацидоз.
- Слід розпочати прийом гліклазиду в дозі 40 мг уранці та використовувати глюкометр і тест-смужки для визначення рівня глюкози (якщо можливо) та/або негайно звернутися до лікаря первинної медичної допомоги, щоб обговорити початок лікування. Потрібно проконсультувати пацієнта щодо симптомів і лікування потенційної гіпоглікемії, спричиненої гліклазидом [34].
- Оригінальна настанова JBDS щодо стероїдів була написана з використанням преднізолону 1 раз на добу як основного стероїду [30]. Саме вплив преднізолону на глюкозу зумовив застосування гліклазиду. Проте разом з іншими ГК тривалої дії, що застосовуються в пацієнтів із раком, наприклад із дексаметазоном, гліклазид не може бути обраний як препарат сульфонілсечовини вибору.
- Слід уникати застосування гліклазиду в пацієнтів із тяжкою печінковою або нирковою недостатністю (розрахункова швидкість клубочкової фільтрації <30 мл/хв/1,73 м2). У таких ситуаціях лікуванням вибору майже завжди буде інсулінотерапія, тому щодо її початку варто звернутися за порадою до фахівців у галузі діабетології.
- Може знадобитися збільшити дозу гліклазиду на 40 мг на добу, якщо рандомно визначений рівень глюкози в плазмі залишається на рівні ≥12 ммоль/л або цільові показники глікемії не досягнуті. Пацієнти, які приймають високі дози ГК (тобто преднізолон у дозі ≥20 мг на добу або еквівалент), можуть потребувати більшого поступового підвищення дози. Гліклазид можна титрувати до максимальної дози 240 мг уранці, а також можна розпочати прийом вечірньої дози гліклазиду для досягнення максимальної добової дози 320 мг (але на цьому етапі слід отримати пораду спеціаліста щодо титрування дози!). У настанові JBDS містяться спеціальні вказівки щодо лікування гіперглікемії та терапії ГК, а також докладна інформація про подальше підвищення дози гліклазиду або додавання інсуліну, якщо рівень глюкози крові залишається високим [35].
- Якщо рівень глюкози в плазмі крові підніметься вище 20 ммоль/л або в пацієнта виникне блювання, біль у животі чи відзначатиметься ступор, слід виключити кетоацидоз / гіперосмолярний гіперглікемічний стан (ГГС), які потребують негайного невідкладного лікування [36, 37]. Якщо кетоацидоз/ГГС було виключено, скеруйте пацієнта до фахівця в галузі діабетології для подальшого лікування.
Початок застосування ІКТІВ (алгоритм 2)
Алгоритм 2 описує схему лікування пацієнтів з онкологічним захворюванням, які не мають попередньо діагностованого ЦД та розпочинають терапію ІКТІВ. Було продемонстровано, що в приблизно 75% осіб, у яких розвинулися гіперглікемія/діабет, індуковані застосуванням ІКТІВ, також виникає кетоацидоз [38-40] і відзначається тенденція до різкого та значного підвищення рівня глюкози в крові [41]. Близько третини осіб, які отримують ІКТІВ, можуть паралельно отримувати й високі дози стероїдів із приводу неендокринних імуноопосередкованих побічних реакцій, і вони також перебувають у групі ризику розвитку гіперглікемії, індукованої стероїдами. Порівняно з «класичним» ЦД 1 типу діабет, індукований ІКТІВ, має тенденцію до швидшого початку, блискавичного перебігу та високої частоти негативного результату аналізу на наявність антитіл [41].
- Перед початком лікування ІКТІВ пацієнти мають бути проінформовані про рідкісний, але потенційно серйозний ризик розвитку ЦД. Потрібно докладно пояснити пацієнтам, якими можуть бути ознаки й симптоми гіперглікемії, та порадити їм негайно звернутися до лікаря, щоб уникнути потенційно загрозливих для життя ситуацій [41].
- Рівень глюкози крові слід перевіряти при проведенні кожного циклу лікування та/або за появи симптомів гіперглікемії під час терапії ІКТІВ.
- Якщо рівень глюкози в плазмі крові становить ≥20 ммоль/л або пацієнт має підозрілі симптоми, виключіть кетоацидоз/ГГС [36, 37]. Тоді як більшість випадків кетоацидозу виникає при тяжкій гіперглікемії, приблизно в 1 з 20 випадків він розвивається при концентрації глюкози в крові <13 ммоль/л. Якщо хворий має інші симптоми, як-от запах ацетону у видихуваному повітрі, глибоке дихання (дихання Куссмауля), варто запідозрити кетоацидоз, незалежно від рівня глюкози крові.
- Слід виконати аналіз на антитіла до острівцевого апарату підшлункової залози (наприклад, до глутаматдекарбоксилази-65 (GAD65), транспортера цинку-8 або антитіла до острівцевих клітин) [42].
- У разі розвитку ІКТІВ-індукованого діабету майже завжди потрібно починати інсулінотерапію, а отже, необхідне термінове направлення пацієнта до спеціаліста з діабетології. Зважаючи на ризик різкої гіперглікемії, потрібне термінове лікування. При діагностуванні кетоацидозу або ГГС необхідна термінова госпіталізація.
- Не було продемонстровано, що високі дози ГК здатні зумовлювати зворотній розвиток індукованої ІКТІВ панкреатичної токсичності та діабету на відміну від інших токсичних ефектів, пов’язаних із застосуванням цих протипухлинних препаратів. Також існує ймовірність того, що будь-які високі дози ГК тільки посилять гіперглікемію, тому в цьому випадку їх слід застосовувати з обережністю, якщо взагалі варто це робити [27, 42].
- Відмовтеся від терапії ІКТІВ, якщо є докази виникнення невідкладної ситуації, пов’язаної зі спричиненим цими препаратами діабетом. Розгляньте можливість відновлення терапії ІКТІВ після того, як було розпочато лікування гіперглікемії [42]. У тих осіб, які отримують подвійні режими лікування із застосуванням ІКТІВ і хіміотерапії, алгоритм лікування ІКТІВ-індукованої гіперглікемії (алгоритм 2) повинен мати пріоритет над алгоритмом лікування гіперглікемії, спричиненої СППЗ (алгоритм 1).
Особи з уже наявним ЦД
Вважається, що близько 20% усіх хворих на рак уже мають ЦД [2, 24]. Проходження протипухлинного лікування може бути вкрай серйозним стресом для цих людей; однак важливо, щоб вони отримували адекватну підтримку медичних працівників для здійснення належного лікування наявного в них ЦД.
Перед початком терапії СППЗ/ГК
- Документально зафіксуйте тип діабету, наявність будь-яких попередніх його ускладнень, а також рівень обізнаності про гіпоглікемію.
- У всіх пацієнтів із ЦД слід перевіряти вихідний рівень глюкози в плазмі крові, а також HbA1c у тих осіб, у яких цей показник не перевіряли протягом 3 місяців.
- Якщо рівень глюкози в плазмі крові становить ≥20 ммоль/л, виключіть кетоацидоз або ГГС [36, 37]. Хоча більшість випадків кетоацидозу виникає при тяжкій гіперглікемії, приблизно в 1 з 20 випадків він розвивається при концентрації глюкози в крові <13 ммоль/л. Якщо пацієнт має інші симптоми, як-от запах ацетону у видихуваному повітрі, глибоке дихання (дихання Куссмауля), слід запідозрити кетоацидоз, незалежно від рівня глюкози крові.
- Під час консультування перед хіміотерапією медичний працівник має переконатися, що пацієнт із ЦД перебуває в контакті зі своїм лікарем (зазвичай у рамках первинної ланки медичної допомоги), якого слід поінформувати про те, що розпочато системне протипухлинне лікування. У разі погіршення контролю глікемії лікар має надати термінову консультацію або направити пацієнта до спеціалістів у галузі діабетології.
- Осіб зі вже наявним ЦД слід повідомити про ймовірне збільшення вираженості гіперглікемії під час проведення терапії, до складу якої входять ГК. Пацієнтам із ЦД варто порадити ретельний самоконтроль глікемії та підтримання зв’язку зі своїм лікарем, який здійснює ведення з приводу ЦД.
Для пацієнтів із ЦД 2 типу, які не отримують інсулінотерапію (алгоритм 3)
Алгоритм 3 описує схему лікування пацієнтів із раком і ЦД 2 типу, які отримують пероральні цукрознижувальні препарати та починають терапію СППЗ або ГК.
■ Якщо рівень глюкози в плазмі крові становить ≥12 ммоль/л у двох випадках вимірювання, спочатку перевірте наявність симптомів гіперглікемії (поліурія, ніктурія, втома, спрага, розмитість зору, головні болі, сплутаність свідомості, зниження маси тіла) та наявність кетонурії/кетонів у крові, щоб виключити кетоацидоз.
■ Якщо пацієнт уже приймає такі препарати сульфонілсечовини, як гліклазид або меглітиніди (стимулятори секреції інсуліну), збільште ранкову дозу гліклазиду до максимальної (240 мг); можна розпочати прийом вечірньої дози гліклазиду для досягнення максимальної добової дози 320 мг. Титрування дози метформіну також може бути доцільним. Пацієнтам, які не використовують інсулін для лікування ЦД, може знадобитися перехід на інсулінотерапію, особливо тим, хто вже приймає більш ніж один цукрознижувальний препарат (включаючи похідні сульфонілсечовини) або отримує ГК.
■ Переконайтеся, що пацієнт не має симптомів гіпоглікемії ані вдень, ані вночі. Якщо пацієнт уже приймає максимальну дозу цукрознижувального препарату або рівень глюкози в плазмі залишається ≥12 ммоль/л, незважаючи на збільшення дози, зверніться до лікаря, який здійснює ведення діабету.
■ Якщо пацієнт дотримується лише дієтичного режиму або приймає інші препарати, що не є похідними сульфонілсечовини (наприклад, метформін, інгібітори дипептидилпептидази-4, піоглітазон, інгібітори натрійзалежного котранспортера глюкози-2), розпочніть прийом гліклазиду в дозі 40 мг щодня вранці та скеруйте пацієнта до лікаря, що спеціалізується на веденні діабету. Розгляньте можливість збільшення дози на 40 мг під час візитів до лікаря, якщо рівень глюкози в крові постійно перевищує цільовий діапазон 6-12 ммоль/л. Хворим, які приймають високі дози ГК, може знадобитися більш значне поступове збільшення дози: гліклазид можна титрувати до максимальної дози 240 мг уранці, а також можна розпочати прийом вечірньої дози гліклазиду для досягнення максимальної добової дози 320 мг. Із приводу титрування дози в тих пацієнтів, які вже приймають препарат у дозі 160 мг без покращення глікемічного контролю, доцільно звернутися за порадою до спеціаліста в галузі діабетології.
■ Відомо, що низка протипухлинних препаратів спричиняють нефротоксичність і гепатотоксичність й обидва ці ускладнення можуть потребувати корегування режиму лікування ЦД. Ці випадки можуть потребувати спеціального втручання діабетологів.
■ В осіб, які отримують ІКТІВ і мають ЦД 2 типу в анамнезі, раптова зміна рівнів глюкози крові або клінічних симптомів може свідчити про дисфункцію підшлункової залози, спричинену імунотерапією, і в цих пацієнтів потрібно розпочати лікування інсуліном.
Для пацієнтів, які отримують інсулінотерапію (алгоритм 4)
Алгоритм 4 описує режим лікування пацієнтів із раком і ЦД, які вже лікуються інсуліном і починають терапію СППЗ або ГК.
- Як зазначено вище, якщо рівень глюкози в плазмі крові становить ≥12 ммоль/л у двох випадках вимірювання, спочатку слід перевірити наявність симптомів гіперглікемії та кетонурії/кетонів у крові, щоб виключити кетоацидоз.
- В усіх випадках варто зв’язатися з фахівцями в галузі ведення діабету для консультації щодо титрації доз інсуліну. Якщо можливості зв’язатися з такими фахівцями немає, титруйте інсулін на 10-20% від початкової дози щодня; проте може знадобитися збільшення дози інсуліну до 40%, особливо в разі прийому перших доз високодозових ГК для підтримки еуглікемії [43] (див. рекомендації JBDS щодо лікування гіперглікемії та застосування ГК) [35]. Алгоритм 4 надає додаткові відомості щодо титрування доз інсуліну відповідно до типу інсуліну, який отримує пацієнт.
- Пацієнти із ЦД 1 типу мають особливо високий ризик неконтрольованої гіперглікемії, тому тісний зв’язок із фахівцем у галузі ведення діабету є для них дуже важливим.
- Пацієнти мають знати про «правила лікарняного дня» під час уведення інсуліну (включаючи визначення рівня глюкози в капілярній кров й наявності кетонів у крові що 4-6 годин, продовження режиму інсулінотерапії в разі поганого самопочуття / зменшеного споживання їжі) та на початку терапії можуть потребувати відповідних нагадувань (листівки з правилами) [44]. Пацієнтів із ЦД 1 типу слід заохочувати якомога раніше звертатися по консультацію та лікування, якщо вони погано почуваються через гіперглікемію ± наявність кетонів.
- Для пацієнтів із ЦД 1 типу, які не приймають їжу або перебувають у стані кахексії, важливо не пропускати введення базального інсуліну, щоб уникнути кетоацидозу.
ЦІЛЬОВІ ПОКАЗНИКИ ГЛІКЕМІЇ
Рекомендований цільовий рівень глікемії становить 6,0-10,0 ммоль/л, допустимий діапазон – 6,0-12,0 ммоль/л. Однак пацієнти з раком у термінальній стадії, яким надається медична допомога вже наприкінці їхнього життя, не потребують такого суворого контролю глікемії [46]: цільові рівні мають становити не нижче 6,0 ммоль/л і не вище 15 ммоль/л [35].
МОНІТОРИНГ РІВНІВ ГЛЮКОЗИ КРОВІ
Під час лікування ГК або лікування осіб із високим ризиком гіперглікемії (табл. 4) моніторинг рівня глюкози в капілярній крові потрібно проводити принаймні 1 раз на день [35].
Визначення рівнів глюкози в капілярній крові варто продовжувати щодня на терапії ГК/СППЗ або після збільшення дози цих препаратів. Показники глікемії слід оцінювати й після припинення лікування, поки вони залишаються вищими за 12 ммоль/л. Якщо рівні глікемії в капілярній крові постійно нижчі за 10 ммоль/л і застосування СППЗ/ГК було припинено, то оцінку глікемії можна припинити (якщо пацієнт не отримує ІКТІВ). У міру того, як дози стероїдів або СППЗ зменшуються чи прийом цих препаратів припиняється, лікування гіперглікемії так само потрібно буде титрувати в бік зниження доз. Наприклад, щотижневе зниження дози преднізолону на 5 мг (із 20 мг) може потребувати зниження дози інсуліну на 20-25% або зниження дози гліклазиду на 40 мг.
РИЗИК ГІПОГЛІКЕМІЇ
Утруднене споживання їжі та нудота/блювання внаслідок основного онкологічного захворювання або лікування піддають пацієнтів ризику гіпоглікемії. Симптоми гіпоглікемії включають пітливість, утомлюваність, запаморочення, відчуття голоду, серцебиття, зміни настрою, блідість шкірних покривів і сплутаність свідомості. Пацієнти, в яких на тлі застосування ІКТІВ уперше виник дефіцит інсуліну, часто мають лабільний контроль глікемії; тому їх варто проконсультувати щодо ризиків і симптомів гіпоглікемії [41]. Задля уникнення гіпоглікемії може знадобитися дотримання «м’якших» цільових рівнів глікемії. ІКТІВ також можуть спричиняти гіпопітуїтаризм, що призводить до вторинної надниркової недостатності. Це може зумовити гіпоглікемію (разом із будь-яким із таких проявів, як гіпонатріємія, гіперкаліємія та гіпотензія). Адреналіт, що призводить до первинної надниркової недостатності, трапляється дуже рідко. Прояви надниркової недостатності варіюють від безсимптомних змін лабораторних показників до гострого погіршення самопочуття, при цьому лікування залежить від ступеня тяжкості порушень.
До лікування слід залучити ендокринологів. Онкологи мають знати й про інші причини недостатності надниркових залоз або гіпофіза, що призводять до гіпоглікемії, включаючи метастази в цих зонах, хірургічне втручання, опромінення, застосування протигрибкових препаратів класу азолів і неналежне раптове припинення лікування ГК.
Особи, які приймають гліклазид, також мають отримати консультації щодо симптомів і лікування потенційної гіпоглікемії, спричиненої застосуванням цього препарату.
ВЕДЕННЯ ДІАБЕТУ В ТЕРМІНАЛЬНІЙ СТАДІЇ ОНКОЛОГІЧНОГО ЗАХВОРЮВАННЯ
Глікемічні цілі в осіб, які отримують лікування в термінальній стадії онкологічного захворювання, зазвичай відрізняються від традиційних, оскільки лікування часто зосереджується на симптоматичному полегшенні, хоча воно має бути збалансованим із глікемічним контролем. Рівень глюкози крові має бути не нижчим за 6,0 ммоль/л і не вищим за 15 ммоль/л [35].
Література
Joharatnam-Hogan N., Chambers P., Dhatariya K., Board R.; the Joint British Diabetes Society for Inpatient Care (JBDS), UK Chemotherapy Board (UKCB). A guideline for the outpatient management of glycaemic control in people with cancer. Diabet. Med. 2022; 39: e14636. https://doi.org/10.1111/dme.14636.
