Ведення пацієнтів з гіпереозинофільним синдромом*. Частина 1
Переклала й адаптувала канд. мед. наук Ольга Королюк
Еозинофіли – це термінально диференційовані лейкоцити з цитоплазматичними гранулами, які містять біологічно активні молекули: еозинофілпероксидазу, еозинофільний катіонний білок, основний базовий білок і декілька цитокінів, зокрема трансформувальний фактор росту-β. Еозинофіли утворюються в кістковому мозку з мультипотентних гемопоетичних стовбурових клітин, які перетворюються на попередники еозинофілів, котрі диференціюються в зрілі клітини. Зрілі еозинофіли залишають кістковий мозок і потрапляють у кров, де циркулюють приблизно 1 день, після чого мігрують у тканини: слизові оболонки травного тракту, тимус, селезінку, лімфатичні вузли та матку. В інших здорових тканинах та органах людини еозинофіли зазвичай не трапляються. Щодо функції, то еозинофіли значною мірою сприяють захисту господаря від зовнішніх патогенів, але останнім часом їх пов’язують з регуляцією ремоделювання та фіброзу тканин, а також з регуляцією інших імунних реакцій.
Еозинофілія визначається як підвищений рівень еозинофілів у периферичній крові, що спостерігається при кількох запальних і реактивних станах.
У нормі абсолютна кількість еозинофілів (АКЕ) в периферичній крові становить (0,05-0,5)×109/л; в аспіратах кісткового мозку на зрілі еозинофіли припадає 1-6%.
За класифікацією еозинофільних розладів Міжнародної кооперативної робочої групи з еозинофільних розладів (ICOG-EO) 2011 року з переглядом 2022 року, АКЕ >0,5×109/л визначають як еозинофілію, АКЕ ≥1,5×109/л – як гіпереозинофілію (ГЕ). Своєю чергою, за ступенем підвищення АКЕ виділяють легку еозинофілію, помірну та тяжку ГЕ: (0,5-1,49)×109/л; (1,5-5,0)×109/л і >5,0×109/л відповідно. За тривалістю еозинофілія класифікується на епізодичну, тимчасову та стійку (персистивну). Єдиних критеріїв для визначення стійкої еозинофілії немає: 1) АКЕ >1,5×109/л упродовж ≥6 місяців (Chusid M.J. et al., 1975); 2) АКЕ >1,5×109/л упродовж ≥4 тижнів (Khoury J.D. et al., 2022); 3) АКЕ ≥1,5×109/л, зареєстрована принаймні двічі впродовж щонайменше 2 тижнів (Робоча конференція з еозинофільних розладів і синдромів; Відень, 2021).
Виявлення основної причини транзиторної ГЕ та підтипу гіпереозинофільного синдрому (ГЕС) має вирішальне значення для вибору найбільш відповідного лікування й оптимальної тактики подальшого спостереження. Після першого виявлення ГЕ потреба в лікуванні або застосуванні стратегії «спостереження й очікування» завжди ґрунтується на клінічних симптомах і потенційному ураженні органів унаслідок еозинофілії. Отже, менеджмент має визначатися індивідуально.
Критерієм тканинної ГЕ є принаймні одна з таких умов: 1) еозинофіли становлять >20% усіх ядерних клітин у зрізах кісткового мозку; 2) патолог задокументував масивну еозинофільну інфільтрацію тканин порівняно з «нормальними фізіологічними діапазонами»; 3) імунофарбування виявляє виражене позаклітинне відкладення білків, що походять від еозинофілів.
Персистивна ГЕ може асоціюватися з інфільтрацією органів і тканин, що призводить до їх пошкодження, спричиненого вивільненням молекул – ефекторів еозинофілів. Пов’язане з ГЕ пошкодження органів-мішеней асоціюється зі значною захворюваністю та смертністю. ГЕ без ознак ураження органів-мішеней класифікують як ГЕ невідомого значення (ГЕНЗ).
ГЕ з ураженням органів, спричиненим еозинофільною інфільтрацією, визначають як ГЕС – гетерогенну групу рідкісних захворювань, які важко діагностувати та лікувати. Значні досягнення у виявленні генетичних змін, що лежать в основі ГЕ, сприяли виявленню нових варіантів ГЕС; отже, їх класифікація потребує постійного оновлення.
Метою заяви SIAAIC є огляд оновлених визначень і класифікацій ГЕ та ГЕС і принципів їх ведення від діагностики й оцінювання ураження органів до вибору лікування. Основна увага приділяється первинному й ідіопатичному ГЕС (ГЕСІ).
Визначення та класифікація ГЕС
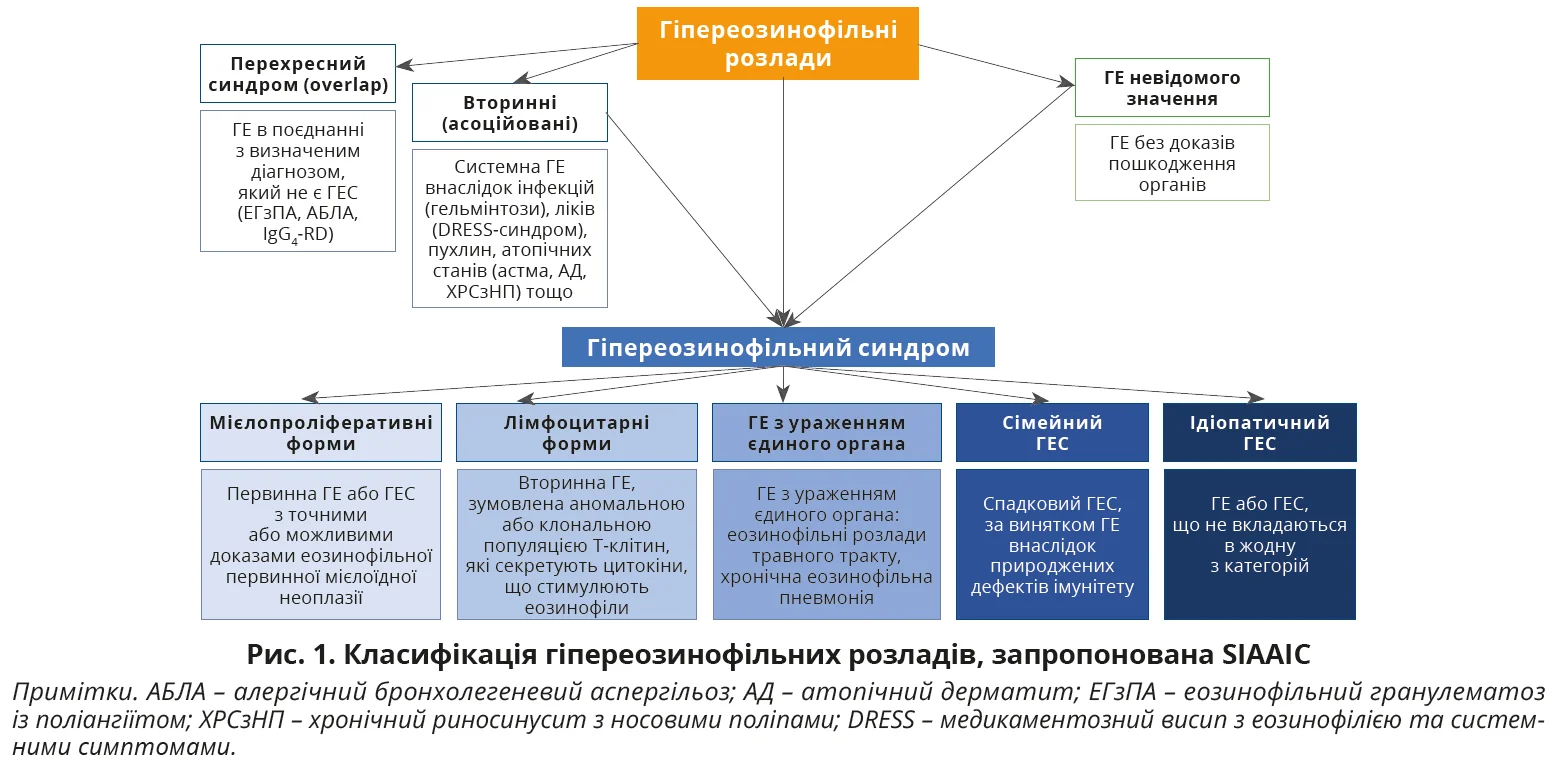
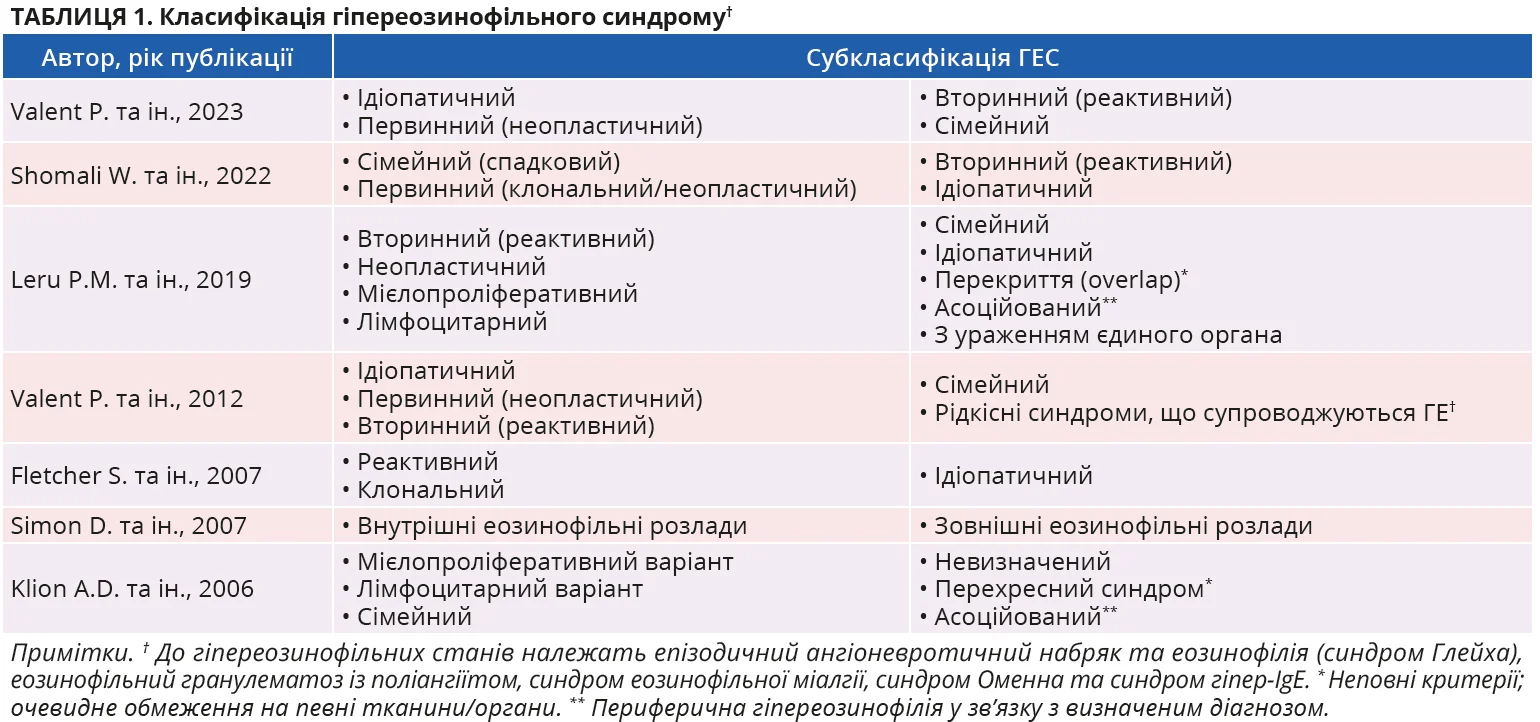
Попередні спроби класифікації ГЕС підсумовано в таблиці 1. Більшість авторів виділяють первинну (клональну), вторинну (реактивну) й ідіопатичну ГЕ, коли причина не встановлена. Найчастіше трапляється вторинна ГЕ, причинами якої можуть бути алергічні хвороби, імунодефіцитні стани, інфекції, ендокринні розлади, лейкемії, лімфоми та солідні пухлини.
Робоча група SIAAIC мала на меті створити легку для розуміння класифікацію, яка загалом відображає клінічну картину, основні механізми та потенційне значення різних гіпереозинофільних розладів.
На відміну від інших класифікацій, SIAAIC розмежовує ГЕ та ГЕС, оцінюючи потенційну еволюцію гіпереозинофільних розладів у бік ГЕС. Перехресний синдром (overlap) і реактивні гіпереозинофільні розлади є окремими підгрупами. Фактично overlap стосується поєднання ГЕ з визначеним станом, не пов’язаним з ГЕ, але з хронічним перебігом з потенційним поліорганним тягарем. Натомість вторинні ГЕ виникають у відповідь на специфічний тригер (алергени або патогени) та зазвичай характеризуються ураженням одного органа. Щоб виділити клональний фон і потенційну еволюцію, лімфоцитарний підтип відокремлено від реактивних форм ГЕС.
Діагностика
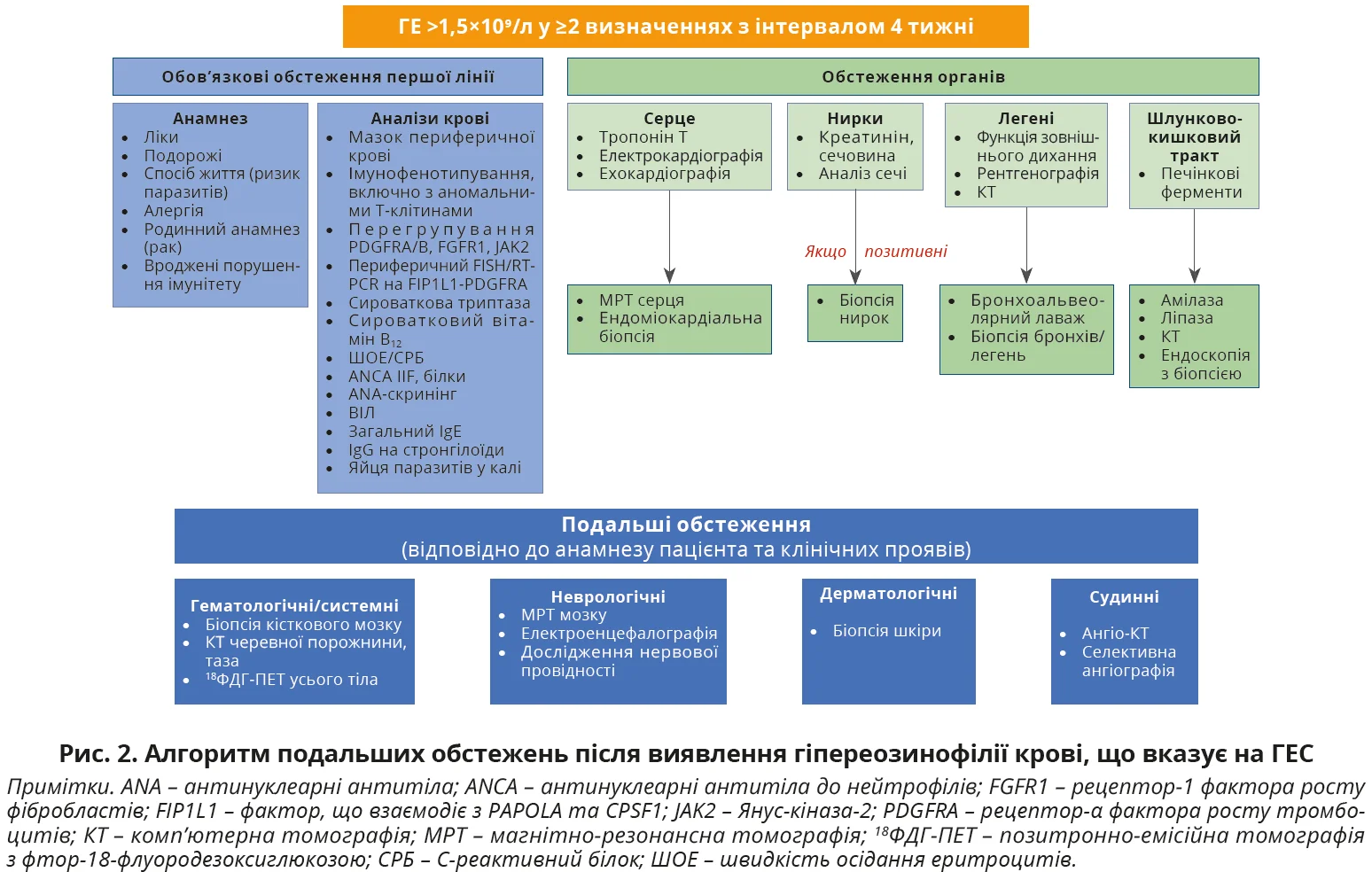
Симптоми та тяжкість хвороби в різних пацієнтів з еозинофілією значно відрізняються. Цікаво, що клінічні прояви ГЕ можуть бути однаковими незалежно від причини. На першому етапі діагностичного обстеження підтверджується наявність ГЕ. Надалі обстеження зосереджується на визначенні етіології ГЕ. Початкова оцінка має враховувати сімейні особливості, оскільки вкрай рідко можлива сімейна ГЕ. Наявність або відсутність реактивного процесу встановлюється на підставі клінічних і лабораторних ознак. Якщо підтверджено реактивну ГЕ (ГЕР), подальші зусилля спрямовуються на виявлення специфічного причинного стану (запалення, інфекція, пухлина, гіперчутливість до ліків), адже лікування ГЕР переважно спрямоване на лікування основного захворювання. У разі виявлення первинної клональної ГЕ вкрай важливо визначити основне гематологічне новоутворення. Пацієнтам без супутнього реактивного стану й ознак клональності попередньо встановлюється діагноз ГЕНЗ і призначається ретельне спостереження впродовж певного часу з акцентом на виявлення ураження органів. Для оцінки ураження органів обстеження розширюється (рис. 2). Пацієнтам з ураженням органів, пов’язаним з ГЕ, встановлюється діагноз ГЕС.
-
Виключення вторинної ГЕ
Завжди слід виключати вторинні причини еозинофілії, адже їх усунення або лікування основної хвороби визначає менеджмент у таких випадках.
Серед вірусних і бактерійних інфекцій легка еозинофілія переважно трапляється при туберкульозі та ВІЛ-інфекції, особливо за наявності паразитарних або грибкових ускладнень. Натомість ГЕ асоціюється з гельмінтозами або грибковими інфекціями. Інфекція, спричинена Strongyloides stercoralis – гельмінтом, що передається через ґрунт, поширена в усьому світі, може зумовлювати дискомфорт у животі або залишатися цілковито безсимптомною в хронічній стадії. З тяжкою ГЕ асоціюються паразитарний міозит, спричинений Trichinella та Sarcocystis, інфекції, зумовлені анкілостомами та Toxocara сanis; легеневі інфекції, спричинені грибком Coccidioides immitis або гельмінтами Paragonimus і Dirofilaria immitis. Покрита кіркою короста та розриви ехінококових кіст іноді провокують еозинофілію. Гельмінт Anisakis simplex, який зазвичай потрапляє в організм із сирою рибою, може спричиняти біль у животі та кропив’янку; в разі кропив’янки іноді можлива еозинофілія, хоча в більшості випадків шлунково-кишкового анізакідозу еозинофілія відсутня; описано декілька випадків збільшення кількість еозинофілів в асцитичній рідині в пацієнтів з кишковим анізакідозом, а також у плевральній рідині в пацієнта з легеневим анізакідозом.
Частою причиною ГЕ є гіперчутливість до ліків. Прояви медикаментозно індукованої ГЕ дуже варіабельні: від ураження одного органа до декількох систем. Загалом застосування антибіотиків (β-лактами, хінолони) асоціюється з безсимптомною еозинофілією. Прикладом ураження одного органа є інтерстиційний нефрит. Поява макулопапульозного висипу можлива при застосуванні β-лактамних антибіотиків, сульфаніламідних протимікробних засобів, алопуринолу, протиепілептичних препаратів, діуретиків і нестероїдних протизапальних препаратів (НПЗП). За наявності лихоманки, гепатиту та морбіліформного висипу слід підозрювати DRESS-синдром, який можуть спричинити протиепілептичні засоби, β-лактами, хінолони, НПЗП, протитуберкульозні засоби, алопуринол.
Ключові висновки
- Вторинну ГЕ можуть спричинити певні інфекції або ліки.
- Паразитарні інфекції (гельмінтози) найчастіше асоціюються з ГЕ.
- Медикаментозно індукована ГЕ іноді призводить до відтермінованої реакції гіперчутливості, потенційно небезпечної для життя (DRESS-синдром).
-
Неопластична ГЕ
Декілька гематологічних злоякісних новоутворень можуть зумовити ГЕ або бути причиною вторинних ГЕ/ГЕС, що характеризується розширенням еозинофільного ряду через надмірне утворення інтерлейкіну-5 (ІЛ-5) за відсутності змін геному. Геномні перебудови притаманні первинним ГЕ/ГЕС, які класифікують на гематологічні злоякісні новоутворення, що призводять до клональної або поліклональної еозинофілії. Перша категорія охоплює гостру мієломоноцитарну лейкемію з еозинофілією та хронічну мієлоїдну лейкемію.
Гостра мієломоноцитарна лейкемія з еозинофілією (раніше FAB M4Eo) є рідкісною формою гострої мієлобластної лейкемії, що характеризується аномаліями 16-ї хромосоми [(inv(16)(p13.1q22) або t(16;16)(p13.1;q22)/CBFB::MYH11]. Симптоми хвороби зумовлені панцитопенією (анемія, інфекції через лейкопенію, кровотечі внаслідок тромбоцитопенії), а не збільшенням кількості незрілих еозинофілів у крові.
Хронічна мієлоїдна лейкемія – мієлопроліферативне новоутворення, що характеризується наявністю Філадельфійської хромосоми та конститутивно активною тирозинкіназою BCR-ABL1; характеризується збільшенням кількості циркулювальних нейтрофілів, мієлоїдних попередників, базофілів та еозинофілів. У цьому випадку еозинофіли зрідка переважають над нейтрофілами та не асоціюються зі специфічними симптомами.
До гематологічних злоякісних новоутворень, що призводять до поліклональної еозинофілії, відносять Т-клітинні та В-клітинні лімфоми, В-клітинну гостру лімфобластну лейкемію й системний мастоцитоз. Навіть після хіміотерапії Т-клітинна лімфобластна лімфома, Т-клітинна лейкемія / лімфома дорослих і ангіоімунобластна Т-клітинна лімфома асоціюються з вторинною та поліклональною периферичною еозинофілією в 30% пацієнтів. Обидва варіанти шкірної Т-клітинної лімфоми (синдром Сезарі, грибоподібний мікоз) асоціюються з підвищеним сироватковим рівнем IgE й еозинофілією у 20% пацієнтів. Визначення клональності Т-клітинних рецепторів при виявленні еозинофілії корисне для діагностики невідомих Т-клітинних лімфом. В-клітинні годжкінські та негоджкінські лімфоми зазвичай асоціюються з поліклональною тканинною еозинофілією, але еозинофілія периферичної крові здебільшого є легкою. При B-клітинних гострих лімфобластних лейкеміях виникнення поліклональної еозинофілії в периферичній крові є рідкісним явищем і зазвичай асоціюється з транслокацією t(5;14). Еозинофілія може передувати появі клінічних проявів. Причиною системного мастоцитозу є клональна проліферація тучних клітин з мутацією D816V гена c-KIT. Хвороба характеризується системним або алергічним ураженням шкіри (пігментна кропив’янка), селезінки, печінки, лімфатичних вузлів, кісток і кісткового мозку. Вторинна та поліклональна еозинофілія в периферичній крові трапляється у 20% пацієнтів.
Солідні пухлини також можуть асоціюватися з поліклональною еозинофілією як своєрідним епіфеноменом, зокрема аденокарциноми легень, шлунка та товстої кишки, а також плоскоклітинні карциноми (шкіра, носоглотка, сечовий міхур, шийка матки, піхва, член, молочна залоза). Поліклональна еозинофілія зазвичай випереджує клінічні прояви вказаних солідних пухлин.
-
Молекулярна діагностика гематологічних новоутворень
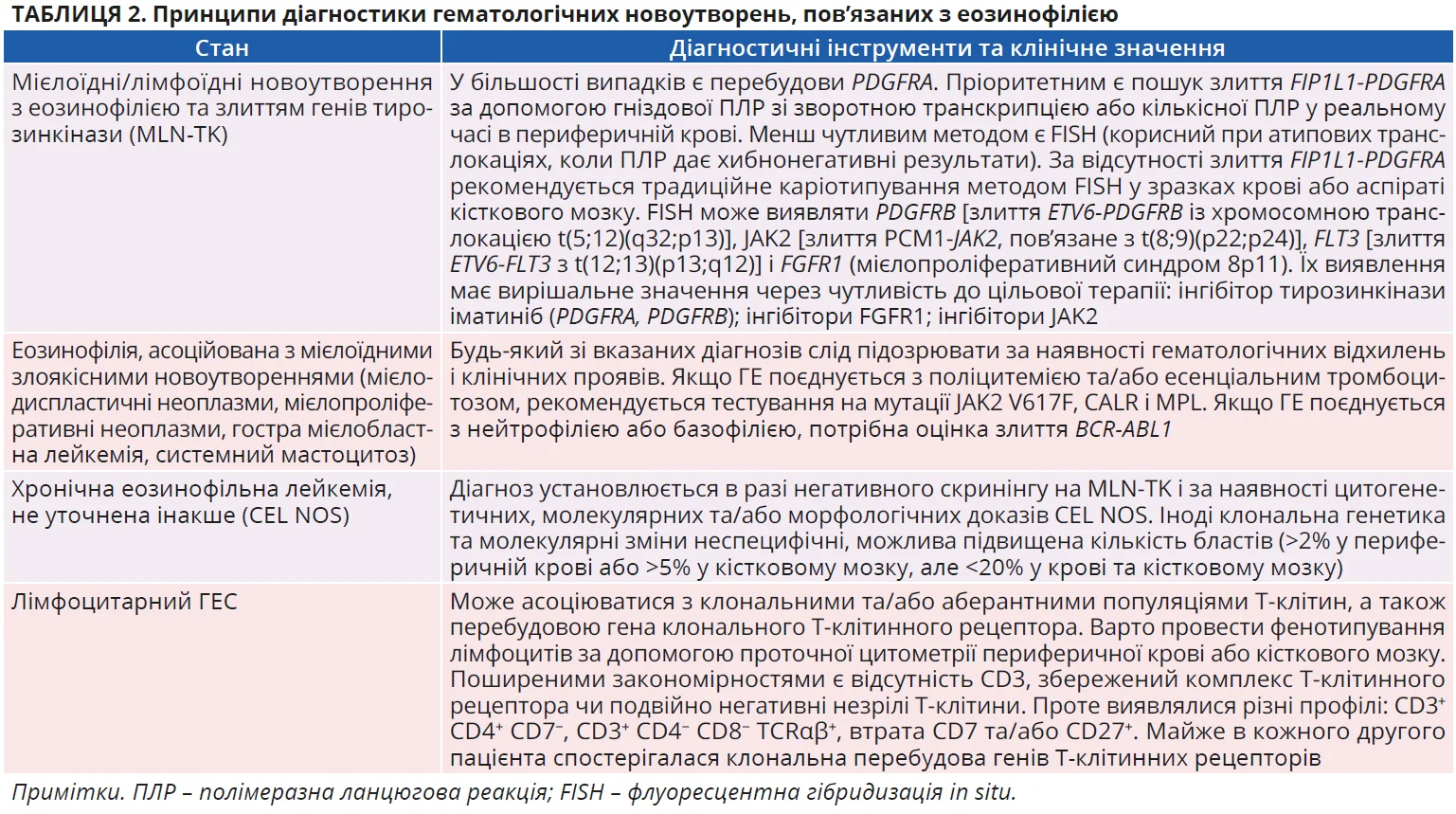
На клональну природу персистивної ГЕ вказують: 1) клінічні характеристики (гепатомегалія, спленомегалія); 2) лабораторні зміни (цитопенія, тромбоцитоз, поліцитемія, моноцитоз, базофілія, підвищений рівень вітаміну B12 та/або триптази в сироватці крові); 3) неможливість нормалізувати кількість еозинофілів у крові за допомогою системних кортикостероїдів. Принципи діагностики гематологічних новоутворень, які асоціюються з еозинофілією, підсумовує таблиця 2.
Ключові висновки
- Після виключення вторинних причин потрібно виключити клональні хвороби кісткового мозку.
- ПЛР / кількісна ПЛР у реальному часі або FISH корисні для оцінювання злиття генів FIP1L1-PDGFRA та менш поширених мутацій і перебудов, включно з PDGFRB, FGFR1 і FLT3 JAK2.
- Фенотипування лімфоцитів за допомогою проточної цитометрії виявляє клональні та/або аберантні популяції Т-клітин, які асоціюються з лімфоцитарним ГЕС.
-
Оцінювання системного ураження
У пацієнтів з ГЕС можливе ураження органів з фіброзом, тромбозом, еритемою шкіри чи слизових оболонок, набряком / ангіоневротичним набряком, пухирями, виразками або екземою, легеневими проявами, ураженнями травного тракту, периферичною або центральною нейропатією з неврологічним дефіцитом, еозинофільним васкулітом. За результатами ретроспективного аналізу даних 188 пацієнтів з діагнозом ГЕС у 37% була уражена шкіра, у 25% – легені, у 14% – травний тракт, у 5% – серце й у 4% – центральна нервова система (ЦНС).
Отже, після виключення вторинних причин пацієнти зі стійкою ГЕ мають пройти детальне обстеження із застосуванням методів візуалізації та гістологічних досліджень, навіть за відсутності клінічних симптомів.
Першим кроком для оцінювання стану легень є оцінювання функції зовнішнього дихання та дифузійної здатності легень за моноокисом вуглецю (DLCO). Комп’ютерна томографія (КТ) може виявити зміни у вигляді «матового скла», ділянки консолідації або вузликові зміни. Біопсія легень виявляє еозинофільні інфільтрати в стінках дихальних шляхів і альвеолярних перегородках, а також скупчення еозинофілів і макрофагів у повітряних просторах.
Характерні для ГЕС ураження серця охоплюють пристінкові тромби, ендоміокардіальний фіброз і рестриктивну кардіоміопатію із застійною серцевою недостатністю. Через відсутність симптомів на ранніх стадіях ураження серця обов’язково треба виконати ехокардіографію (ЕхоКГ). Магнітно-резонансна томографія (МРТ) дає змогу виявити ледь помітні порушення та диференціювати запальну й фіброзну стадії процесу. За відсутності еозинофілії в периферичній крові можна розглядати доцільність ендоміокардіальної біопсії після ретельного оцінювання співвідношення ризику та користі.
Ураження травного тракту може бути ізольованим або супроводжуватися ураженням інших систем. Еозинофілія тканин, оцінена за допомогою езофагофіброгастродуоденоскопії (ЕФГДС) або колоноскопії, вважається патологічною, коли пікова кількість еозинофілів становить ≥15 клітин на поле зору великого збільшення у стравоході, ≥30 клітин у шлунку або тонкій кишці та ≥60 клітин у товстій кишці.
Ключові висновки
- ГЕС визначають як системний стан з патобіологічним навантаженням еозинофілів, включно з порушеннями коагуляції, запаленням і пошкодженням тканин.
- Питання ураження органів потребує спеціального розгляду та проведення відповідних досліджень.
* Скорочений огляд заяви Італійського товариства алергії, астми та клінічної імунології (SIAAIC).
Література
Caminati M., Brussino L., Carlucci M., et al. Managing patients with hypereosinophilic syndrome: a statement from the Italian Society of Allergy, Asthma, and Clinical Immunology (SIAAIC). Cells. 2024 Jul 11; 13 (14): 1180. doi: 10.3390/cells13141180.