Ведення харчової алергії: фокус на елімінаційні дієти
Підготувала канд. біол. наук Олександра Демецька
Харчова алергія є значущою проблемою громадського здоров’я: на неї страждають понад 220 млн людей у світі [1]. Поширеність харчової алергії неухильно зростає, причому показники є вищими серед дітей. Таку динаміку пов’язують не лише з генетичними факторами, а й із чинниками довкілля: змінами харчування, урбанізацією, забрудненням довкілля, мікробним навантаженням.
Зазначена ситуація актуалізує необхідність чіткого розуміння факторів ризику, основних харчових алергенів, а також ролі своєчасного дієтичного менеджменту поряд із сучасними методами діагностики та напрямами лікування харчової алергії.
Поширеність і патогенез алергічних захворювань: роль харчових алергенів
Алергічні хвороби – це група розладів, спричинених порушеними імунними відповідями, опосередкованими імуноглобулінами Е (IgE), на вплив алергенів. Вони проявляються такими клінічними симптомами, як почервоніння та свербіж очей, чхання, закладеність носа, ринорея, кашель, а також свербіж і набряк шкіри [1].
У розвинених країнах алергічні хвороби, як-от астма, алергічний риніт і атопічний дерматит, трапляються дуже часто. У країнах, що розвиваються, різке зростання захворюваності на ці стани, ймовірно, зумовлене змінами способу життя за західним зразком [2].
Дані сучасних досліджень свідчать про те, що дієта й харчування відіграють ключову роль як у розвитку, так і в тяжкості перебігу алергічних захворювань. Компоненти харчування можуть по-різному регулювати шляхи алергічного запалення через метаболіти організму та кишкової мікробіоти, позитивно або негативно впливаючи на перебіг алергії. Зокрема, широкий спектр нутрієнтів – вітаміни A, D та E, мінерали (цинк, залізо, селен), харчові волокна, жирні кислоти й фітохімічні сполуки – продемонстрували потенційну ефективність у профілактиці або лікуванні алергічних захворювань шляхом пригнічення запалення 2-го типу (алергоорієнтованої імунної відповіді, опосередкованої Т-хелперними клітинами 2-го типу та цитокінами) [2].
Як багатофакторне захворювання, харчова алергія формується під впливом генетичних чинників, факторів довкілля та їх взаємодії. До основних факторів ризику розвитку алергії або сенсибілізації до харчових алергенів належать стать (зокрема вищий ризик у хлопчиків у дитячому віці), раса й етнічна приналежність (підвищена поширеність серед дітей азійського й афроамериканського походження), а також генетична схильність [2]. Окрім того, ймовірну роль відіграють атопічні супутні хвороби, зменшений контакт з мікроорганізмами в ранньому дитинстві внаслідок надмірно стерильних умов (гігієнічна гіпотеза), особливості кишкового мікробіому, рівень сироваткового вітаміну D, харчові чинники (зокрема низьке споживання ω3-поліненасичених жирних кислот і антиоксидантів), застосування антацидів, ожиріння, час уведення прикорму та негастроінтестинальні шляхи надходження харчових алергенів.
У країнах з високим рівнем доходу, зокрема в США, переважна більшість випадків харчової алергії в дітей зумовлена переліком продуктів, до якого належать коров’яче молоко, яйця, кунжут, пшениця, соя, арахіс, деревні горіхи, риба, молюски та ракоподібні (рис. 1) [1].
Водночас окремі харчові алергії характеризуються високою ймовірністю спонтанного зникнення або формування імунної толерантності до підліткового віку. За даними літератури, алергія на молоко зникає приблизно в 50% випадків у віці 5-10 років, алергія на яйця – майже в половини дітей віком 2-9 років, алергія на пшеницю – в 50% дітей до 7 років, а алергія на сою – приблизно в 45% дітей до 6 років [1].
Натомість інші харчові алергії зазвичай мають персистентний характер і зберігаються протягом дитячого віку й надалі. Зокрема, алергія на арахіс минає лише приблизно у 20% випадків до 4 років, тоді як алергія на деревні горіхи – у близько 10%. Своєю чергою, алергія на насіння, рибу та морепродукти переважно зберігається протягом життя [1].
Діагностика харчової алергії та принципи дієтичного ведення
Самостійне вилучення нутритивно важливих продуктів з раціону може завдавати більше шкоди, ніж користі, особливо в дітей раннього віку. Тому адекватні дієтичні рекомендації мають надаватися лише на підставі підтвердженого діагнозу харчової алергії, встановленого за допомогою відповідних обстежень [4].
Точна ідентифікація причинних харчових продуктів є ключовою умовою для персоніфікованого ведення харчової алергії. У цьому контексті застосування сучасних діагностичних методів, зокрема компонентної алергодіагностики й оцінювання реактивності до окремих епітопів, дає змогу здійснити цілеспрямований аналіз хвороби та розробити індивідуалізований терапевтичний підхід. Важливими інструментами діагностики харчової алергії залишаються ретельний клінічний і дієтичний анамнез, шкірні прик-тести, визначення специфічних IgE до харчових алергенів, елімінаційні дієти та подальші пероральні харчові провокаційні проби.
Пероральна харчова провокаційна проба може проводитися у відкритому форматі, як одинарний сліпий тест або, оптимально, в межах подвійно сліпого плацебо-контрольованого дослідження (ПСПКД).
На сьогодні ПСПКД залишається золотим стандартом діагностики харчової алергії, хоча його виконання, особливо в дитячій популяції, є технічно складним і пов’язане з ризиком серйозних ускладнень, зокрема тяжких анафілактичних реакцій [3].
Попри те що клінічний і дієтичний анамнез часто надає цінну інформацію, в багатьох випадках потрібні підтверджувальні лабораторні чи інструментальні дослідження. Позитивні результати алергологічних тестів in vivo або in vitro можуть підтримувати підозру на харчову алергію, однак через їхню обмежену специфічність наявність сенсибілізації сама собою не є достатнім доказом клінічної значущості без відповідного підтвердження з анамнезу [3].
Підтверджений діагноз харчової алергії дає змогу обґрунтовано визначити перелік продуктів, які підлягають вилученню, та є основою для розроблення нутритивно збалансованої індивідуалізованої елімінаційної дієти. Важливою складовою дієтичного ведення є також навчання дітей та їхніх батьків навичкам читання й інтерпретації харчових етикеток з метою виявлення явних і прихованих алергенів, що сприяє запобіганню повторних реакцій і розвитку тяжчих проявів алергії.
Оскільки перебіг харчової алергії може змінюватися із часом, діагноз потребує періодичного перегляду для оцінювання ймовірності формування толерантності або появи нових харчових тригерів. Регулярне повторне оцінювання є особливо важливим у дитячому віці, оскільки своєчасна реінтродукція продуктів може сприяти розширенню раціону та покращенню якості життя.
У частини осіб IgE-опосередкована харчова алергія зумовлює необхідність тривалого або довічного вилучення окремих продуктів. Водночас в інших випадках продукт, який раніше добре переносився, може зумовлювати розвиток алергічної реакції вже в дорослому віці. Незалежно від віку, етнічного походження чи соціально-економічного статусу всі особи з харчовою алергією потребують індивідуалізованих рекомендацій щодо харчування для підтримання здорового раціону та якості життя [3].
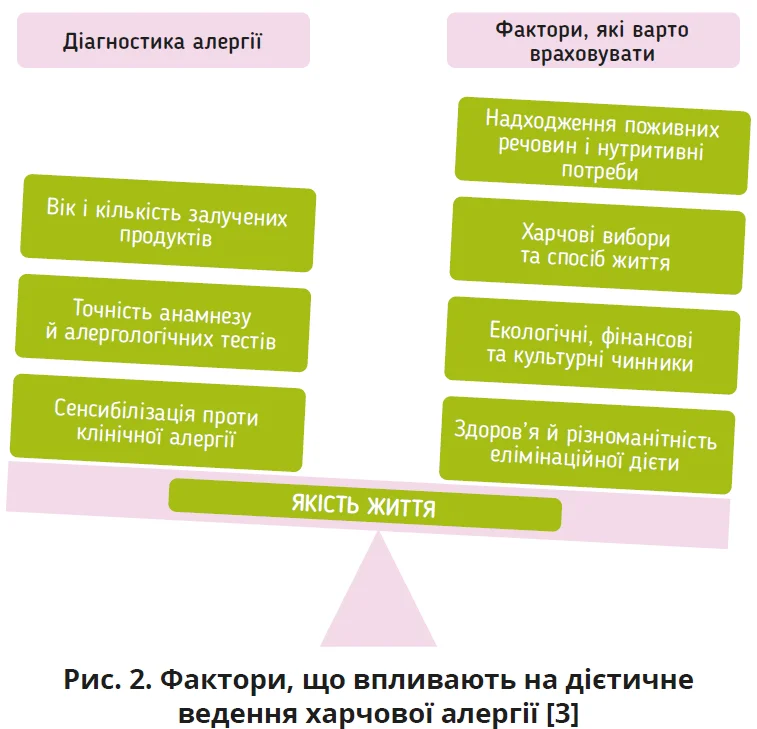
Найважливішим аспектом дієтичного ведення є впевненість у правильності встановленого діагнозу й обґрунтованості елімінації одного чи кількох продуктів. Невиправдане обмеження раціону може не лише негативно впливати на ріст і нутритивну повноцінність харчування, але й спричиняти втрату толерантності до продуктів, які раніше вживалися без симптомів [3]. Отже, наслідки необґрунтованих елімінаційних дієт можуть бути значними й істотно впливати на якість життя людини та її родини (рис. 2).
Загалом діагностика та ведення харчової алергії є процесом пошуку оптимального балансу. Поєднання точного діагнозу з комплексним підходом до дієтичного менеджменту дає змогу досягти стану рівноваги та мінімізувати негативний вплив харчової алергії на повсякденне життя.
Наслідки необґрунтованих елімінаційних дієт
Вилучення продуктів з раціону має ґрунтуватися виключно на чітко підтвердженій ідентифікації причинного алергену за даними анамнезу та відповідних діагностичних тестів. Елімінаційні дієти є обмежувальними за своєю природою й можуть призводити до нутритивних ускладнень, особливо за тривалого застосування в дитячому віці. До потенційних наслідків належать порушення росту, недостатній приріст маси тіла, а також дефіцити кальцію та вітаміну D [3].
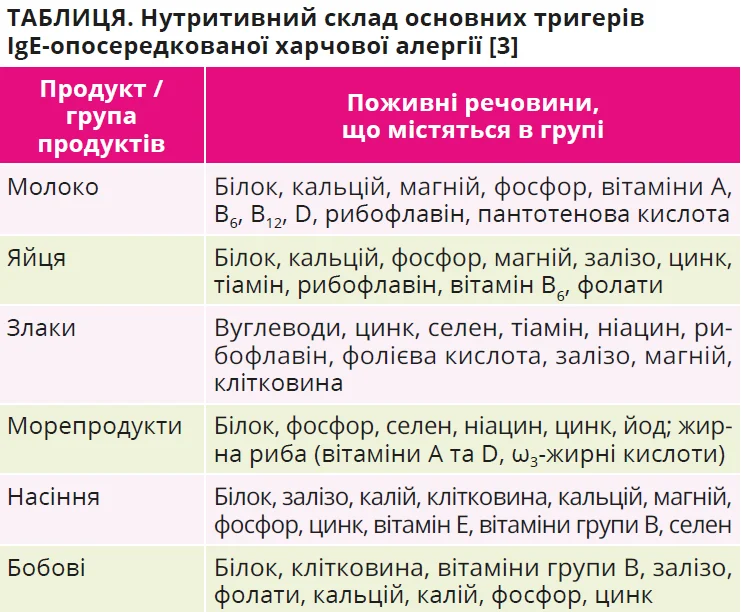
У дітей і молоді з алергією на білки коров’ячого молока описано зниження мінеральної щільності кісткової тканини й підвищений ризик дефіциту мікронутрієнтів, навіть за умови достатнього або надмірного споживання енергії та білка. Вираженість нутритивних порушень залежить від вихідного складу раціону, кількості та тривалості вилучених продуктів, віку, наявності супутніх захворювань, доступності кваліфікованої дієтологічної підтримки (табл.).
Особливо високий ризик порушення харчової повноцінності спостерігається при вилученні базових продуктів харчування, зокрема коров’ячого молока чи пшениці, а також у разі розширення переліку елімінації. Тривале вилучення молочних продуктів асоціюється з вищим ризиком затримки росту порівняно з алергією на арахіс або деревні горіхи, що підкреслює важливість ретельного оцінювання доцільності та наслідків елімінаційних дієт.
Маркування харчових продуктів
Ефективне дієтичне ведення харчової алергії потребує здатності коректно інтерпретувати харчові етикетки й оцінювати потенційні ризики під час споживання багатокомпонентних продуктів. Це сприяє підвищенню безпеки харчування, формуванню відчуття контролю та зниженню психологічного навантаження.
Попри суттєве покращення обов’язкового маркування алергенів у Європейському Союзі, США й Австралії, надана інформація часто залишається складною для сприйняття. Крім того, чинні законодавчі вимоги не завжди охоплюють усі клінічно значущі алергени та ризики ненавмисної контамінації, що може негативно впливати на якість життя осіб з харчовою алергією [3].
Широке використання попереджувального маркування (precautionary allergen labelling – PAL) за відсутності уніфікованих стандартів ускладнює управління ризиками. Споживачі часто не розуміють, чи ґрунтуються такі позначки на реальній оцінці ризику, внаслідок чого PAL може ігноруватися або хибно трактуватися. Це, своєю чергою, підвищує ймовірність випадкових алергічних реакцій, значній частині яких потенційно можна було б запобігти, особливо в ситуаціях, що сприймаються як безпечні.
Персоніфікована тактика елімінаційної дієти: практичні аспекти
Під час дієтичного ведення пацієнта потрібно комплексно оцінювати низку взаємопов’язаних чинників. Зокрема, слід виконувати скринінг нутритивних ризиків і враховувати наявні клінічні симптоми. Важливими є харчові вподобання або непереносимості, можливі труднощі з прийманням їжі.
Крім медичних аспектів, варто брати до уваги економічні фактори, зокрема бюджет домогосподарства, а також доступ до продуктових магазинів. Раціон має бути адаптований до культурно релевантних продуктів з огляду на тижневий графік, час і місце їди.
Практичне значення мають наявні кухонні інструменти, рівень знань і навичок із приготування їжі, а також розуміння того, хто саме відповідає за приготування їжі та годування. Додатково потрібно враховувати кількість дітей і дорослих у домогосподарстві, оскільки це безпосередньо впливає на організацію харчування та можливості дотримання дієтичних рекомендацій [3].
Метою здорового харчування за наявності алергій є забезпечення організму всіма необхідними поживними речовинами та формування різноманітного збалансованого раціону з огляду на індивідуальну переносимість продуктів. Раціон має включати різні за смаком і текстурою цілісні, поживні, переважно мінімально оброблені продукти, що сприяють кращому харчовому вибору та прийняттю різноманітної їжі.
Здорова дієта зазвичай базується на продуктах рослинного походження – овочах, фруктах, бобових, крупах, а також включає ферментовані продукти, за умови їхньої безпечності для людини з алергією. Таке харчування забезпечує надходження клітковини, заліза, цинку, ω3-жирних кислот і водночас обмежує споживання цукру, солі й ультраперероблених інгредієнтів [5].
Індивідуальний підбір продуктів і своєчасне використання безпечних альтернатив алергенам є ключовими для підтримання здоров’я, нормальної роботи імунної системи та зниження ризику алергічних проявів у повсякденному житті.
За наявності харчової алергії часто виникає потреба в модифікації раціону шляхом заміни алергенних продуктів альтернативними інгредієнтами. Така заміна має здійснюватися усвідомлено та персоніфіковано, зважаючи на спектр сенсибілізації, нутритивну цінність продуктів і ризик перехресної алергії. Для безпечного вибору багатокомпонентних харчових продуктів необхідним є ретельне читання етикеток і, за потреби, звернення до виробника для уточнення інформації щодо складу та можливого забруднення алергенами. Важливо пам’ятати, що деякі замінники самі собою можуть бути алергенами, і невдалий вибір здатен призвести до заміни одного алергену іншим [6].
Заміна молочних продуктів
Під час приготування їжі або випічки коров’яче молоко можна замінювати рослинними напоями, зокрема рисовими, мигдалевими, кокосовими, кеш’ю, конопляними, гороховими чи соєвими. Вибір конкретного продукту має враховувати смакові властивості, оскільки деякі напої (наприклад, кокосовий) можуть істотно змінювати органолептичні характеристики страв. Перевагу слід віддавати збагаченим (фортифікованим) продуктам, до яких додано кальцій і вітамін D. Використання дитячих молочних сумішей для приготування їжі не рекомендується через втрату поживних речовин при нагріванні та можливу зміну смаку.
Рослинні напої істотно різняться за поживною цінністю. Соєве молоко є найближчим за білковим складом до коров’ячого, тоді як рисові, мигдалеві й кеш’ю-напої містять значно менше білка та жиру, навіть за умови збагачення мікронутрієнтами. Слід також розрізняти охолоджені кокосові напої, які використовують для напоїв і сніданків, і консервоване кокосове молоко, придатне для приготування супів, соусів і десертів.
Для заміни вершкового масла доцільно використовувати спеціальні безмолочні жирові спреди або маргарини, що не містять молочних білків (казеїну, сироваткових білків), а також соєві жирові замінники за відсутності сенсибілізації до сої. Перевагу слід віддавати продуктам з низьким умістом води та стабільним жировим складом, що особливо важливо під час випічки.
Заміна йогурту та сиру
Альтернативою молочному йогурту можуть бути продукти на основі мигдалевого, кеш’ю, кокосового, вівсяного, горохового або соєвого молока. Замість традиційного сиру рекомендовано використовувати веганські або вегетаріанські аналоги, з обов’язковою перевіркою складу на наявність інших потенційних алергенів, зокрема деревних горіхів.
Заміна яєць
У випічці кожне яйце може бути замінене функціональними комбінаціями інгредієнтів, зокрема яблучним пюре з розпушувачем, розім’ятим бананом, сумішшю меленого насіння льону з водою або поєднанням води, рослинної олії та розпушувача. Вибір замінника залежить від типу виробу й бажаного сенсорного результату.
Безпшеничні альтернативи
До безпшеничних видів борошна та крохмалів належать мигдалеве, кукурудзяне, пшоняне, картопляне, рисове, тапіокове борошно, а також борошно з кіноа. У більшості випадків такі продукти можна використовувати в кількостях, еквівалентних пшеничному борошну, зважаючи на рекомендації виробника. Можливим є також приготування домашніх безглютенових сумішей на основі рисового борошна з додаванням картопляного та тапіокового крохмалів.
Заміна арахісового масла
Замість арахісового масла можуть використовуватися соєве масло, масло з насіння соняшнику, тахіні (кунжутна паста) або масла з деревних горіхів за умови відсутності сенсибілізації до відповідних алергенів [6].
Загалом елімінаційна дієта реалізується поетапно та передбачає тимчасове вилучення найімовірніших харчових тригерів, ретельний контроль складу продуктів, систематичне спостереження за симптомами та подальшу поступову реінтродукцію окремих продуктів. Аналіз змін самопочуття під час кожного із цих етапів дає змогу оцінити індивідуальну переносимість їжі й обґрунтувати доцільність подальшої елімінації або повернення продуктів до раціону.
Лікування та профілактика ускладнень
Натепер не існує радикального лікування харчової алергії: основною стратегією ведення залишаються елімінація причинного алергену та контроль клінічних проявів. Попри доведену ефективність уникнення алергенів і фармакотерапії, люди з харчовою алергією зберігають ризик розвитку тяжких алергічних реакцій у разі випадкового контакту з алергеном [1].
Лікування харчової алергії передбачає повне вилучення алергенного продукту з раціону, уважне ознайомлення зі складом харчових продуктів та обізнаність щодо альтернативних назв алергенів. Важливим компонентом профілактики ускладнень є навчання й інформування, зокрема наявність індивідуального плану дій на випадок невідкладного стану із чіткими інструкціями щодо застосування адреналіну та визначення ситуацій, які потребують негайного звернення по медичну допомогу [7].
Антигістамінні препарати відіграють важливу роль у симптоматичному контролі легких і помірних алергічних проявів, як-от свербіж, кропив’янка, ринорея або набряк слизових оболонок. Вони застосовуються як складова комплексного підходу до ведення харчової алергії та сприяють зменшенню вираженості симптомів і покращенню повсякденного функціонування. Вибір конкретного препарату, режиму та тривалості застосування має здійснюватися індивідуально з огляду на клінічну ситуацію й рекомендації лікаря.
Зважаючи на значний психологічний та емоційний тягар хвороби, важливими складовими комплексного ведення є психологічна підтримка, а також формування навичок безпечної поведінки в повсякденному житті. Тривала співпраця з лікарем-алергологом є ключовою для оптимізації лікувальної тактики та динамічного спостереження.
У частини осіб, особливо при не-IgE-опосередкованих формах харчової алергії, можливе природне формування толерантності до окремих харчових продуктів. Водночас деякі алергічні стани можуть зберігатися протягом тривалого часу, що зумовлює потребу в додаткових або альтернативних терапевтичних підходах.
Пероральна імунотерапія розглядається як перспективний підхід для підвищення порогів толерантності та в окремих випадках може сприяти формуванню стійкої нечутливості. Проте цей метод часто супроводжується алергічними реакціями, а досягнутий ефект може бути нестійким після припинення регулярного вживання алергену. Загалом імунотерапія спрямована на десенсибілізацію імунної відповіді, однак її ефективність і безпечність залишаються варіабельними.
Останніми роками зростає інтерес до застосування біологічних препаратів, зокрема моноклональних антитіл, як потенційного інструменту модифікації перебігу харчової алергії. Водночас їхня здатність змінювати природний перебіг хвороби наразі остаточно не визначена, а широке клінічне застосування потребує подальших досліджень.
Висновки
Харчування є ключовим чинником, що впливає на перебіг алергічних захворювань, зокрема харчової алергії, через участь у регуляції імунної відповіді, запальних процесів і функції кишкового бар’єра. Нераціональний склад раціону може спричиняти зниження імунної толерантності та посилення алергічного запалення, тоді як збалансоване харчування з адекватним надходженням макро- та мікронутрієнтів відіграє важливу роль у підтриманні імунного гомеостазу.
Елімінаційні дієти залишаються базовим елементом ведення харчової алергії, однак їх застосування має ґрунтуватися виключно на підтвердженому діагнозі та супроводжуватися регулярним оцінюванням нутритивного статусу. Тривале вилучення продуктів з високою харчовою цінністю потребує персоніфікованого дієтичного підходу, зокрема обґрунтованої заміни алергенних продуктів безпечними альтернативами, з метою запобігання нутритивним дефіцитам, порушенню росту та зниженню якості життя, особливо в дитячому віці. Медикаментозна терапія відіграє допоміжну роль у контролі симптомів і не може розглядатися як альтернатива елімінації причинного алергену.
Отже, оптимальне ведення харчової алергії передбачає поєднання обґрунтованих елімінаційних дієт, персоніфікованого дієтичного менеджменту, фармакотерапії та готовності до невідкладної допомоги в разі тяжких реакцій. Дослідження з урахуванням нутритивного статусу, стану кишкової мікробіоти й фенотипу хвороби є необхідними для подальшої оптимізації та персоналізації елімінаційних дієтичних стратегій.
Вибір антигістамінних препаратів у клінічній практиці не є універсальним і потребує персоніфікованого підходу. Низка засобів, які демонструють ефективність у лікуванні інших алергічних захворювань, зокрема алергічного риніту або атопічного дерматиту, здатні виявляти обмежену клінічну користь при симптомах харчової алергії.
Супрастин® (хлоропірамін) належить до антигістамінних препаратів першого покоління та може застосовуватися для симптоматичного усунення гострих клінічних проявів харчової алергії, зокрема шкірного свербежу, кропив’янки та набряку, у складі комплексного підходу до ведення пацієнтів.
Препарат характеризується швидким початком дії, вираженим антигістамінним ефектом та добре вивченим профілем застосування. Він може розглядатися як засіб невідкладної або тимчасової допомоги на етапі підбору, елімінування або заміни причинно-значущих харчових продуктів.
Призначення препарату, вибір режиму та тривалості застосування мають здійснюватися лікарем з урахуванням клінічної ситуації, віку пацієнта та наявних супутніх станів.
Література
- Garcia-Carmona Y., Curotto de Lafaille M.A. Advances in food allergy immunotherapy: current strategies and role of antibodies isotypes. Cells. 2025; 14 (12):900. doi: 10.3390/cells14120900.
- Zhang P. The role of diet and nutrition in allergic diseases. Nutrients. 2023; 15 (17): 3683. doi: 10.3390/nu15173683. PMID: 37686715; PMCID: PMC10490368.
- Skypala I.J., et al. Food allergy – a holistic approach to dietary management. A joint EAACI Research & Outreach Committee and INDANA review. Pediatr. Allergy Immunol. 2023; 34 (9): e14019. doi: 10.1111/pai.14019. PMID: 37747742.
- Leone L., et al. Nutritional management of food allergies: prevention and treatment. Front. Allergy. 2023 Jan 6; 3: 1083669. doi: 10.3389/falgy.2022.1083669.
- Vlieg-Boerstra B., et al. EAACI Prevention Working Group. Guidance for healthy complementary feeding practices for allergy prevention in developed countries: an EAACI interest group report. Pediatr. Allergy Immunol. 2025; 36 (7): e70150. doi: 10.1111/pai.70150. PMID: 40686257.
- Food Allergy Research & Education (FARE). Substitutions for Common Allergens. 2025. Available at: https://www.foodallergy.org/resources/substitutions-common-allergens-pdf.
- Huerta Hernández R.E., Ortega Martell J.A. Tratamiento en pacientes con alergia alimentaria [Treatment for living with food allergy]. Rev. Alerg. Mex. 2023; 70 (4): 280-283. doi: 10.29262/ram.v70i4.1313.