Проблема атопічного дерматиту в педіатричній практиці
Автор: Оксана Іванівна МАЦЮРА, докторка медичних наук, професорка кафедри педіатрії та медичної генетики ДНТ «Львівський національний медичний університет ім. Данила Галицького»
Всесвітня організація охорони здоров’я визнала алергію хворобою XXI століття. Упродовж останнього десятиліття захворюваність на харчову алергію, атопічний дерматит (АД), алергічний риніт, бронхіальну астму подвоїлася, що дістало назву «епідемії» алергії [1].
Переконливо доведено: шкіра є органом, який бере активну участь у розвитку атопічних реакцій. І найчастіше атопічний марш дебютує власне шкірними проявами алергії, що можуть проявлятися як харчова алергія або АД [5].
АД є хронічним алергічним захворюванням, яке розвивається в осіб з генетичною схильністю до атопії та характеризується рецидивним перебігом, типовим висипом, підвищенням імуноглобуліну E (IgE) й гіперчутливістю до специфічних (алергенів) і неспецифічних подразників [7]. Слід зазначити, що АД сьогодні розглядають як системне захворювання, оскільки в патологічний процес утягується не лише шкіра, а й інші органи та системи (травний канал, нервова система тощо).
Етіологія
АД – багатофакторна хвороба. Багатогранність і неоднозначність факторів, які зумовлюють розвиток цієї патології, породжують складнощі у вивченні її етіології [3]. Однак сьогодні доведено, що серед чинників, які зумовлюють виникнення дерматиту, особливу вагу має генетично детермінована схильність до атопічних захворювань [5]. Слід зазначити, що для АД притаманна полігенна форма успадкування.
Патогенез
В основі патогенезу АД у переважної більшості дітей лежать IgE-опосередковані (атопічні) імунопатологічні реакції. Водночас у 10-30% хворих за цієї патології підвищений рівень IgE не реєструється, оскільки в них патогенетичним підґрунтям АД є інші імунні та неімунні (псевдоалергічні) механізми запалення [6].
За останні роки суттєво розширилися уявлення стосовно ролі шкіри у формуванні імунної відповіді на алерген. Ініціація імунної відповіді здійснюється в асоційованій зі шкірою лімфоїдній тканині. Дендритні клітини шкіри першими розпізнають і захоплюють антиген і, мігруючи в регіональні лімфовузли, презентують його для Т-лімфоцитів. Саме в регіональних лімфовузлах відбувається каскад імунних реакцій, який призводить до перетворення В-лімфоцитів на плазматичні клітини, що й синтезують антитіла. Надалі антитіла й сенсибілізовані лімфоцити повертаються до шкіри та призводять до реалізації імунної запальної відповіді, яка клінічно проявляється симптомами АД [9]. До загострення хвороби можуть призводити чинники (тригери) не лише алергенної, але й неалергенної природи. Серед тригерів неалергенного походження найчастіше реєструються метеофактори, психоемоційні навантаження, тютюновий дим, харчові добавки, ксенобіотики, полютанти [4].
Фактори ризику
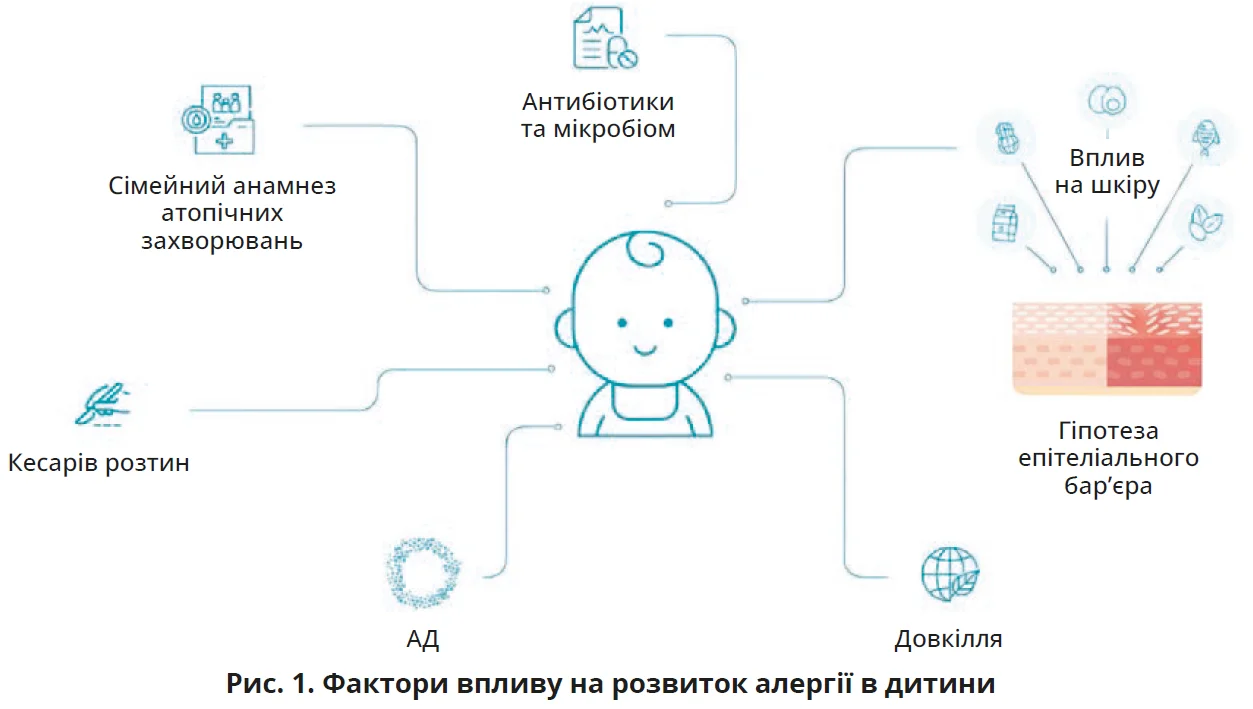
Шкіра є найбільшим і основним захисним органом організму, який служить фізичним бар’єром першого порядку проти зовнішнього середовища. Ранній вплив антигенів через шкіру може бути головним фактором розвитку алергії.
На рисунку 1 показано основні фактори, які збільшують ризики розвитку алергії: обтяжений сімейний анамнез щодо алергії, шкідливий вплив довкілля, кесарів розтин, антибіотикотерапія та порушення мікробіому, АД у дитини, епікутанна сенсибілізація [2].
Європейські й американські настанови рекомендують раннє зволоження та захист шкірного бар’єра як базову стратегію профілактики, адже сухість шкіри в немовлят підвищує ризик дебюту АД. Правильний догляд може відтермінувати розвиток екземи та пов’язаних дерматозів або запобігти йому [4].
Існує гіпотеза подвійного впливу алергенів, яка стверджує, що пероральний вплив харчових антигенів у високих дозах призводить до толерантності, шкірний вплив у низьких дозах – до сенсибілізації. Тому для профілактики алергії дуже важливою є індукція оральної толерантності, а не сенсибілізація алергенами через уражену та подразнену шкіру [2].
Клінічні прояви
АД – хронічне захворювання з дуже поліморфними змінами на шкірі, які іноді геть непросто однозначно трактувати. Перші ознаки хвороби найчастіше виникають на 2-7-му місяці життя. Часто таким симптомам передує поява лусочок на волосистій частині голови та брів (гнейс).
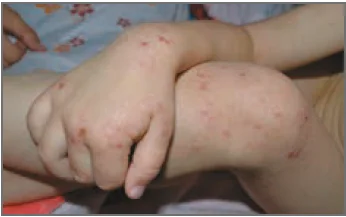
Першими проявами дерматиту є почервоніння й сухість шкіри на щоках і по тілу. За відсутності адекватного лікування процес прогресує та поширюється на інші ділянки обличчя (крім носогубного трикутника й носа), волосисту частину голови, вуха, тулуб, розгинальні поверхні кінцівок. Нерідко висип спостерігається на сідницях, навколо ануса [10].
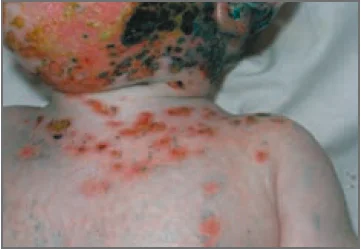
Поступово процес прогресує, і на тлі гіперемії та набряклості шкіри з’являються мікровезикули, які швидко руйнуються, оголюючи ділянки мокнуття, де надалі утворюються кірочки й лусочки. Іноді на тлі типового висипу виділяються дрібні папульозні елементи. Вогнища ураження зазвичай розміщуються симетрично. Після припинення мокнуття, відшарування кірочок і лусочок на місцях ураження залишається гладка шкіра інтенсивного рожевого забарвлення [8].
Нерідко АД перебігає по-іншому, коли на тлі загальної сухості шкіри спостерігаються гіперемія й інфільтрація, котрі опускаються з волосистої частини голови на лоб, щоки, вушні раковини, в завушні та шийні складки, а іноді на тулуб і кінцівки. Мікровезикул і мокнуття немає. За відсутності адекватного лікування процес прогресує, у складках може виникнути мацерація епідермісу, а за вушними раковинами – тріщини, які нерідко кровоточать.
В окремих пацієнтів АД характеризується появою на шкірі спини, сідниць, стегон, гомілок і розгинальних поверхонь рук вогнищ округлої або овальної форми різних розмірів. Шкіра у вогнищі ураження набрякла, має синюшно-рожеве забарвлення та дещо виступає над рівнем здорової шкіри. Це супроводжується нестерпним свербінням, а після розчухування у вогнищах ураження з’являється мокнуття з подальшим утворенням кірочок [12].
З віком у багатьох пацієнтів спостерігається клінічна трансформація шкірних висипань з утворенням епідермодермальних папул, які не відрізняються за кольором від навколишньої шкіри, зливаються між собою й утворюють вогнища суцільної папульозної інфільтрації та ліхеніфікації. Вогнища ураження локалізуються на шиї, в ліктьових і підколінних згинах, на тильній поверхні кистей, у пахвових і пахвинних складках, іноді навколо рота, очей і в ділянці статевих органів. Через постійне свербіння утворюються екскоріації, відзначаються тріщини, які кровоточать і формують серозно-геморагічні кірочки [4, 7].
Дітей турбує інтенсивне свербіння шкіри, котре особливо підсилюється вночі. Через це хворі погано сплять, стають дратівливими, капризними, а іноді озлобленими й агресивними.
Отже, АД у дітей характеризується поліморфними змінами на шкірі. Під час огляду таких пацієнтів виявляють збільшення периферичних лімфатичних вузлів, причому ступінь їх збільшення корелює з тяжкістю перебігу хвороби та поширеністю процесу на шкірі.
Діагностика
Шлях до діагнозу АД починається з ретельного аналізу анамнезу й об’єктивного обстеження. Визначальними клінічними ознаками є типовий характер висипу, що супроводжується свербінням, і рецидивний характер перебігу хвороби з ремісіями в літній період. Загальновизнаними залишаються діагностичні критерії, запропоновані ще 1980 року J.M. Hanifin і G. Rajka. Згідно із цими рекомендаціями виділяють головні та додаткові критерії.
Головні («великі») діагностичні критерії:
- свербіння шкіри;
- типова морфологія та локалізація уражень шкіри: в дітей перших 3 років – висипання на обличчі й розгинальних поверхнях кінцівок, у старших – ліхеніфікація та розчухування на згинальних ділянках кінцівок;
- хронічний рецидивний перебіг;
- початок хвороби в ранньому дитячому віці (до 2 років);
- атопія в анамнезі або спадкова схильність до атопії.
Додаткові («малі») діагностичні критерії:
- фолікулярний гіперкератоз;
- іхтіоз / підсилення малюнка на долонях;
- підвищений рівень сироваткового IgE;
- еозинофілія в крові;
- часті інфекційні ураження шкіри, переважно стафілококової, грибкової та герпетичної етіології;
- локалізація шкірного процесу на кистях і стопах;
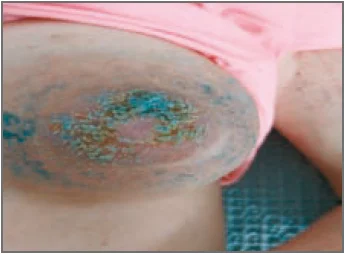
- екзема сосків;
- рецидивний кон’юнктивіт;
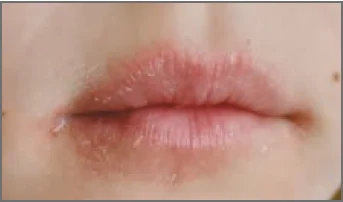
- хейліт;
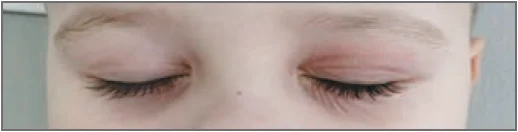
- додаткові суборбітальні складки Денні – Моргана;
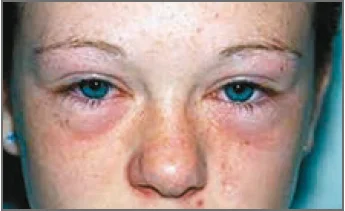
- періорбітальна гіперпігментація, темні кола під очима;
- еритродермія;
- білий дермографізм тощо.
Діагноз АД встановлюється при комбінації не менш ніж 3 «великих» і 3 «малих» критеріїв за тривалості збереження симптоматики не менш ніж 6 тижнів [1].
У більшості випадків атопічний анамнез і типова клініка захворювання дають змогу встановити діагноз і тяжкість перебігу АД. Однак на цьому діагностичний пошук не має закінчуватися.
Наступним етапом має бути визначення причини хвороби в кожної дитини. Це завдання вирішує специфічна алергодіагностика. Комплексний підхід до специфічної алергодіагностики включає:
- Вивчення алергологічного анамнезу (харчовий щоденник).
- Шкірні тести (за умови можливості їх проведення).
- Визначення специфічних IgE в сироватці крові.
Основою основ був, є й, мабуть, буде алергологічний анамнез. Кожен лікар, працюючи з пацієнтом, має пояснити правила ведення харчового щоденника. Ба більше, можна розробити та роздрукувати прості в застосуванні варіанти щоденника й рекомендувати їх пацієнтам.
- Диференційна діагностика
Попри всі наведені вище діагностичні можливості, перед лікарями нерідко постає дуже непроста проблема диференційної діагностики АД з іншою патологією. Найчастіше доводиться диференціювати АД з іншими хворобами шкіри: контактним, пелюшковим, себорейним дерматитами, мікробною екземою, коростою, псоріазом, рожевим лишаєм, іхтіозом тощо.
Ба більше, частим ускладненням АД є нашарування вторинної інфекції. Постійне тертя й розчухування шкіри призводять до порушення її бар’єрної функції та приєднання інфекції, найчастіше бактеріальної (стафілокок, стрептокок), вірусної (герпес) чи грибкової. У таких складних ситуаціях діагностичний пошук потребує додаткових досліджень (мікроскопія та культуральне дослідження лусочок шкіри на патологічну флору, бактеріологічне дослідження пустул на флору й чутливість до антибіотиків тощо) [11].
Лікування
Лікувальна тактика за АД має визначатися етіологічними факторами, патогенетичними механізмами, фазою хвороби та ґрунтуватися на індивідуально підібраних програмах.
Основні напрями лікування включають:
- дієтотерапію (елімінацію причинно-значущих харчових алергенів);
- контроль за довкіллям;
- фармакотерапію – системну та місцеву;
- реабілітаційне (протирецидивне) лікування;
- навчальні програми для пацієнтів і членів їхніх сімей [1, 6, 12].
Найефективнішою, безперечно, є етіотропна терапія, спрямована на усунення контакту з факторами, які спричиняють загострення хвороби. Це можуть бути алергени різного походження, лікарські засоби, харчові добавки, хімічні речовини й різноманітні інфекційні та фізичні чинники.
Ще зовсім недавно традиційно вважали, що причиною АД є виключно харчова алергія. Однак життя довело, що ситуація видається далеко не такою однозначною: лише в 30-40% дітей АД пов’язаний з харчовою алергією. Водночас частіше говорять про зростання питомої ваги побутової, пилкової сенсибілізації у виникненні цієї патології. Усунути або зменшити вплив причинно-значущих факторів можна за допомогою режиму максимального оберігання від контакту з ними. Методами його реалізації є:
- Індивідуальна гіпоалергенна дієта з виключенням причинно-значущих алергенів.
- Гіпоалергенні умови побуту, одягу, житла з метою виключити або зменшити експозицію з інгаляційними та контактними алергенами.
- Санація хронічних вогнищ інфекції [9].
Одним з основних напрямів і сьогодні є підбір індивідуального харчування. Правильно побудована дієта не лише обмежує надходження в організм алергенів, але й має специфічний гіпосенсибілізаційний вплив і сприяє поліпшенню стану органів травлення, що, своєю чергою, підвищує толерантність організму до харчових алергенів.
Мати повинна ретельно вести харчовий щоденник, який дає змогу виявляти причинно-значущі харчові алергени для кожної дитини індивідуально. Під час складання дієти слід пам’ятати, що дитина має отримувати відповідну до віку кількість різноманітних харчових інгредієнтів.
Слід обмежити контакти дитини з подразниками (використання грубого вовняного чи синтетичного одягу, засобів гігієни). Як подразник може виступати висока чи низька температура, що провокує помірне потовиділення або різку сухість шкіри. Нігті на пальцях рук мають бути коротко підстриженими, щоби зменшити ушкодження шкіри при розчухуванні; після душу чи ванни слід використовувати пом’якшувальні креми або олії (емоленти).
Важливим моментом у лікуванні є санація хронічних вогнищ інфекції, оскільки інфекція може бути причиною розвитку АД та його загострень.
Пріоритетом тривалої терапії АД як хронічної патології є превентивна стратегія, мета якої – забезпечити контроль над захворюванням шляхом профілактики рецидивів.
Насамперед особливо важливо інформувати пацієнта та його родину про хворобу й можливості її лікування.
Зовнішня терапія АД є дуже важливою й непростою темою. Вона має бути патогенетично обґрунтованою та проводитися диференційовано, з огляду на патологічні зміни на шкірі.
Зовнішня терапія базується на таких критеріях:
- зменшення й усунення ознак запалення шкіри та пов’язаних з ним симптомів шляхом призначення протизапальних, антигістамінних препаратів;
- лікування та профілактика вторинної інфекції;
- підвищення бар’єрної функції шкіри, відновлення водно-ліпідної плівки епідермісу із застосуванням пом’якшувальних і живильних засобів, що значною мірою сприяє зменшенню та ліквідації сухості шкіри;
- елімінація біологічно активних речовин і деструктивних субстанцій і захист шкіри від несприятливого впливу зовнішнього середовища шляхом призначення очищувальних і зволожувальних засобів [10].
Перед застосуванням зовнішніх лікарських засобів треба очистити шкіру хворої дитини від гною, кірок, лусочок, залишків використаних препаратів, які подразнюють шкіру. Очищення шкіри сприяє тіснішому контакту з нею лікарських речовин, а отже, дає змогу досягти бажаного терапевтичного ефекту.
Досить частою помилкою лікарів є заборона купатися дітям з АД, особливо під час загострення. Ми є прихильниками щоденних гігієнічних ванн, які очищують і зволожують шкіру, підсилюють проникнення зовнішніх препаратів, створюють відчуття комфорту, приносять дитині задоволення. Після купання шкіру потрібно промокнути (не терти!) й одразу нанести пом’якшувальні та зволожувальні засоби.
Для лікування запалення шкіри використовують топічні кортикостероїди та топічні інгібітори кальциневрину – пімекролімус і такролімус.
Топічним засобом для відновлення шкірного бар’єра й усунення подразнення є Бепантен®Сенсідерм, який містить чотири різні зволожувачі (хумектанти):
- пантенол (вітамін B5) – зволожує шкірний бар’єр і забезпечує оптимальні умови для природного процесу регенерації шкіри;
- гліцерин – підтримує утримання води та тривале зволоження;
- пентиленгліколь – вологозв’язувальний агент;
- натрію піролідонкарбонат – природний зволожувальний фактор.
Унікальна формула крему Бепантен® Сенсідерм, виготовлена за ліпідно-ламелярною технологією (Lipid Lamellar Technology™), дає змогу зв’язуватися з ліпідами пошкодженої шкіри, безпечно відновлюючи шкірний бар’єр, запобігаючи втраті води та проникненню алергенів, подразників і патогенів, полегшуючи інтенсивність свербежу [6].
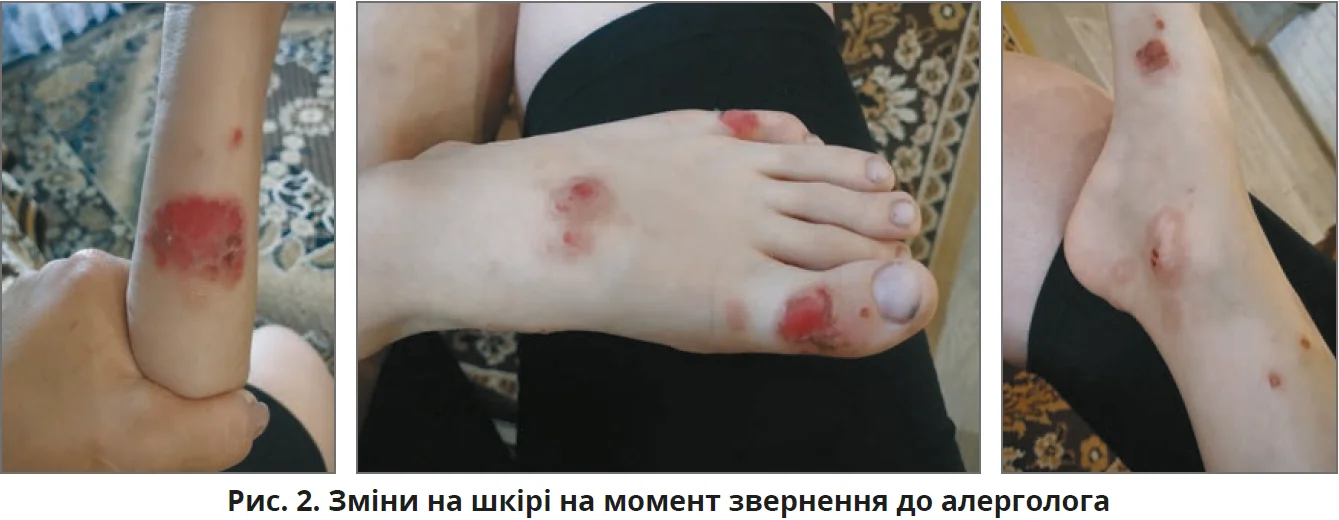
Клінічний випадок
Хлопчик віком 6 років страждає на прояви дерматиту з раннього віку.
Скарги на момент звернення – на висипання по тілу, дуже виражене свербіння, неспокій, порушення сну. Пацієнт відчуває посилення свербіння після купання, тому водні гігієнічні процедури скоротили до 1 разу на 5 днів. Жодні засоби для зволоження шкіри не використовує.
Два останні роки захворювання має тяжкий і неконтрольований перебіг зі свербінням. Амбулаторне лікування (антигістамінні препарати, топічні та системні глюкокортикостероїди) під контролем сімейного лікаря, дерматолога, інфекціоніста – з нестійким ефектом. Обтяжений сімейний анамнез: у батька – бронхіальна астма, у матері – псоріаз.
Діагноз: АД, тяжкий перебіг (SCORAD 64), фаза загострення.
Призначено лікування:
- щоденне купання з емолентом у воді комфортної температури;
- топічний стероїд двічі на добу протягом 7 днів, з них перші 3 дні – вологі примочки;
- Бепантен® Сенсідерм на уражені ділянки двічі на добу.
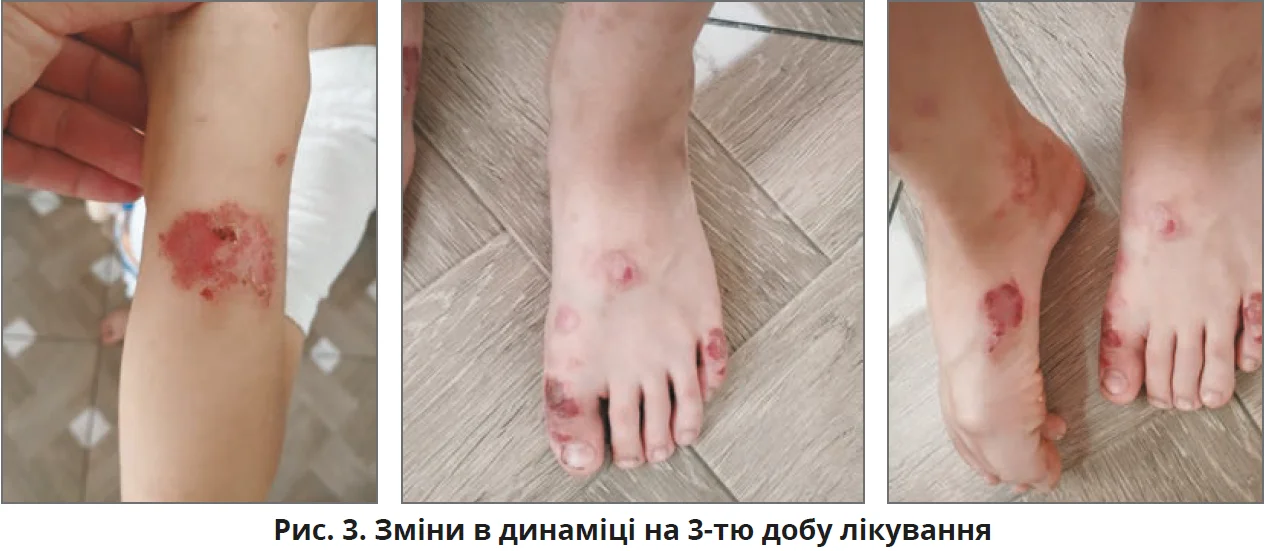
У зв’язку з позитивною динамікою змін на шкірі, покращенням загального самопочуття пацієнта, зменшенням свербіння та нормалізацією сну проведено корекцію на 8-му добу лікування:
- скасування топічного стероїду;
- Бепантен® Сенсідерм двічі на день – продовжити;
- щоденне купання з емолентом.
Із 14-го дня лікування спостерігалося досягнення повного контролю стану й усунення симптому свербіння.
Призначено зовнішнє застосування інгібіторів кальциневрину за проактивною схемою та продовжено догляд емолентами.
Отже, успішна терапія АД є непростим завданням, яке потребує великої уваги лікаря, витримки батьків і має включати комплекс терапевтичних заходів, що підбираються індивідуально та проводяться систематично й тривало.
Ретельний догляд за шкірою дає змогу запобігти транскутанній сенсибілізації та, відповідно, профілактувати розвиток шкірних і респіраторних алергозів.
Література
- Беш Л.В., Беш О.М., Мацюра О.І. Антигістамінні препарати в педіатрії: доказова медицина і реальна клінічна практика. Алергія в дитини. 2019; 23-24: 2-4.
- Brandwein M., Enten Vissoker R., Jackson H., et al. Redefining the role of nutrition in infant food allergy prevention: a narrative review. Nutrients. 2024 Mar 14; 16 (6): 838. doi: 10.3390/nu16060838.
- Boguniewicz M. Atopic dermatitis: best of guidelines and yardstick. Allergy Asthma Proc. 2025; 46 (1): 19-25. doi: 10.2500/aap.2025.46.240087.
- Choi U.E., Deng J., Parthasarathy V., et al. Risk factors and temporal associations of progression of the atopic march in children with early-onset atopic dermatitis. J. Am. Acad. Dermatol. 2025; 92 (4): 732-740. doi: 10.1016/j.jaad.2024.10.107.
- Darlenski R., Kozyrskyj A.L., Fluhr J.W., Caraballo L. Association between barrier impairment and skin microbiota in atopic dermatitis from a global perspective: unmet needs and open questions. J. Allergy Clin. Immunol. 2021 Dec; 148 (6): 1387-1393. doi: 10.1016/j.jaci.2021.10.002.
- Farzam K., Sabir S., O’Rourke M.C. Antihistamines. 2023 Jul 10. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2025 Jan. https://pubmed.ncbi.nlm.nih.gov/30844215.
- Guttman-Yassky E., Renert-Yuval Y., Brunner P.M. Atopic dermatitis. Lancet. 2025; 405 (10478): 583-596. doi: 10.1016/S0140-6736(24)02519-4.
- Hu W., Li H., Zeng L., et al. Data mining in FAERS: association of newer-generation H1-antihistamines with nervous system disorders. BMC Pharmacol. Toxicol. 2024; 25 (1): 95. Published 2024 Dec 18. doi: 10.1186/s40360-024-00822-x.
- Jamalyan K.R., Azaryan H.G. Comparative efficacy of combined antihistamine and montelukast therapy in adult patients with atopic dermatitis. Postepy Dermatol. Alergol. 2024 Feb; 41 (1): 32-40. doi: 10.5114/ada.2023.135759.
- Sroka-Tomaszewska J., Trzeciak M. Molecular mechanisms of atopic dermatitis pathogenesis. Int. J. Mol. Sci. 2021 Apr 16; 22 (8): 4130. doi: 10.3390/ijms22084130.
- Wan J. Changes in the epidemiology of atopic dermatitis: putting them into context. Br. J. Dermatol. 2024 Jan 23; 190 (2): 143-144. doi: 10.1093/bjd/ljad443.
- Wienholtz N.K., Vestergaard C., Deleuran M., et al. Atopisk eksem [Atopic dermatitis]. Ugeskr Laeger. 2025; 187 (14): V10240722. Published 2025 Mar 31.doi: 10.61409/V10240722.