Пробіотик для профілактики антибіотик-асоційованої діареї: вибір згідно з даними доказової медицини та положеннями міжнародних настанов
Переклала канд. мед. наук Тетяна Можина
Сучасна медицина немислима без антибіотикотерапії: антибіотики (АБ) активно призначають лікарі різноманітних спеціальностей для лікування інфекцій дихальних шляхів, захворювань травного та сечостатевого трактів, гінекологічної й андрологічної патологій, для профілактики під час багатьох оперативних утручань. На жаль, застосування таких потужних ліків супроводжується певною кількістю побічних дій, однією з найпоширеніших і найвідоміших є антибіотик-асоційована діарея (ААД).
Поширеність ААД значно різниться залежно від географічного ареалу та популяції хворих: захворюваність на ААД у дітей у США коливається від 6% серед амбулаторних пацієнтів до 80% серед госпіталізованих хворих [17]; у Китаї серед госпіталізованих дітей вона становить 16,80-70,59% [28]; за даними турецьких дослідників, ААД виникає у 8,93% дітей, які перебувають на стаціонарному лікуванні [12]. Найчастіше ААД розвивається в хлопчиків (р=0,027; відносний ризик (ВР) 3,36), у дітей віком від 1 місяця до 3 років (р=0,01; ВР 4,23), пацієнтів, які додатково отримують ібупрофен (р=0,044; ВР 2,63) [12], а також в осіб похилого та літнього віку [2, 27]. «АБ можуть збільшувати наслідки кишкового дисбактеріозу в уразливих групах населення, котрі вже мають його ознаки», – підкреслюють відомі вчені [6, 13].
ААД: від дефініції до патогенетичного лікування
Відповідно до одного з перших визначень ААД виникає за тривалого застосування АБ і призводить до кишкового дисбіозу [3]. Сучасні погляди дещо змінилися: нині підкреслюють, що кишківник являє собою домівку для великої кількості мікробів, включаючи бактерії, віруси, гриби, еукаріоти й археї, які разом утворюють складну гастроінтестинальну мікробіоту, котра відіграє важливу роль у підтримці здоров’я, та що саме порушення рівноваги в цьому складному мікробіомі на тлі прийому АБ спочатку призводить до виникнення дисбіозу, на тлі якого потім і розвивається діарея [28]. Зі збільшенням ступеня дисбіозу клінічні прояви ААД прогресують від легкої діареї до гострих і тяжких захворювань, як-от псевдомембранозний коліт за умов інфікування Clostridium difficile [3]. Нині відомо, що тяжкість клінічних проявів ААД пов’язана з типом призначеного АБ, спектром його дії та тривалості застосування, вихідним станом здоров’я пацієнта й мікробіологічними характеристиками патогенів [10]. Одним з ефективних способів профілактики та лікування ААД вважають усунення явищ дисбіозу за допомогою таких біологічно активних агентів, як пробіотики (живі мікроорганізми, котрі при введенні в достатній кількості можуть давати користь для здоров’я хазяїна) [8, 16, 21, 23]. Деякі вчені вважають, що з цією метою також можуть бути застосовані пребіотики (субстрати, які вибірково утилізуються мікроорганізмами хазяїна, даючи користь для здоров’я), синбіотики (суміші, що складаються з пробіотиків і пребіотиків) і постбіотики (препарати неживих мікроорганізмів та їхніх компонентів, які дають користь для здоров’я хазяїна). Проте впевнену доказову базу щодо доцільності та безпечності застосування при ААД мають усього два пробіотичні штами: Lacticaseibacillus rhamnosus і Saccharomyces cerevisiae var. boulardii (які раніше, до оновлення класифікації, називалися Lactоbacillus rhamnosus і Saccharomyces boulardii відповідно) [8, 16, 21, 23]. Причому велика кількість останніх міжнародних настанов наголошує на доцільності використання S. boulardii як у дітей, так і в дорослих [8, 16, 21, 23].
S. boulardii: властивості й особливості
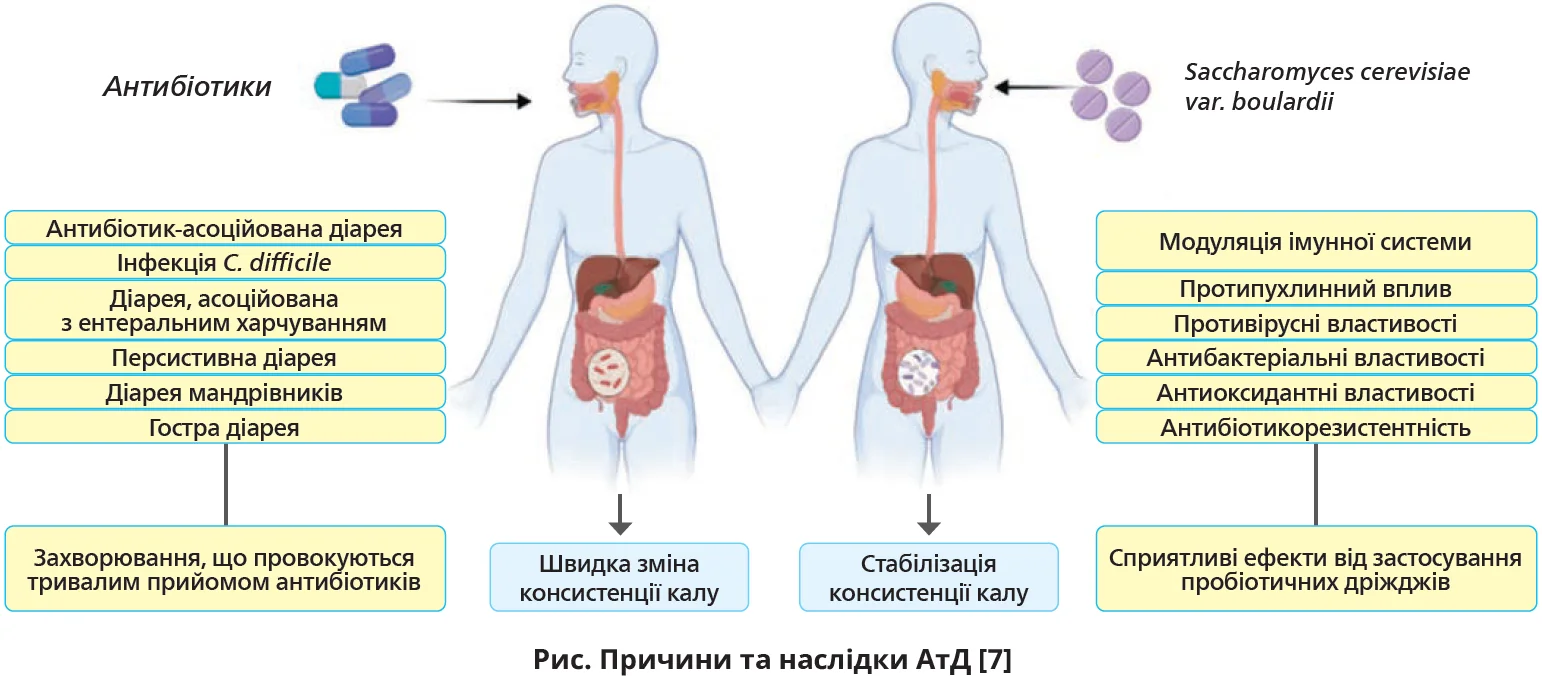
Зазначене одностайне рішення різних авторитетних міжнародних товариств пояснюється великою кількістю доказових даних, що яскраво підтверджують доцільність цієї рекомендації. Ключом, який відкриває скриньку такого безпрецедентного успіху S. boulardii, є унікальні властивості цього пробіотика, його значні біотерапевтичні переваги та добрий профіль безпеки [1, 20]. S. boulardii, як і велика кількість інших пробіотиків, допомагає поліпшити та відновити кишковий мікробіом, конкуруючи з патогенами за поживні речовини, ріст і адгезію, зміцнює слизовий бар’єр кишківника, сприяючи виникненню протизапального ефекту та модуляції імунної системи [4]. З іншого боку, S. boulardii одночасно чинить антибактеріальний, противірусний, антиканцерогенний, антиоксидантний, протизапальний та імуномодулювальний впливи, що дає змогу вважати ці дріжджі потужним біотерапевтичним засобом (рис.) [1].
Особливо цінують S. boulardii за її здатність протидіяти формуванню біоплівок C. difficile, зменшувати товщину біоплівки порівняно з іншими одновидовими бактеріями [14]. Інші властивості S. boulardii, як-от оптимальна температура росту 37 °C, природна стійкість до АБ, кислотності шлункового соку та протеолізу, також зробили значний внесок у високу клінічну ефективність цього пробіотика [19].
Комбінація S. boulardii та L. rhamnosus: доведені переваги
Добре відомо, що пробіотичні штами L. rhamnosus і S. boulardii здатні рости, розмножуватися в товстому кишківнику після прийому АБ та відновлювати кишкову мікробіоту, проте нещодавно було опубліковано дані, які доводять значне посилення протидіарейної активності за їх одночасного прийому [7, 18].
Факт пригнічення синтезу коротколанцюгових жирних кислот, інгібування росту та часткового знищення популяцій корисних бактерій із родів Bacteroidetes, Firmicutes, Bifidobacterium на тлі прийому АБ, особливо широкого спектра дії, нині не викликає жодних сумнівів [7]. Доведено, що одночасне застосування комбінації L. rhamnosus GG та/або S. boulardii супроводжується стимулювальним впливом на найпоширеніші групи бактерій у бактеріальній спільноті товстого кишківника, відновленням умісту коротколанцюгових жирних кислот, значним збільшенням чисельності Bifidobacteriaceae, причому S. boulardii захищає та сприяє виживанню L. rhamnosus GG під час антибіотикотерапії [7]. Вчені вважають, що комбіноване застосування L. rhamnosus GG та S. boulardii є добрим способом обмеження шкідливого впливу АБ (амоксициліну / клавуланової кислоти) на кишковий мікробіом [7].
Синергічна взаємодія L. rhamnosus і S. boulardii доведена в іншому експериментально-клінічному дослідженні: встановлено, що комбінація цих пробіотиків «добре імітує вплив рідної мікробіоти та відтворює природні умови товстого кишківника в дорослих і дітей» [18]. Автори роботи зазначили, що обидва штами зростають разом, не проявляючи антагоністичних ефектів, а їх спільне культивування зумовлює збільшення синтезу бутирату (стимульованого L. rhamnosus GG), пропіонату (стимульованого S. boulardii) й етанолу (продукованого S. boulardii) порівняно з контролем. Окрім цього, комбінація L. rhamnosus GG та S. boulardii демонструє сильнішу протипатогенну активність щодо ентеротоксигенної Escherichia coli, обмежуючи її здатність продукувати ентеротоксини порівняно з окремим застосуванням кожного штаму. Одночасне використання обох штамів дає змогу знизити кількість патогенної E. coli, її токсинів на 40-57% у дітей і дорослих, сприяючи відновленню функціонування кишкової мікробіоти та запобігаючи інвазії патогенів під час антибіотикотерапії [18].
S. boulardii та L. rhamnosus у боротьбі з ААД: доказові дані
Ефективність S. boulardii та L. rhamnosus у профілактиці ААД настільки добре доведена, що нині ми можемо навести тільки дані тих метааналізів і систематичних оглядів, що були опубліковані протягом останніх 3 років. Один із них підтвердив ефективність зазначених пробіотичних штамів у профілактиці ААД та підкреслив, що S. boulardii запобігає появі ААД в усіх групах пацієнтів – як амбулаторних, так і стаціонарних, як у дітей, так і в дорослих, тоді як L. rhamnosus GG краще захищає амбулаторних пацієнтів різного віку [22]. Автори систематичного огляду дійшли такого висновку: «Для профілактики ААД доцільно вибирати пробіотик із доведеною ефективністю, наприклад S. boulardii або L. rhamnosus GG» [22]. Метааналіз, представлений експертами Кокранівського товариства, підтримує доцільність застосування пробіотиків як профілактики ААД та наполягає на використанні високих доз (≥5 млрд КУО/добу) [9]. Інший метааналіз демонструє додаткові переваги зазначених пробіотиків: вони не тільки вірогідно знижують поширеність ААД й інфекції C. difficile в дітей, госпіталізованих у відділення невідкладної допомоги, а й сприяють зниженню частоти виникнення пневмонії при проведенні штучної вентиляції легень [5].
Нещодавно представлено велику за обсягом наукову роботу – огляд даних 20 систематичних оглядів, у яких аналізувалася ефективність пробіотиків у профілактиці та лікуванні ААД у дітей [24].
Це масштабне дослідження підтвердило, що застосування високих доз (5-40 млрд КУО/добу) пробіотиків чинить статистично вірогідний вплив, запобігаючи розвитку ААД, при цьому найефективнішими визнані тільки два пробіотичні штами: L. rhamnosus і S. boulardii [24].
Ерадикація Helicobacter pylori: місце для пробіотиків
Проведення ерадикації Н. pylori є одним із найпоширеніших приводів для використання АБ у гастроентерологічній практиці. Введення пробіотика S. boulardii дає змогу не тільки запобігти розвитку ААД, а й покращити ефективність ерадикації.
За даними одноцентрового проспективного рандомізованого контрольованого дослідження (РКД), додавання S. boulardii до потрійної антигелікобактерної терапії на основі антифлоксацину (представник четвертого поколінням фторхінолонів, відносно нещодавно розроблений у Китаї) сприяє зменшенню тривалості та частоти виникнення діареї порівняно з контролем (р<0,001) [11]. В іншому багатоцентровому РКД (n=360) доведено, що застосування S. boulardii разом із потрійною схемою ерадикації дає змогу вірогідно знизити частоту загальних побічних ефектів (27,8 проти 38,5%; р=0,034), діареї (11,2 проти 21,2%; р=0,012), тривалості діареї (5,0 проти 7,7 дня; p=0,032) та частоти виникнення тяжкої діареї (4,7 проти 10,1%; p=0,04) порівняно з контролем [26].
Метааналіз 18 досліджень (n=3592) продемонстрував, що прийом S. boulardii асоційований із підвищенням ефективності ерадикації (ВР 1,09; 95% довірчий інтервал (ДІ) 1,05-1,13), зменшенням частоти виникнення загальних побічних ефектів (ВР 0,47; 95% ДІ 0,36-0,61), діареї (ВР 0,33; 95% ДІ 0,23-0,47), запорів (ВР 0,37; 95% ДІ 0,23-0,57) [29]. Окрім того, частота необхідності дострокового припинення ерадикаційної терапії в групі S. boulardii була значно нижчою, ніж у групі контролю (ВР 0,33; 95% ДІ 0,16-0,69; р=0,003) [29]. Інший метааналіз 11 РКД (n=724) констатував, що прийом Lactobacillus під час ерадикації H. pylori асоційований із підвищенням імовірності видалення патогенної бактерії (ВР 1,16; 95% ДІ 1,08-1,25; р<0,0001) та зниженням частоти порушення смаку (ВР 0,36; 95% ДІ 0,17-0,74; р=0,005) [25].
COVID-19: іще один привід для профілактики ААД
Нещодавно перелік станів, за яких застосовується антибіотикотерапія з використанням АБ широкого спектра дії, поповнився тяжким перебігом коронавірусної хвороби (COVID-19). Поки що немає систематичних оглядів або метааналізів, які розкривають доцільність профілактичного застосування пробіотиків, але вже опубліковано результати РКД, в якому доведено, що ад’ювантне призначення S. boulardii (500 мг/добу) протягом 10 діб асоційоване зі зменшенням частоти розвитку діареї (13,3%; 95% ДІ 4,5-22,2) порівняно з плацебо (30,0%; 95% ДІ 18,1-41,9) [15]. Прийом S. boulardii сприяв значному зниженню ризику діареї в госпіталізованих хворих на COVID-19, які отримували антибіотикотерапію (співвідношення шансів (СШ) 0,35; 95% ДІ 0,14-0,90; р=0,03) та скороченням тривалості діареї (3,12 дня; 95% ДІ 2,58-3,66) порівняно з плацебо (5,27 дня; 95% ДІ 4,22-6,32; р=0,011). Використання S. boulardii супроводжувалося скороченням тривалості перебування в стаціонарі (11,6833 дня; 95% ДІ 11,20-12,16) порівняно з плацебо (12,73 дня; 95% ДІ 12,13-13,33; p=0,01) [15].
Міжнародні практичні настанови
Дорослі
Відомі міжнародні товариства рекомендують використання пробіотиків для профілактики ААД. Зокрема, оновлення настанови Всесвітньої гастроентерологічної організації (WGO) «Пробіотики та пребіотики», представлене цьогоріч, передбачає застосовування пробіотиків для профілактики й лікування ААД у дорослих, причому перше й друге місця в рекомендаціях займають, відповідно, штами S. boulardii та L. rhamnosus GG, які експерти рекомендують призначати в дозі ≥5 млн КУО/добу протягом усього курсу антибіотикотерапії [8]. «Застосування цих пробіотичних штамів дає змогу знизити ризик розвитку ААД», – авторитетно стверджують представники WGO, зважаючи на дані доказової медицини. Зазначена настанова також пропонує таку схему застосування L. rhamnosus для профілактики ААД: 2×1010 КУО 2 рази на добу [8].
Консенсусний звіт Маастрихт VI / Флоренція з лікування інфекції H. pylori [16], як й італійські рекомендації з цього самого питання [21], передбачають застосування окремих пробіотиків для профілактики ААД при проведенні ерадикаційної терапії, причому експерти Маастрихт VI / Флоренція обмежують коло можливих пробіотичних штамів, зосереджуючи увагу лікарів-практиків саме на призначенні S. boulardii та Lactobacillus як найефективніших пробіотиків «у зменшенні побічних ефектів, пов’язаних із застосуванням АБ» [16].
Діти
Європейське товариство педіатричної гастроентерології, гепатології та харчування (ESPGHAN) цьогоріч представило рекомендації з використання пробіотиків у разі гастроентерологічних захворювань, у якому таким чином визначає свою позицію з цього питання (табл.).
Бажана: ефективна комбінація для профілактики ААД
На українському фармацевтичному ринку представлено комбінований пробіотик, який містить штами S. boulardii та L. rhamnosus, рекомендовані провідними міжнародними товариствами для профілактики ААД, – Бажана (виробник – Sopharma). У кожній капсулі Бажани міститься 2,5×109 КУО S. boulardii й 1×109 КУО L. rhamnosus, поєднання котрих,як свідчать дані доказової медицини, посилює виразність протидіарейної дії. Згідно з міжнародними настановами з метою профілактики ААД варто приймати щонайменше 2 капсули Бажани задля досягнення потрібної концентрації S. Boulardii (≥5 млрд КУО/добу) 1 раз на добу. Починати прийом Бажани слід одночасно з початком антибіотикотерапії та продовжувати протягом усього курсу застосування протимікробних засобів. За потреби тривалість прийому Бажани може бути подовжена до 1 місяця.
Висока ефективність, безпечність і добрий профіль переносимості дають змогу призначати Бажану для профілактики ААД як у дорослій, так і в педіатричній і геріатричній популяціях. Наявність у складі Бажани L. Acidophilus (2,5×109 КУО) та пребіотика інуліну (25 мг), що підсилює біологічну активність мікрофлори, можна вважати додатковою перевагою, яка допомагає швидко відновити кількість корисних бактерій у кишковому мікробіомі.
Висновки
Згідно з даними доказової медицини пробіотики є ефективним і безпечним способом профілактики ААД, але тільки два пробіотичні штами рекомендовані WGO й ESPGHAN – S. boulardii та L. rhamnosus. Консенсусний звіт Маастрихт VI / Флоренція також наполягає на застосуванні S. boulardii та Lactobacillus у дорослих при проведенні ерадикаційної терапії; за потреби лікування інфекції H. pylori в дітей експерти ESPGHAN радять віддавати перевагу S. boulardii. Комбінація S. boulardii та L. rhamnosus, яка міститься у високодозовому синбіотику Бажана, забезпечує посилення протидіарейного ефекту та робить доцільним його застосування в схемах профілактики/лікування ААД у дітей, дорослих і літніх осіб, які перебувають як на амбулаторному, так і на стаціонарному лікуванні.
Література
- Abid R., Waseem H., Ali J., et al. Probiotic yeast Saccharomyces: back to nature to improve human health. J. Fungi (Basel). 2022; 8 (5): 444. doi: 10.3390/jof8050444.
- Barbosa M.L.L., Albano M.O., Martins C., et al. Role of probiotics in preventing Clostridioides difficile infection in older adults: an integrative review. Front. Med. (Lausanne). 2023; 10: 1219225. doi: 10.3389/fmed.2023.1219225.
- Bartlett J.G. Clinical practice. Antibiotic-associated diarrhea. N. Engl. J. Med. 2022; 346: 334-339. doi: 10.1056/NEJMcp011603.
- Choudhury J., Makkar A., Sharma V., et al. A real-world perspective of co-amoxiclav prescription pattern with probiotics for pediatric patients with respiratory tract infections: results of quantitative and qualitative approach in Indian outpatient settings. Cureus. 2023; 15 (3): e36269. doi: 10.7759/cureus.36269.
- Darbandi A., Banar M., Koupaei M., et al. Clinical efficacy of probiotics in prevention of infectious diseases among hospitalized patients in ICU and non-ICU wards in clinical randomized trials: a systematic review. Health Sci. Rep. 2023; 6 (8): e1469. doi: 10.1002/hsr2.1469.
- Doar N.W., Samuthiram S.D. Qualitative analysis of the efficacy of probiotic strains in the prevention of antibiotic-associated diarrhea. Cureus. 2023; 15 (6): e40261. doi: 10.7759/cureus.40261.
- Duysburgh C., Van den Abbeele P., Morera M., et al. Lacticaseibacillus rhamnosus GG and Saccharomyces cerevisiae boulardii supplementation exert protective effects on human gut microbiome following antibiotic administration in vitro. Benef. Microbes. 2021; 12 (4): 59-73. doi: 10.3920/BM2020.0180.
- Guarner F., Khan A.G., Garisch J., et al. World Gastroenterology Organisation Global Guidelines: Probiotics and Prebiotics. October 2011. J. Clin. Gastroenterol. 2023. Available at: https://www.worldgastroenterology.org/guidelines/probiotics-and-prebiotics/probiotics-and-prebiotics-english.
- Guo Q., Goldenberg J.Z., Humphrey C., et al. Probiotics for the prevention of pediatric antibiotic-associated diarrhea. Cochrane Database Syst. Rev. 2019; 4 (4): CD004827. doi: 10.1002/14651858.CD004827.pub5.
- Hayes S.R., Vargas A.J. Probiotics for the prevention of pediatric antibiotic-associated diarrhea. Explore (NY). 2016; 12: 463-466. doi: 10.1016/j.explore.2016.08.015.
- He X.J., Wang X.L., Sun D., et al. The efficacy and safety of Saccharomyces boulardii in addition to antofloxacin-based bismuth quadruple therapy for Helicobacter pylori eradication: a single-center, prospective randomized-control study. Therap. Adv. Gastroenterol. 2023; 16: 17562848221147763. doi: 10.1177/17562848221147763.
- Kaya G., Usta D., Sag E., et al. Incidence and risk factors for antibiotic-associated diarrhea among hospitalized children. Pediatr. Infect. Dis. J. 2023; 42 (9): 745-749. doi: 10.1097/INF.0000000000003994.
- Kesavelu D., Jog P. Current understanding of antibiotic-associated dysbiosis and approaches for its management. Ther. Adv. Infect.
Dis. 2023; 10: 20499361231154443. doi: 10.1177/20499361231154443. - Lacotte P.A., Simons A., Bouttier S., et al. Inhibition of in vitro Clostridioides difficile biofilm formation by the probiotic yeast Saccharomyces boulardii CNCM I-745 through modification of the extracellular matrix composition. Microorganisms. 2022; 10 (6): 1082. doi: 10.3390/microorganisms10061082.
- Maev I.V., Andreev D.N., Sokolov P., et al. Efficacy of Saccharomyces boulardii CNCM I-745 probiotic drug in the prevention and treatment of diarrhea in hospitalized patients with new coronavirus infection COVID-19. Ter. Arkh. 2022; 94 (10): 1163-1170. doi: 10.26442/00403660.2022.10.201881.
- Malfertheiner P., Megraud F., Rokkas T., et al. European Helicobacter and Microbiota Study Group. Management of Helicobacter pylori infection: the Maastricht VI / Florence consensus report. Gut. 2022: gutjnl-2022-327745. doi: 10.1136/gutjnl-2022-327745.
- McFarland L.V., Ozen M., Dinleyici E. Comparison of pediatric and adult antibiotic-associated diarrhea and Clostridium difficile infections. World J. Gastroenterol. 2016; 22: 3078-3104. doi: 10.3748/wjg.v22.i11.3078.
- Moens F., Duysburgh C., van den Abbeele P., et al. Lactobacillus rhamnosus GG and Saccharomyces cerevisiae boulardii exert synergistic antipathogenic activity in vitro against enterotoxigenic Escherichia coli. Benef. Microbes. 2019; 10 (8): 923-935. doi: 10.3920/BM2019.0064.
- Pais P., Almeida V., Yılmaz M., et al. Saccharomyces boulardii: what makes it tick as successful probiotic? J. Fungi (Basel). 2020; 6 (2): 78. doi: 10.3390/jof6020078.
- Puri A.S. The role of yeast probiotics in gastrointestinal conditions: an overview. J. Assoc. Physicians India. 2023; 71 (4): 11-12. doi: 10.5005/japi-11001-0235.
- Romano M., Gravina A.G., Eusebi L., et al. Management of Helicobacter pylori infection: Guidelines of the Italian Society of Gastroenterology (SIGE) and the Italian Society of Digestive Endoscopy (SIED). Dig. Liver Dis. 2022; 54 (9): 1153-1161. doi: 10.1016/j.dld.2022.06.019.
- Storr M., Stengel A. Klinische Evidenz zu Probiotika in der Prävention einer Antibiotika-assoziierten Diarrhö: Systematischer Review. MMW Fortschr Med. 2021; 163 (Suppl. 4): 19-26. doi: 10.1007/s15006-021-9762-5.
- Szajewska H., Canani R.B., Domellöf M., et al. Probiotics for the management of pediatric gastrointestinal disorders: position paper of the ESPGHAN special interest group on gut microbiota and modifications. J. Pediatr. Gastroenterol. Nutr. 2023; 76 (2): 232-247. doi: 10.1097/MPG.0000000000003633.
- Yang Q., Hu Z., Lei Y., et al. Overview of systematic reviews of probiotics in the prevention and treatment of antibiotic-associated diarrhea in children. Front. Pharmacol. 2023; 14: 1153070. doi: 10.3389/fphar.2023.1153070.
- Yu M., Zhang R., Ni P., et al. Efficacy of Lactobacillus-supplemented triple therapy for H. pylori eradication: a meta-analysis of randomized controlled trials. PLoS One. 2019; 14 (10): e0223309. doi: 10.1371/journal.pone.0223309.
- Zhao L., Zhang Y., Wang Y., et al. Gut microbiota diversity of hospitalized older adult patients with and without antibiotic-associated diarrhea. Aging Clin. Exp. Res. 2023; 35 (7): 1541-1555. doi: 10.1007/s40520-023-02436-5.
- Zhao Y., Yang Y., Aruna, et al. Saccharomyces boulardii combined with quadruple therapy for Helicobacter pylori eradication decreased the duration and severity of diarrhea: a multi-center prospective randomized controlled trial. Front. Med. (Lausanne). 2021; 8: 776955. doi: 10.3389/fmed.2021.776955.
- Zheng Y., Wu Q., Fang F., et al. Expert consensus on diagnosis, treatment and prevention of antibiotic-associated diarrhea in children. Chin. J. Appl. Clin. Pediatr. 2021; 36: 424-430. doi: 10.3760/cma.j.cn101070-20210201-00137.
- Zhou B.G., Chen L.X., Li B., et al. Saccharomyces boulardii as an adjuvant therapy for Helicobacter pylori eradication: a systematic review and meta-analysis with trial sequential analysis. Helicobacter. 2019; 24 (5): e12651. doi: 10.1111/hel.12651.