Пробіотики в лікуванні атопічного дерматиту й алергічного риніту: чи є місце для них?
Переклала й адаптувала канд. мед. наук Тетяна Можина
Протягом останніх декількох десятиліть статистичні звіти констатують значне зростання поширеності алергічних захворювань: майже 20% населення земної кулі страждає на атопічний дерматит (АД), харчову алергію (ХА), бронхіальну астму (БА), алергічний риніт (АР) [1].
Згідно з даними Європейської академії алергології та клінічної імунології (EAACI), 30% європейців мають ознаки алергії, при цьому 50% клінічних випадків, пов’язаних з алергією, залишаються недіагностованими [2].
Алергія, одна з хвороб цивілізації, заважає переважно мешканцям великих міст: понад 40% дітей, що мешкають у мегаполісах, страждають від алергії, майже 50% із них не мають установленого діагнозу та не отримують потрібні ліки [3]. Подібні дані підтверджують вітчизняні вчені, констатуючи зростання поширеності АД й АР у мешканців Києва та Київської області [4]. Суттєвий негативний вплив алергічних захворювань на систему охорони здоров’я, суспільство пов’язують зі значними прямими й опосередкованими витратами на лікування, частою хронізацією, негативним впливом на якість життя, високим рівнем госпіталізацій, пропусками занять у школі, високим рівнем тимчасової непрацездатності [1].
Патогенетичний зв’язок, який поєднує всі перелічені алергічні захворювання, іноді об’єднують у межах теорії «атопічного маршу», згідно з якою ХА й АД є початком атопії, а через декілька років вони трансформуються в БА чи АР [5]. Спричиняти появу ХА, першої ластівки атопічного маршу, може не тільки прийом антибіотиків протягом вагітності /
перших місяців життя, спосіб розродження, тип вигодовування [6], а й обтяжений сімейний анамнез щодо атопії (відносний ризик, ВР 1,893; 95% довірчий інтервал, ДI 1,313-2,730), ХА (ВР 2,096; 95% ДI 1,686-2,594), АД (ВР 1,954; 95% ДІ 1,645-2,322), БА (ВР 1,516; 95% ДI 1,370-1,678) АР / алергічного кон’юнктивіту (ВР 1,287; 95% ДI 1,191-1,392) [7].
Патогенетичні механізми АД й АР
Усі алергічні захворювання мають спільні патогенетичні механізми: на тлі генетично зумовленої схильності розвивається невідповідна імунна відповідь із залученням Т-хелперів (Th) 2 типу – клітин, що реагують на антигени навколишнього середовища чи їжі [8]. Саме активація та диференціювання специфічних Th2-клітин свідчить про ініціювання каскаду імунологічних реакцій, які призведуть до вироблення антигеноспецифічного імуноглобуліну Е (IgE) з наступною IgE-залежною активацією тучних клітин, залученням еозинофілів і синтезом прозапальних цитокінів (інтерлейкінів – ІЛ-4, ІЛ-5, ІЛ-13) [8]. Повторний вплив алергенів на організм зумовить перехресне зв’язування IgE на поверхні тучних клітин, вивільнення медіаторів гіперчутливості, зокрема гістаміну, та появу клінічної симптоматики алергії [8].
Така особлива й вирішальна роль Th2-клітин, цитокінів у розвитку атопії зробила їх своєрідними мішенями для розроблення ефективних способів лікування алергічних захворювань [1]. Серед різноманітних препаратів, здатних інгібувати активацію Th2-клітин і синтез прозапальних цитокінів, особливу увагу приділяють пробіотикам. Вважають, що основний механізм дії пробіотиків при алергії полягає у відновленні балансу між пулами Th1/Th2, вмістом прозапальних і протизапальних цитокінів, індукцією популяції Treg та їх активації [6, 9]. До іншого специфічного механізму дії пробіотиків відносять зменшення вмісту алергеноспецифічного IgE та збільшення концентрації коротколанцюгових жирних кислот; доведено також їхню здатність зміцнювати й підтримувати цілісність епітеліального бар’єра, збільшувати продукцію субстанцій із протимікробними властивостями, знижувати бактеріальну транслокацію та конкуренто інгібувати виживання патогенів (рис. 1) [6, 9].
Наявні доказові дані дали можливість експертам Всесвітньої організації алергії (World Allergy Organization, WAO) представити у 2015 р. документ «Настанова щодо профілактики алергічних захворювань: пробіотики», в якому вони схвалили та рекомендували прийом пробіотиків вагітним, жінкам, що годують, і новонародженим із групи високого ризику алергії «через наявність чистої вигоди в запобіганні розвитку екземи» [10]. Настанова Всесвітньої гастроентерологічної організації (World Gastroenterology Organisation, WGO) «Пробіотики та пребіотики» також визнає доцільність використання пробіотиків у осіб з АД [11].
Нещодавно опубліковані систематичні огляди та метааналізи доводять здатність пробіотиків зменшувати тяжкість перебігу АД, знижувати значення індексу SCORAD – SCORing Atopic Dermatitis (середня різниця, СР -7,90; 95% ДІ від -7,25 до -6,92; р<0,00001) і поліпшувати якість життя (СР -7,68; 95% ДІ від -14,08 до -1,29; р=0,02) [12]. Подібні дані отримано в інших метааналізах, які також констатують покращення індексу SCORAD і зменшення інтенсивності свербежу [13]. Прийом пробіотика асоціюється зі зменшенням тяжкості захворювання в короткостроковій (стандартизована різність
середніх, СРС 0,63; 95% ДІ 0,02-1,25) і довгостроковій (СРС 1,57; 95% ДІ 0,66-2,49) перспективах і сприяє вірогідному покращенню якості життя хворих на АД (СРС 0,74; 95% ДІ 0,39-1,09) протягом тривалого періоду порівняно з контролем [14]. Доведено, що застосування пробіотиків асоційовано зі зменшенням поширеності АД у дітей (ВР 0,86; 95% ДІ 0,78-0,95) і зниженням імовірності розвитку цього різновиду атопії в новонароджених, якщо їхня мати приймали пробіотик протягом вагітності [15]. Продемонстровано як профілактичну (ВР 0,70; 95% ДІ 0,57-0,84; р=0,0002), так і терапевтичну (зважена середня різниця, ЗСР -7,23; 95% ДІ від -10,59 до -3,88; р<0,0001) ефективність пробіотиків щодо АД [16].
Слід відзначити декілька особливостей новітніх метааналізів: на відміну від ранніх робіт вони переконливо доводять доцільність застосування багатокомпонентних пробіотиків завдяки їхній більшій ефективності порівняно з монокомпонентними пробіотичними препаратами [16, 17]. «Лише змішані пробіотичні штами сприяють значному зниженню захворюваності на AД», – стверджують W. Jiang і співавт. [16]. Іншою характерною рисою сучасних систематичних оглядів є встановлення умов ефективної профілактики АД у новонароджених: із цією метою треба не просто давати дитині пробіотик від моменту її народження, а призначити пробіотичні штами матері впродовж останніх тижнів вагітності, а потім давати народженому малюкові [16, 18] протягом перших 6 місяців життя [18].
Серед великої кількості пробіотичних штамів найефективнішими в подоланні явищ АД визнано штами Lactobacillus rhamnosus: метааналіз 11 рандомізованих контрольованих досліджень довів, що застосування L. rhamnosus асоціюється зі зниженням ризику розвитку атопічної екземи в дітей віком ≤2 років (ВР 0,60; 95% ДІ 0,47-0,75; р<0,00001) і 6-7 років (ВР 0,62; 95% ДІ 0,50-0,75; р<0,00001) [19].
Алергічний риніт
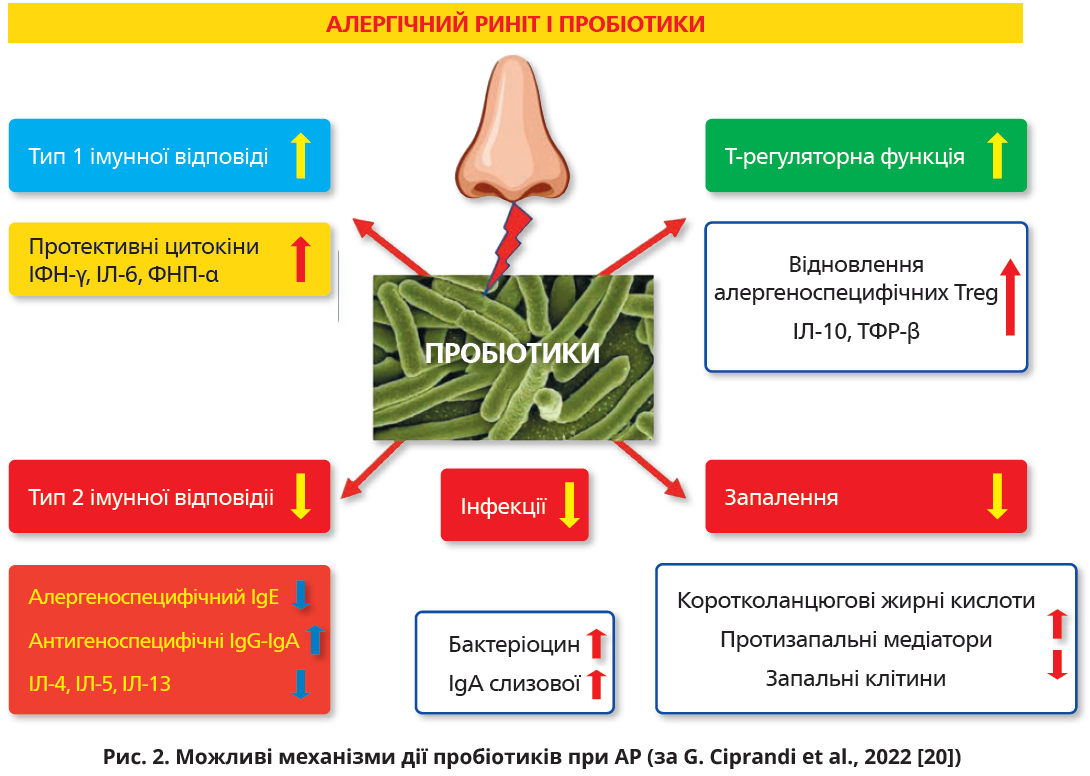
Попри те що поки жодна міжнародна настанова не містить положень за чи проти застосування пробіотиків у хворих на АР, систематичні огляди та метааналізи доводять доцільність включення пробіотичних штамів у схеми терапії АР. Протягом 2022 р. опубліковано п’ять метааналізів і декілька оглядів, що розкривають механізми дії (рис. 2) й ефективність пробіотиків у лікуванні АР
як у дорослих, так і в дітей [20-23].
В одному з них, який ґрунтується на результатах 28 досліджень, стверджується, що прийом пробіотиків асоційований із вірогідним нівелюванням клінічних ознак АР у дорослих (СРС -0,29; 95% ДІ
від -0,44 до -0,13; р=0,0003), покращенням якості життя згідно з опитувальником Rhinoconjunctivitis Quality of Life Questionnaire (RQLQ) порівняно з контролем (СРС -0,64; 95% ДІ від -0,79 до -0,49; р<0,00001) завдяки нормалізуванню співвідношення Th1/Th2 (СР -2,47; 95% ДІ від -3,27 до -1,68; р<0,00001) [21]. Інший метааналіз 30 рандомізованих контрольованих досліджень (n=2708) констатував вірогідний вплив пробіотиків на значення опитувальника RQLQ (СР -9,43; р<0,00001), вираженість назальних симптомів як за RQLQ (СР -1,52; р=0,03), так і за шкалою Rhinitis Total Symptom Score – RTSS (СР -1,96; р=0,02) порівняно з плацебо [22].
Призначення пробіотиків дітям, хворим на АР, сприяє нівелюванню назальних симптомів захворювання (ВР 1,21; 95% ДІ 1,04-1,40; р=0,01), зниженню показників шкали TNSS (ЗСР 2,58; 95% ДІ від -2,77 до -2,39; р<0,00001) і загальної кількості балів за опитувальником Pediatric RQLQ (PRQLQ), зменшенню частоти виникнення симптомів АР (ЗСР -9,51; 95% ДІ від -10,34 до -8,69; р<0,00001) і рівня занепокоєння (ЗСР -9,27; 95% ДІ від -10,13 до -8,41; р<0,00001) [23]. Крім цього, прийом пробіотиків асоціюється зі зниженням сироваткового вмісту IЛ-4 (ЗСР -13,86 нг/л; 95% ДІ від -15,92 до -11,81; р<0,00001), IЛ-6 (ЗСР -13,70 пг/мл; 95% ДІ від -16,34 до -11,07; р<0,00001) та IЛ-17 (ЗСР -5,41 пг/мл; 95% ДІ від -7,29 до -3,52; р<0,00001) і зростанням рівнів ІФН-γ (ЗСР 9,08 нг/л; 95% ДІ 8,10-10,06; р<0,00001) та IЛ-10 (ЗСР 7,82 пг/мл; 95% ДІ 5,01-10,63; р<0,00001) у сироватці крові. Застосування пробіотиків дає змогу знизити тривалість використання цетиризину в дітей з АР (ЗСР -2,88 дня; 95% ДІ від -4,50 до -1,26; р<0,0005) [23].
Незважаючи на такий прискіпливий інтерес до пробіотиків, автори метааналізів не змогли однозначно визначити найефективніші пробіотичні штами, але підкреслили потужний терапевтичний потенціал L. rhamnosus в ад’ювантній терапії АР [20].
Бажана – пробіотик для ад’ювантної терапії АД й АР
З огляду на положення настанов WAO та WGO [10, 11], результати метааналізів і систематичних оглядів [16, 17, 19, 20], ефективна пробіотична терапія при АД й АР ґрунтується на призначенні комбінованих пробіотичних препаратів, одним з основних активних компонентів яких мають бути штами L. rhamnosus.
Серед великої кількості пробіотичних засобів слід виокремити синбіотик Бажана (фірма-виробник – Sopharma), який містить суміш пробіотичних штамів L. rhamnosus, L. acidophilus, ліофілізовані дріжджі Saccharomyces boulardii та пребіотик інулін. L. rhamnosus разом із L. acidophilus зменшують синтез прозапальних цитокінів, сприяють збільшенню концентрації протективних цитокінів, зниженню рівня антигеноспецифічних IgE [20]. Встановлено, що молочнокислі бактерії L. rhamnosus зменшують поширеність АД [19], мінімізують явища ХА за непереносимості коров’ячого молока [24], покращують стан хворих на АР [20], сприяють кращому засвоєнню поживних речовин і розмноженню корисних бактерій, підтримують травлення та нормалізують активність імунної системи [25]. Наявність у Бажані пробіотичних штамів S. boulardii надає препарату прямі протимікробні властивості, які проявляються у виведенні патогенних мікроорганізмів із кишківника та створенні умов для розмноження власної сапрофітної мікрофлори [25]. Пребіотик інулін підтримує та підсилює дію пробіотиків. Бажана має дві форми випуску (капсули, порошок-саше), які можуть призначатися дорослим і дітям від 3 років [25]. Ураховуючи склад та особливості дії пробіотичних штамів, синбіотик Бажана можна включати в схеми лікування хворих на АД, АР як ефективний ад’ювантний засіб.
Ключові положення
- Поширеність алергічних захворювань продовжує зростати в усьому світі.
- Алергічні захворювання, в тому числі АД й АР, мають спільні патогенетичні механізми.
- Настанови WAO та WGO передбачають застосування пробіотиків при АД як додаткових засобів.
- Доцільність використання пробіотиків при АР підтверджують систематичні огляди та метаналізи.
- Найефективнішим при АД, АР вважається застосування комбінованих пробіотиків і використання штамів L. rhamnosus.
- Синбіотик Бажана, який містить пробіотичні штами L. rhamnosus, L. acidophilus, S. boulardii
і пребіотик інулін, може бути включений у схеми лікування хворих на АД, АР як ад’ювантний засіб.
Література
- Dierick В., der Molen Т., Flokstra-de Blok B., et al. Burden and socioeconomics of asthma, allergic rhinitis, ato-pic dermatitis and food allergy. Expert Review of Pharmacoeconomics & Outcomes Research. 2020; 20 (5): 437-453. doi: 10.1080/14737167.2020.1819793.
- The European Academy of Allergy and Clinical Immunology (EAACI). Advocacy Manifesto Tackling the Allergy Crisis in Europe – Concerted Policy Action Needed. June 2015 Version. Available at: http://www.eaaci.org/outreach/public- declarations.html.
- Mazur M., Czarnobilska M., Dyga W., et al. Trends in the epidemiology of allergic diseases of the airways in children growing up in an urban agglomeration.
- Clin. Med. 2022; 11: 2188. doi: 10.3390/jcm11082188.
- Duda L., Okhotnikova O., Sharikadze O., et al. Comparative analysis of prevalence of the most common allergy diseases in children of the Kyiv region (Ukraine). Georgian Med. News. 2019; 291: 53-58.
- Paller Amy S.A.S. The atopic march and atopic multimorbidity: many trajectories, many pathways. J. Allergy Clin. Immunol. 2019; 143 (1): 46-55.
- Sharma G., Im S.H. Probiotics as a potential immunomodulating pharmabiotics in allergic diseases: current status and future prospects. Allergy Asthma Immunol. Res. 2018; 10 (6): 575-590. doi: 10.4168/aair.2018.10.6.575.
- Feng H., Xiong X., Chen Z., et al. Prevalence and influencing factors of food allergy in global context: a meta-analysis. Int. Arch. Allergy Immunol. 2023; 12: 1-33. doi: 10.1159/000527870.
- Kuruvilla M., Lee F., Lee G. Understanding asthma phenotypes, endotypes, and mechanisms of disease. Clin. Rev. Allergy Immunol. 2019; 56 (2): 219-233.
- Sharma G., Im S.H. Probiotics as a potential immunomodulating pharmabiotics in allergic diseases: current status and future prospects. Allergy Asthma Immunol. Res. 2018 Nov; 10 (6): 575-590. doi: 10.4168/aair.2018.10.6.575.
- Fiocchi A., Pawankar R., Cuello-Garcia C., et al. World Allergy Organization – McMaster University Guidelines for Allergic Disease Prevention (GLAD-P): probiotics. World Allergy Organ. J. 2015; 8 (1): 4. doi: 10.1186/s40413-015-0055-2.
- Guarner F., Khan A.G., Garisch J., et al. World Gastroenterology Organisation Global Guidelines: probiotics and prebiotics. Update 2017. J. Clin. Gastroenterol. 2012; 46 (6): 468-81. doi: 10.1097/MCG.0b013e3182549092.
- Umborowati M.A., Damayanti D., Anggraeni S., et al. The role of probiotics in the treatment of adult atopic dermatitis: a meta-analysis of randomized controlled trials. J. Health Popul. Nutr. 2022; 41 (1): 37. doi: 10.1186/s41043-022-00318-6.
- Sodré C.S., Vieira M.S., Estefan J., et al. The effect of probiotics on the clinical status of adult patients with atopic dermatitis: a systematic review. Eur. J. Med. Res. 2022; 27 (1): 94. doi: 10.1186/s40001-022-00713-z.
- Li Y., Zhang B., Guo J., et al. The efficacy of probiotics supplementation for the treatment of atopic dermatitis in adults: a systematic review and meta-analysis. J. Dermatolog. Treat. 2022; 33 (6): 2800-2809. doi: 10.1080/09546634.2022.2080170.
- Pan H., Su J. Association of probiotics with atopic dermatitis among infant: a meta-analysis of randomized controlled trials. Oxid. Med. Cell. Longev. 2022; 2022: 5080190. doi: 10.1155/2022/5080190.
- Jiang W., Ni B., Liu Z., et al. The role of probiotics in the prevention and treatment of atopic dermatitis in children: an updated systematic review and meta-analysis of randomized controlled trials. Paediatr. Drugs. 2020; 22 (5): 535-549. doi: 10.1007/s40272-020-00410-6.
- Sun S., Chang G., Zhang L. The prevention effect of probiotics against eczema in children: an update systematic review and meta-analysis.
J. Dermatolog. Treat. 2022; 33 (4): 1844-1854. doi: 10.1080/09546634.2021.1925077. - Li L., Han Z., Niu X., et al. Probiotic supplementation for prevention of atopic dermatitis in infants and children: a systematic review and meta-analysis.
Am. J. Clin. Dermatol. 2019; 20 (3): 367-377. doi: 10.1007/s40257-018-0404-3. - Voigt J., Lele M. Lactobacillus rhamnosus used in the perinatal period for the prevention of atopic dermatitis in infants: a systematic review and meta-analysis of randomized trials. Am. J. Clin. Dermatol. 2022; 23 (6): 801-811. doi: 10.1007/s40257-022-00723-x.
- Ciprandi G., Tosca M.A. Probiotics in allergic rhinitis management: is there a positioning for them? Allergies. 2022; 2: 119-127. doi: 10.3390/allergies2030011.
- Luo C., Peng S., Li M., et al. The efficacy and safety of probiotics for allergic rhinitis: a systematic review and meta-analysis. Front. Immunol. 2022; 13: 848279. doi: 10.3389/fimmu.2022.848279.
- Yan S., Ai S., Huang L., et al. Systematic review and meta-analysis of probiotics in the treatment of allergic rhinitis. Allergol. Immunopathol. (Madr.). 2022; 50 (3): 24-37. doi: 10.15586/aei.v50i3.507.
- Wang X., Tan X., Zhou J. Effectiveness and safety of probiotic therapy for pediatric allergic rhinitis management: a systematic review and meta-analysis.
Int. J. Pediatr. Otorhinolaryngol. 2022; 162: 111300. doi: 10.1016/j.ijporl.2022.111300.
- Tan W., Zhou Z., Li W., et al. Lactobacillus rhamnosus GG for cow’s milk allergy in children: a systematic review and meta-analysis. Front. Pediatr. 2021; 9: 727127. doi: 10.3389/fped.2021.727127.
- Бажана. Інструкція. https://compendium.com.ua/dec/526752.
Освітньо-практичний журнал Allergy Practice №1 2023р.