Поточні стратегії лікування алергічного риніту: основні положення міжнародних рекомендацій ARIA, ICAR та японської настанови
Автор: Сергій Вікторович ЗАЙКОВ, доктор медичних наук, професор кафедри фтизіатрії і пульмонології Національного університету охорони здоров’я України ім. П.Л. Шупика (м. Київ), президент ВГО «Асоціація алергологів України»
 Зростання поширеності та захворюваності на алергічний риніт (АР) у всьому світі стало приводом для ретельного вивчення особливостей виникнення цієї патології та розроблення підходів до її лікування.
Зростання поширеності та захворюваності на алергічний риніт (АР) у всьому світі стало приводом для ретельного вивчення особливостей виникнення цієї патології та розроблення підходів до її лікування.
Протягом останніх 3 років опубліковано декілька міжнародних настанов, які регламентують різні діагностичні нюанси та терапевтичні стратегії лікування АР: оновлені рекомендації ARIA (2020) [1], настанова Японського товариства алергології (2020) [3] та міжнародний консенсус із лікування АР (ICAR-Allergic Rhinitis 2023) [5]. У цьому огляді наведено основні положення зазначених консенсусних документів.
Визначення
Згідно з визначенням, яке формулює японська настанова, АР являє собою алергічне захворювання слизової оболонки носа 1 типу, що характеризується пароксизмальним і повторюваним чханням, водянистою ринореєю й утрудненням носового дихання через закладений ніс [3]. У положеннях ICAR-Allergic Rhinitis 2023 також наголошується, що виникнення АР ґрунтується на IgE-опосередкованій реакції гіперчутливості 1 типу внаслідок впливу алергена (АГ) [5].
Епідеміологія
Автори всіх зазначених настанов одностайно підкреслюють зменшення захворюваності на інфекційний риносинусит і зростання кількості хворих на АР [1, 3, 5]; нині поширеність АР у світі варіює в межах 5-50% залежно від географічного регіону [5]. Результати епідеміологічних досліджень констатують вірогідне збільшення поширеності АР; в Японії в 1998 р. вона становила 29,8%, у 2008 р. зросла до 39,4% та досягла 49,2% у 2019 р. [2]. Згідно з даними національного британського когортного дослідження, поширеність сенсибілізації до такої повсюдно поширеної рослини, як тимофіївка лугова, зростає зі збільшенням віку: високу чутливість до цієї рослини мають 9,7% дітей віком 4 роки, 28,4% популяції 8-річних дітей та 37,1% підлітків віком 16 років [4].
Чинники ризику
Зазвичай виникнення АР пов’язують зі впливом інгаляційних АГ, як-от кліщі Dermatophagoides (основний АГ домашнього пилу), пилок (дерев, трав і бур’янів), гриби, комахи та шерсть домашніх тварин [3, 5]. Спричиняють розвиток АР генетична схильність і поліморфізм генів, до яких призводять виникнення атопічного дерматиту (CD14, IL-33 та TYRO3), забруднення довкілля, куріння, високий соціально-економічний статус, тоді як грудне вигодовування, ранній контакт із домашніми тваринами, особливо собаками, мікробне різноманіття вважають чинниками, що захищають від виникнення АР [5].
Патофізіологія
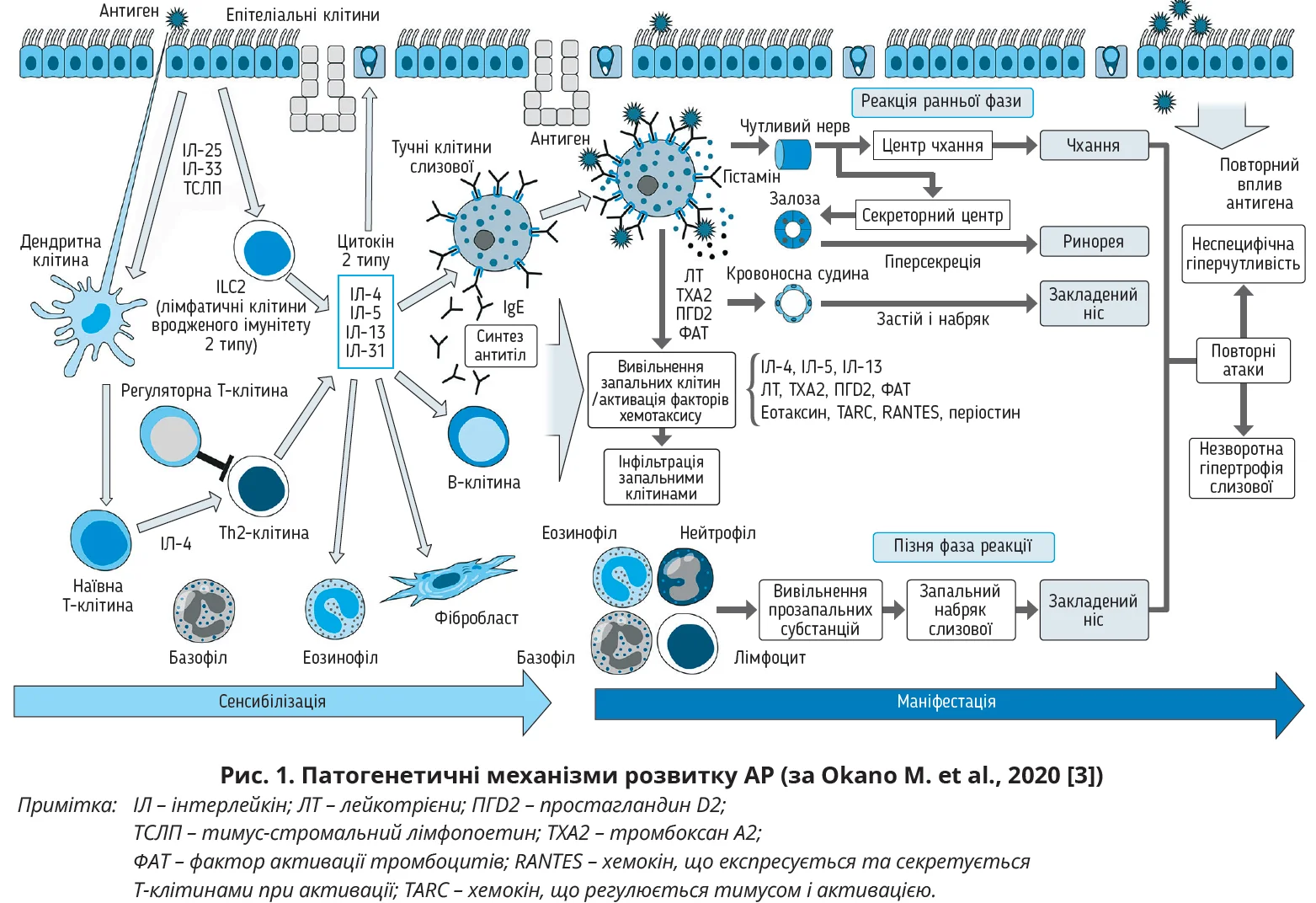
Розрізняють дві патофізіологічні фази розвитку АР: ранню та пізню. У сенсибілізованих осіб інгаляційні АГ проходять через епітеліальні клітини слизової оболонки носа та зв’язуються з IgE тучних клітин, які локалізуються в поверхневому шарі слизової оболонки. Взаємодія АГ – антитіло зумовлює вивільнення біологічно активних речовин із тучних клітин, у тому числі гістаміну та пептиду LT [3]. У ранній фазі захворювання ці субстанції подразнюють сенсорні нервові закінчення та кровоносні судини слизової оболонки носа, що призводить до виникнення чхання, водянистої ринореї, набряку слизової оболонки, закладеного носа. На пізній стадії, яка розвивається через 6-10 годин після контакту з АГ, різні запальні клітини, в тому числі активовані еозинофіли, інфільтрують слизову оболонку носа у відповідь на дію прозапальних цитокінів (рис. 1). Отже, рання фаза АР спричинена IgE-опосередкованою реакцією АГ – антитіло 1 типу; пізня фаза характеризується інфільтрацією запальними клітинами, а повторний вплив АГ спричиняє неспецифічну гіперчутливість і незворотний набряк слизової.
Класифікація
Відповідно до класичних уявлень, АР класифікують на сезонний і цілорічний [3]. Сезонний АР асоційований із дією АГ на відкритому повітрі, тоді як цілорічний АР зумовлений впливом АГ у приміщенні. Проте кліматичні зміни та полісенсибілізація вносять певні труднощі у використання цієї класифікації. Додатково розрізняють інтермітувальний АР, який визначають як виникнення симптомів рідше ніж 4 дні протягом тижня або менше ніж 4 тижні поспіль. Персистентний, або стійкий, АР характеризують як наявність симптомів понад 4 доби на тиждень протягом принаймні 1 місяця [5]. Японські спеціалісти наполягають на класифікації АР залежно від тяжкості захворювання та розрізняють легкий, помірний, тяжкий і дуже тяжкий перебіг (табл. 1) [3].
Клінічні прояви
Основні клінічні прояви АР добре відомі – це чхання, ринорея та закладений ніс. Виникнення чхання пояснюють зв’язуванням гістаміну з H1-рецепторами, які розташовані на закінченнях трійчастого нерва в слизовій оболонці носа. Аферентні нервові волокна передають сигнал до центру чхання в довгастому мозку, що призводить до пароксизмального та сильного звуження діафрагми, міжреберних м’язів. Подразнювальний вплив гістаміну на трійчастий нерв зумовлює розвиток гіперчутливості слизової, мінімального, але стійкого запального процесу [3].
Крім чхання, подразнення сенсорного нерва провокує виникнення парасимпатичного рефлексу, який ґрунтується на вивільненні ацетилхоліну з парасимпатичних нервових закінчень і його зв’язуванні з мускариновими рецепторами. Гістамін безпосередньо впливає на судини слизової оболонки носа, спричиняючи витікання плазми та виникнення ринореї [3].
Набряк слизової оболонки носа пояснюють інтерстиціальним її набряком унаслідок витікання плазми та розширення назальних судин. Відзначається прямий вплив гістаміну, ФАТ, ПГD2, кінінів і особливо пептиду LT; останній вивільняється з еозинофілів і відіграє важливу роль у набряку слизової під час пізньої фази реакції [3].
Діагностика
Ретельний збір анамнезу має вирішальне значення в діагностиці АР і обов’язково має супроводжуватися належним фізикальним оглядом [3, 5].
Згідно з положеннями японської настанови, остаточний діагноз АР ґрунтується на пароксизмальному виникненні відповідних клінічних симптомів (чхання, свербіж у носі, водяниста ринорея, закладений ніс) та інтраназальних ознак (набряк слизової оболонки, водяниста ринорея), позитивних назальних тестах на еозинофіли, ідентифікації етіологічних АГ за результатами шкірних проб або визначенні вмісту сироваткового алергеноспецифічного IgE [3].
На відміну від японської настанови, положення ICAR-Allergic Rhinitis 2023 поділяють діагностичні дослідження на окремі групи: рекомендовані, опціональні та нерекомендовані [5]. Рекомендуються обов’язкове проведення клінічного огляду (збір анамнезу, фізикальний огляд), використання валідованих опитувальників, виконання шкірних тестів з АГ і визначення алергеноспецифічного IgE. До опціональних тестів, які проводять виключно за рішенням лікаря, віднесені назальна ендоскопія, шкірні внутрішньодермальні проби, змішані шкірні проби, загальний рівень сироваткового IgE, назальний секреторний IgE, назальні провокаційні тести, назальна цитологія, риноманометрія, акустична ринометрія, пікова швидкість інспіраторного назального потоку. ICAR-Allergic Rhinitis 2023 не рекомендує проведення рентгенологічного дослідження та назальної гістології, а також не вважає за доцільне визначати вміст оксиду азоту в повітрі, що видихається, та концентрацію назального оксиду азоту [5].
Лікування
Загальні положення
Практичні настанови, що розглядаються, мають схоже ставлення до базисного нефармакологічного лікування АР. У кожній із них передбачаються уникнення контакту з АГ, прибирання приміщення, зниження вологості в кімнатах, що вважається запорукою ефективної боротьби з домашніми кліщами [1, 3, 5]. Рекомендуються носіння масок, окулярів для запобігання контакту з пилком, а також уникання контакту з тваринами, які здатні провокувати АР, проведення своєчасної гігієнічної обробки домашніх улюбленців [3]. Положення ІCAR-Allergic Rhinitis 2023 передбачають проведення санітарних заходів проти тарганів, гризунів та обмеження впливу професійних АГ [5].
Фармакотерапія
Поточні стратегії лікування АР ґрунтуються на фармакологічній блокаді основних патогенетичних механізмів ранньої та пізньої фаз алергічного каскаду. Рекомендації ARIA, ІCAR-Allergic Rhinitis 2023 та японська настанова мають певні особливості у виборі та призначенні фармакологічної терапії хворим на АР.
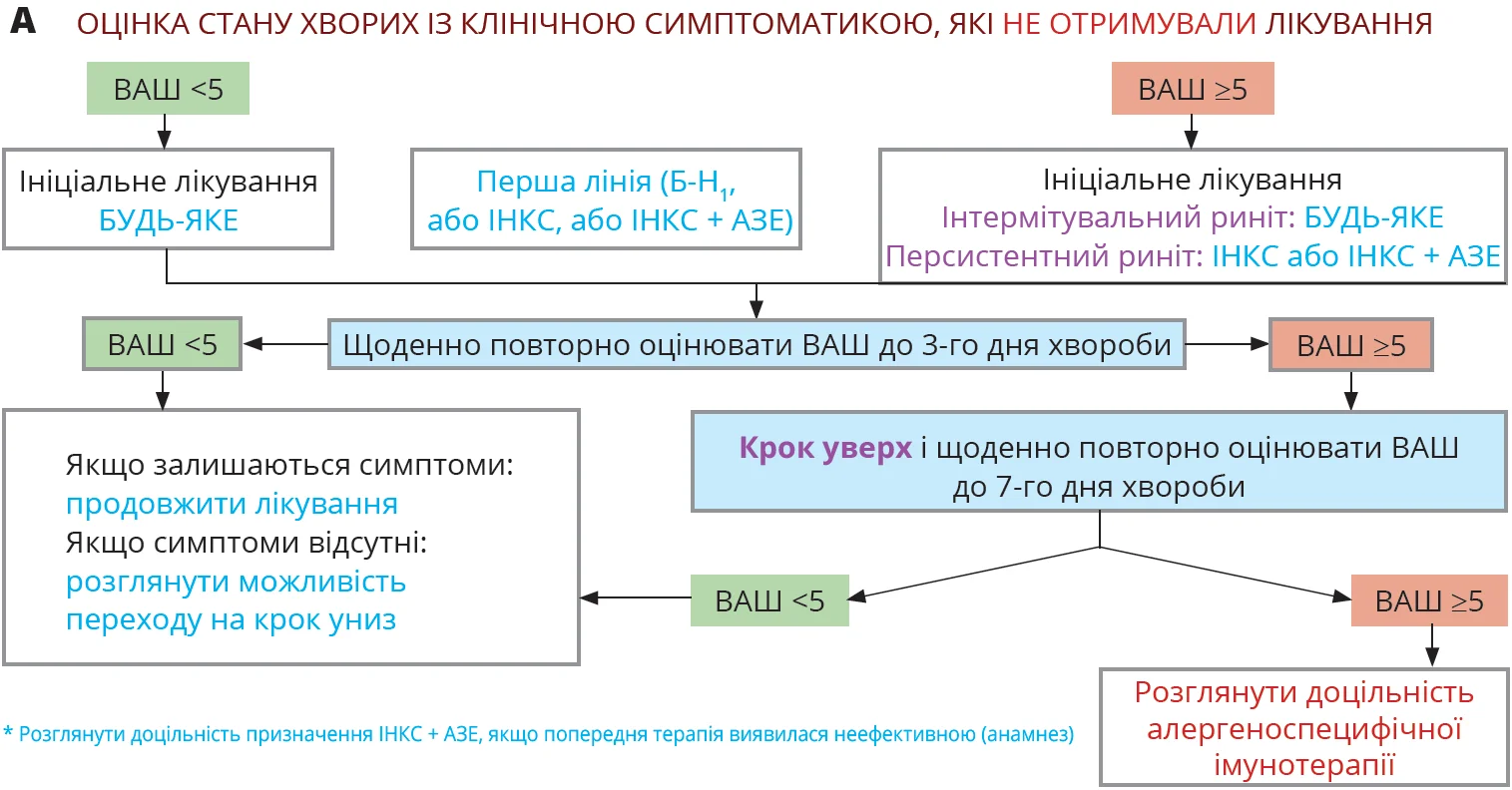
ARIA. Алгоритм заснований на використанні візуальної аналогової шкали (ВАШ) та віддає перевагу призначенню антигістамінних препаратів (АГП) із групи блокаторів Н1-рецепторів (Б-Н1) та інгаляційних кортикостероїдів – ІНКС (рис. 2).
Слід зазначити, що за потреби застосування комбінованої терапії експерти ARIA наполягають на комбінації ІНКС саме з азеластином (АЗЕ).
Японська настанова. Передбачає застосування ширшого спектра фармацевтичних засобів із різноманітних груп з урахуванням патогенетичних особливостей виникнення АР (табл. 2).
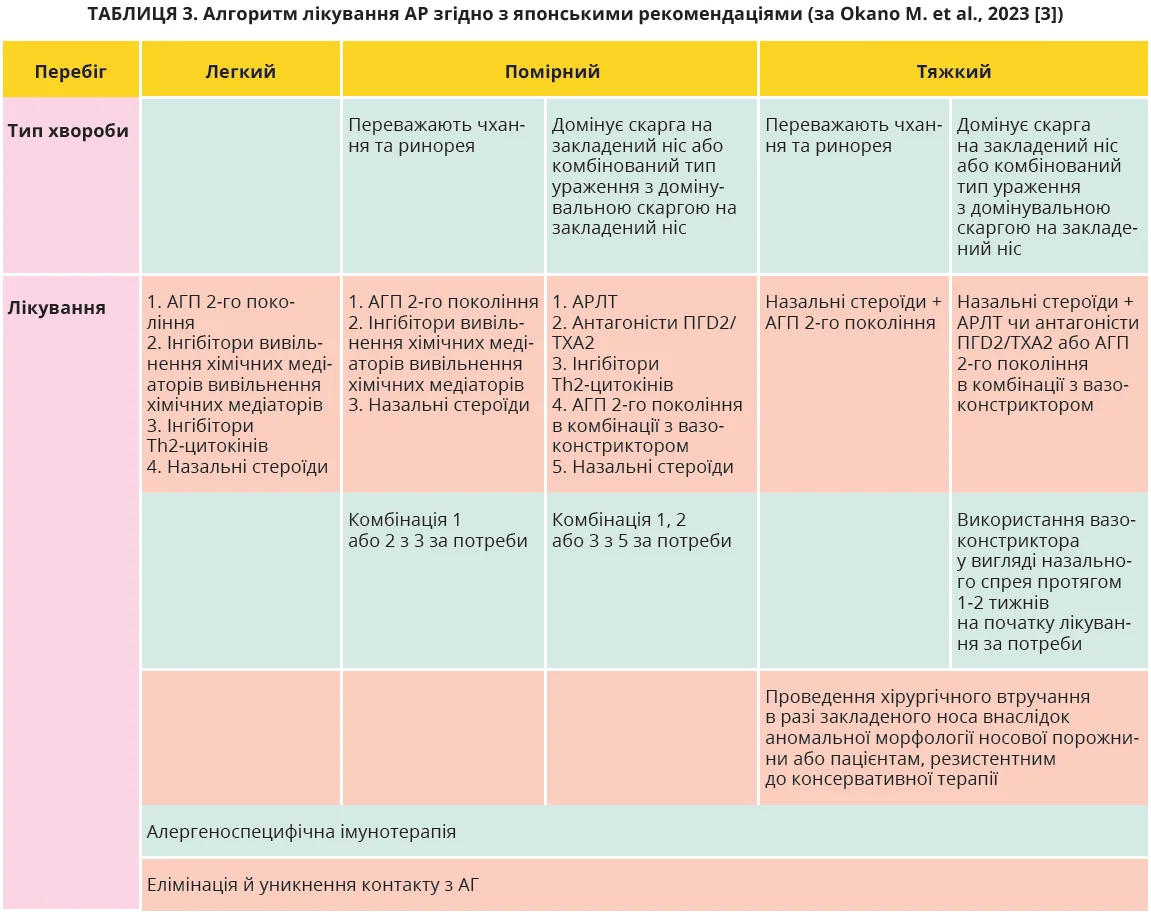
Фахівці Японського товариства алергології пропонують інший алгоритм фармакотерапії хворих на АР, який передбачає призначення одного засобу або комбінації декількох ліків залежно від тяжкості захворювання (табл. 3).
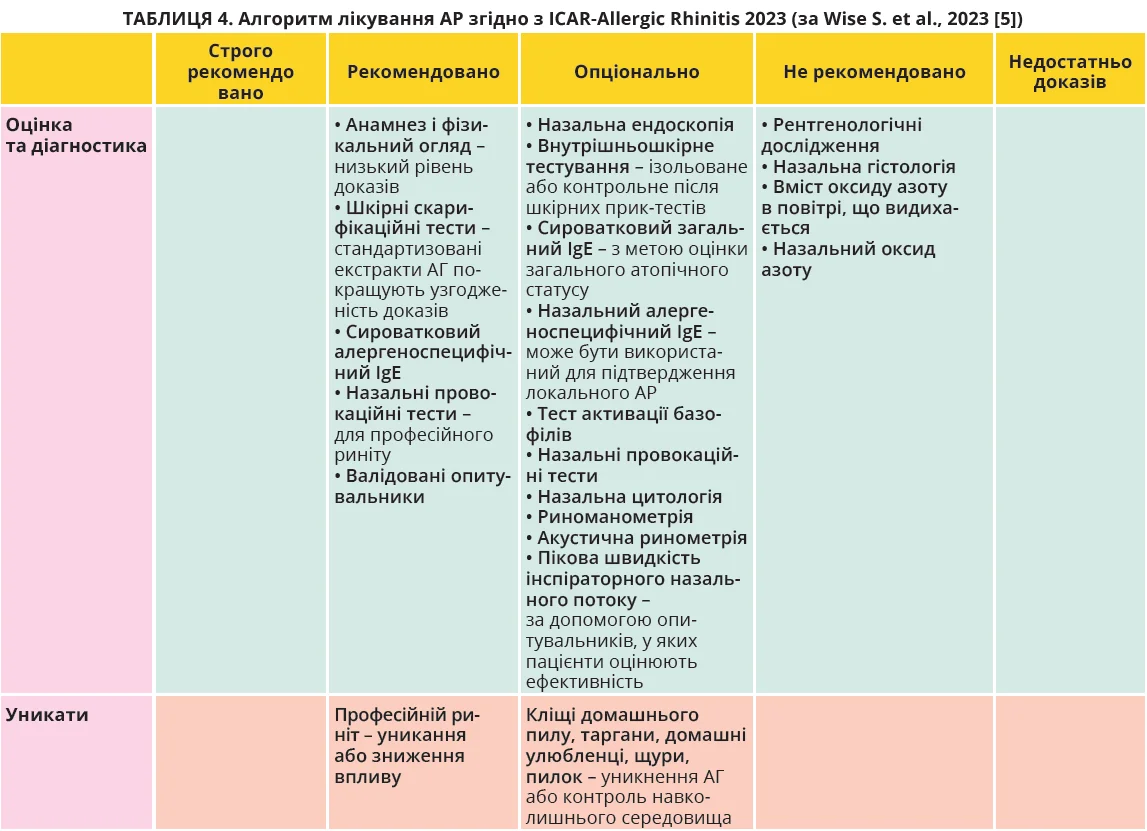
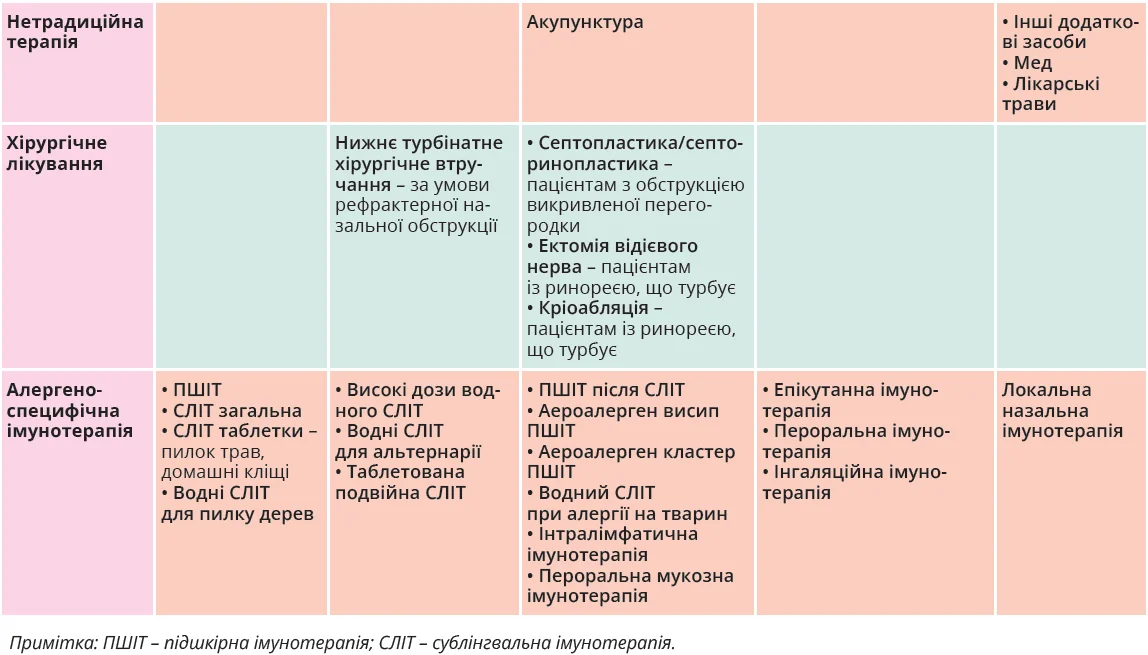
ІCAR-Allergic Rhinitis 2023. Оновлені рекомендації дещо подібні до положень японської настанови, передбачаючи застосування різноманітних фармацевтичних засобів. На відміну від ARIA та японських рекомендацій, алгоритм ІCAR-Allergic Rhinitis 2023 побудований з урахуванням ступеня доказовості рекомендованих втручань (табл. 4).
Висновки
АР є поширеною патологією, його лікування регламентується різними міжнародними документами. Поточні стратегії лікування АР представлено в рекомендаціях ARIA, ICAR-Allergic Rhinitis 2023 та японській настанові. Два останні погоджувальні документи містять усебічний аналіз умов виникнення, особливостей перебігу АР і пропонують різні підходи до його лікування з огляду на ступінь тяжкості захворювання, передбачаючи застосування різноманітних сучасних ліків. Усі рекомендації підтримують призначення монотерапії Б-Н1 2-го покоління, ІНКС або застосування їх комбінації, японська настанова та ICAR-Allergic Rhinitis 2023 підтримують використання АРЛТ / антагоністів ПГD2/ТХА2 у комбінації з іншими засобами за тяжкого перебігу АР, неефективності попередньої терапії.
Література
- Bousquet J., Schünemann H.J., Togias A., et al. Allergic Rhinitis and Its Impact on Asthma Working Group. Next-generation Allergic Rhinitis and Its Impact on Asthma (ARIA) guidelines for allergic rhinitis based on Grading of Recommendations Assessment, Development and Evaluation (GRADE) and real-world evidence. J. Allergy Clin. Immunol. 2020; 145 (1): 70-80.e3. doi: 10.1016/j.jaci.2019.06.049.
- Matsubara A., Sakashita M., Gotoh M., Kawashima K., Matsuoka T., Kondo S., et al. Epidemiological survey of allergic rhinitis in Japan 2019. Nippon Jibiinkoka Gakkai Kaiho (Tokyo). J. Otolaryngol. Jpn. 2020; 123: 485e90 (in Japanese).
- Okano M., Fujieda S., Gotoh M., et al. Executive summary: Japanese guidelines for allergic rhinitis 2020. Allergol. Int. 2023 Jan; 72 (1): 41-53. doi: 10.1016/j.alit.2022.11.003.
- Westman M., Åberg K., Apostolovic D., et al. Mechanisms for the Development of Allergies (MeDALL) consortium. Sensitization to grass pollen allergen molecules in a birth cohort-natural Phl p 4 as an early indicator of grass pollen allergy. J. Allergy Clin. Immunol. 2020; 145 (4): 1174-81.
- Wise S.K., Damask C., Roland L.T., et al. International consensus statement on allergy and rhinology: Allergic rhinitis – 2023. Int. Forum Allergy Rhinol. 2023 Apr; 13 (4): 293-859. doi: 10.1002/alr.23090.
Освітньо-практичний журнал Allergy Practice №2 2023р.