Оновлена інформація щодо останніх нововведень і досягнень у сфері харчової алергії
Переклала й адаптувала канд. мед. наук Тетяна Можина
Харчова алергія (ХА) є глобальною проблемою системи охорони здоров’я. Поточні дослідження надають багато інформації щодо нововведень і досягнень у розумінні та лікуванні ХА. Представляємо оновлення нашої попередньої статті [1], яке висвітлює останні досягнення в цій галузі з фокусом на біомаркерах десенсибілізації та досягненні толерантності.
Роль бар’єрної функції при ХА
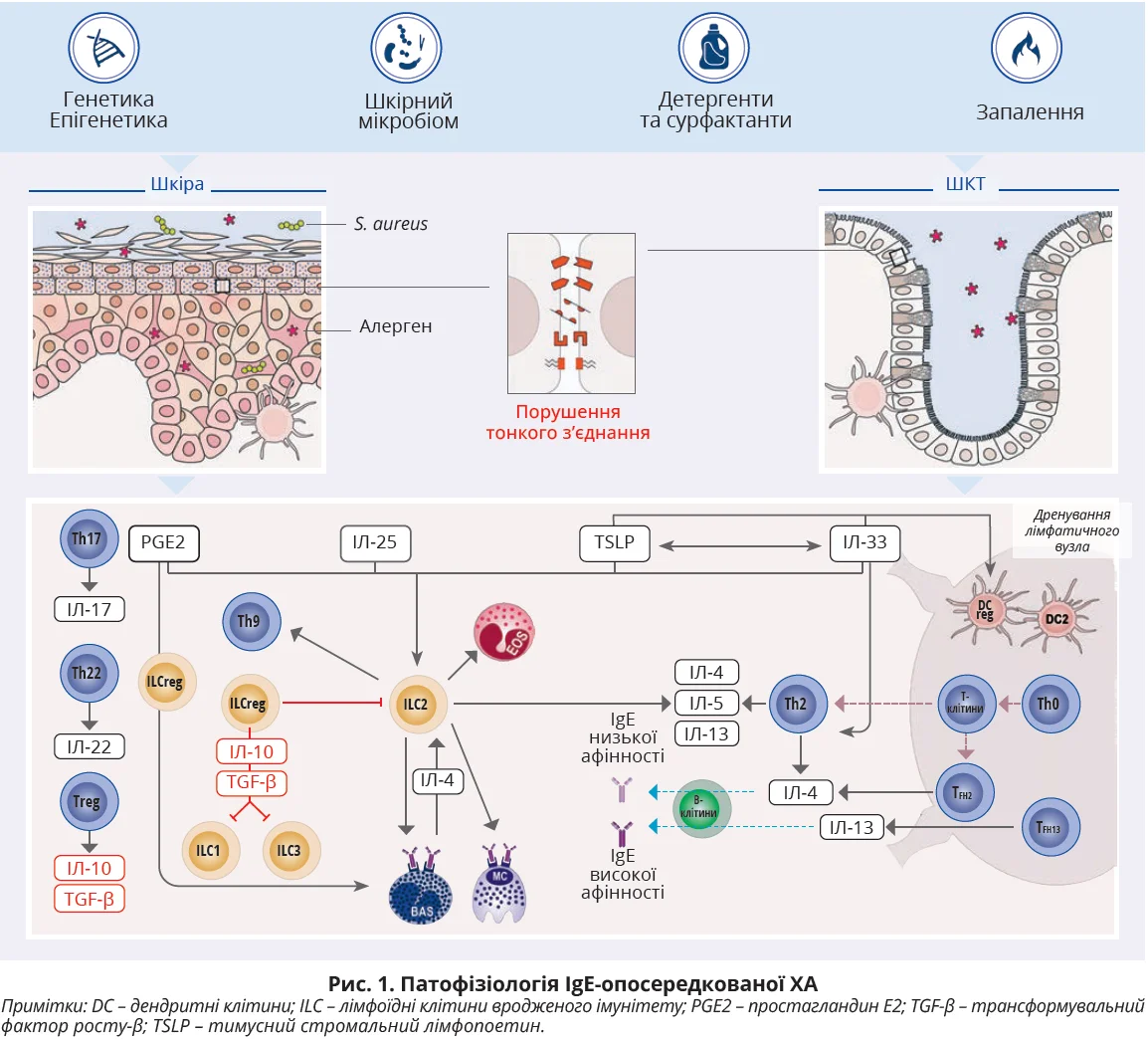
На межі між «експосомом» (сукупній мірі впливу чинників навколишнього середовища на людину протягом усього її життя) й організмом людини епітеліальні клітини діють як перший фізичний захисний бар’єр, відіграючи важливу роль у підтримці тканинного гомеостазу. Експосом представлений зовнішніми (алергени, забруднювачі, мийні засоби, мікроби) та внутрішніми (мікробіота, продукти метаболізму) чинниками [2]. Підтримка належної бар’єрної функції має вирішальне значення в забезпеченні відповідної імунної відповіді на алергени (рис. 1). Отже, дисфункція епітеліального бар’єра та зміна проникності шкіри, що спричинені генними мутаціями або однонуклеотидними поліморфізмами ключових генів, включаючи філагрин, SPINK5 [3], SERPINB7, KLK7, клаудин-1 [4, 5], асоційовані з розвитком атопічного дерматиту (АтД) та ХА [6-10]. Порушення епітеліального бар’єра виникає внаслідок зменшення кількості керамідів, антимікробних пептидів, серинової протеази, шкірного та кишкового дисбіозу, які виникають під впливом екзогенних чинників, наприклад мийних засобів [4, 11, 12].
АтД пов’язують із розвитком ХА за допомогою гіпотези подвійного впливу алергенів, яка передбачає первинний вплив алергену на пошкоджену шкіру без попереднього впливу на шлунково-кишковий тракт (ШКТ), що спричиняє запальну імунну відповідь Th2-типу. Навпаки, первинний вплив алергену на ШКТ сприяє регуляторній імунній відповіді й індукції толерантності [14, 15]. Отже, сенсибілізація до харчових алергенів і розвиток ХА, ймовірно, пов’язані з дисфункцією шкірного бар’єра та мікробною колонізацією [4, 15-17].
Коменсальні бактерії потрібні для захисту шкірної мікробіоти, дозрівання Т-лімфоцитів і активації вироблення антимікробних пептидів кератиноцитами. Дисбактеріоз шкірного мікробіому, який зазвичай діагностують за кількістю золотистого стафілокока, позитивно корелює з тяжкістю АтД, будучи перспективним біомаркером АтД [18, 19].
Використання емолієнтів визнано базовою стратегією лікування АтД, мета якої полягає в підтримці бар’єрної функції шкіри. Концепція нівелювання бар’єрної дисфункції in vivo за допомогою зволожувачів є темою досліджень, що тривають. Нині використовують різні формули емолієнтів, включаючи найпоширенішу парафінову/нафтову основу та триліпідну базу (3:1:1 – кераміди, холестерин і вільні жирні кислоти) [20, 21]. Емолієнти здатні зменшити тяжкість і подовжити час між загостреннями АтД [22], знижуючи втрату води шкірою [21] та покращуючи загальну гідратацію. Це має вирішальне значення для шкіри новонароджених, яка має тонкий роговий шар зі зниженим умістом ліпідів і зволожувальних речовин. Емолієнти, зокрема триліпідні формули, підвищують толерантність і забезпечують зростання індексу IgG4/IgE, вмісту інтерлейкіну-10 (ІЛ-10), LAP+ Т-лімфоцитів, а також зниження IЛ-4, що продукують CD4+ Т-лімфоцити [20]. Крім того, вільні жирні кислоти, присутні у складі триліпідних засобів, здатні активувати рецептори, що активуються проліфераторами пероксисом (PPARs), кількість яких при АтД зазвичай знижена, зменшуючи таким чином інтенсивність запалення.
Механізми та потенційні біомаркери ХА. Імунотерапія
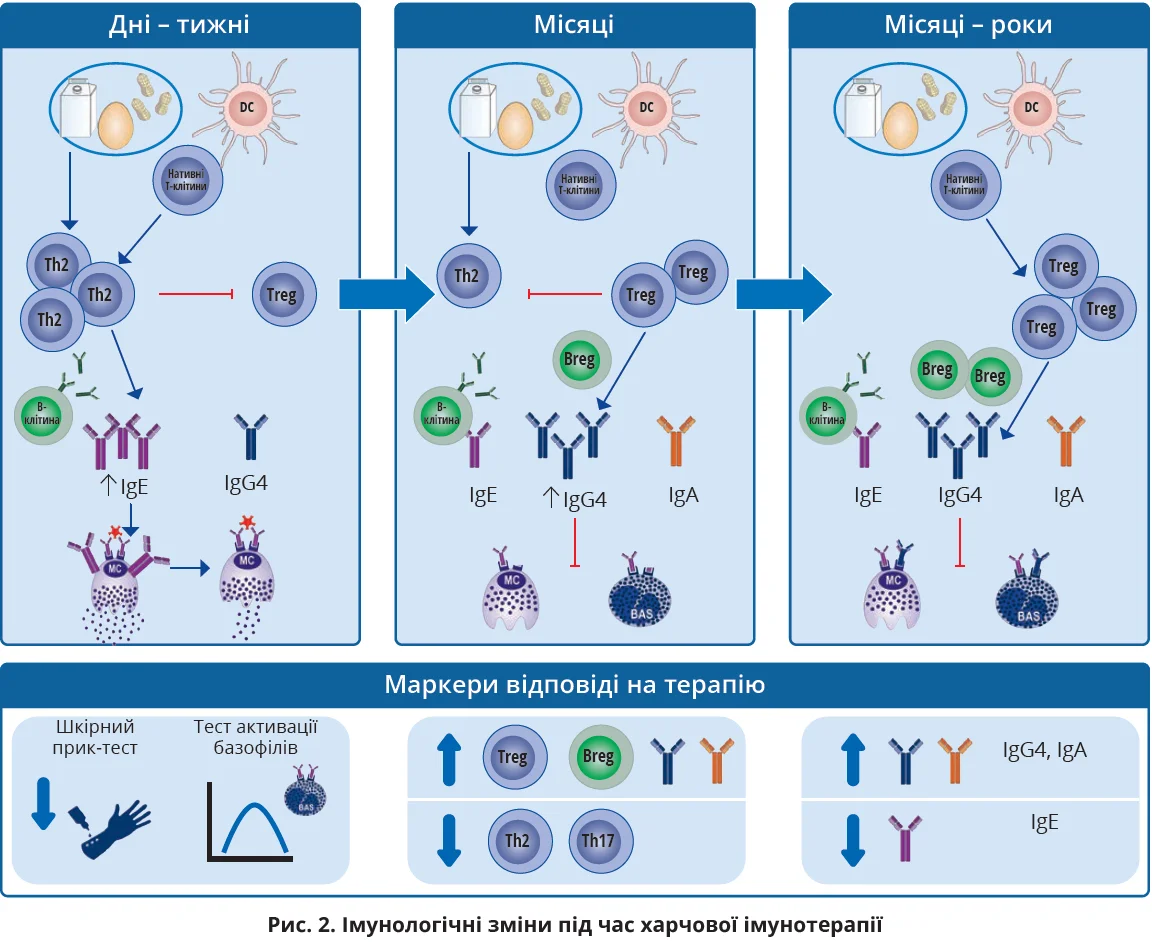
Нині алергеноспецифічна імунотерапія (АІТ) вважається найбільш перспективним і дослідженим методом лікування ХА. Проте залежно від використовуваного підходу існують деякі обмеження з безпеки, ефективності, часу підвищення дози, вартості та ступеня захисту. Незважаючи на значне вдосконалення терапевтичних концепцій, потрібні альтернативні стратегії, здатні індукувати розвиток толерантності з кращим профілем безпеки. Досліджуються різні шляхи та дози введення алергенів: пероральна (ПІТ), епікутанна (ЕПІТ) і сублінгвальна (СЛІТ) імунотерапія. Вважають, що АІТ забезпечує досягнення вагомих результатів, якщо відповідний алерген уводиться в його нативній або модифікованій формі, починаючи з підпорогового рівня, а потім у зростальних дозах із метою досягнення десенсибілізації та підвищення порогу толерантності (рис. 2).
Найпоширенішою формою АІТ є ПІТ (підтримувальні дози – від 125 мг до 4 г) [90]. У разі прийому алергену в підпорогових кількостях спостерігають зниження чисельності алерген-індукованих базофілів і активацію тучних клітин; такі зміни є одними з перших імунних змін, що спостерігаються. Під час початкового збільшення дозування одночасно з десенсибілізацією констатують посилення продукції алергеноспецифічного IgE (сIgE) та тимчасове збільшення алергеноспецифічних ефекторних клітин 2 типу [90-93]. Транзиторне збільшення продукції TGF-β CD4+ Т-клітинами також асоційоване з успішною десенсибілізацією. У дорослих пацієнтів, які проходили ПІТ алергеном арахісу, спостерігали транзиторну еозинофілію стравоходу та гастроінтестинальну еозинофілію, що може бути пов’язано з появою скарг з боку ШКТ [94]. За продовження імунотерапії активність Th2-клітин знижується, тоді як кількість регуляторних клітин, що продукують IЛ-10 (Tregs і Bregs), значно зростає [70, 95]. Ця пізня фаза асоційована зі збільшенням сIgG, сIgG4 та сIgA, а також зниженням індексу сIgE / загальний IgE [90, 93, 96]. Проте визначення вмісту сIgA як сурогатного маркера відповіді слизової оболонки, здається, не дає змоги прогнозувати розвиток стійкої толерантності або успішної десенсибілізації [97]. Ранній початок ПІТ (до досягнення 4 років), зниження сIgE на початковому етапі корелюють із підвищенням імовірності десенсибілізації та досягнення ремісії після закінчення ПІТ [98]. Ці дані підкреслюють важливість раннього початку терапії для зупинення/уповільнення прогресування специфічної ХА, що лікується, на додаток до її профілактики. Тканиноспецифічні ефекти ПІТ у людини вивчені недостатньо й можуть відіграти важливу роль [99, 100].
При СЛІT використовується в 100 разів менша доза алергену (підтримувальна доза становить 2-5 мг/добу). Це має певні переваги в механізмах локальної пероральної толерантності СЛІT [101, 102]. Зазначені механізми включають поглинання алергенів оральними антигенпрезентувальними клітинами в сублінгвальній слизовій оболонці.
На ранніх стадіях СЛІТ транзиторне підвищення сIgE пояснюється індукцією перемикання з IgG+ В-клітин на короткоживучі IgE+ плазмобласти [105]. Важливо, що збільшення сIgE внаслідок впливу алергену при проведенні СЛІТ не пов’язано з різнобічністю IgE [105]. Нещодавно досліджували ефективність СЛІТ у лікуванні ХА, асоційованій із пилком берези, за допомогою рекомбінантного Mal d 1, який знижував популяцію Th2-клітин, синтез IЛ-4 [106] та підвищував рівень IgG із функціональною блокувальною активністю [107]. До додаткових біомаркерів СЛIT відносять сIgA в слині, котрий, як вважають, інгібує поглинання алергену на поверхні слизової оболонки та впливає на результати СЛІТ алергеном арахісу [108]. Довготривале 5-річне дослідження ефективності СЛІТ алергеном арахісу підтвердило, що лікування сприяє зниженню сIgE, результатів шкірного прик-тесту та розмірів елементів висипу, збільшенню індексу IgG4/IgE, зменшенню активації базофілів [109].
EПIT безпосередньо впливає на імунні клітини шкіри. Десенсибілізація індукується шляхом застосування шкірного пластиру з дуже низькими дозами алергену в діапазоні 50-250 мкг [102, 110]. Алерген поглинається в роговому шарі шкіри клітинами Лангерганса, які мігрують до лімфатичних вузлів та індукують диференціацію Foxp3+ Treg [111].
Окрім того, стимулюються кишкові LAP+FoxP3- Tregs і знижується ризик анафілаксії завдяки TGF-β-залежному інгібуванню активації тучних клітин [112]. Незважа чи на те що EПIT характеризують як безпечну та добре переносиму, її результативність у досягненні десенсибілізації є остаточно не зрозумілою.
Оновлення підходів до клінічної терапії
Протягом останніх років на підходи до лікування ХА значно вплинула пандемія коронавірусної хвороби (COVID-19) [157-160], що зумовила активне використання телемедицини [161]. ПІТ продовжує набирати обертів як альтернатива відмові від їжі при лікуванні ХА. У США [162] та Європі нещодавно схвалили перший фармацевтичний продукт для лікування ХА в дітей віком 4-17 років. В інших країнах [163, 164] віддають перевагу застосуванню харчових продуктів для проведення ПІТ. Дебати щодо найкращого застосування ПІТ тривають, при цьому занепокоєння викликає ризик виникнення тяжких алергічних реакцій у разі ПІТ, які потрібно збалансувати для зменшення тяжкості реакції при її випадковому виникненні. Дані, отримані в математичній моделі свідчать, що харчова десенсбілізіація здатна знизити вірогідність розвитку повноцінної алергічної реакції при випадковому споживанні алергену [165, 166]; величина розміру цього ефекту варіює залежно від досягнутого порогу десенсібілізації. Нещодавній метааналіз стверджує, що при ПІТ розвиваються менш тяжкі алергічні реакції порівняно з плацебо [167].
Стає дедалі очевиднішим, що тривалість ПІТ потрібно продовжувати з метою підтримання її ефективності, як показано в дослідженнях POISED [125], POIMD [168] та IMPACT [98]. Після досягнення підтримувальної дози 4 г/добу арахісового білка, 120 дітей і дорослих у межах дослідження POISED рандомізували для прийому 300 мг арахісу абовідсутності його застосування; за станом хворих ретельно спостерігали протягом усього періоду спостереження. Більшість із пацієнтів втратили десенсибілізацію, та навіть постійне вживання 300 мг призвело до зниження порогу чутливості порівняно зі вживанням більшої кількості арахісу (4 г/добу) [125]. У дослідженні POIMD 1-місячна відмова від арахісу після проведення ПІТ алергеном арахісу призвела до зниження максимально переносимої кількості арахісу більш ніж на 7 г [168]. Аналогічно в дослідженні IMPACT 26-тижнева відмова від арахісу після ПІТ алергеном арахісу супроводжувалася збереженням толерантності тільки у 21% хворих, які отримали лікування [98].
Простішим може бути застосування ПІТ без підвищення дозування. Miura та співавт. повідомили про результати застосування фіксованої дози молочної ПІТ у дітей 1, 2 і 3 років [171]. Діти з тяжкою алергією на молоко отримували фіксовану дозу молока на добу (3 мл) із щорічним проведенням пероральної провокаційної проби за допомогою молока (до 25 мл); досягли зазначеної мети 27, 52 та 61% дітей відповідно. Базовий рівень сIgE прогнозував добру ефективність втручання; в учасників зафіксовано значне зниження сIgE до казеїну зі збільшенням споживання молока та казеїноспецифічного IgG4. Менш інтенсивні режими лікування можуть зробити терапію ХА доступнішою, хоча ефективність її залишається під питанням [172].
Альтернативні шляхи пероральної харчової десенсибілізації продовжують вивчатися. СЛІТ демонструє значну ефективність із мінімальними серйозними побічними діями. Проте цей підхід асоційований із високим рівнем відсіву учасників [177, 178]. Імовірність значного зниження ризику та можливість впровадження в широких масштабах потребують подальших досліджень.
Хоча EПIT продемонструвала сприятливу безпеку та переносимість, її десенсибілізувальна здатність залишається невизначеною [110]. При проведенні EПIT у дітей віком 4-12 років не виявлено жодного епізоду тяжкої анафілаксії, при цьому з дослідження вибули лише 4 пацієнти з 294 [179]. Довгострокове спостереження підтвердило стабільність десенсибілізації протягом 52-130 тижнів, але без розвитку додаткової десенсибілізації після 1 року терапії [117].
У лікуванні ХА відбуваються певні зміни: крім імунотерапії з’являються нові методи, які включають неповне вилучення їжі. Наприклад, у японських настановах щодо лікування ХА (2020) [180] підкреслюється, що метою пероральних провокаційних проб є не тільки діагностика ХА, а й визначення безпечної кількості продуктів для постійного вживання. Коли пацієнти не мають сильної алергії (наприклад, синдром «пилок – їжа», анафілаксія, спричинена фізичним навантаженням, дієта з вилученням пряженого молока / яєць), широко прийнятим підходом є дозвіл на споживання невеликої кількості харчових алергенів [181]. Загалом цей підхід ґрунтується на розумінні того, що більшість людей із ХА не мають тяжкої алергії та можуть переносити прийом невеликої кількості алергенів. Однак потрібне подальше дослідження порогових доз [182-185], а також маркування продуктів. Підпорогова кількість алергенів у харчовому раціоні трапляється при використанні пряженого молока / яєць [186], хоча поки що не зрозуміло, чи буде включення зазначених продуктів у раціон людей з алергією на молоко/яйця ефективнішим за ПІТ.
Діти, які мали алергію на непечені яйця, але були толерантними до печених і перенесли ПІТ алергеном курячого яйця, мали вірогідно більше шансів досягти стійкої толерантності протягом 2 років, аніж діти, які вживали печені яйця [187]. У дітей з алергією на печені яйця можуть виникнути тяжкі алергічні реакції, тому пацієнтів потрібно ретельно відбирати й контролювати введення в раціон хлібобулочних виробів на підставі негативних пероральних провокаційних тестів.
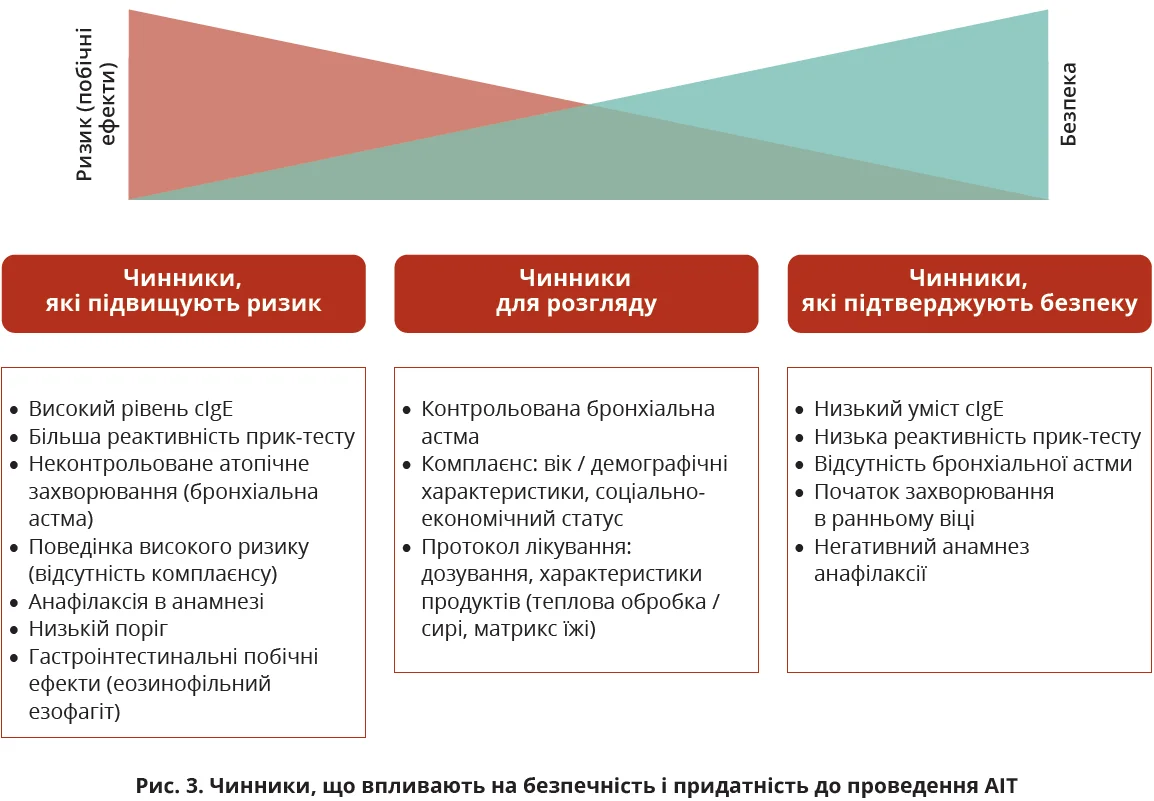
Підбір оптимальної терапії вимагає врахування ризиків і переваг для пацієнта. Оцінка ризику ускладнюється багатьма чинниками, в тому числі неузгодженістю у визначенні тяжкості ХА (рис. 3). Консенсус із визначення ступеня тяжкості ХА (DEFASE) [188] намагається стандартизувати тяжкість захворювання. Визнання недоліків у лікуванні ХА збільшило увагу до спільного з хворими прийняття рішень шляхом проведення двосторонніх обговорень цінностей і цілей пацієнтів, ризиків і переваг [162].
Прогностичні чинники успіху впливають на обговорення ризиків і переваг імунотерапії. Пацієнти молодшого віку, зокрема діти дошкільного віку, мають більшу ймовірність досягнення толерантності, що дає змогу завершити лікування до виникнення значної тривоги щодо стану їхнього здоров’я [193]. Проте невеликий вік асоційований із тим, що багато дітей, яким призначають ПІТ, мають певні ризики, в тому числі трансформації харчової непереносимості в ХА [194]. Статистичний аналіз підтверджує, що пацієнти з низьким умістом сIgE, меншими результатами прик-тесту мають найбільшу ймовірність досягнення десенсибілізації [169]; при цьому найбільшу користь від десенсибілізації отримують хворі з найвищими значеннями цих показників.
Отже, клінічне лікування ХА продовжує вдосконалюватися. Визнано потребу в довготривалому лікуванні, надалі вивчатимуться менш інтенсивні підходи до досягнення десенсибілізації, включаючи фіксоване дозування, низькі підтримувальні дози, альтернативні шляхи, біологічні ад’юванти або монотерапію. Покращення здатності до визначення ризик-фенотипу й пацієнтоцентрований підхід сприятимуть удосконаленню імунотерапії та стимулюватимуть вивчення альтернативних методів лікування.
Висновок
Подальше вдосконалення потенційних біомаркерів імунотерапії сприятиме покращенню лікування ХА та забезпечить упровадження розробленої терапії в клінічну практику. Поточні дослідження ХА допоможуть отримати додаткову інформацію, як краще модифікувати терапію та покращити профіль безпеки наявних режимів лікування.
Література
Locke A., et al. An update on recent developments and highlights in food allergy. Allergy. 2023; 00: 1-17. doi: 10.1111/all.15749.