Новітні терапевтичні агенти в лікуванні хронічної спонтанної кропив’янки
Підготувала Ганна Гаврюшенко
Хронічна спонтанна кропив’янка (ХСК) – це опосередкована тучними клітинами хвороба шкіри, яка проявляється уртикарними висипаннями, ангіоневротичним набряком чи їх поєднанням, що тривають понад 6 тижнів. ХСК є поширеним станом і вражає близько 1% загальної популяції, причому в понад 80% пацієнтів вона триває більш ніж 1 рік. Приблизно в 40% пацієнтів ХСК має значний негативний вплив на якість життя; частими коморбідними станами є тривожність, депресія, розлади сну та сексуальна дисфункція.
ХСК нерідко має непередбачуваний перебіг і погано піддається фармакотерапії. Н1-антигістамінні препарати (Н1-АГП) 2-го покоління, котрі є першою лінією лікування, дають змогу досягти повного контролю над хворобою менш ніж у 10% пацієнтів. Близько 70% пацієнтів з антигістамінорезистентною ХСК не досягають повного контролю при лікуванні омалізумабом, препаратом другої лінії. Отже, існує нагальна потреба в розробленні нових ефективних методів лікування ХСК, що дадуть змогу досягти повного контролю хвороби, а також модифікувати її перебіг і сприяти тривалій ремісії після скасування препарату.
У цьому огляді представлено оновлену інформацію про сучасний стан розвитку методів лікування ХСК, у тому числі про новітні препарати, які перебувають на фінальних етапах розроблення та клінічних випробувань і невдовзі можуть бути впроваджені в лікарську практику, а також про потенційні терапевтичні мішені при ХСК.
Фармакотерапія ХСК: сучасний стан, проблеми та виклики
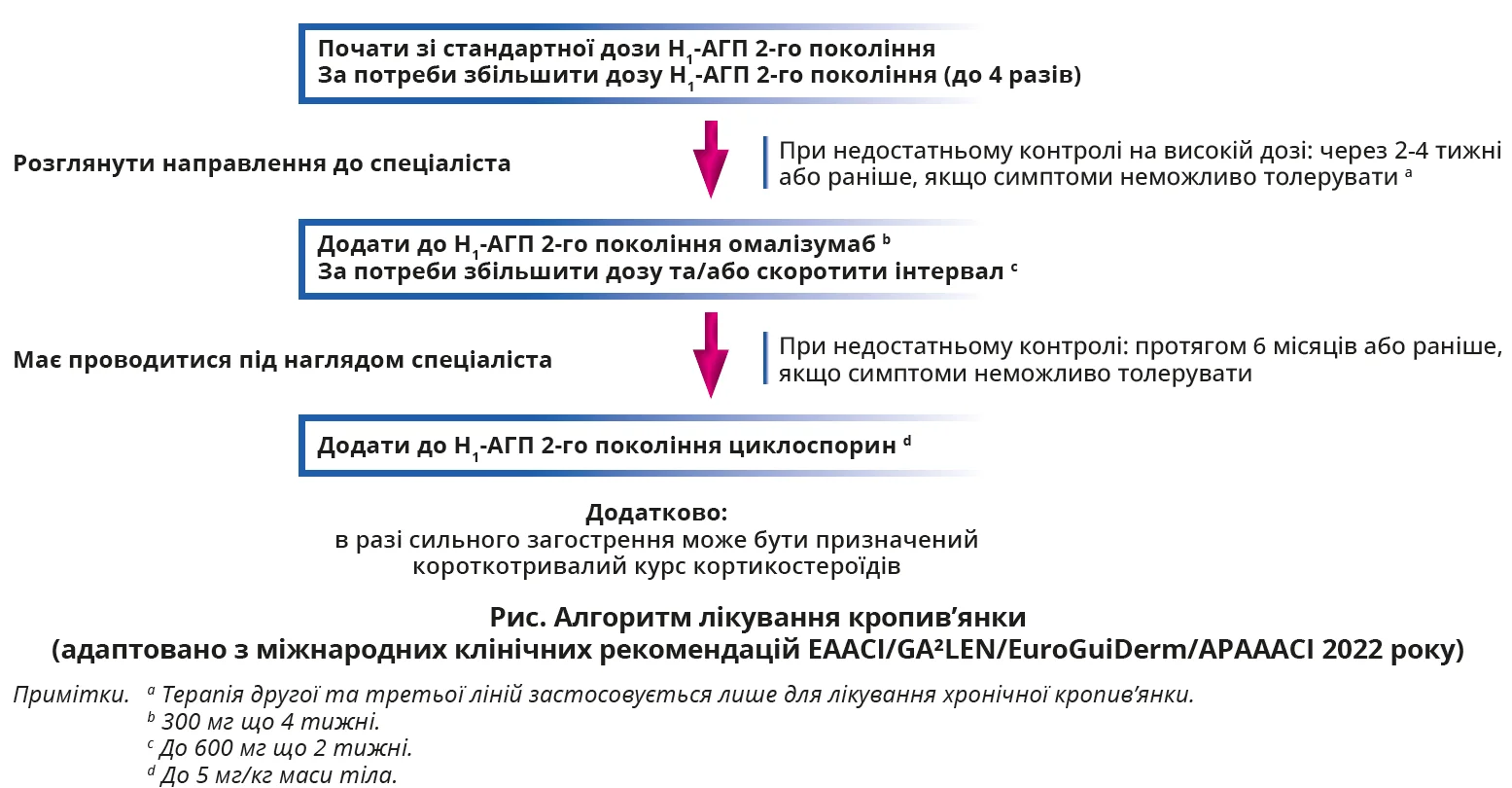
Згідно з міжнародними клінічними рекомендаціями 2022 року метою лікування ХСК є захист від виникнення уртикарного висипу й ангіоневротичного набряку [2]. Алгоритм фармакологічного лікування кропив’янки подано на рисунку. Для оцінювання контролю ХСК широко використовується UCT (Urticaria Control Test; табл. 1), тоді як активність хронічної індукованої кропив’янки (ХІК) в умовах клінічних досліджень оцінюється за допомогою UAS7 (Weekly Urticaria Activity Score; табл. 2).
Повний (16 балів UCT) та хороший контроль хвороби (12-15 балів UCT) під час приймання Н1-АГП 2-го покоління в стандартних і підвищених дозах може бути досягнений приблизно в 7 та 21% пацієнтів відповідно [11]. Близько 30% пацієнтів з ХСК, рефрактерною до антигістамінів (UCT <11), досягають повного контролю при лікуванні омалізумабом, препаратом другої лінії [11, 13]. Циклоспорин А (препарат третьої лінії) може покращити клінічну оцінку перебігу хвороби в більшості резистентних до Н1-АГП 2-го покоління пацієнтів, але він пов’язаний з розвитком ускладнень, як-от артеріальна гіпертензія, ниркова дисфункція та широка імуносупресія [11, 14]. Зважаючи на вищевказане, існує нагальна потреба в розробленні та впровадженні нових ефективних і безпечних методів лікування ХСК.
Новітні препарати для лікування ХСК
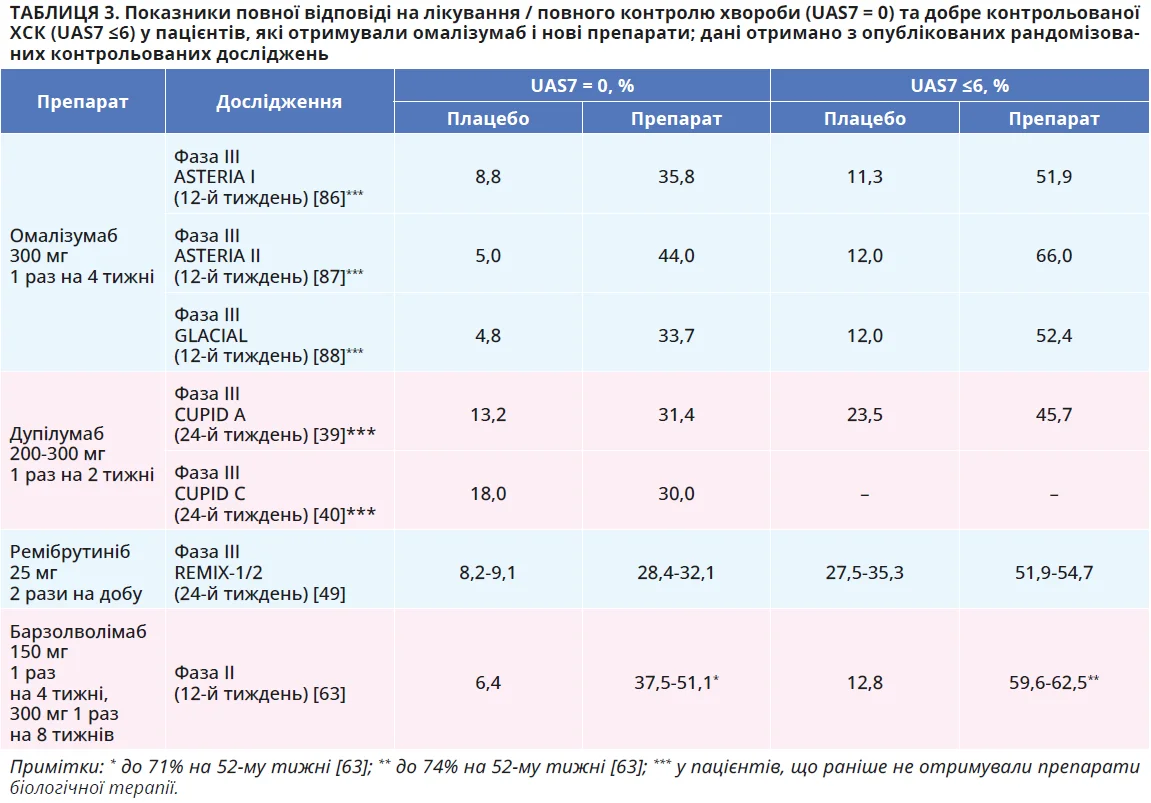
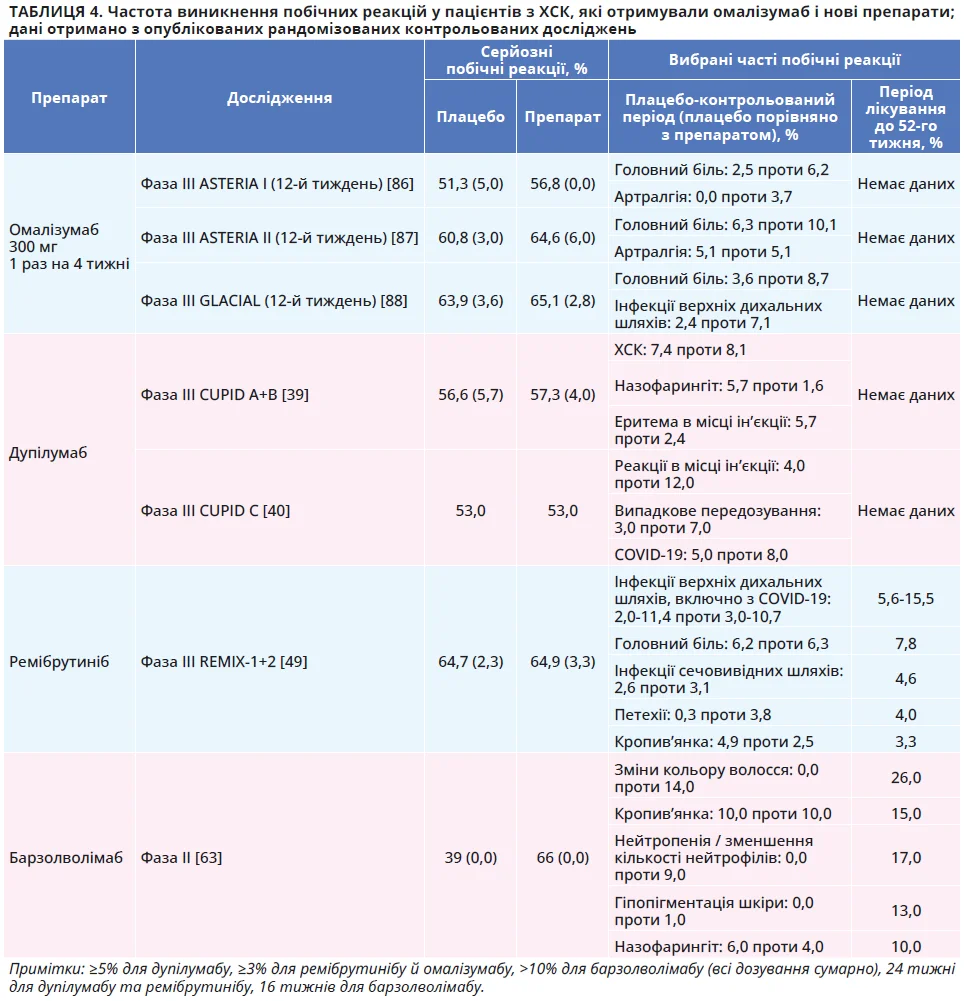
Нині активно впроваджуються нові методи лікування, спрямовані на різні ланки патогенезу ХСК та ефективні для резистентних до Н1-АГП 2-го покоління й омалізумабу пацієнтів. Зокрема, нещодавно став доступним анти-IL-4Rα-препарат дупілумаб, а інші агенти, як-от інгібітори тирозинкінази Брутона (ремібрутиніб) і анти-KIT-препарати (барзолволімаб), перебувають на фінальних стадіях розроблення [17]. Клінічні дослідження демонструють високу ефективність і хорошу переносимість цих засобів: 30-31, 28-32 та 38-51% пацієнтів з ХСК продемонстрували повну відповідь на терапію дупілумабом (фаза III, тиждень 24), ремібрутинібом (фаза III, тиждень 24) і барзолволімабом (фаза II, тиждень12) відповідно. Найпоширенішими небажаними явищами були реакції в місці введення дупілумабу (12%), інфекції дихальних шляхів (11%), головний біль (6%) і петехії (4%) для ремібрутинібу та зміни кольору волосся (14%), нейтропенія / зниження кількості нейтрофілів (9%) і гіпопігментація шкіри (1%) для барзолволімабу.
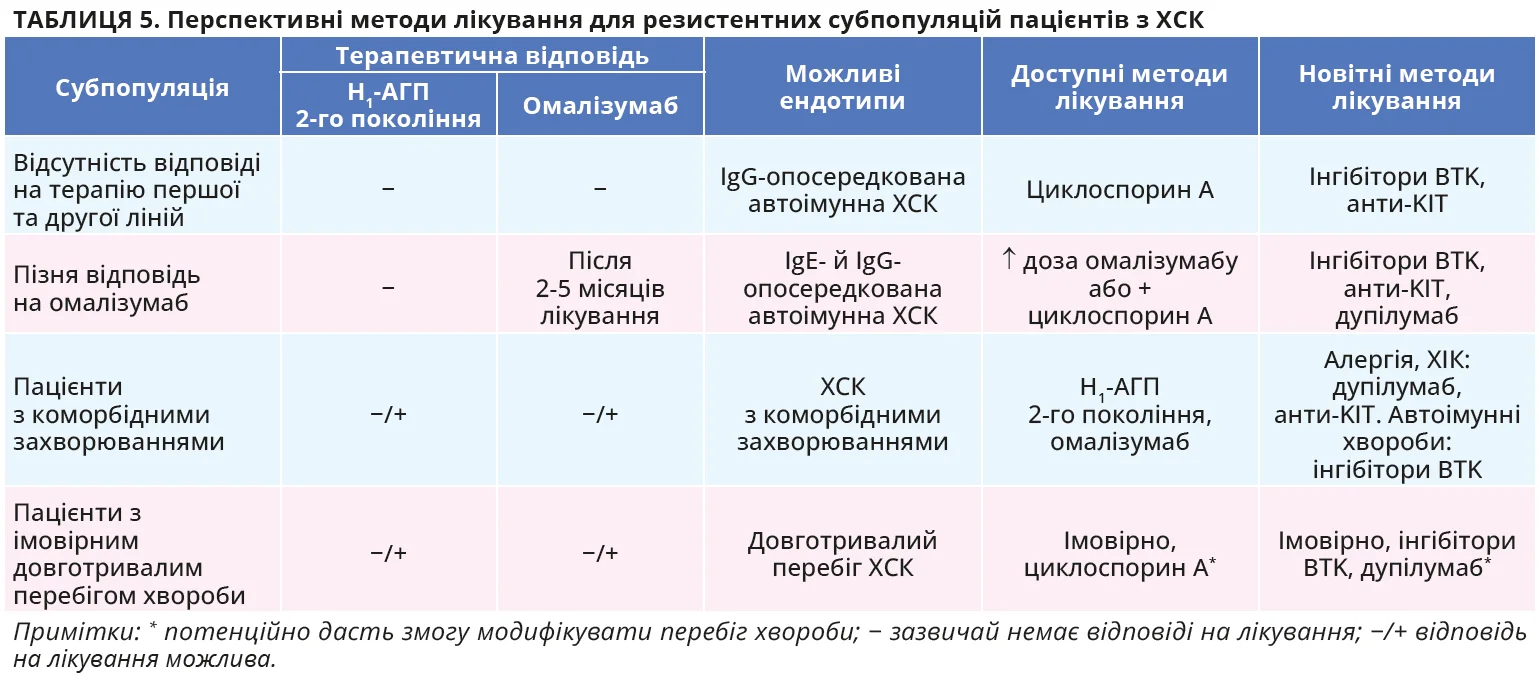
Докладніша інформація про результати клінічних досліджень і профіль безпеки нових препаратів для лікування ХСК подана в таблицях 3 та 4 відповідно. У таблиці 5 наведено дані про підгрупи пацієнтів з ХСК, для котрих упровадження новітніх препаратів є особливо перспективним.
Анти-IL-4Rα-препарати
Запалення 2-го типу, що перебігає за участю тучних клітин, активованих Th2-клітин і під впливом таких цитокінів, як інтерлейкін-4 (IL-4) й інтерлейкін-13 (IL-13), відіграє важливу роль у патогенезі ХСК [17]. IL-4 й IL-13 головним чином продукуються Т-клітинами, тучними клітинами та базофілами [24, 25]. IL-13 частково розділяє сигнальні шляхи з IL-4 завдяки спільному рецепторному субодиничному ланцюгу – IL-4Rα [26-29]. Обидва цитокіни можуть спричиняти розвиток ХСК через стимуляцію вироблення IgE, а також авто-IgE й авто-IgG, активацію шкірних нервових волокон та/або підвищення чутливості тучних клітин до інших стимулів, як-от агоністи рецептора MRGPRX2.
Дупілумаб – це моноклональне антитіло, яке блокує IL-4Rα, тим самим пригнічуючи передачу сигналу як від IL-4, так і від IL-13. Ефективність і профіль безпеки дупілумабу в пацієнтів з рефрактерністю до АГП й омалізумабу або з непереносимістю/відсутністю відповіді на омалізумаб оцінювалися в рандомізованих плацебо-контрольованих дослідженнях III фази – LIBERTY-CSU CUPID A та B. Крім того, в дослідженні LIBERTY-CSU CUPID C вивчали ефективність і безпеку дупілумабу як доповнення до H1-антигістамінних засобів у пацієнтів, у яких симптоми зберігалися, незважаючи на антигістамінну терапію, та які не отримували омалізумаб.
На сьогодні дупілумаб затверджений для лікування таких запальних захворювань 2-го типу, як атопічний дерматит, бронхіальна астма та вузликове пруриго [42]. Нещодавно він також був схвалений у Японії й Об’єднаних Арабських Еміратах для застосування в пацієнтів з ХСК віком від 12 років, у яких захворювання не піддається належному контролю за допомогою наявної терапії. Наразі дупілумаб перебуває на етапі регуляторного розгляду в країнах Європи та Північної Америки.
Інгібітори BTK
У патогенезі ХСК крослінкінг рецепторів FcεRI є ключовим механізмом активації шкірних тучних клітин і подальшого вивільнення ними прозапальних медіаторів. Після активації FcεRI вмикається внутрішньоклітинна сигнальна мережа, в якій тирозинкіназа Брутона (BTK) відіграє центральну роль [43, 44]. Окрім тучних клітин, BTK експресується також у базофілах, В-клітинах, моноцитах і тромбоцитах, де бере участь у сигнальних шляхах, пов’язаних з В-клітинними рецепторами (BCR) та Toll-подібними рецепторами (TLR).
Інгібування BTK запобігає FcεRI-опосередкованій дегрануляції та синтезу цитокінів de novo в тучних клітинах [47]. Отже, терапевтичне блокування BTK може не лише зменшити дегрануляцію тучних клітин і базофілів, але й пригнітити активацію BCR і TLR-шляхів, потенційно обмежуючи експансію автореактивних клональних В-клітин [45]. У цьому контексті інгібітори BTK забезпечують подвійний механізм дії в лікуванні ХСК: ефективно пригнічують активацію ефекторних клітин (тучних клітин і базофілів) і водночас знижують вироблення автоантитіл.
Ремібрутиніб – це пероральний високоселективний незворотний інгібітор BTK. Його ефективність і безпеку оцінювали в подвійно сліпих плацебо-контрольованих дослідженнях III фази REMIX-1 і REMIX-2. У них брали участь, відповідно, 470 і 455 пацієнтів з ХСК віком ≥18 років, які не досягли адекватного контролю симптомів у разі застосування Н1-АГП 2-го покоління. Об’єднаний аналіз результатів цих досліджень продемонстрував ефективність ремібрутинібу та сприятливий профіль його безпеки [49].
Наразі ремібрутиніб додатково вивчається в когорті пацієнтів з ХІК, а також серед підлітків з ХСК.
KIT-таргетні препарати
Тирозинкіназний рецептор KIT і його ліганд – фактор стовбурових клітин (ФСК) – є важливими для розвитку та диференціації тучних клітин з гемопоетичних стовбурових клітин, а також для регуляції вивільнення ними прозапальних медіаторів [60, 61].
Барзолволімаб – гуманізоване моноклональне антитіло класу IgG1κ, яке з високою афінністю зв’язується з рецептором KIT і блокує взаємодію з ФСК, тим самим запобігаючи його активації. Ефективність барзолволімабу при антигістамінорезистентній ХСК була продемонстрована в клінічному дослідженні II фази за участю 208 пацієнтів (NCT05368285) [62]. Препарат виявився ефективним незалежно від попереднього застосування омалізумабу [63].
Наразі триває програма клінічних досліджень III фази, що включає два дослідження (EMBARQ-CSU1 та EMBARQ-CSU2), у яких оцінюються ефективність і безпека барзолволімабу в дорослих пацієнтів з ХСК, рефрактерною до Н1-АГП 2-го покоління.
У дослідження також залучені пацієнти, які раніше отримували біологічну терапію.
Інші потенційні препарати для лікування ХСК
Інгібітори JAK
Сімейство Янус-кіназ (JAK) включає чотири цитоплазматичні тирозинкінази – JAK1, JAK2, JAK3 і Tyk2, які зв’язуються безпосередньо з внутрішньоклітинними доменами рецепторів цитокінів (наприклад, IL-4R, IL-5R, IL-6R, IL-13R) і активуються багатьма цитокінами. Після активації JAK фосфорилюють білки STAT, що мігрують у ядро й активують експресію прозапальних цитокінів, як-от IL-4, IL-13, IL-31 та TSLP [67, 68].
Інгібітори JAK продемонстрували ефективність у лікуванні низки дерматологічних захворювань, у тому числі атопічного дерматиту [68]. Проте опубліковані дані щодо ефективності цих препаратів у лікуванні ХСК поки що обмежені. Зокрема, Mansouri та колеги повідомили про чотири випадки ХСК й один випадок уртикарного васкуліту, успішно контрольовані за допомогою тофацитинібу (5 мг двічі на добу), а Shibu та колеги описали ще п’ять випадків ХСК, чутливих до тофацитинібу [70, 71]. У пацієнтів спостерігалося покращення або досягнення ремісії навіть після безуспішної терапії Н1-АГП 2-го покоління, кортикостероїдами, циклоспорином A й іншими імуносупресантами. Водночас варто брати до уваги потенційні ризики застосування інгібіторів JAK, зокрема розвиток опортуністичних інфекцій (наприклад, Herpes zoster), цитопеній, венозного тромбозу та гіперліпідемії [67].
Інгібітори MRGPRX2
MRGPRX2 – це нещодавно описаний рецептор, який бере участь в IgE-незалежних шляхах активації тучних клітин [72, 73]. Ступінь залучення цього й інших не-FcεRI-залежних механізмів у дегрануляцію тучних клітин у разі ХСК поки що остаточно не з’ясований. Однак, з огляду на значущу роль MRGPRX2, його інгібітори розглядаються як перспективні терапевтичні агенти при різних опосередкованих тучними клітинами хворобах [72].
Підходи до терапії, спрямованої на MRGPRX2, умовно поділяються на три категорії: 1) пряме блокування рецептора MRGPRX2; 2) пригнічення внутрішньоклітинної сигналізації, зокрема шляхом зменшення концентрації кальцію в цитозолі; 3) альтернативні механізми, як-от активація CD300f – супресора MRGPRX2-залежної активації тучних клітин [72]. Наразі тривають клінічні дослідження I та II фаз MRGPRX2-спрямованих терапевтичних агентів у лікуванні ХСК.
Висновки та перспективи
Ландшафт терапії ХСК динамічно розширюється: біосиміляри омалізумабу вже виходять на ринок, а нові малі молекули та біологічні препарати стануть доступними в найближчі 1-2 роки. Зокрема, CT-P39 (Omlyclo®) – перший біосиміляр омалізумабу був нещодавно схвалений для використання в Європі. Такі препарати, як дупілумаб і ремібрутиніб, можуть незабаром отримати схвалення для терапії резистентної до Н1-АГП 2-го покоління ХСК у різних країнах світу. Вони також мають потенціал для лікування пацієнтів, які не відповідають на анти-IgE-терапію або мають супутні хвороби.
Ендотипування пацієнтів з ХСК – наприклад, диференціація між автоімунною, автоалергічною, перехресною або FcεRI-незалежною формами – разом з виявленням специфічних біомаркерів, як-от загальний рівень IgE та базофільні тести, сприятиме персоналізованому підходу в межах прецизійної медицини, оптимізуючи ефективність терапії. Деякі терапевтичні підходи, зокрема інгібітори BTK й анти-KIT-препарати, демонструють потенціал у лікуванні складних для контролю ендотипів ХСК, як-от автоімунна форма ХСК.
У довгостроковій перспективі ще специфічніші новітні методи можуть покращити результати лікування ХСК. До таких методів належать вплив одночасно на декілька цитокінових шляхів (наприклад, біспецифічні або триспецифічні антитіла [82]), комбіноване застосування препаратів (наприклад, омалізумаб з дупілумабом), модуляція кишкового мікробіому [83], а також вакцинотерапія, спрямована проти IgE, IL-4 та/або IL-13 [84]. Зрештою, майбутні дослідження з довготривалим спостереженням покажуть, чи зможуть нові терапевтичні агенти, як-от інгібітори BTK або дупілумаб, змінити перебіг хвороби та стати проривом у терапії ХСК.
Література
Kolkhir P., Fok J.S., Kocatürk E., et al. Update on the treatment of chronic spontaneous urticaria. Drugs. 2025 Apr; 85 (4): 475-486. doi: 10.1007/s40265-025-02170-4.