Монтелукаст у педіатричній популяції: невропсихіатрична безпека (огляд доказових даних)
Підготувала канд. мед. наук Тетяна Можина
Монтелукаст, найширше використовуваний модифікатор лейкотрієнів, являє собою селективний антагоніст лейкотрієнових рецепторів (АЛР) із виразною протизапальною та бронхолітичною активністю. Нині він має декілька офіційних показань до застосування як у дорослій, так і в педіатричній популяції: бронхіальна астма (БА) [4, 22, 25, 32], алергічний риніт (АР) [21], профілактика астматичного нападу, спричиненого фізичним навантаженням (рис. 1) [31]; інколи його також призначають поза зареєстрованими показаннями: хронічне обструктивне захворювання легень, синдром обструктивного апное сну (СОАС) [15]. Протягом останніх років з’являються докази доцільності використання монтелукасту в схемах лікування весняного алергічного кератокон’юнктивіту [12], ішемічної хвороби серця та гострого коронарного синдрому, профілактиці тромботичних ускладнень [3], терапії COVID-19 [1], атопічного дерматиту [6].
Сучасна доказова база ефективності
Монтелукаст зробив значний внесок у досягнення контролю над перебігом БА завдяки своїм протизапальній і бронхолітичній діям, а простота його застосування, одноразовий пероральний режим прийому зробили препарат надзвичайно затребуваним у педіатричній практиці [17]. Доказовий портфель монтелукасту продовжує поповнюватися новими свідоцтвами ефективності: рандомізовані контрольовані дослідження (РКД), систематичні огляди та метааналізи підтверджують високу результативність препарату в лікуванні педіатричної БА [26], СОАС [18], підтримують доцільність його комбінації з інгаляційними кортикостероїдами (ІКС) у зв’язку зі значним підвищенням ефективності останніх у лікуванні БА [29]. Результативність монтелукасту в нівелюванні СОАС, який зазвичай виникає в дітей на тлі хронічного аденоїдиту, настільки висока, що нині його застосування вважається ефективним способом уникнути хірургічного втручання з видалення гіпертрофованих аденоїдів і мигдаликів [15]. Сприятливий вплив монтелукасту на СОАС у дітей підтверджують експерти Кокранівського товариства [16]. Встановлено, що монтелукаст не тільки ефективно нівелює симптоми АР (середня різниця -0,28; 95% довірчий інтервал (ДІ) від -0,54 до -0,023; р=0,033) порівняно з плацебо [30], а й на відміну від антигістамінних засобів краще запобігає появі патологічних ознак уночі (середня різниця -0,04; 95% ДІ від -0,08 до -0,01; р=0,008) [28].
Невропсихіатричний профіль безпеки
Результати РКД
Отримання таких разючих даних щодо ефективності препарату супроводжувалося ретельним аналізом загального профілю безпеки монтелукасту. Первинно накопичені дані давали змогу вважати монтелукаст відносно безпечним препаратом для застосування в педіатричній практиці, оскільки частота повідомлень про виникнення побічних дій була зіставною з такою в контрольній групі [5]. Результати РКД, інструкція до препарату попереджали про низький ризик розвитку небажаних реакцій і перелічували найімовірніші з них: лихоманка, інфекція верхніх дихальних шляхів і загострення БА. Добру переносимість і високу безпеку перорального монтелукасту відзначено у великій кількості досліджень, автори яких не спостерігали жодних серйозних побічний дій на тлі його застосування [12, 15, 26]. Нещодавно опубліковане проспективне двоцентрове когортне дослідження підтвердило добрий профіль безпеки монтелукасту та можливість його застосування у вагітних, оскільки прийом препарату не супроводжувався виникненням серйозних уроджених аномалій (скореговане відношення шансів (ВШ) 0,78; 95% ДІ 0,23-2,05; p=0,653), мертвонародженням, спонтанними абортами, передчасними пологами, низькою вагою при народженні [13].
І ось на тлі досить вдалого та впевненого існування монтелукасту на міжнародному фармацевтичному ринку спочатку з’являються поодинокі повідомлення, а потім результати РКД, в яких описується здатність монтелукасту провокувати різноманітні невропсихіатричні побічні дії: порушення сну, включаючи нічні кошмари, галюцинації, дезорієнтацію, безсоння, сомнамбулізм, психомоторну гіперактивність, дратівливість, неспокій, тривожність, збудження, агресивну поведінку або ворожість, тремор, депресію, суїцидальні думки, порушення уваги, погіршення пам’яті [8-10, 33].
Причому зазначені побічні ефекти спостерігали як у пацієнтів із психічними захворюваннями в анамнезі, так і без них [9].
Наведемо дані масштабного епідеміологічного дослідження, в якому аналізували ймовірність розвитку різноманітної невропсихіатричної симптоматики у хворих на БА (n=72 490) й АР (n=82 456): на тлі прийому монтелукасту цей ризик визнаний імовірним, але невеликим (ВШ 1,11; 95% ДІ 1,04-1,19) [33]. Найчастіше хворих на БА турбували тривожні розлади (ВШ 1,21; 95% ДІ 1,05-1,20), тоді як пацієнтам з АР більше докучало безсоння (ВШ 1,15; 95% ДI 1,05-1,27) [33]. Канадські дослідники зафіксували 898 невропсихіатричних випадків і порівняли частоту їх виникнення в контрольній групі дітей (n=3497) [10]. Виявилося, що ризик розвитку будь-якої психоневрологічної події є вищим у тих дітей, які приймали монтелукаст із приводу БА (ВШ 1,91; 95% ДІ 1,15-3,18; р=0,01), причому найчастіше маленькі пацієнти страждали від тривоги (48,6%) та/або порушення сну (26,1%) [10].
Аналіз бази даних VigiBase
Розглядаючи питання безпеки будь-якого лікарського засобу, зазвичай аналізують інформацію, що міститься у VigiBase – найбільшій усесвітній базі даних щодо індивідуальної безпеки ліків (ICSR), яка створена та працює під патронатом Всесвітньої організації охорони здоров’я. Дані, накопичені у VigiBase, використовуються фармацевтичною промисловістю, академічними установами та регуляторними органами для визначення статистичної ймовірності виникнення побічних дій, оновлення періодичних звітів, порівнянь зареєстрованих ICSR із даними фармацевтичних компаній тощо.
Відомості про невропсихіатричні побічні дії монтелукасту надходять у VigiBase та зберігаються там. Як свідчить один з аналітичних оглядів цієї бази даних, у загальній популяції монтелукаст провокує виникнення депресії (звітне ВШ (ЗВШ) 6,93; 95% ДІ 6,5-7,4), головного болю (ЗВШ 1,85; 95% ДІ 1,75-1,970), безсоння (ЗВШ 5,08; 95% ДІ 4,8-5,4), тривожності (ЗВШ 5,11; 95% ДІ 4,8-5,5), задишки (ЗВШ 1,30; 95% ДІ 1,20-1,41), запаморочення (ЗВШ 0,89; 95% ДІ 0,82-0,97) [11]. У педіатричній популяції прийом монтелукасту асоційований із розвитком агресії (ЗВШ 24,99; 95% ДІ 23,5-26,6), суїцидальних думок (ЗВШ 20,4; 95% ДІ 19-22), кошмарів (ЗВШ 22,46; 95% ДІ 20,9-24,2) [11]. Інші вчені, які також ретроспективно аналізували звіти ICSR, представлені у VigiBase, констатували, що застосування монтелукасту в немовлят <2 років переважно асоційоване з розладами сну, в дітей 2-11 років – із депресією/тривогою, в підлітків 12-17 років – із суїцидальною поведінкою, депресією/занепокоєнням [2]. Нещодавній аналіз VigiBase підтвердив імовірність виникнення кошмарів на тлі прийому монтелукасту, причому найбільше поширення цього симптому зафіксовано в дітей 5-10 років [27]. Покращення стану пацієнтів зазвичай визначають після скасування препарату, яке сприяє повному нівелюванню невропсихіатричної симптоматики [27].
Механізм виникнення
Нині точні механізми впливу монтелукасту на мозок не відомі; припускають, що його метаболіти можуть перешкоджати детоксикації глутатіону або порушувати регуляцію різних нейромедіаторних шляхів, зокрема тих, які беруть участь у регуляції гіпоталамо-гіпофізарно-надниркової осі [19].
Ставлення та рекомендації офіційних регуляторів
Американський регулятор
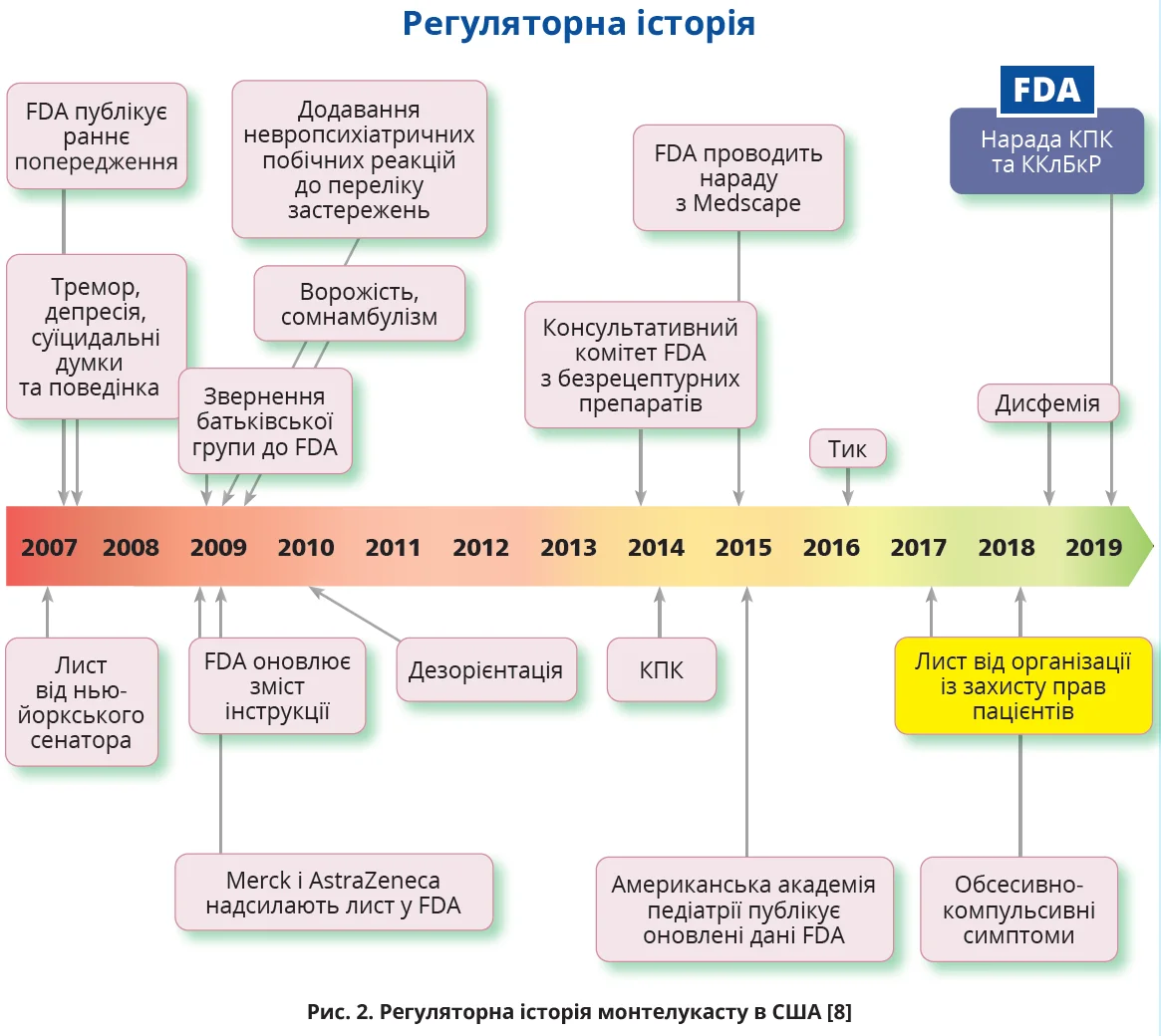
Ця інформація, безперечно, привернула увагу регуляторних органів, і першим на проблему відреагувало Управління з контролю продуктів харчування та лікарських засобів США (FDA). Перші 9 років активного клінічного застосування монтелукасту майже не затьмарювалися повідомленнями щодо особливостей його невропсихіатричного профілю безпеки, поки у 2007 р. FDA не отримало листа від американського сенатора, в якому він інформував регуляторний орган щодо появи тремору, депресії, суїцидальних думок у пацієнтів, які приймали зазначений АЛР (рис. 2) [8]. Того самого року FDA публікує раннє попередження, а у 2009 р. в інструкції до монтелукасту з’являється інформація щодо можливих невропсихіатричних побічних реакцій.
У 2009-2010 рр. перелік можливих побічних дій доповнили агресивна поведінка, сомнамбулізм і дезорієнтація. Через 5 років питання невропсихіатричної безпеки монтелукасту розглянули Консультативний комітет FDA з безрецептурних препаратів і Консультативний педіатричний комітет (КПК); у 2015 р. експерти FDA після наради з представниками найбільшої електронної медичної бази даних Pubmed представили оновлений звіт щодо безпеки монтелукасту, який презентувала медичній спільноті Американська академія педіатрії [8]. Протягом 2016-2019 рр. прийом монтелукасту почали пов’язувати з можливим розвитком тику, обсесивно-компульсивного синдрому, дисфемії (функціонального порушення артикуляції). Результатом спільної наради КПК та Консультативного комітету FDA з лікарської безпеки та корекції ризику (ККлБкР), що відбулась у 2019 р., стало прийняття рішення щодо вивчення механізмів невропсихіатричних побічних дій монтелукасту, встановлення чинників ризику та з’ясування наявності/відсутності симптомів скасування, розроблення спеціального інформаційного листка-вкладиша для пацієнтів і порад для лікарів, додавання до інструкції особливого застереження, котре для максимального привертання уваги медиків і пацієнтів розміщують у чорній рамці [8].
Незважаючи на всі розглянуті докази невропсихіатричних побічних дій, в остаточному звіті щодо клінічного застосування монтелукасту представники FDA зазначили, що всі препарати мають потенційні побічні ефекти, але продумане використання може максимізувати користь і мінімізувати ризики. Згідно з наявною доказовою базою користь від застосування монтелукасту перевищує можливу шкоду [9]. «Виявлення побічних ефектів потребує пильності й знань від лікарів, які призначають ліки, та батьків, котрі стежать за своїми дітьми» [24].
Британський регулятор
Британський регулятор, підтримуючи ставлення FDA до питання невропсихіатричної безпеки монтелукасту, зауважує, що такі несприятливі реакції виникають надзвичайно рідко: протягом 2014-2018 рр. у Великій Британії виписано понад 14 млн рецептів на монтелукаст, при цьому зафіксовано тільки 219 випадків, підозрілих щодо виникнення невропсихіатричних реакцій [20]. «Установлено, що порушення сну, депресію й агресію відчуває 1 зі 100 пацієнтів, які приймають цей АЛР, порушення уваги або пам’яті констатує 1 із 1000 хворих, надзвичайно рідко фіксують появу галюцинацій і суїцидальної поведінки: 1 з 10 000 осіб», – підкреслюють експерти [20]. Британський регулятор зазначає, що такі монтелукаст-асоційовані невропсихічні реакції, як нічні жахи, депресія, безсоння, агресія, тривожність і суїцидальна поведінка, можуть виникнути як у дорослих, так і в дітей, але найчастіше в педіатричній популяції фіксують нічні кошмари, агресію та зміни поведінки. Зважаючи на невелику частоту виникнення невропсихіатричних побічних дій і високу терапевтичну активність препарату, британський регулятор не бачить підстав для обмеження застосування препарату у хворих на БА, тим паче його відкликання з ринку [20].
Рекомендації FDA лікарям, які призначають монтелукаст [8, 23]
- Рекомендуємо призначати монтелукаст для лікування АР лише пацієнтам із неадекватною реакцією / непереносимістю альтернативних методів терапії.
- Перед призначенням препарату розпитайте пацієнта щодо наявності будь-якого психіатричного захворювання в анамнезі.
- Враховуйте ризики та переваги монтелукасту, приймаючи рішення про призначення/продовження лікування.
- Призначаючи монтелукаст усім пацієнтам, повідомляйте про ризик виникнення невропсихіатричних побічних явищ.
- Порадьте пацієнтам і батькам / особам, які здійснюють догляд за дитиною, припинити прийом монтелукасту та негайно звернутися до лікаря при виникненні змін у поведінці / нових невропсихічних симптомів, суїцидальних думок і поведінки.
- Варто спостерігати за всіма пацієнтами, які приймають монтелукаст, контролюючи появу невропсихічних симптомів.
- Заохочуйте пацієнтів та їхніх батьків/опікунів ознайомитися з інструкцією для медичного застосування, котру вони отримують разом із рецептом на монтелукаст, де пояснюються можливі ризики та надається інша важлива інформація.
Рекомендації британського регулятора лікарям, які призначають монтелукаст [20]
- Рекомендуємо пацієнтам та особам, які здійснюють догляд за хворими, уважно ознайомитися з переліком невропсихічних реакцій в інструкції для медичного застосування та негайно звернутися по медичну допомогу в разі їх виникнення.
- Ретельно оцінити ризик і користь від продовження лікування при виникненні невропсихічних реакцій.
- Знати про нещодавно виявлені невропсихічні реакції у вигляді заїкання й обсесивно-компульсивних симптомів.
Рекомендації британського регулятора пацієнтам, які приймають монтелукаст [20]
- Важливо, щоби ви або ваша дитина не припиняли прийом монтелукасту без попередньої консультації з лікарем.
- Про побічні реакції, що впливають на сон, поведінку та настрій в осіб, які приймають монтелукаст, повідомляють не часто.
- Завжди читайте інструкцію, яка додається до ваших ліків або ліків вашої дитини, та звертайтеся до лікаря, якщо ви підозрюєте будь-які серйозні побічні реакції на монтелукаст.
Європейський регулятор
Європейське медичне агентство (EMA) схвалило використання монтелукасту в педіатричній популяції у 2008 р.; відтоді на сайті цього регулятора ми не змогли знайти будь-які оновлення з приводу невропсихічних побічних дій або попереджень щодо його застосування [14].
Місце монтелукасту в сучасних настановах
Вищеописані застереження підвищили рівень уважності лікарів, але майже не відобразилися на положеннях міжнародних настанов. Сучасні японські рекомендації щодо лікування БА в дітей (2020) передбачають призначення АЛР за помірного, середньотяжкого й тяжкого перебігу персистивної астми як комбінованої терапії з ІКС із 1-го по 4-й крок лікування БА [4]. Японські рекомендації передбачають застосування монтелукасту в дітей 2-15 років. Оновлена Глобальна ініціатива з астми (GINA, 2023) для дітей віком 6-11 років рекомендує використовувати монтелукаст із метою запобігання загостренням і контролювання симптомів БА на 2-4-му кроках як терапію другої лінії [25]. Оновлені французькі рекомендації (2021) також допускають призначення монтелукасту при лікуванні БА в комбінації з ІКС [22]. Український уніфікований клінічний протокол підкреслює, що монтелукаст застосовується для монотерапії БА як альтернатива ІКС у лікуванні легкої персистивної БА та вірус-індукованої бронхіальної обструкції в дітей з інтермітивною БА; він також може додатково призначатися до ІКС за відсутності належного контролю при лікуванні ІКС [31]. За потреби скасування монтелукасту з будь-якої причини можна не переживати за погіршення перебігу БА: скасування цього АЛР не супроводжується вірогідними змінами функціонального стану легень, у тому числі об’єму форсованого видиху [7].
Резюме
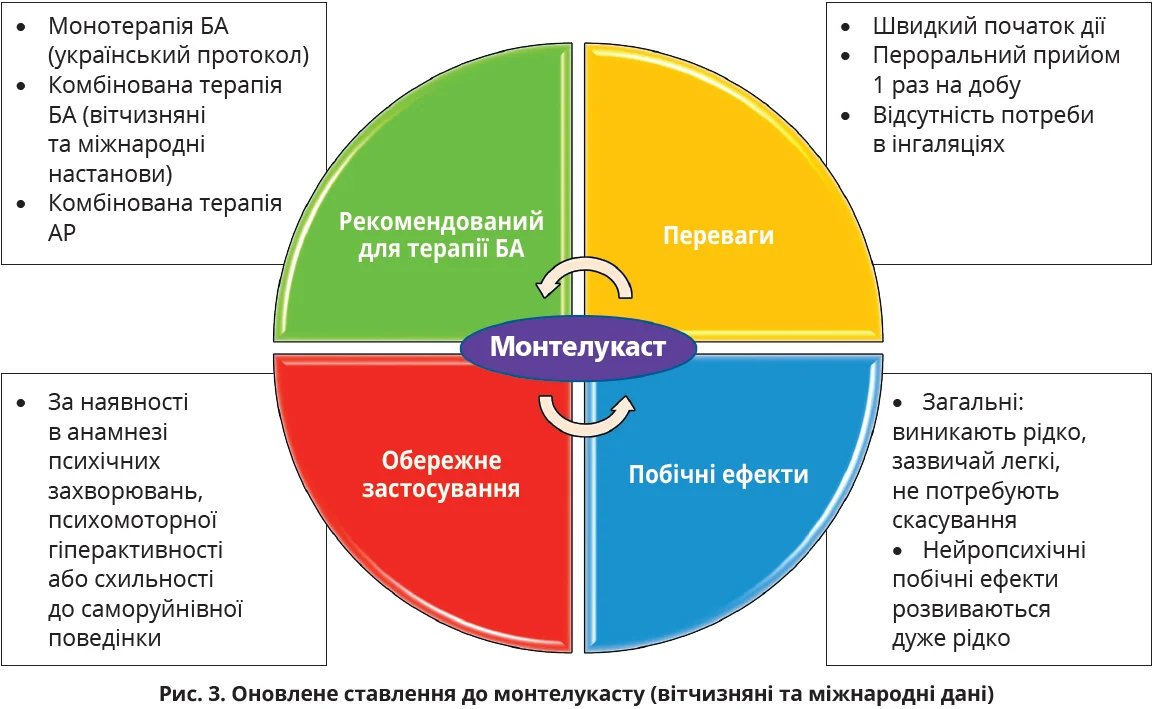
Експерти вважають, що монтелукаст, як і будь-який лікарський препарат, варто призначати пацієнтам, зваживши користь і ризик. При цьому монтелукаст як і раніше залишається препаратом для лікування БА в режимі як монотерапії (український протокол), так і комбінованої (вітчизняні та міжнародні настанови), а також АР (міжнародні рекомендації) (рис. 3). Протипоказання до призначення монтелукасту не змінилися: його не можна застосовувати в дітей до 2 років, у разі підвищеної чутливості до препарату, фенілкетонурії. За вагітності та в період грудного вигодовування монтелукаст слід застосовувати, тільки якщо очікувана користь для матері перевищує потенційні ризики для плода/дитини.
Монтелукаст має високий рівень безпеки, загальні побічні ефекти розвиваються рідко, зазвичай бувають легкими та не потребують скасування препарату; невропсихіатричні побічні ефекти розвиваються дуже рідко. Враховуючи можливий (хоч і вкрай рідкісний) розвиток психоневрологічних симптомів, слід утримуватися від призначення монтелукасту пацієнтам, які мають психічні захворювання, психомоторну гіперактивність або схильність до саморуйнівної поведінки. При первинному призначенні монтелукасту потрібно попереджати пацієнтів та/або їхніх батьків про потенційно можливі психоневрологічні побічні явища. У разі розвитку побічних психоневрологічних явищ слід негайно скасувати препарат і провести корекцію базисної терапії. Водночас надмірна обережність може призвести до того, що ефективне лікування не буде призначено, а це обмежить імовірність досягнення контролю над перебігом захворювання та не забезпечить покращення якості життя.
Зважаючи на те що абсолютна більшість пацієнтів із БА й АР ефективно та тривало приймають монтелукаст на тлі доброї переносимості, відсутності будь-яких небажаних побічних ефектів, офіційні регулятори та міжнародні настанови не вважають за доцільне відмовлятися від застосування цього препарату. Обмежень за тривалістю прийому монтелукасту немає: в разі ефективності та відсутності побічних явищ він може використовуватися місяці та навіть роки.
Література
- Aigner L., Pietrantonio F., Bessa de Sousa D.M., et al. The leukotriene receptor antagonist montelukast as a potential COVID-19 therapeutic. Front. Mol. Biosci. 2020; 7: 610132. doi: 10.3389/fmolb.2020.610132.
- Aldea Perona A., García-Sáiz M., Sanz Álvarez E. Psychiatric disorders and montelukast in children: a disproportionality analysis of the VigiBase. Drug Saf. 2016; 39 (1): 69-78. doi: 10.1007/s40264-015-0360-2.
- Alomair B.M., Al-Kuraishy H.M., Al-Gareeb A., et al. Montelukast and acute coronary syndrome: the endowed drug. Pharmaceuticals (Basel). 2022 Sep 14; 15 (9): 1147. doi: 10.3390/ph15091147.
- Arakawa H., Adachi Y., Ebisawa M., et al. Japanese guidelines for childhood asthma 2020. Allergol. Int. 2020; 69 (3): 314-330. doi: 10.1016/j.alit.2020.02.005.
- Bisgaard H., Skoner D., Boza M., et al. Safety and tolerability of montelukast in placebo-controlled pediatric studies and their open-label extensions. Pediatr. Pulmonol. 2009; 44: 568-79.
- Chin W.K., Lee S. A systematic review on the off-label use of montelukast in atopic dermatitis treatment. Int. J. Clin. Pharm. 2018; 40 (5): 963-976. doi: 10.1007/s11096-018-0655-3.
- Dixon E.G., King C., Lilley A., et al. Deprescribing montelukast in children with asthma: a systematic review. BMJ Open. 2022; 12 (1): e053112. doi: 10.1136/bmjopen-2021-053112.
- FDA Joint Meeting of the Pediatric and Drug Safety and Risk Management Advisory Committees Neuropsychiatric Events with the use of Montelukast in Pediatric Patients. 2019. Available at: https://www.fda.gov/media/131182/download.
- FDA requires Boxed Warning about serious mental health side effects for asthma and allergy drug montelukast (Singulair); advises restricting use for allergic rhinitis.
- Glockler-Lauf S.D., Finkelstein Y., Zhu J., et al. Montelukast and neuropsychiatric events in children with asthma: a nested case-control study. J. Pediatr. 2019; 209: 176-182.e4. doi: 10.1016/j.jpeds.2019.02.009.
- Haarman M.G., van Hunsel F., de Vries T.W. Adverse drug reactions of montelukast in children and adults. Pharmacol. Res. Perspect. 2017; 5 (5): e00341. doi: 10.1002/prp2.341.
- Hardas A., Singh N., Mohanty A., et al. Efficacy of montelukast in preventing seasonal recurrence of vernal keratoconjunctivitis in children. Eye (Lond.). 2022; 36 (5): 978-984. doi: 10.1038/s41433-021-01484-3.
- Hatakeyama S., Goto M., Yamamoto A., et al. The safety of pranlukast and montelukast during the first trimester of pregnancy: a prospective, two-centered cohort study in Japan. Congenit. Anom. (Kyoto). 2022; 62 (4): 161-168. doi: 10.1111/cga.12471.
- EMA. Singular. Available at: https://www.ema.europa.eu/en/medicines/human/referrals/singulair#key-facts-section.
- Ji T., Lu T., Qiu Y., et al. The efficacy and safety of montelukast in children with obstructive sleep apnea: a systematic review and meta-analysis. Sleep Med. 2021; 78: 193-201. doi: 10.1016/j.sleep.2020.11.009.
- Kuhle S., Hoffmann D.U., Mitra S., et al. Anti-inflammatory medications for obstructive sleep apnoea in children. Cochrane Database Syst. Rev. 2020; 1 (1): CD007074. doi: 10.1002/14651858.
- Lee Y.J., Kim C.K. Montelukast use over the past 20 years: monitoring of its effects and safety issues. Clin. Exp. Pediatr. 2020; 63 (10): 376-381. doi: 10.3345/cep.2019.00325.
- Liming B.J., Ryan M., Mack D., et al. Montelukast and nasal corticosteroids to treat pediatric obstructive sleep apnea: a systematic review and meta-analysis. Otolaryngol. Head Neck Surg. 2019; 160 (4): 594-602. doi: 10.1177/0194599818815683.
- Marques C.F., Marques M.M., Justino G.C. The mechanisms underlying montelukast’s neuropsychiatric effects – new insights from a combined metabolic and multiomics approach. Life Sci. 2022; 310: 121056. doi: 10.1016/j.lfs.2022.121056.
- Montelukast (Singulair): reminder of the risk of neuropsychiatric reactions. Medicines and Healthcare products Regulatory Agency. Available at: https://www.gov.uk/drug-safety-update/montelukast-singulair-reminder-of-the-risk-of-neuropsychiatric-reactions.
- Okubo K., Kurono Y., Ichimura K., et al. Japanese guidelines for allergic rhinitis 2020. Allergol. Int. 2020; 69 (3): 331-345. doi: 10.1016/j.alit.2020.04.001.
- Raherison-Semjen C., Guilleminault L., Billiart I., et al. Updated guidelines (2021) for management and follow-up of asthmatic patients of the French Society of Pneumology (SPLF) and the French Society of Pediatric Pneumology and Allergology (SP2A). Short version. Respir. Med. Res. 2022; 81: 100898. doi: 10.1016/j.resmer.2022.100898.
- FDA. Risks may include suicidal thoughts or actions. Available at: https://www.fda.gov/drugs/drug-safety-and-availability/fda-requires-boxed-warning-about-serious-mental-health-side-effects-asthma-and-allergy-drug.
- Skoner D.P., Golant A.K., Norton A., et al. Is this medication safe for my child? How to discuss safety of commonly used medications with parents. J. Allergy Clin. Immunol. Pract. 2022; 10 (12): 3064-3072. doi: 10.1016/j.jaip.2022.07.032.
- The Global Strategy for Asthma Management and Prevention. 2023. Available at: https://ginasthma.org/wp-content/uploads/2023/07/GINA-2023-Pocket-Guide-WMS.pdf.
- Wang X.P., Yang L.D., Zhou J.F. Montelukast and budesonide combination for children with chronic cough-variant asthma. Medicine (Baltimore). 2018; 97 (30): e11557. doi: 10.1097/MD.0000000000011557.
- Watson S., Kaminsky E., Taavola H., et al. Montelukast and nightmares: further characterisation using data from VigiBase. Drug Saf. 2022; 45 (6): 675-684. doi: 10.1007/s40264-022-01183-2.
- Wei C. The efficacy and safety of H1-antihistamine versus montelukast for allergic rhinitis: a systematic review and meta-analysis. Biomed. Pharmacother. 2016; 83: 989-997. doi: 10.1016/j.biopha.2016.08.003.
- Wei Y., Li D.S., Liu J., et al. Therapeutic effect and safety of montelukast sodium combined with budesonide in children with cough variant asthma: a meta analysis. Zhongguo Dang Dai Er Ke Za Zhi. 2016; 18 (11): 1100-1105. doi: 10.7499/j.issn.1008-8830.2016.11.009.
- Xiao J., Wu W., et al. A network meta-analysis of randomized controlled trials focusing on different allergic rhinitis medications. Am. J. Ther. 2016; 23 (6): e1568-e1578. doi: 10.1097/MJT.0000000000000242.
- Інструкція лікарського засобу Монтелукаст-Тева [Електронний ресурс]. – Режим доступу: https://compendium.com.ua/dec/263418.
- Уніфікований клінічний протокол первинної та вторинної (спеціалізованої) медичної допомоги «Бронхіальна астма у дітей». 2021 [Електронний ресурс]. – Режим доступу: https://zakon.rada.gov.ua/rada/show/v2856282-21#Text.
- Paljarvi T., Forton J., Luciano S., et al. Analysis of neuropsychiatric diagnoses after montelukast initiation. JAMA Netw. Open. 2022; 5 (5): e2213643. doi: 10.1001/jamanetworkopen.2022.13643.