Міжнародний алергологічний і ринологічний консенсус: алергічний риніт (2023)
Огляд доказових даних і рекомендацій щодо класифікації, диференційної діагностики, епідеміології, чинників ризику та протективних чинників щодо розвитку алергічного риніту
Підготувала Ганна Гаврюшенко
За різними даними, алергічний риніт (АР) може траплятися в 5-50% населення в усьому світі. Рівень захворюваності на АР, тривалість і серйозність його перебігу, зважаючи на соціальні, екологічні та кліматичні зміни, демонструють тенденцію до зростання. Значна поширеність АР, його хронічний перебіг і множинні коморбідні стани, висока вартість лікування, а також негативний вплив на якість життя та працездатність пацієнтів ставлять АР на п’яте місце серед захворювань, що становлять найбільший соціоекономічний тягар для системи охорони здоров’я США. Тож подальше вивчення АР і впровадження доказових методик діагностики, лікування та профілактики цього захворювання є вкрай важливими. У цьому матеріалі, що є першим у серії публікацій, присвячених оновленому Міжнародному алергологічному та ринологічному консенсусу з питань АР (2023), представлено стислий огляд новітніх даних щодо класифікації, диференційної діагностики, епідеміології, чинників ризику та протективних чинників щодо розвитку АР.
Визначення, класифікація та диференційна діагностика АР
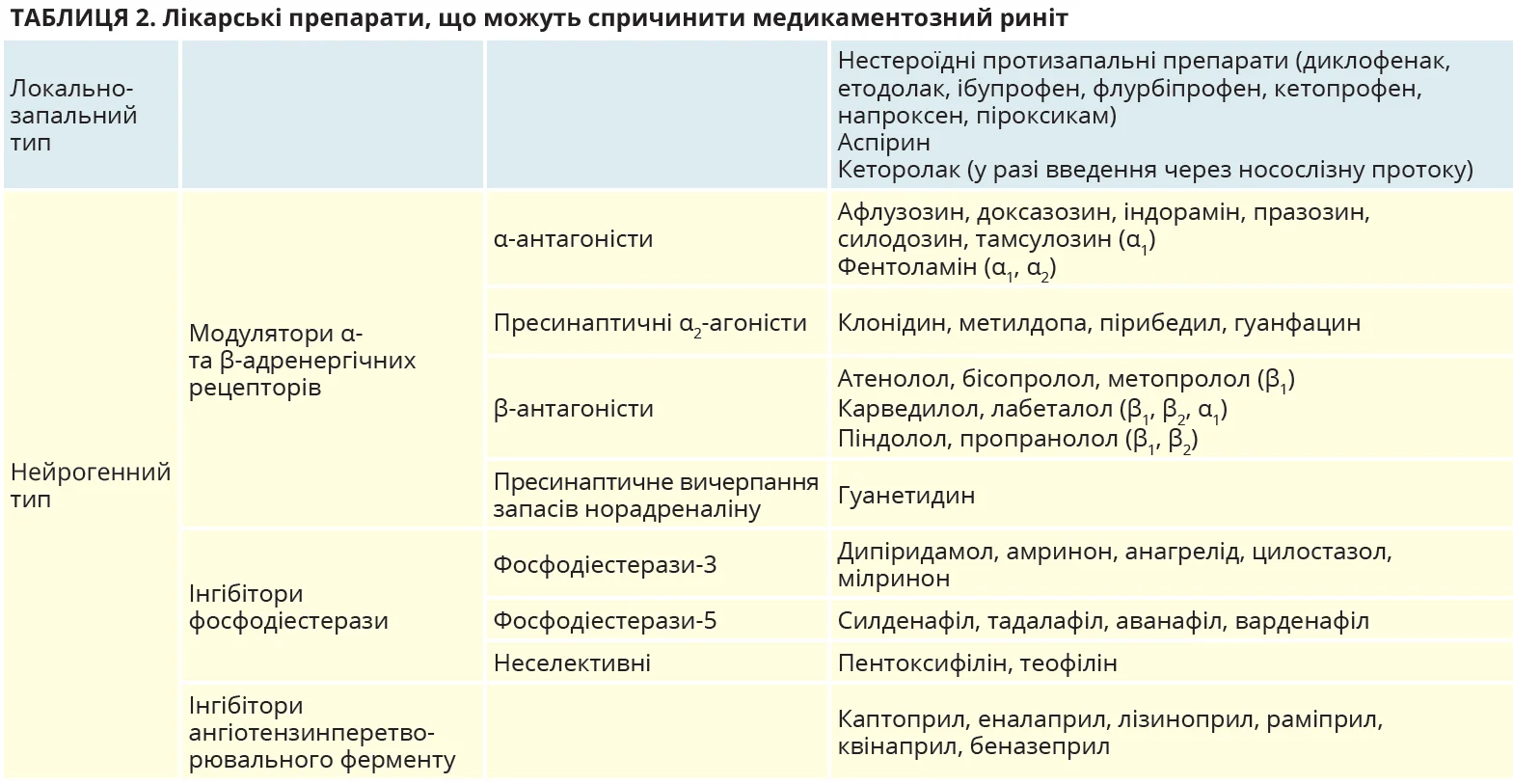
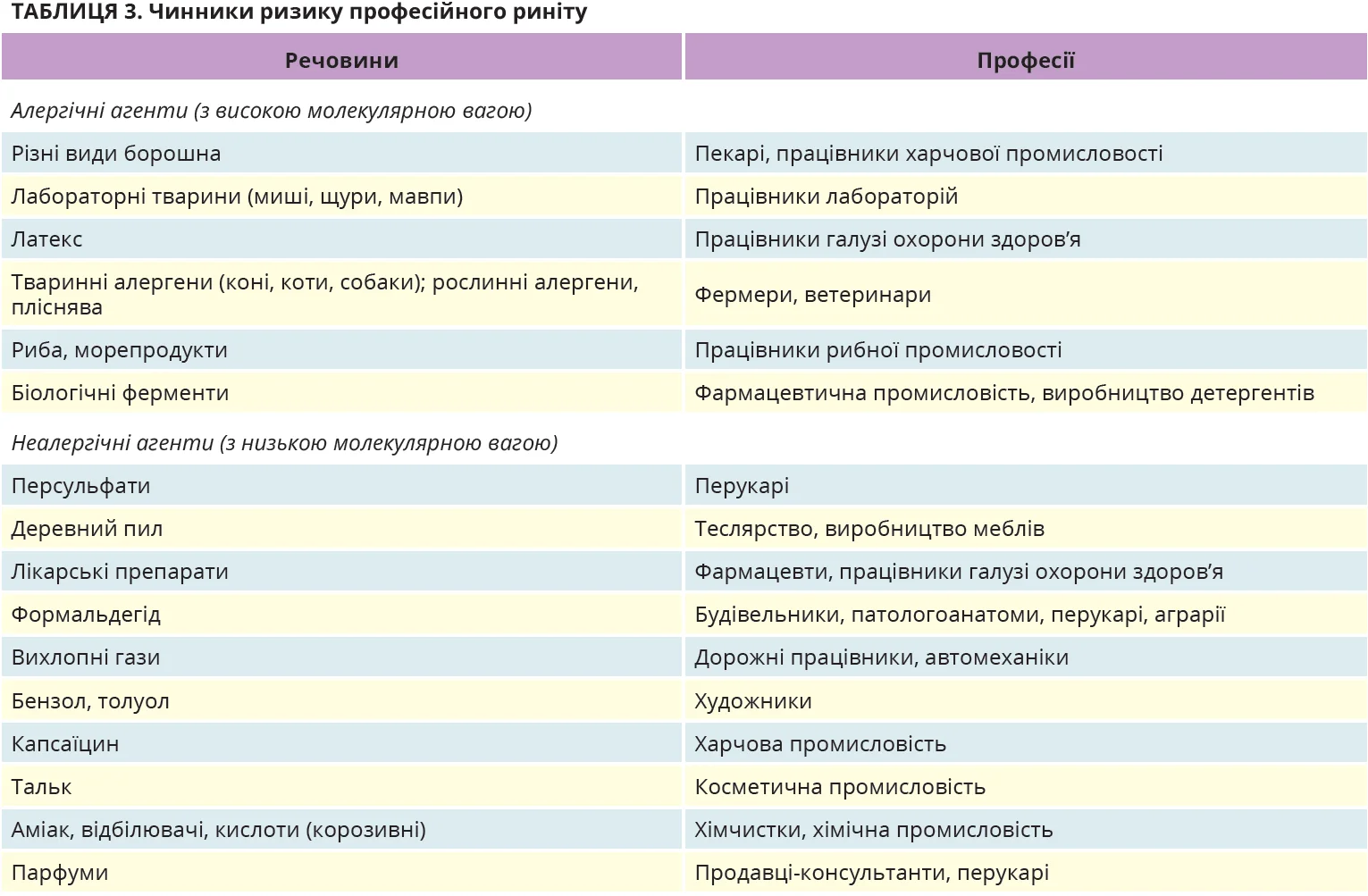
АР – це IgE-опосередкована реакція гіперчутливості 1 типу, що виникає внаслідок впливу алергену на слизову оболонку носа сенсибілізованої людини. Класичні симптоми АР, як-от ринорея, закладеність/обструкція носа, свербіж у носі та чхання, є неспецифічними й можуть супроводжувати багато інших станів, не пов’язаних з алергією (стислі рекомендації щодо диференційної діагностики АР подано в таблицях 1-4).
Крім того, наявність АР має потужну асоціацію з подальшим розвитком астми. Це підтверджує теорію об’єднаних дихальних шляхів, згідно з якою в основі запальних захворювань верхніх і нижніх дихальних шляхів лежать подібні патофізіологічні механізми.
У різних публікаціях поширеність АР у світовій популяції коливається від 5 до 50% залежно від визначення АР, що використовується в дослідженні. Сенсибілізація до алергенів може бути визначена за допомогою шкірних тестів або виявлення алергеноспецифічних IgE in vitro, проте багато людей, які є сенсибілізованими до певних алергенів, не мають проявів алергії. Отже, кореляція сенсибілізації з наявністю клінічної симптоматики має вирішальне значення в діагностиці АР.
АР майже відсутній у немовлят і дітей раннього віку та найчастіше виникає в дітей шкільного віку, що пов’язано з гіперреактивною відповіддю Т-хелперів 2 типу в цьому віці. Частота захворюваності на АР у популяції зростає до настання дорослого віку. Первинний контакт з алергенами зумовлює в атопічних індивідуумів швидку продукцію алергеноспецифічних IgE. Подальша експозиція алергенів у таких осіб спричиняє розвиток імунних реакцій негайного та відкладеного типів, що призводить до клінічних проявів АР. Імунні реакції негайного типу, як-от свербіж, закладеність носа та ринорея, виникають через лічені хвилини після повторного контакту з алергеном, тоді як реакції відкладеного типу, до яких належать гіпосмія, гіперреактивність, підсилення закладеності носа та ринореї, проявляються через 4-8 годин.
Згідно з традиційною класифікацією виокремлюють сезонний АР, асоційований із надвірними алергенами, як-от пилок, і цілорічний АР, що зумовлюється хатніми алергенами, до яких належать пилові кліщі й інші хатні комахи, а також лупа домашніх тварин. АР, спричинений пліснявими грибками, може бути як надвірним, так і хатнім. Проте, враховуючи кліматичні, екологічні зміни, а також випадки полісенситизації, дедалі частіше клінічний перебіг АР не можна віднести до сезонного або цілорічного. Тому було запропоновано новітній метод класифікації АР, заснований на тривалості та персистентності симптомів, згідно з яким існує інтермітивний АР, за якого симптоми тривають менш ніж 4 дні на тиждень та/або менш ніж 4 послідовні тижні, а також персистивний АР, за якого симптоми проявляються більш ніж 4 дні на тиждень протягом щонайменше 4 послідовних тижнів. Ще одна класифікація АР заснована на виразності клінічних проявів, що впливають на якість життя пацієнта, як-от порушення сну, негативний вплив на щоденну активність і заняття спортом, зниження працездатності та виникнення загрозливих симптомів. АР із легким перебігом не спричиняє вищевказаних порушень, тоді як наявність хоча б одного з наведених симптомів указує на середньотяжкий перебіг АР, а наявність ≥2 порушень характерна для тяжкого АР.
Огляд чинників підвищеного ризику та протективних чинників щодо розвитку АР
Спадкові чинники, як-от наявність АР у членів родини, відіграють важливу роль у розвитку алергічного та неалергічного риніту. Близнюкові дослідження вказують на те, що генетичні чинники становлять 70-80% індивідуальної схильності до розвитку АР, але жодний єдиний ген чи поліморфізм не є повністю відповідальним за спадкову схильність. Велика кількість генів та їхніх варіантів, комплексні генні взаємодії в організмі вносять свій вклад у ризики дебюту захворювання, а також його перебіг, персистентність і тяжкість проявів. Останнім часом проводяться численні великі дослідження повногеномних асоціацій (GWAS), які є найдостовірнішим методом визначення чинників спадкової схильності до багатофакторних захворювань, до яких і належить АР. У ході таких досліджень підтверджуються дані стосовно визначної ролі в схильності до АР таких генних локусів, як HLA-DQB1/DQA1, IL1RL1, TLR1/10, WDR36, LRRC, IL7R, що кодують гени, котрі впливають, зокрема, на імунорегуляторні механізми, продукцію цитокінів і хемокінів, презентацію антигенів і впізнавання патогенів. Велику увагу дослідники приділяють також вивченню епігенетичних механізмів, що являють собою зв’язок між чинниками довкілля та геномом. Нещодавні дослідження вказують на те, що загальновідомі чинники ризику алергії, як-от вплив паління матері на внутрішньоутробний розвиток плода, потужно впливають на профілі метилювання ДНК у дітей; це, своєю чергою, призводить до підвищеної схильності до порушень продукції IgE та розвитку АР. Такі епігенетичні дослідження висвітлюють спільні патогенетичні механізми розвитку АР, астми й інших алергічних захворювань, а також виявляють нові мішені для розроблення лікарських препаратів.
Вплив ранньої експозиції інгаляційних алергенів (як-от пилові кліщі, пилок, шкірні лусочки домашніх тварин, грибкові антигени) на ризик розвитку АР залишається неясним. Не було встановлено чіткої асоціації між ранньою сенситизацією до антигенів пилових кліщів і подальшим розвитком АР. Є дані, що як украй низькі, так і вкрай високі рівні експозиції до цього алергену можуть мати протективний вплив. Концентрація кліщового алергену менш ніж 2 мг на 1 г хатнього пилу вважається безпечною для первинного запобігання розвитку алергії в атопічних дітей. Суперечливою є також інформація щодо ролі пліснявих антигенів у розвитку АР. Тоді як у деяких новітніх дослідженнях установлено асоціацію між ранньою експозицією до грибкових антигенів і підвищеним ризиком розвитку АР, виявити дозозалежні ефекти чи визначити безпечні для популяції рівні концентрації пліснявих антигенів не вдалося.
Великі лонгітудинальні дослідження демонструють асоціацію між розвитком сенсибілізації до пилку в ранньому дитинстві та подальшим розвитком АР. Зокрема, прояви сезонної алергії майже не спостерігаються в сенсибілізованих дітей до 3 років, тоді як у віковій групі 3-12 років частота захворюваності на АР серед сенсибілізованих дітей демонструє щорічний приріст у 2%. У зв’язку зі змінами довкілля через глобальне потепління, як-от подовження сезону цвітіння, відзначається підвищення рівнів сенсибілізації до пилку серед дітей, що в майбутньому може призвести до зростання частоти АР у дорослих.
Дані літератури щодо ефектів ранньої експозиції до алергенів домашніх тварин на розвиток АР протягом життя є суперечливими. Тоді як деякі дослідження демонструють захисний вплив контакту дітей першого року життя з домашніми тваринами, особливо собаками, на подальший розвиток АР, інші дослідження вказують, що рання експозиція до лупи тварин є чинником підвищеного ризику. Переважна більшість досліджень не встановлює значущої асоціації між раннім контактом із домашніми тваринами та розвитком АР у майбутньому, тому наразі не є можливим надати доказові рекомендації з цього приводу.
Обмеження вживання вагітними та жінками, що годують груддю, високоалергенних продуктів, як-от коров’яче молоко, яйця, арахіс і риба, не асоційоване зі зниженням схильності до АР у їхніх дітей; але було виявлено асоціацію між підвищеним умістом жирної риби й горіхів у материнській дієті та зниженням алергічних ризиків у дітей. Грудне вигодовування тривалістю щонайменше 4-6 місяців є рекомендованим для всіх немовлят, зважаючи на численні позитивні ефекти для матері та дитини, а також наявні дані щодо можливого протективного впливу на розвиток АР у дітей. Раннє (до 2 років життя) виникнення сенсибілізації до харчових алергенів у дітей пов’язане з вищими ризиками розвитку АР протягом дитинства, особливо коли харчова чутливість комбінується із сенсибілізацією до інгаляційних алергенів. Проте не існує чіткої кореляції між обмеженням уживання дітьми високоалергенних продуктів і нижчими ризиками розвитку АР. Отже, жорсткі обмеження дієти для вагітних і жінок, які годують груддю, дітей не рекомендовані з метою профілактики АР, а введення прикормів для немовлят у віці 4-6 місяців має відбуватися для всіх дітей незалежно від їхньої сімейної історії алергічних захворювань та індивідуального атопічного ризику.
Переважна більшість наявних досліджень демонструють кореляцію між високим соціоекономічним статусом і збільшеним ризиком розвитку АР як на індивідуальному рівні, так і на рівні держав. Тобто вплив соціоекономічних чинників на частоту виникнення АР перетинається з гігієнічною гіпотезою розвитку алергічних захворювань, яка стверджує, що часті рекурентні інфекції в ранньому дитинстві асоційовані з нижчим ризиком розвитку алергії протягом життя. Наразі погляди наукової спільноти еволюціонують у напрямі гіпотези біорізноманіття, що переносить акцент із захисного впливу контакту з окремими інфекційними мікроорганізмами на позитивний вплив мікробіологічного різноманіття на розвиток імунної системи дитини. Наприклад, описано протективні ефекти життя в сільській місцевості та контакту зі свійськими тваринами в ранньому дитинстві на зниження частоти алергічних захворювань протягом життя, а також негативну кореляцію між збільшенням числа дітей у родині й частотою АР у цих дітей. Численні дослідження фекальної та шкірної мікробіоти демонструють, що високе біорізноманіття мікробіому кишківника та шкіри в дитинстві й дорослому віці асоційоване з нижчою частотою алергічних захворювань.
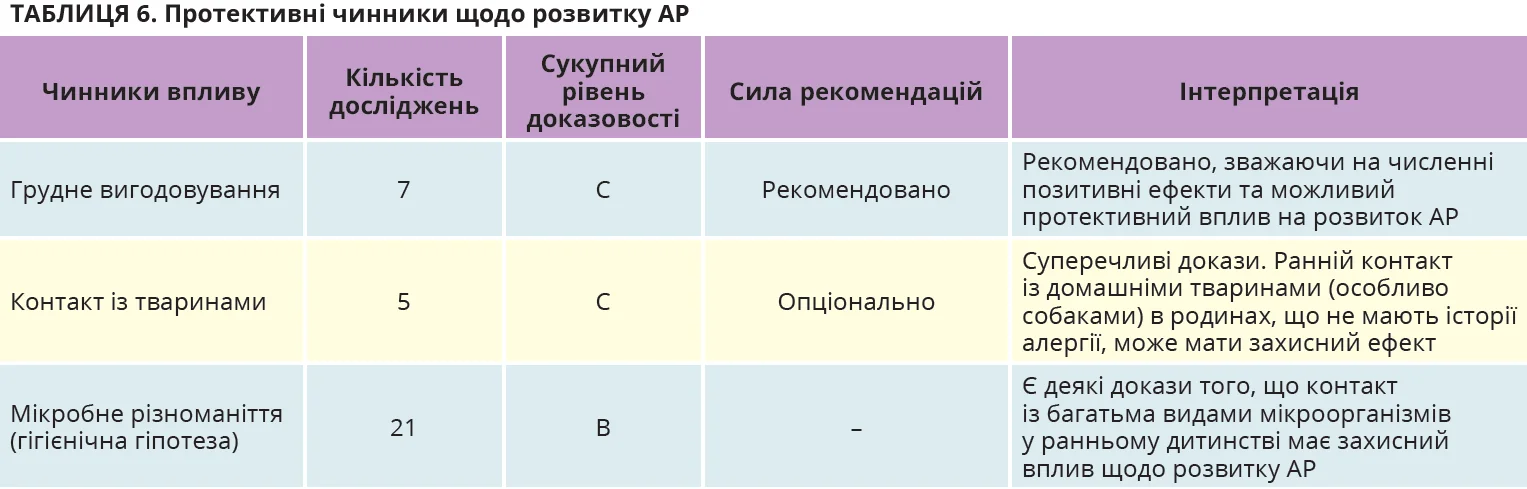
Огляд доказових даних щодо чинників підвищеного та зниженого ризику розвитку АР і відповідні рекомендації подано в таблицях 5 і 6.
Література
Wise S.K., Damask C., Roland L.T., et al. International consensus statement on allergy and rhinology: Allergic rhinitis – 2023. Int. Forum Allergy Rhinol. 2023;
13: 293-859. https://doi.org/10.1002/alr.23090.