Медикаментозна алергія: практичне оновлення 2022 р. Хіміотерапевтичні засоби для лікування раку
Переклала й адаптувала д-р мед. наук Лариса Стрільчук
Гіперчутливі реакції – це несприятливі реакції на певні препарати, які зазвичай не можна передбачити та які не пов’язані з відомими побічними ефектами цих препаратів. У розвитку деяких з таких реакцій лежать імунні механізми, тому вони відносяться до медикаментозної алергії. Натомість інші не мають алергічного компоненту та є наслідком активності інших компонентів імунної системи.
Тяжкість негайних РГЧ варіює від нетяжкого шкірного висипу до анафілаксії; вони зазвичай опосередковані опасистими клітинами. Відтерміновані реакції виникають через 6-24 години після введення препарату та пов’язані з ефектами Т-лімфоцитів. Місцеві специфічні реакції (мукозит, алопеція, синдром «рука – нога», зміни нігтів) призводять до скасування препарату та є зворотними. Можуть також виникати доброякісні відтерміновані екзантеми, які підлягають симптоматичному лікуванню пероральними H1-гістаміноблокаторами (Н1-ГБ), і тяжкі шкірні реакції (синдром Стівенса – Джонсона й токсичний епідермальний некроліз, сироваткова хвороба, DRESS-синдром і гострий генералізований екзантематозний пустульоз), які зазвичай свідчать про потребу в абсолютному уникненні причинного препарату.
Відсутність стандартизованого підходу до ведення пацієнтів із РГЧ нерідко призводить до уникнення хіміопрепаратів першої лінії в осіб, які могли би без ускладнень перенести повторне введення препарату.
Основні підходи до медичної допомоги в разі підозри на РГЧ до хіміопрепарату включають десенсибілізацію, шкірні проби для стратифікації ризику, стратифікацію ризику без шкірних проб і пробного введення препарату, уникнення причинного препарату (за наявності альтернативного засобу аналогічної ефективності). Якщо клінічна оцінка відповідає РГЧ, емпірична десенсибілізація є доцільною та безпечною й може навіть бути проведена за неможливості виконати шкірні проби (наприклад, за умови амбулаторного прийому без доступу до хіміотерапевтичних препаратів для проби). Кандидатами для проведення десенсибілізації до хіміопрепаратів є особи з РГЧ 1 типу (опосередкованими опасистими клітинами й IgE-залежними), включаючи анафілаксію. Для внутрішньовенних препаратів найчастіше використовують трьохетапні протоколи десенсибілізації, хоча чимраз збільшується доказова база того, що одноетапні протоколи мають аналогічну ефективність і безпеку, даючи можливість простішої та менш часозатратної десенсибілізації.
Пацієнти без переконливого анамнезу РГЧ не потребують десенсибілізації та зазвичай добре відповідають на повторне введення хіміотерапевтичного засобу. До таких пацієнтів належать особи із симптомами свербежу або набряку губ без об’єктивних ознак ураження шкіри під час інфузії чи з виникненням почервоніння шкіри без свербежу, висипу або кропив’янки через кілька годин після введення препарату. Якщо симптоми є нетяжкими (відчуття припливу жару чи свербіж без кропив’янки, біль у спині) або пацієнт занепокоєний повторним уведенням препарату, може застосовуватися премедикація H1-ГБ та інфузія препарату з меншою швидкістю.
Десенсибілізація має виконуватися в тих випадках, коли для препаратів першої лінії немає доцільної альтернативи. Тривалість десенсибілізації може становити кілька годин і передбачати подвоєння дози раз на 15-20 хвилин.
Консенсусне твердження 28. У пацієнтів із негайними реакціями на хіміопрепарати, для котрих причинний препарат є оптимальним, може проводитися десенсибілізація.
Консенсусне твердження 29. У пацієнтів із реакціями не негайного типу або анамнезом реакцій, який не відповідає РГЧ до хіміопрепаратів, можуть застосовуватися сповільнені інфузії, поступове підвищення дози та/або премедикація без сенсибілізації.
Препарати платини
РГЧ виникають у 8-16% пацієнток із гінекологічними новоутвореннями, які отримують карбоплатин, у 5-20% пацієнтів, які отримують цисплатин, й у ≤24% пацієнтів із різними видами раку, які отримують оксаліплатин. Препарати на основі платини зазвичай спричиняють РГЧ після кількох курсів лікування, що свідчить про ймовірний IgE-опосередкований механізм виникнення. Зокрема, для карбоплатину ймовірність РГЧ становить 1% для осіб, які отримали ≤6 інфузій, 27% – для осіб, які отримали ≥7 інфузій, і ≤46% для осіб, які отримали >15 інфузій. Пікова поширеність РГЧ на карбоплатин спостерігається після 8-9-го введення, що загалом відповідає другому або третьому циклу лікування після рецидиву злоякісної пухлини. Премедикація кортикостероїдами (КС) та Н1-ГБ не запобігає рецидивам РГЧ й анафілактичним реакціям.
Повідомлення про перехресну реактивність між препаратами платини є суперечливими, але найнижчі показники перехресної реактивності притаманні парі оксаліплатин – цисплатин.
При стратифікації ризику та виборі тактики ведення пацієнтів з анамнезом негайних алергічних реакцій (АР) на хіміотерапевтичні препарати на основі платини враховують тяжкість первинної РГЧ та результати шкірних проб. Останні також дають змогу виявити випадки, в яких десенсибілізація може бути непотрібною. Проте, допомагаючи уникнути непотрібної десенсибілізації завдяки виявленню випадків істинної алергії, протоколи стратифікації ризику водночас створюють додаткові проблеми у зв’язку з підвищенням фінансових і часових витрат, потребою в багатьох візитах до клініки та потенційним відтермінуванням лікування. Безпечним методом ведення пацієнтів після РГЧ на препарати платини залишається емпірична десенсибілізація.
Консенсусне твердження 30. У стратифікації ризику та веденні пацієнтів з анамнезом негайних АР на хіміопрепарати на основі платини можуть допомогти дані про первинну РГЧ і результати шкірної проби.
Шкірні проби використовуються тоді, коли вони можуть вплинути на прийняття рішення щодо лікування, не відтерміновуючи надання допомоги. Слід зауважити, що приблизно у 8-8,5% випадків негативних шкірних проб у пацієнта все одно розвивається РГЧ, причому іноді – під час спроби проведення десенсибілізації. Результат проби може змінитися з негативного на позитивний після наступних контактів із карбоплатином, якщо часовий інтервал між пробою та розвитком РГЧ перевищує 6 місяців.
Шкірні проби не варто проводити з препаратами, здатними провокувати утворення на шкірі пухирів, як-от доксорубіцин. Карбоплатин у дозі 10 мг/мл також зумовлює локальний некроз шкіри, тому для інтрадермального введення максимальною концентрацією є 5 мг/мл.
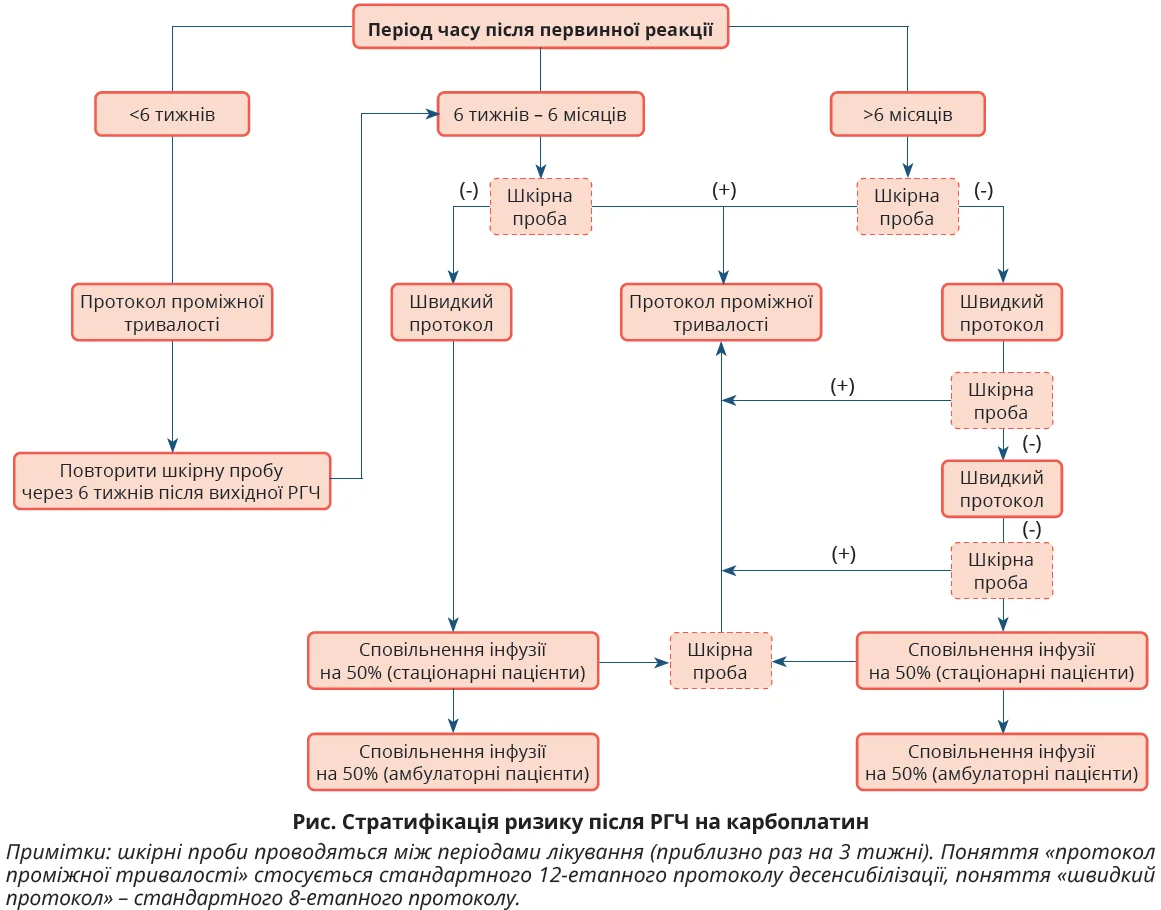
Для пацієнтів із РГЧ на карбоплатин запропоновано протокол стратифікації ризику на основі трьох серійних шкірних проб (рис.); вивчаються також одноетапні протоколи.
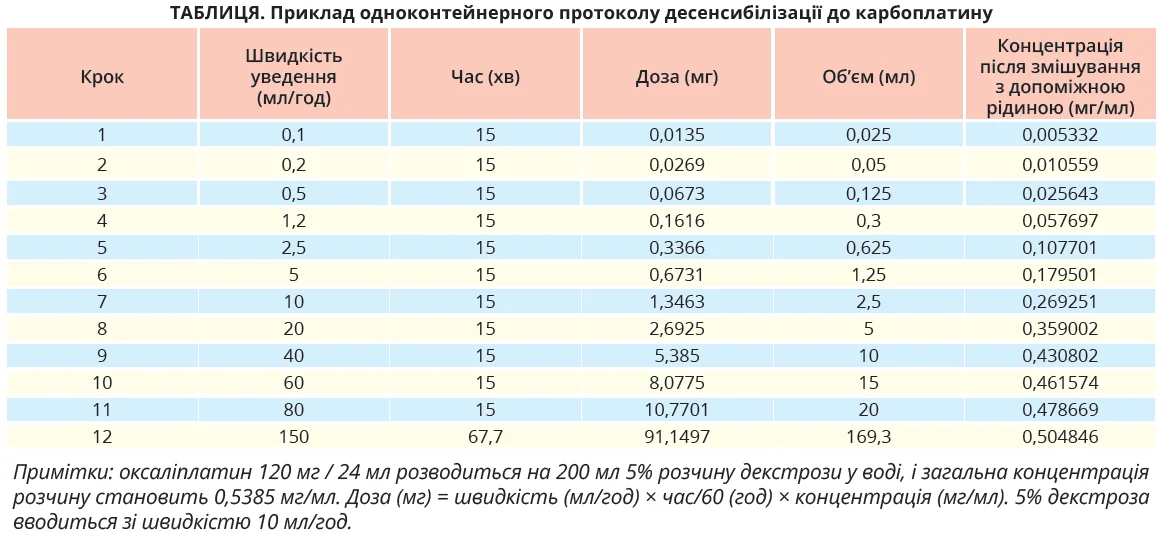
Для пацієнтів із позитивним результатом шкірної проби запропоновано різні протоколи десенсибілізації, найвивченіший з яких передбачає 12 кроків і є досить успішним. Складність цих протоколів зумовила винайдення й випробування одноетапного протоколу (табл.).
Таксани (паклітаксел, доцетаксел)
РГЧ при застосуванні таксанів зазвичай є наслідком впливу допоміжних речовин (наприклад, ліпідного розчинника Cremophor-EL і полісорбатів), а не активної субстанції. На відміну від РГЧ до препаратів на основі платини, роль шкірних проб у разі РГЧ на таксани не з’ясована. Для стратифікації ризику та вибору тактики лікування застосовується оцінка тяжкості первинної РГЧ. Премедикація системними КС та Н1-ГБ здатна зменшити частоту реакцій на таксани з 30 до 3%. У разі тяжких первинних РГЧ може проводитися емпірична десенсибілізація.
Консенсусне твердження 31. У стратифікації ризику та веденні пацієнтів з анамнезом негайних АР на таксани можуть допомогти дані про первинну РГЧ.
При першому введенні паклітакселу та доцетакселу гіперчутливі реакції виникають у 10-50% випадків, що свідчить про прямий, не-IgE-опосередкований механізм їх розвитку. У зв’язку з цим роль шкірних проб після РГЧ на таксани залишається незрозумілою. Якщо причиною реакцій справді є допоміжна речовина Cremophor-EL, шкірні проби недоцільні.
Попереднє введення системних КС та H1-ГБ може зменшити частоту реакцій на таксани з 30 до 3%, а пацієнтам, у яких усе одно розвинулися реакції негайного типу, може бути проведена трьохетапна десенсибілізація (див. протокол для препаратів платини).
Виконання процедури десенсибілізації пов’язане з додатковим навантаженням на медичний персонал, оскільки потрібно підготувати та ввести розведені розчини препарату. Показано, що одноетапний протокол є не гіршим для швидкої десенсибілізації до паклітакселу, ніж багатоетапний. Окрім того, більшість пацієнтів із нетяжкими реакціями на таксани (тобто без респіраторних симптомів і гіпотензії) можуть безпечно продовжувати звичайні або повільні введення цих препаратів без десенсибілізації.
Іншим варіантом для пацієнтів, які зреагували на паклітаксел, є переведення на препарати, що не містять Сremophor-EL (рутинно не використовуються у зв’язку з високою вартістю).
Для паклітакселу описано тяжкі відтерміновані реакції (синдром Стівенса – Джонсона й токсичний епідермальний некроліз, шкірний васкуліт, гострий інтерстиційний пневмоніт, підгострий шкірний червоний вовчак), причому десенсибілізація в таких випадках неефективна.
Інгібітори тирозинкінази (ІТК)
ІТК асоціюються з частим виникненням шкірних і системних побічних ефектів, механізм виникнення котрих радше пов’язаний з ефектами тирозинкінази, ніж з імунологічною гіперчутливістю. Ключовим у стратифікації ризику й формуванні плану лікування є розпізнання та правильне клінічне фенотипування реакцій. Залежно від цього варто приймати рішення щодо зменшення дози, скасування препарату, лікування КС, виконання пробного введення препарату або десенсибілізації.
Пацієнти, які отримують хіміотерапію, мають бути обізнані з найважливішими та найімовірнішими побічними реакціями, щоби вчасно звернутися до свого лікаря для раннього їх усунення.
Лікування дерматологічних побічних ефектів передбачає застосування топічних і системних КС, антибіотиків, топічних препаратів сечовини та саліцилової кислоти, перорального ізотретиноїну. За наявності свербежу можуть призначатися H1-ГБ та габапентин. У деяких випадках дозу ІТК зменшують або взагалі скасовують ці препарати, а після зникнення шкірних змін знову розпочинають уведення в нижчій дозі. Негайне скасування препарату рекомендовано й за появи бульозної або ексфоліативної висипки. Для профілактики висипів на шкірі можуть застосовуватися нестероїдні протизапальні препарати, міноциклін або доксициклін.
Інгібітори імунних контрольних точок (ІІКТ)
Доступні натепер ІІКТ являють собою моноклональні антитіла, які блокують специфічні імунні контрольні точки, зумовлюючи активацію та проліферацію T-лімфоцитів. Такий механізм дії водночас спричиняє органоспецифічні імунні побічні ефекти, більшість з яких мають незначну або помірну тяжкість і включають дерматит, тиреоїдит й інші ендокринопатії, гепатит, коліт, інтерстиційний нефрит, пневмоніт, рідко – міокардит і енцефаліт. Лікування таких реакцій потребує мультидисциплінарного підходу.
Поширеними побічними ефектами є також утомлюваність, свербіж без шкірного висипу, артралгія, втрата апетиту, схуднення. Інфузійні реакції, асоційовані з ІІКТ, зазвичай є нетяжкими й виникають у ≤25% випадків. У разі призначення авелумабу реакції можуть бути тяжчими та потребувати лікування Н1-ГБ й ацетамінофеном. Для лікування свербежу дієвим є габапентин. Загалом, якщо реакція є нетяжкою, призначається симптоматична та підтримувальна терапія, а застосування хіміопрепарату продовжують. У разі висипки симптоматичними препаратами є топічні КС чи пероральні Н1-ГБ, а при ендокринопатіях – гормонозамісна терапія. За тяжких токсичних реакцій ІІКТ скасовують і призначають системні КС (0,5-2 мг/кг/добу з поступовим зниженням дози протягом 4-6 тижнів). Повторне введення ІІКТ має бути спільним рішенням лікаря та пацієнта на підставі зважування ризиків і переваг. Вивчається також повторне введення ІІКТ у поєднанніз селективною імуносупресивною терапією. Частота рецидивування при повторному введенні того самого ІІКТ становить ≤50% і є більшою в разі коліту, пневмоніту та гепатиту.
Аспарагіназа
Реакції негайного типу на введення аспарагінази відзначають у 3-45% пацієнтів. Існують 3 типи аспарагінази: нативна, отримана з Escherichia coli, пегільована аналогічного походження й нативна, отримана з Erwinia chrysanthemi. При реакції на один із препаратів може бути доцільною зміна на інший тип. Хоча премедикація КС зменшує частоту РГЧ, невідомо, чи вона здатна запобігти утворенню антитіл до аспарагінази.
Література
Khan D.A., Banerji A., Blumenthal K.G., et al. Drug allergy: a 2022 practice parameter update. J. Allergy Clin. Immunol. 2022 Dec; 150 (6): 1333-1393. doi: 10.1016/j.jaci.2022.08.028.