Медикаментозна алергія: диференційна діагностика та лікування алергічного висипу
Підготувала лікарка-алерголог Ірина Калікіна
Медикаментозна алергія залишається актуальною проблемою та потребує постійного оновлення підходів до діагностики й лікування. Відсутність уніфікованих протоколів ведення пацієнтів з реакціями гіперчутливості до лікарських засобів (РГЛЗ) ускладнює надання медичної допомоги.
 Аспекти цієї проблеми було представлено в доповіді Інни Володимирівни Гогунської, докторки медичних наук, професорки, провідної наукової співробітниці ДУ «Інститут отоларингології ім. проф. О.С. Коломійченка НАМН України» (м. Київ), на Міжнародному міждисциплінарному конгресі «Ефективність і безпечність лікарських засобів: стандарти діагностики та лікування» в межах проєкту «Життя без алергії. International».
Аспекти цієї проблеми було представлено в доповіді Інни Володимирівни Гогунської, докторки медичних наук, професорки, провідної наукової співробітниці ДУ «Інститут отоларингології ім. проф. О.С. Коломійченка НАМН України» (м. Київ), на Міжнародному міждисциплінарному конгресі «Ефективність і безпечність лікарських засобів: стандарти діагностики та лікування» в межах проєкту «Життя без алергії. International».
РГЛЗ являють собою широкий спектр патологічних станів, кожен з яких має власні клінічні прояви, механізми розвитку та підходи до лікування [1]. Вони класифікуються за часом виникнення. Негайні (гострі) РГЛЗ охоплюють кропив’янку, ангіоневротичний набряк та/або анафілаксію, що виникають майже завжди протягом першої години з моменту вживання ліків. Відтерміновані (пізні) реакції виникають пізніше ніж через 6 годин, переважно через 24 години після приймання препарату.
У 2023 році Європейська академія алергії та клінічної імунології (EAACI) представила оновлену класифікацію реакцій гіперчутливості, яка розподіляла медикаментозні реакції на запальні / керовані імунною системою (з підтипами, регульованими антитілами та клітинами) й реакції з прямою відповіддю на хімічні речовини. Проте на конгресі EAACI 2025 було представлено нову, ще більш деталізовану номенклатуру реакцій на ліки, яка готується до публікації (рис. 1).
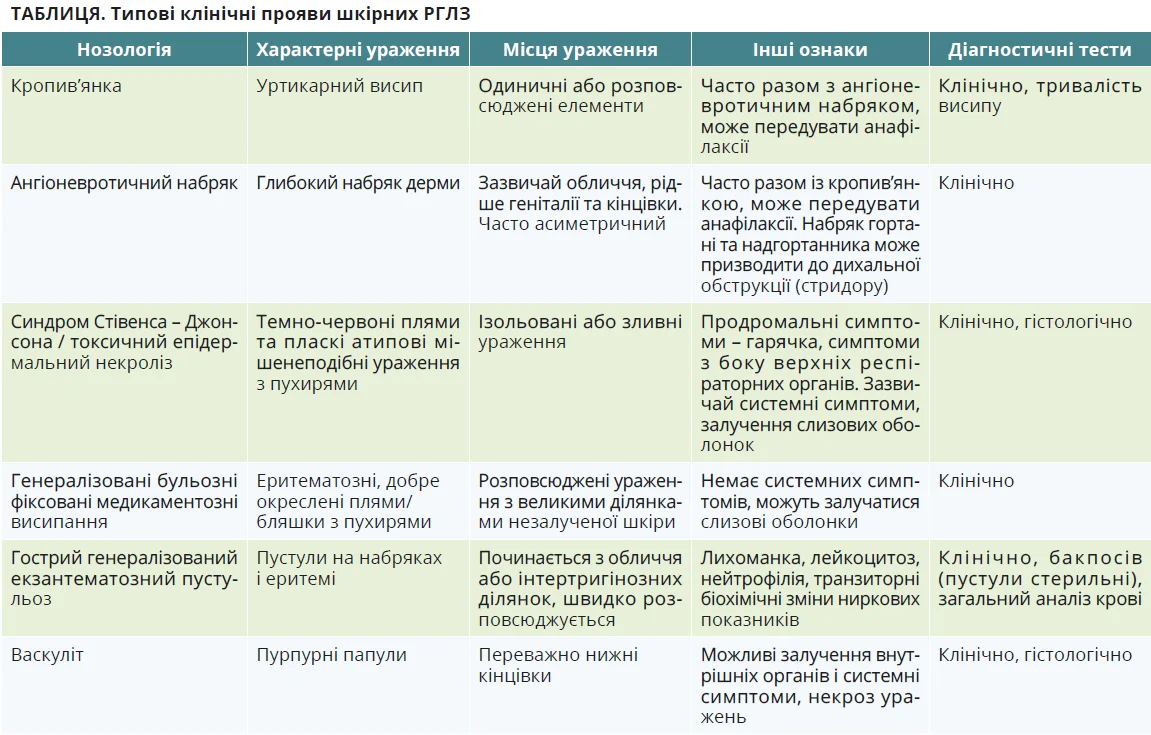
Диференційна діагностика алергічного висипу є критично важливою для визначення правильної тактики лікування [1]. Під час оцінювання пацієнта з висипом потрібно звертати увагу на характерні ознаки при маніфестації, що допомагають розрізнити різні типи шкірних реакцій (табл.).
Підозрювати тяжку відтерміновану РГЛЗ можна при клінічних ознаках, які вказують на потенційно небезпечний перебіг хвороби [2]:
- виражене залучення обличчя;
- атипові вогнища ураження;
- бульозні ураження;
- розповсюджена темно-червона еритема;
- значний пустульоз;
- болючість шкіри;
- залучення слизових оболонок;
- генералізована лімфаденопатія;
- підвищений рівень ферментів печінки;
- лабораторні ознаки ураження нирок;
- температура тіла >38,5 °C;
- зміни в загальному аналізі крові (анемія, гранулоцитопенія, тромбоцитопенія, нейтрофілія, еозинофілія);
- гіпокомплементемія;
- гепатит, нефрит, пневмоніт.
Взаємодія вірусних інфекцій і лікарських засобів
На окрему увагу заслуговує взаємодія вірусних інфекцій і медикаментів у розвитку РГЛЗ. При інфекції вірусом Епштейна – Барр (інфекційний мононуклеоз) призначення ампіциліну або амоксициліну може спричинити генералізований макулопапульозний висип. Подібна реакція може виникати й у хворих на цитомегаловірусну інфекцію [3].
При ВІЛ-інфекції сульфаніламіди (триметоприм/сульфаметоксазол) частіше спричиняють синдром Стівенса – Джонсона. Віруси герпесу людини 6-го та 7-го типів асоціюються з DRESS-синдромом, найчастішими препаратами-тригерами при цьому є протиепілептичні засоби (фенітоїн, карбамазепін, ламотриджин), алопуринол і сульфаніламіди. DRESS-синдром також часто зумовлює реактивацію вірусу простого герпесу [4].
Діагностика РГЛЗ
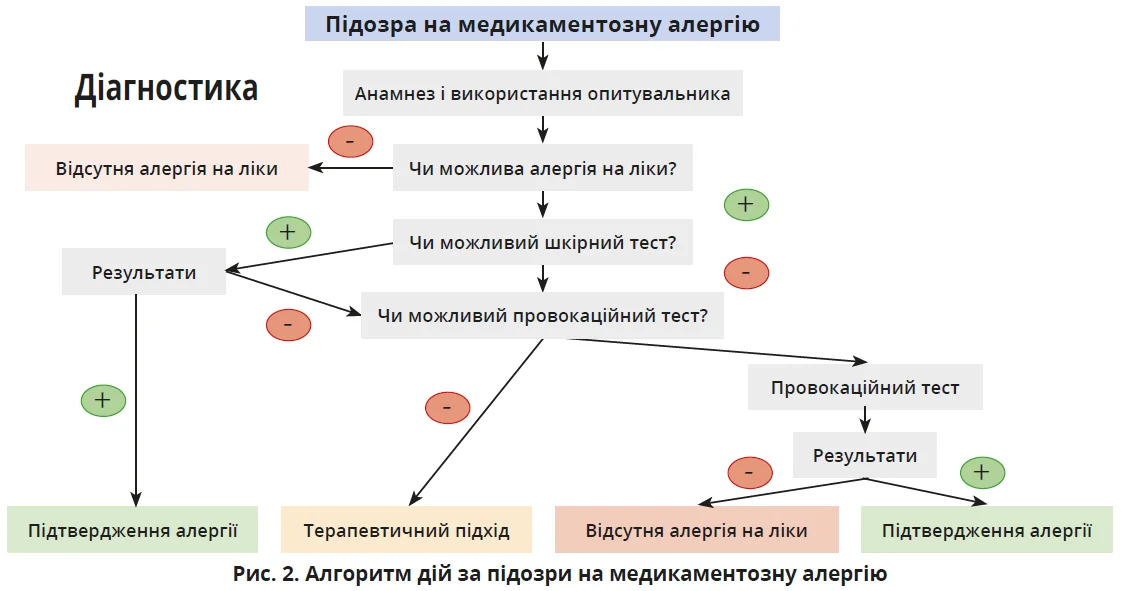
Діагностика медикаментозної алергії ґрунтується на комплексному підході, який охоплює збір анамнезу, використання опитувальника, шкірні та провокаційні тести. Алгоритм діагностики передбачає послідовне оцінювання можливості алергії на ліки та вибір відповідних методів обстеження (рис. 2).
Провокаційний тест на медикаментозну гіперчутливість є золотим стандартом у діагностиці РГЛЗ. Згідно з позиційним документом EAACI/ENDA 2023 року [5] провокаційний тест на ліки – це контрольоване введення препарату з метою діагностики реакцій гіперчутливості. Важливо розуміти, що тест відтворює симптоми після контакту з препаратом, але не визначає механізм реакції.
Алгоритм діагностики та лікування реакцій гіперчутливості до біологічних препаратів
Реакції гіперчутливості можуть виникати на широкий спектр ЛЗ, включно з біологічними препаратами, які дедалі ширше застосовуються. Алгоритм ведення пацієнта з реакцією гіперчутливості на моноклональні антитіла залежить від типу та тяжкості проявів [6].
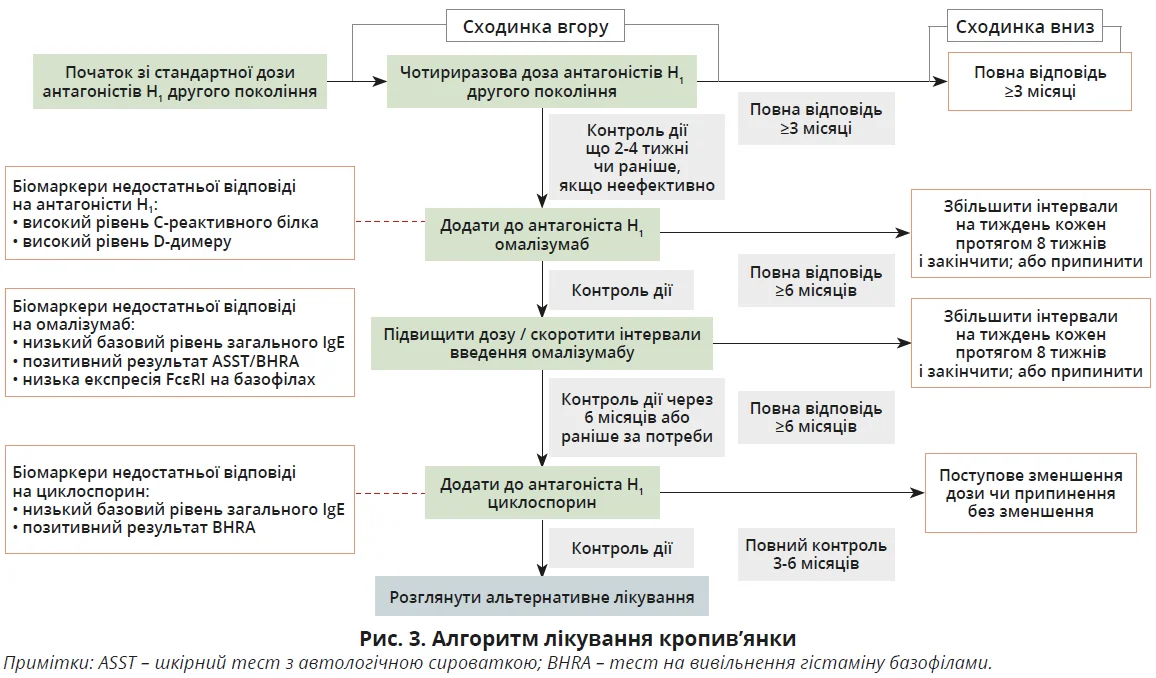
Кропив’янка є одним з найпоширеніших проявів медикаментозної алергії, тому питання ефективного лікування цього стану заслуговує на окрему увагу. Міжнародні настанови чітко визначають місце антигістамінних препаратів у терапії кропив’янки та критерії вибору оптимального препарату. Згідно з міжнародною настановою EAACI/GA²LEN/EuroGuiDerm/APAAACI 2021 року основою терапії кропив’янки є H1-антигістамінні препарати другого покоління [7] (рис. 3).
Рекомендації щодо застосування та дозування антигістамінних препаратів
Неседативні H1-антигістамінні препарати другого покоління слід застосовувати щодня для запобігання виникненню пухирів і ангіоневротичного набряку, а не за потреби. Це підтверджується їхнім профілем безпеки (доступні дані про безпеку протягом кількох років безперервного використання), результатами рандомізованих контрольованих досліджень і досліджень у реальному житті.
Сучасні H1-антигістамінні препарати другого покоління мають мінімальний седативний ефект або не мають його взагалі, не мають антихолінергічних ефектів. Більшість H1-антигістамінних препаратів другого покоління було протестовано спеціально для кропив’янки, і дані підтверджують ефективність використання біластину, цетиризину, дезлоратадину, ебастину, фексофенадину, левоцетиризину, лоратадину та рупатадину.
Рекомендовано збільшити дозу H1-антигістамінного препарату другого покоління до 4 разів у пацієнтів із хронічною кропив’янкою, котрі не реагують на стандартні дози, як лікування другої лінії, перш ніж розглядати інші методи терапії. Кілька досліджень підтверджують користь використання чотириразових стандартних доз біластину, цетиризину, дезлоратадину, ебастину, фексофенадину, левоцетиризину та рупатадину.
Важливі застереження
- Не рекомендовано використовувати різні H1-антигістамінні препарати одночасно.
- У документі GA²LEN наполегливо рекомендовано не використовувати H1-антигістамінні препарати першого покоління при алергії в дорослих і особливо в дітей. Цю думку поділяє ініціатива ARIA.
Біластин: фармакологічні властивості та клінічна ефективність
Оригінальний біластин (Ніксар®) є неседативним антигістамінним препаратом другого покоління, що включено до Переліку оригінальних (інноваційних) лікарських засобів, зареєстрованих в Україні [8]. Біластин продемонстрував високу ефективність у лікуванні сезонного й цілорічного алергічного ринокон’юнктивіту та кропив’янки [9].
Селективність до H1-гістамінових рецепторів
Одним із ключових факторів ефективності антигістамінних препаратів є їхня селективність до H1-гістамінових рецепторів. Біластин показав найвищу селективність серед досліджуваних препаратів другого покоління [9].
Висока спорідненість біластину до H1-рецепторів забезпечує виражену антигістамінну активність за мінімального впливу на інші рецептори, що зменшує ризик небажаних ефектів.
Біластин продемонстрував у спостереженнях in vitro найвищу здатність зв’язуватися з H1-гістаміновими рецепторами порівняно з іншими антигістамінними препаратами другого покоління [10]. У дослідженнях на тканинах мозочка морської свинки біластин показав зв’язування з Н1-рецепторами в 3,2 раза сильніше, ніж цетиризин, і в 5,6 раза сильніше, ніж фексофенадин.
В експериментах на ізольованій кишці морської свинки для блокування гістамінової реакції біластину потрібна була у 8 разів менша концентрація, ніж цетиризину, і в 3 рази менша, ніж фексофенадину.
Порівняльна ефективність збільшених доз у разі кропив’янки
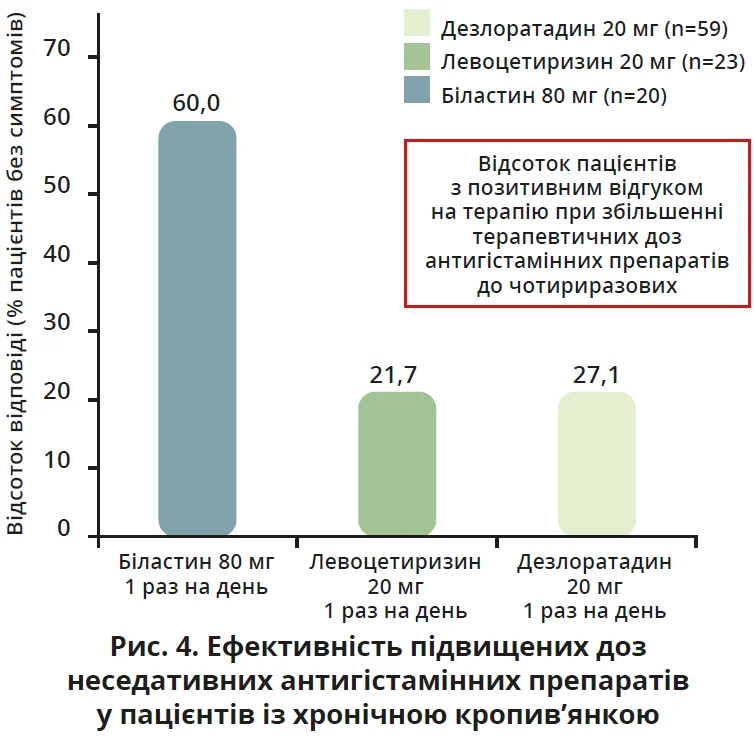
У клінічних дослідженнях порівняльної ефективності збільшених доз неседативних антигістамінних препаратів у пацієнтів із хронічною кропив’янкою біластин мав найліпші результати. При збільшенні дози до чотириразової (80 мг 1 раз на день) позитивний відгук на терапію спостерігався в 60,0% пацієнтів, що значно перевищувало ефективність левоцетиризину 20 мг (21,7%) і дезлоратадину 20 мг (27,1%) [27] (рис. 4).
Вплив на H1-рецептори головного мозку
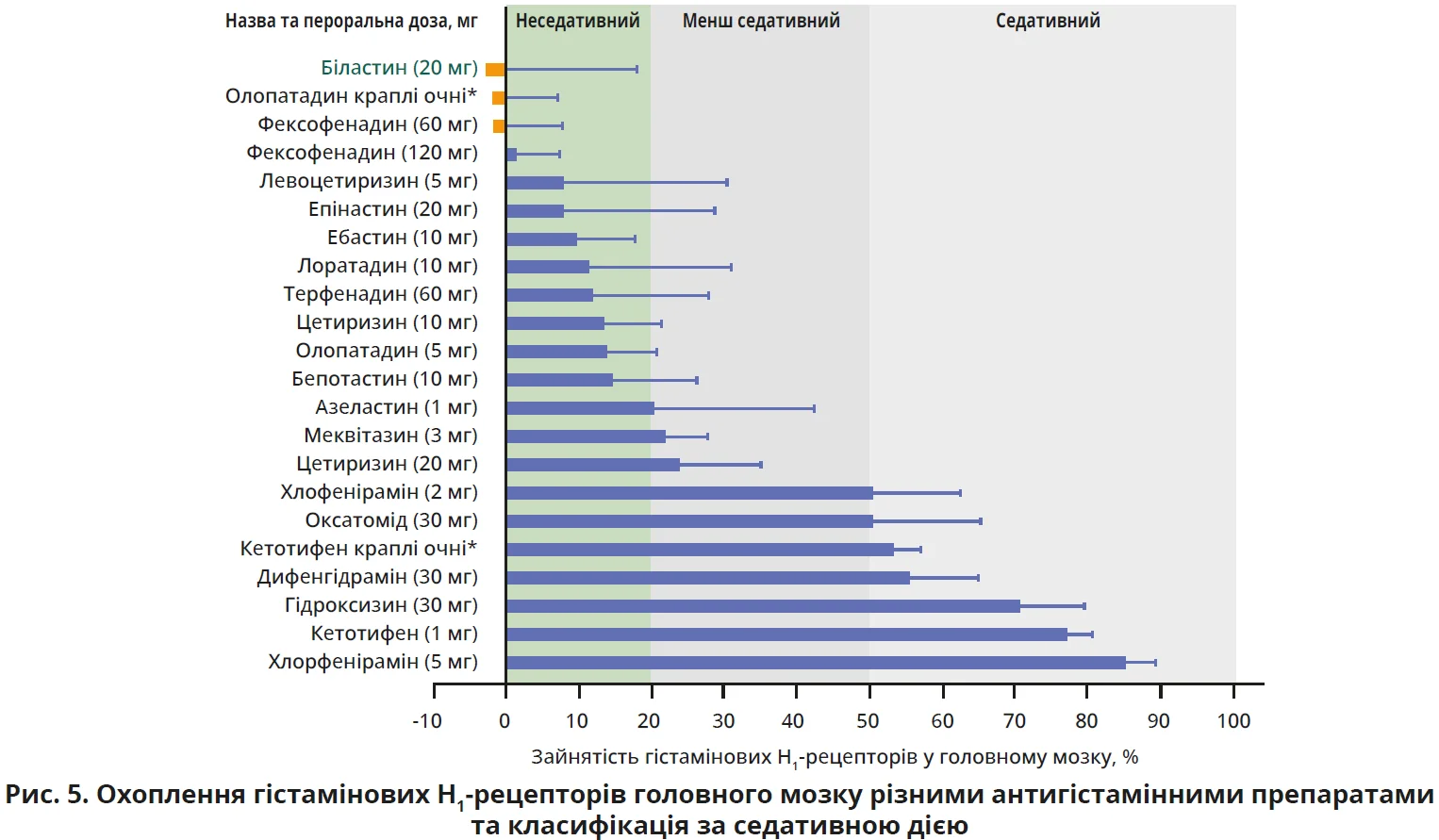
За результатами досліджень охоплення гістамінових H1-рецепторів мозку різними антигістамінними препаратами, біластин можна класифікувати як неседативний препарат, адже він мав нульовий показник (при охопленні H1-рецепторів на ≤20%, в одночасно проведеному тесті когнітивних функцій не було виявлено порушення працездатності) [12] (рис. 5).
Відсутність проникнення крізь гематоенцефалічний бар’єр
Біластин має молекулярну масу 463,6 Да, що перевищує критичний поріг у 450 Да для пасивної дифузії крізь гематоенцефалічний бар’єр [13]. Дослідження з позитронно-емісійною томографією показали, що біластин не проникає в мозок і не спричиняє седативного ефекту [12].
Препарат характеризувався сонливістю на рівні плацебо в пацієнтів із цілорічним алергічним ринітом. У порівняльному дослідженні показник сонливості при застосуванні біластину 20 мг становив 3,7%, що практично не відрізнялося від плацебо (3,2%) і було значно нижчим, аніж у разі застосування цетиризину 10 мг (6,9%) [14]. Біластин відповідає поточним рекомендаціям ARIA застосовувати неседативні H1-антигістамінні препарати [8, 15].
Профіль безпеки
Біластин характеризується сприятливим профілем безпеки та відсутністю потреби в корекції дози в пацієнтів з порушенням функції нирок, печінковою недостатністю й осіб похилого віку.
95% препарату виводиться в незміненому вигляді, що свідчить про мінімальний метаболізм. Біластин не індукував і не пригнічував активність ізоферментів CYP450, що знижує ризик лікарських взаємодій при одночасному прийманні з іншими препаратами.
Психомоторні функції після приймання біластину 20 мг і алкоголю 1 раз на день перебували на тому самому рівні, що й після одночасного застосування алкоголю та плацебо; це підтверджує відсутність негативного впливу на когнітивні функції навіть за випадкового вживання алкоголю.
Практичне значення фармакологічних властивостей біластину
Висока селективність забезпечує швидке й ефективне блокування опосередкованих гістаміном симптомів, тоді як відсутність центральної дії дає пацієнтам змогу зберігати повну працездатність, концентрацію уваги та вести активний спосіб життя без обмежень, пов’язаних із сонливістю.
В Україні оригінальний біластин доступний під торговою назвою Ніксар® у дозуваннях:
- Ніксар® 10 мг – показаний дітям віком від 6 до 11 років з масою тіла не менш ніж 20 кг;
- Ніксар® 20 мг – показаний дорослим і дітям віком від 12 років.
Біластин ефективно застосовується для усунення симптомів сезонного й цілорічного алергічного ринокон’юнктивіту та кропив’янки в дозі 1 таблетка на день, забезпечуючи 24-годинну ефективність [16].
Системне лікування тяжких РГЛЗ
Вертаючись до уповільнених реакцій гіперчутливості до ліків, також варто згадати тяжкі, життєзагрозливі стани, які потребують інтенсивної системної терапії. До таких належать синдром Стівенса – Джонсона та токсичний епідермальний некроліз.
Існують різні підходи до системного лікування тяжких РГЛЗ, однак бракує уніфікованих протоколів ведення таких пацієнтів. Наявні варіанти лікування здебільшого представлені у вигляді поодиноких клінічних випадків або серій клінічних спостережень, а наявна доказова база переважно ґрунтується на думці експертів і консенсусних рекомендаціях [17, 18].
Для системного лікування синдрому Стівенса – Джонсона та токсичного епідермального некролізу розглядаються такі можливі варіанти:
- плазмаферез;
- застосування циклоспорину (імуносупресант, який є інгібітором активації кальциневрину T-лімфоцитів);
- застосування блокаторів фактора некрозу пухлин-α (наприклад, інфліксимабу – одного з п’яти препаратів цієї групи, схвалених Управлінням США з контролю продовольства та медикаментів);
- нормальний людський імуноглобулін;
- системні глюкокортикостероїди.
Висновки
Медикаментозна алергія залишається важливою клінічною проблемою, що потребує комплексного підходу до діагностики та лікування.
Оновлена номенклатура реакцій на ліки, представлена на конгресі EAACI 2025, дає змогу ліпше розуміти патогенетичні механізми РГЛЗ й обирати оптимальну терапевтичну тактику. Диференційна діагностика ґрунтується на ретельному аналізі клінічних проявів, часових характеристик розвитку реакції та результатів діагностичних тестів.
У лікуванні кропив’янки як одного з проявів медикаментозної алергії головна роль відводиться H1-антигістамінним препаратам другого покоління.
Серед них біластин (Ніксар®) займає особливе місце завдяки високій селективності до H1-рецепторів, відсутності проникнення крізь гематоенцефалічний бар’єр, доведеній клінічній ефективності та сприятливому профілю безпеки. Препарат відповідає сучасним міжнародним рекомендаціям EAACI/ARIA й може розглядатися як препарат вибору для лікування алергічного ринокон’юнктивіту та кропив’янки різної етіології.
Література
- Brockow K., Ardern-Jones M.R., Mockenhaupt M., et al. EAACI position paper on how to classify cutaneous manifestations of drug hypersensitivity. Allergy. 2019; 74 (1): 14-27. doi: 10.1111/all.13562. Epub 2018 Dec 5. PMID: 30028512.
- Romano A., Atanaskovic-Markovic M., Barbaud A., et al. Towards a more precise diagnosis of hypersensitivity to beta-lactams – an EAACI position paper. Allergy. 2020; 75 (6): 1300-1315. doi: 10.1111/all.14122. PMID: 31749148.
- Vrysis C., Katsarou A., Lytras T., Katsikas K., Falagas M.E. Rash associated with antibiotic administration in patients with infectious mononucleosis: a systematic review and meta-analysis. Eur. J. Clin. Microbiol. Infect. Dis. 2025 Sep; 44 (9): 2183-2196. doi: 10.1007/s10096-025-05189-3. Epub 2025 Jun 13. PMID: 40512251.
- Descamps V., Valance A., Edlinger C., et al. Association of human herpesvirus 6 infection with drug reaction with eosinophilia and systemic symptoms. Arch. Dermatol. 2001; 137 (3): 301-304. PMID: 11255328.
- Barbaud A., Garvey L.H., Torres M., et al. EAACI/ENDA position paper on drug provocation testing. Allergy. 2024 Mar; 79 (3): 565-579. doi: 10.1111/all.15996. Epub 2023 Dec 28. PMID: 38155501.
- Yang B.C., Castells M. Medical algorithm: diagnosis and treatment of drug hypersensitivity reactions to biologicals. Allergy. 2020; 75 (12): 3293-3296. doi: 10.1111/all.14432. Epub 2020 Jun 18. PMID: 32496608.
- Zuberbier T., Abdul Latiff A.H., Abuzakouk M., et al. The international EAACI/GA²LEN/EuroGuiDerm/APAAACI guideline for the definition, classification, diagnosis, and management of urticaria. Allergy. 2022; 77 (3): 734-766. doi: 10.1111/all.15090. Epub 2021 Oct 20. PMID: 34536239.
- Державний експертний центр МОЗ України. Перелік оригінальних лікарських засобів, зареєстрованих в Україні станом на 2025 рік.
- Wang X.Y., Lim-Jurado M., Prepageran N., Tantilipikorn P., Wang de Y. Treatment of allergic rhinitis and urticaria: a review of the newest antihistamine drug bilastine. Ther. Clin. Risk Manag. 2016; 12: 585-597. doi: 10.2147/TCRM.S105189. PMID: 27110120; PMCID: PMC4835134.
- Corcóstegui R., Labeaga L., Innerárity A., Berisa A., Orjales A. Preclinical pharmacology of bilastine, a new selective histamine H1 receptor antagonist: receptor selectivity and in vitro antihistaminic activity. Drugs R. D. 2005; 6 (6): 371-384. doi: 10.2165/00126839-200506060-00005. PMID: 16274260.
- Sánchez-Borges M., et al. Comparative efficacy of non-sedating antihistamine updosing in patients with chronic urticaria. World Allergy Organization Journal. 2014; 7: 33. Available at: http://www.waojournal.org/content/7/1/33.
- Kawauchi H., Yanai K., Wang D.-Y., et al. Antihistamines for allergic rhinitis treatment from the viewpoint of nonsedative properties. Int. J. Mol. Sci. 2019; 20: 213. doi: 10.3390/ijms20010213.
- Pardridge W.M. Drug transport across the blood-brain barrier. Journal of Cerebral Blood Flow & Metabolism. 2012; 32 (11): 1959-1972. doi: 10.1038/jcbfm.2012.126.
- Sastre J., Mullol J., Valero A., Valiente R., Bilastine Study Group. Efficacy and safety of bilastine 20 mg compared with cetirizine 10 mg and placebo in the treatment of perennial allergic rhinitis. Curr. Med. Res. Opin. 2012; 28 (1): 121-130. doi: 10.1185/03007995.2011.640667. Epub 2011 Nov 30. PMID: 22077106.
- Brożek Jan L., et al. Allergic Rhinitis and its Impact on Asthma (ARIA) Guidelines: Revision Journal of Allergy and Clinical Immunology. 2010; 126 (3): 466-476.
- Державний реєстр лікарських засобів України. Інструкція для медичного застосування препарату Ніксар®.
- Creamer D., Walsh S.A., Dziewulski P., et al. U.K. guidelines for the management of Stevens–Johnson syndrome / toxic epidermal necrolysis in adults. British Journal of Dermatology. 2016; 174 (6): 1194-1227. doi: 10.1111/bjd.14530.
- Chang H.-C., Wang T.-J., Lin M.-H., Chen T.-J. A review of the systemic treatment of Stevens–Johnson syndrome and toxic epidermal necrolysis. Biomedicines. 2022; 10: 2105. doi: 10.3390/biomedicines10092105.
Конфлікт інтересів: на початку доповіді професорка І.В. Гогунська повідомила про конфлікт інтересів (є спікеркою та консультанткою компанії Berlin-Chemie Menarini).