Лікування алергічного риніту: коли, кому та як призначати антигістамінні препарати й інгаляційні кортикостероїди
Автор: Сергій Вікторович ЗАЙКОВ, доктор медичних наук, професор кафедри фтизіатрії і пульмонології Національного університету охорони здоров’я України ім. П.Л. Шупика (м. Київ), президент ВГО «Асоціація алергологів України»
Алергічний риніт (АР), який нині змушує страждати майже 30% населення всього світу (Tohidinik М. et al., 2019), інколи називають наріжним каменем алергології через його значну поширеність і здатність до прогресування. Поширеність АР прогресивно зростає: нині на це захворювання потерпають 10-40% дорослих і 2-25% дітей, що мешкають у розвинених країнах (Zhang Y. et al., 2019). Згідно з даними нещодавно завершеного дослідження CORE поширеність в Україні АР, діагностованого кваліфікованими лікарями, становить 33,4%, тоді як частота симптомів АР, зафіксованих самими пацієнтами, дорівнює 44,7% (Nugmanova D. et al., 2021). Пік захворювання на АР у нашій країні припадає на травень, здебільшого (71,9% випадків) його виникнення провокує пилок (Nugmanova D. et al., 2021).
На перший погляд, захворювання на АР може здатися несерйозним, оскільки воно не чинить значного впливу на смертність та інвалідність, але ця патологія істотно знижує якість життя, обмежує соціальну активність, здатність працювати, вчитися, керувати автомобілем та іншими механізмами, погіршує когнітивні здатності, настрій, відпочинок (Bjermer L. et al., 2019). Соціально-економічний тягар АР є досить значним, оскільки загальні витрати на лікування одного хворого становлять 195,6 євро/рік, а загальні суспільні витрати оцінено в 440,9 млн євро/рік у перерахунку на стандартизовану поширеність захворювання (Li X. et al., 2022).
Патофізіологія
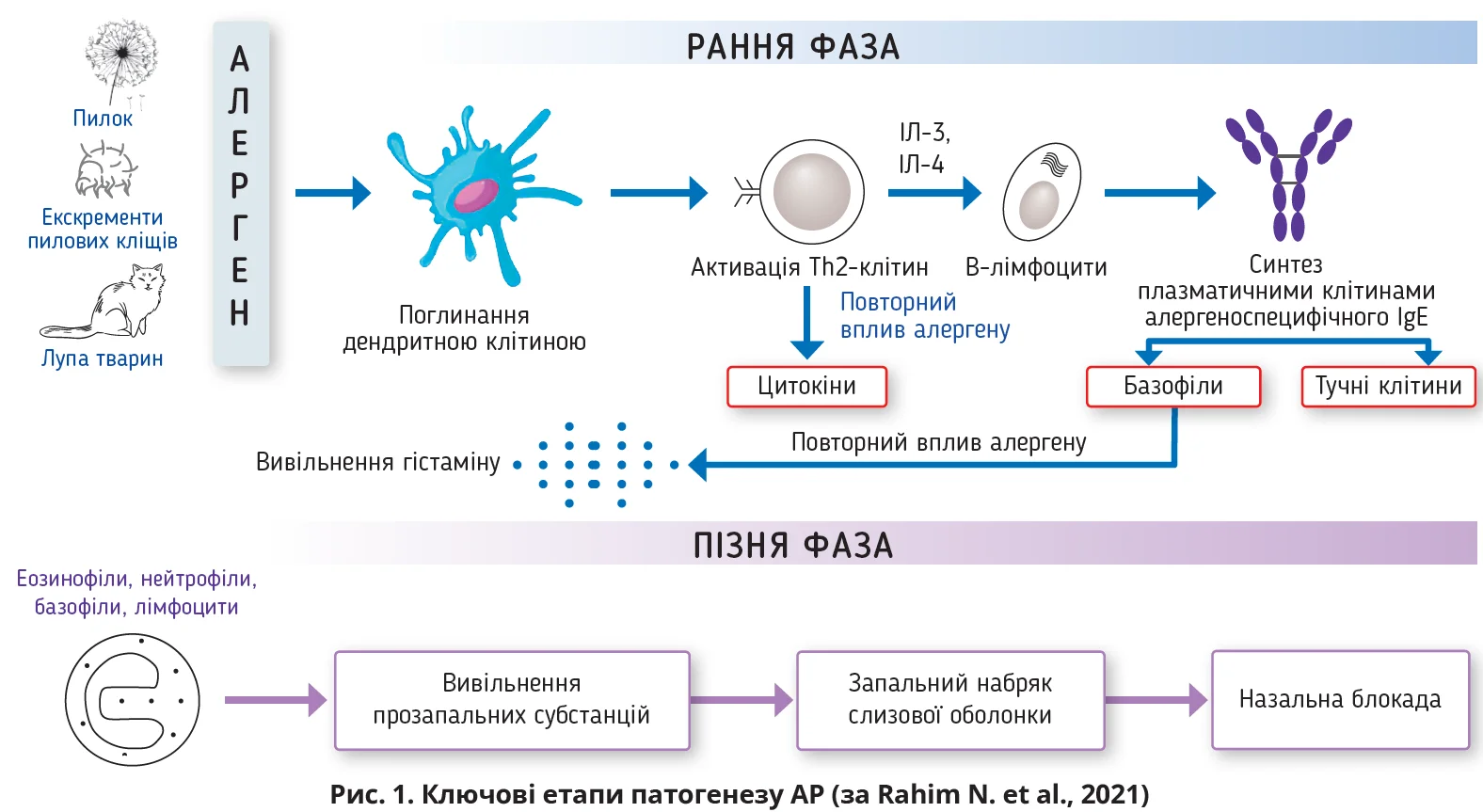
Патофізіологія АР досить складна та ґрунтується на дестабілізації тучних клітин, вивільненні біологічно активних речовин та ініціюванні імунологічних каскадів (рис. 1).
У розвитку АР умовно виділяють ранню та пізню фази; ініціює патологічний процес вплив різноманітних алергенів (пилок, кліщі, таргани та/або шерсть тварин), котрі розпізнаються антигеноспецифічними рецепторами імуноглобуліну Е (IgE), розташованими на тучних клітинах і базофілах, що призводить до дегрануляції тучних клітин. Типовою клінічною характеристикою ранньої фази АР вважають швидку появу (протягом кількох хвилин) назальних (чхання, ринорея) й очних (свербіж, почервоніння, сльозотеча) симптомів. Виникнення цих патологічних ознак пояснюють вивільненням гістаміну з тучних клітин із наступним викидом інших потужних прозапальних цитокінів, ейкозаноїдів (інтерлейкін-3 (ІЛ-3), ІЛ-4, простагландини, кініни), що зумовлює підвищення проникності судин та утворення набряку слизової оболонки (Bjermer L. et al., 2019).
Пізня фаза АР розвивається протягом декількох годин після контакту з алергеном, під час цієї фази відбувається залучення в патологічний процес різноманітних клітин (базофілів, нейтрофілів, Т-лімфоцитів, моноцитів, еозинофілів) і вивільнення численних прозапальних медіаторів (цитокіни, простагландини, лейкотрієни). Під час пізньої фази АР відбувається ремоделювання тканин, розвивається та прогресує назальний венозний застій, зберігається набряк тканин. Унаслідок запалення слизової носа тканини стають чутливішими та сильніше реагують на вплив алергенів. Зміни, що відбуваються під час пізньої фази, а також зміни чутливості тканин спричиняють виникнення бронхіальної гіперреактивності (Bjermer L. et al., 2019). Вивчення особливостей патофізіології АР дало змогу не тільки зрозуміти причини розвитку захворювання, але й розробити найефективніші схеми лікування, що ґрунтуються на призначенні антигістамінних препаратів (АГП) й інгаляційних кортикостероїдів (ІКС).
Механізми дії АГП та ІКС
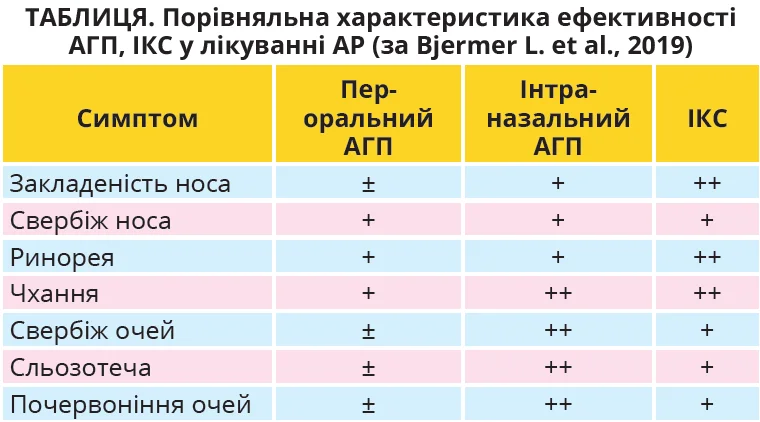
Згідно з поширеним уявленням АГП інгібують Н1-рецептори та запобігають дегрануляції тучних клітин, стабілізуючи їхні клітинні мембрани, змінюючи активність гістамінових рецепторів, перешкоджаючи тим самим негативному впливу гістаміну на нервові закінчення, слизові залози та кровоносні судини (Simons F. et al., 2011). Блокування Н1-рецепторів нейтралізує гістамін-індуковане підвищення проникності судин, сприяє покращенню відтоку капілярної рідини та зменшує ринорею, свербіж у носі, чхання (табл.). Нещодавно доведено, що АГП мають комбінований механізм дії завдяки наявності протизапального й антилейкотрієнового ефектів (Zappia C. et al., 2021). Завдяки АГП відбувається стабілізація тучних клітин, блокується вивільнення прозапальних медіаторів, знижуються вміст і синтез лейкотрієнів, інгібується активність фосфоліпази А2 (Bjermer L. et al., 2019). Є повідомлення, що АГП сприяють зменшенню кількості еозинофілів, нейтрофілів і прозапальних клітин (фактора некрозу пухлин-α (ФНП-α), ІЛ-1β, ІЛ-4, ІЛ-8, гранулоцитарно-макрофагального колонієстимулювального фактора – ГМ-КСФ), які зумовлюють подовження запальної реакції й індукують виникнення симптомів АР пізньої фази (венозний застій, ринорея, гіперчутливість). Обговорюється здатність АГП перешкоджати специфічній імунній взаємодії між T-клітинами та дендритними клітинами (Bjermer L. et al., 2019). Відома значна седативна побічна дія АГП, яка притаманна представникам 1-го покоління цих засобів, значно обмежує їх застосування. Зокрема, пероральні АГП 1-го покоління протипоказані пацієнтам, які потребують пильності, інтелектуальної майстерності та здатності виконувати складні сенсомоторні завдання (Simons F. et al., 2011). Нині в клінічній практиці використовують переважно АГП 2-го покоління, що мають добрий профіль безпеки та не чинять гальмівного ефекту на центральну нервову систему, а їх скасування не супроводжується розвитком тахіфілаксії, що дає змогу застосовувати АГП 2-го покоління протягом тривалого часу.
Яскравим прикладом довготривалого безпечного застосування перорального АГП є результати рандомізованого контрольованого дослідження, згідно з дизайном якого дітям з алергією на побутового пилового кліща призначали 3-річну терапію цетиризином, яка добре переносилася, не супроводжувалася виникненням серйозних побічних дій і дала змогу вірогідно (р=0,0002) зменшити ймовірність розвитку сенсибілізацій до нових алергенів порівняно з прийомом на вимогу (Ciprandi G. et al., 2003).
ІКС вважають потужними інгібіторами пізньої фази АР: вони гальмують залучення в патологічний процес клітин Лангерганса, макрофагів, тучних клітини, Т-клітин, еозинофілів, розташованих у слизовій оболонці носа. Доведено, що ІКС пригнічують вивільнення запальних медіаторів із багатьох клітин, що беруть участь у патофізіології АР: знижують концентрацію IЛ-4, IЛ-5 та IЛ-13 у назальному секреті, інгібують секрецію інтерферону-γ, IЛ-2 й IЛ-17 після впливу алергену (Watts A. et al., 2019). Також ІКС зменшують рівень ФНП-α, ГМ-КСФ, ІЛ-6, ІЛ-8, забезпечують падіння експресії ICAM-1 на слизовій оболонці носа як на ранній, так і на пізній фазі розвитку симптомів АР. Потужна протизапальна дія ІКС здатна знизити або навіть запобігти ремоделюванню дихальних шляхів, зменшити їхню гіперреактивність завдяки інгібуванню функції назальних фібробластів (Bjermer L. et al., 2019). ІКС модифікують транскрипцію генів, які залучені у виникнення та прогресування алергічної реакції, знижуючи вироблення клітинних сигнальних молекул і пригнічуючи міграцію й активацію прозапальних клітин. Така багатогранна дія ІКС дає змогу нівелювати або значно зменшити типові прояви АР, як-от нежить, прозорі виділення з носа, чхання, свербіж у носі, утруднення носового дихання (симптоми ранньої фази), а також закладеність носа та гіперреактивність, що виникають на пізній фазі АР і найістотніше знижують якість життя пацієнтів (Watts A. et al., 2019). На відміну від системного застосування кортикостероїдів, використання ІКС значно рідше призводить до виникнення серйозних побічних ефектів (остеопорозу, пригнічення осі гіпоталамус – гіпофіз – наднирники, затримки росту, формування катаракти, витончення шкіри, появи синців), тому їх застосування дозволено в дітей від 2 років (Scadding G. et al., 2021). Найчастіше в педіатричній і дорослій популяціях використовується мометазон: його включають у короткі та тривалі схеми лікування завдяки добрій довгостроковій результативності та безпеці (Passali D. et al., 2016). Згідно з даними систематичного аналізу ефективність мометазону в лікуванні та/або профілактиці назальних симптомів у разі сезонного й цілорічного АР відповідає рівню доказів Ia. Він не тільки нівелює клінічні ознаки АР, покращує якість життя, а й відновлює здатність відчувати запахи, не чинить системного впливу, не пригнічує активності надниркових залоз, не провокує виникнення атрофії слизової оболонки носа (Passali D. et al., 2016).
Доведено, що призначення АГП разом з ІКС підвищує ефективність останніх завдяки посиленню передачі сигналів і покращенню транскрипційної активності глюкокортикоїдних рецепторів, такий комбінований вплив дає змогу поліпшити ефективність лікування: одночасне застосування ІКС і АГП значніше підвищує якість життя, ефективніше нівелює назальні й офтальмологічні симптоми, ніж монотерапія ІКС (Chitsuthipakorn W. et al., 2022), та дає змогу знизити дозу ІКС, потрібну для досягнення протизапального й терапевтичного ефектів (Zappia C. et al., 2021). Нещодавно опублікований метааналіз довів ефективність ІКС і пероральних АГП у лікуванні як сезонного АР (середня чисельна різниця, СЧР 1,38; 95% довірчий інтервал, ДІ 1,18-1,58 та СЧР 0,62; 95% ДІ 0,35-0,90 відповідно), так і хронічного АР (СЧР 0,82; 95% ДІ 0,66-0,97 та СЧР 0,27; 95% ДІ 0,11-0,42 відповідно) (Meltzer E. et al., 2021).
Лікування АР: міжнародні рекомендації
Різноманітні міжнародні рекомендації регламентують особливості лікування АР, наведемо положення тих із них, які було опубліковано нещодавно. Згідно з рекомендаціями ARIA (2019) терапією першої лінії в симптоматичних хворих на АР, які не отримували лікування раніше, а також у пацієнтів, котрі вже приймали будь-які ліки, вважається призначення АГП (Н1-блокатора) чи ІКС (Bousquet J. et al., 2020).
У 2020 р. Європейський форум із досліджень і освіти в галузі алергії та захворювань дихальних шляхів (European Forum for Research & Education in Allergy & Airway Diseases, EUFOREA) представив кишенькову настанову з лікування АР. У ній у вигляді стислих, практичних і простих у використанні рекомендацій наводиться алгоритм покрокового лікування АР, призначений саме для використання в реальній клінічній практиці (рис. 2).
Відповідно до алгоритму EUFOREA дорослим пацієнтам із підозрою на АР варто призначати ІКС, неседативний пероральний АГП або інтраназальний АГП, зважаючи на домінувальні симптоми, провокувальні чинники, сподівання пацієнтів і супутні захворювання. На другому етапі пацієнтам, які не відповіли на терапію 1-го етапу, варто призначити фіксовану комбінацію ІКС / інгаляційний АГП після підтвердження діагнозу АР, перевірки комплаєнтності та корекції супутніх захворювань. Додатково підвищувати дозу ІКС на цьому етапі не рекомендується. Третій етап передбачає посилення терапії при тяжкому перебігу АР, а також хворим, які не відповіли на терапію 2-го етапу: додатково до фіксованої комбінації ІКС / інгаляційний АГП призначають іпратропіум, антагоністи рецепторів лейкотрієнів, неседативні АГП, офтальмологічні АГП / кромон і назальний/пероральний деконгестант протягом ≤7 діб (Hellings P. et al., 2020).
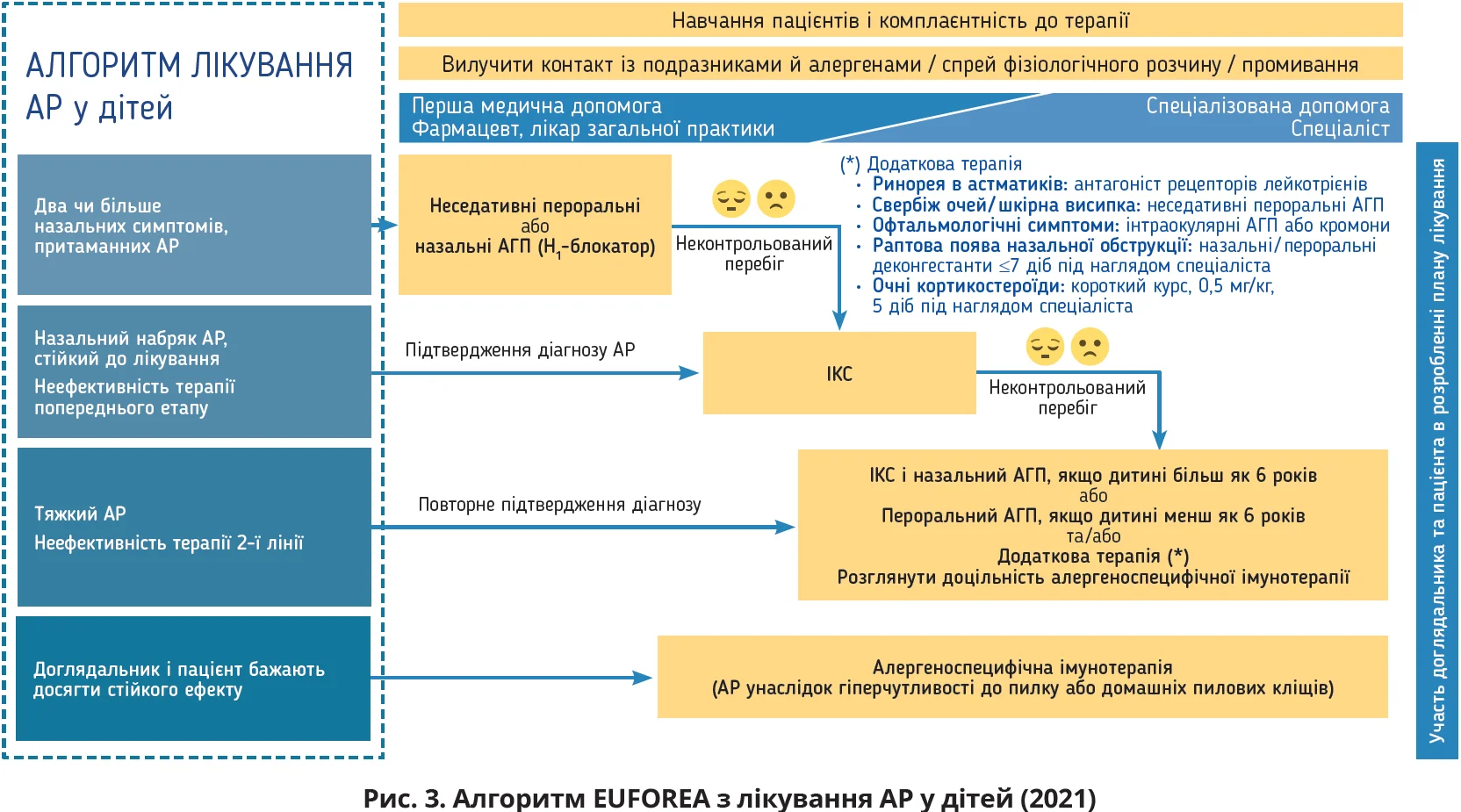
Європейські експерти розробили також педіатричний алгоритм EUFOREA з лікування АР (2021), згідно з яким дітям на першому етапі лікування варто призначати неседативний пероральний або назальний АГП, за умови недостатньої ефективності терапії скасувати АГП та рекомендувати ІКС (Scadding G. et al., 2021). Тяжкий перебіг АР або неефективність терапії 2-ї лінії вважається обґрунтуванням для призначення комбінованої терапії ІКС і назальним АГП дітям віком понад 6 років, у молодших дітей слід застосовувати пероральний АГП та/або додаткову терапію (рис. 3).
Подібні положення містять рекомендації Корейської академії астми, алергії, клінічної імунології (KAAACI): спеціалісти радять призначати хворим на АР комбінацію перорального АГП/ІКС або монотерапію ІКС, зважаючи на прихильність пацієнтів, а також користь і потенційну шкоду від лікування (Yang S. et al., 2023). Такий висновок зроблено на підставі здатності комбінації перорального АГП/ІКС перевищувати ефективність монотерапії ІКС у нівелюванні ринореї (95% ДІ від -0,07 до 0; р<0,05), покращувати якість життя у хворих на ринокон’юнктивіт (середня різниця -0,26; 95% ДІ від -0,51 до -0,02; р=0,04) (Yang S. et al., 2023). Фахівці KAAACI (2023) рекомендують обирати певні АГП: «Комбінація перорального АГП/ІКС забезпечує досягнення швидкого терапевтичного ефекту за умови додавання АГП швидкої дії (левоцетиризин/цетиризин)» (Yang S. et al., 2023).
Висновки
АР є поширеним алергічним захворюванням, фармакологічне лікування котрого ґрунтується на призначенні препаратів двох класів – АГП й ІКС, які, впливаючи на основні ланки патогенезу, інгібують виникнення та прогресування алергічної реакції, знижують вироблення клітинних сигнальних молекул і пригнічують міграцію й активацію прозапальних клітин. Міжнародні рекомендації з лікування АР EUFOREA передбачають призначення пероральних неседативних АГП швидкої дії (цетиризин), ІКС (мометазон) або їх комбінації як терапії першої лінії; педіатричний алгоритм EUFOREA підкреслює доцільність першочергового призначення монотерапії АГП та наступної заміни на монотерапію ІКС за недостатньої ефективності терапії 1-ї лінії.
Література
- Bjermer L., Westman M., Holmström M., et al. The complex pathophysiology of allergic rhinitis: scientific rationale for the development of an alternative treatment option. Allergy Asthma Clin. Immunol. 2019; 15: 24. doi: 10.1186/s13223-018-0314-1.
- Bousquet J., Schünemann H.J., Togias A., et al. Allergic Rhinitis and Its Impact on Asthma Working Group. Next-generation Allergic Rhinitis and Its Impact on Asthma (ARIA) guidelines for allergic rhinitis based on Grading of Recommendations Assessment, Development and Evaluation (GRADE) and real-world evidence. J. Allergy Clin. Immunol. 2020; 145 (1): 70-80.e3. doi: 10.1016/j.jaci.2019.06.049.
- Chitsuthipakorn W., Hoang M.P., Kanjanawasee D., et al. Combined medical therapy in the treatment of allergic rhinitis: systematic review and meta-analyses. Int. Forum Allergy Rhinol. 2022; 12 (12): 1480-1502. doi: 10.1002/alr.23015.
- Ciprandi G., Frati F., Marcucci F., Sensi L., Milanese M., Tosca M.A. Long-term cetirizine treatment may reduce new sensitisations in allergic children: a pilot study. Eur. Ann. Allergy Clin. Immunol. 2003 Jun; 35 (6): 208-11.
- Hellings P.W., Scadding G., Bachert C., et al. EUFOREA treatment algorithm for allergic rhinitis. Rhinology. 2020; 58 (6): 618-622. doi: 10.4193/Rhin20.376.
- Li X., Xu X., Li J., et al. Direct and indirect costs of allergic and non-allergic rhinitis to adults in Beijing, China. Clin. Transl. Allergy. 2022; 12 (4): e12148. doi: 10.1002/clt2.12148.
- Marcucci F., Sensi L.G., Abate P., et al. Anti-inflammatory activity and clinical efficacy of a 3-month levocetirizine therapy in mite-allergic children. Inflamm. Allergy Drug Targets. 2011; 10 (1): 32-8. doi: 10.2174/187152811794352033.
- Meltzer E.O., Wallace D., Friedman H.S., et al. Meta-analyses of the efficacy of pharmacotherapies and sublingual allergy immunotherapy tablets for allergic rhinitis in adults and children. Rhinology. 2021; 59 (5): 422-432. doi: 10.4193/Rhin21.054.
- Nugmanova D., Feshchenko Y., Khegay Y., et al. The Prevalence of Allergic Rhinitis, its Triggers, and Associated Factors in Commonwealth of Independent States Countries (Ukraine, Kazakhstan, and Azerbaijan): Results of the CORE Study. Dubai Med. J. 2021; 4: 81-92. doi: 10.1159/000514318.
- Passali D., Spinosi M.C., Crisanti A., et al. Mometasone furoate nasal spray: a systematic review. Multidiscip. Respir. Med. 2016; 11: 18. doi: 10.1186/s40248-016-0054-3.
- Rahim N.A., Jantan I., Said M.M., et al. Anti-Allergic Rhinitis Effects of Medicinal Plants and Their Bioactive Metabolites via Suppression of the Immune System: a mechanistic review. Front. Pharmacol. 2021; 12: 660083. doi: 10.3389/fphar.2021.660083.
- Scadding G.K., Smith P.K., Blaiss M., et al. Allergic Rhinitis in Childhood and the New EUFOREA Algorithm. Front. Allergy. 2021; 2: 706589. doi: 10.3389/falgy.2021.706589.
- Simons F.E., Simons K.J. Histamine and H1-antihistamines: celebrating a century of progress. J. Allergy Clin. Immunol. 2011; 128 (6): 1139-1150.e4.doi: 10.1016/j.jaci.2011.09.005.
- Tohidinik H.R., Mallah N., Takkouche B. History of allergic rhinitis and risk of asthma; a systematic review and meta-analysis. World Allergy Organ. J. 2019; 12: 100069. doi: 10.1016/j.waojou.2019.100069.
- Watts A.M., Cripps A.W., West N.P., et al. Modulation of Allergic Inflammation in the Nasal Mucosa of Allergic Rhinitis Sufferers With Topical Pharmaceutical Agents. Front. Pharmacol. 2019; 10: 294. doi: 10.3389/fphar.2019.00294.
- Yang S.I., Lee I.H., Kim M., et al. KAAACI Allergic Rhinitis Guidelines: Part 1. Update in Pharmacotherapy. Allergy Asthma Immunol. Res. 2023; 15 (1): 19-31. doi: 10.4168/aair.2023.15.1.19.
- Zappia C.D., Torralba-Agu V., Echeverria E., et al. Antihistamines Potentiate Dexamethasone Anti-Inflammatory Effects. Impact on Glucocorticoid Receptor-Mediated Expression of Inflammation-Related Genes. Cells. 2021; 10: 3026. doi: 10.3390/cells10113026.
- Zhang Y., Zhang L. Increasing Prevalence of Allergic Rhinitis in China. Allergy Asthma Immunol. Res. 2019; 11 (2): 156-169. doi: 10.4168/aair.2019.11.2.156.