Консенсус Всесвітньої організації алергії (WAO) щодо визначення тяжкості харчової алергії
Переклала й адаптувала д-р мед. наук Лариса Стрільчук
Харчова алергія (ХА) – це вагома проблема громадського здоров’я, поширеність якої становить близько 10% загальної популяції світу. Цей патологічний стан асоціюється зі значним емоційним, соціальним і фінансовим тягарем, а також із надмірним навантаженням на систему охорони здоров’я. ХА включає широкий спектр фенотипів і ступенів тяжкості, що відображається в значній варіабельності спричинених харчовими алергенами клінічних проявів і доз цих алергенів, достатніх для провокації реакції.
Діагностика ХА є складною. Найчастіше застосовуються шкірний прик-тест і визначення специфічних імуноглобулінів Е (IgE), але золотим стандартом залишається пероральна провокаційна проба, хоча цей метод і має низку обмежень (ризик тяжких реакцій, висока вартість, низька відтворюваність). Оскільки результати сенсибілізаційних тестів не корелюють із тяжкістю реакції під час провокаційних проб, існує потреба в надійних біомаркерах, здатних допомогти передбачити ризик алергеноспецифічних реакцій та їхню тяжкість.
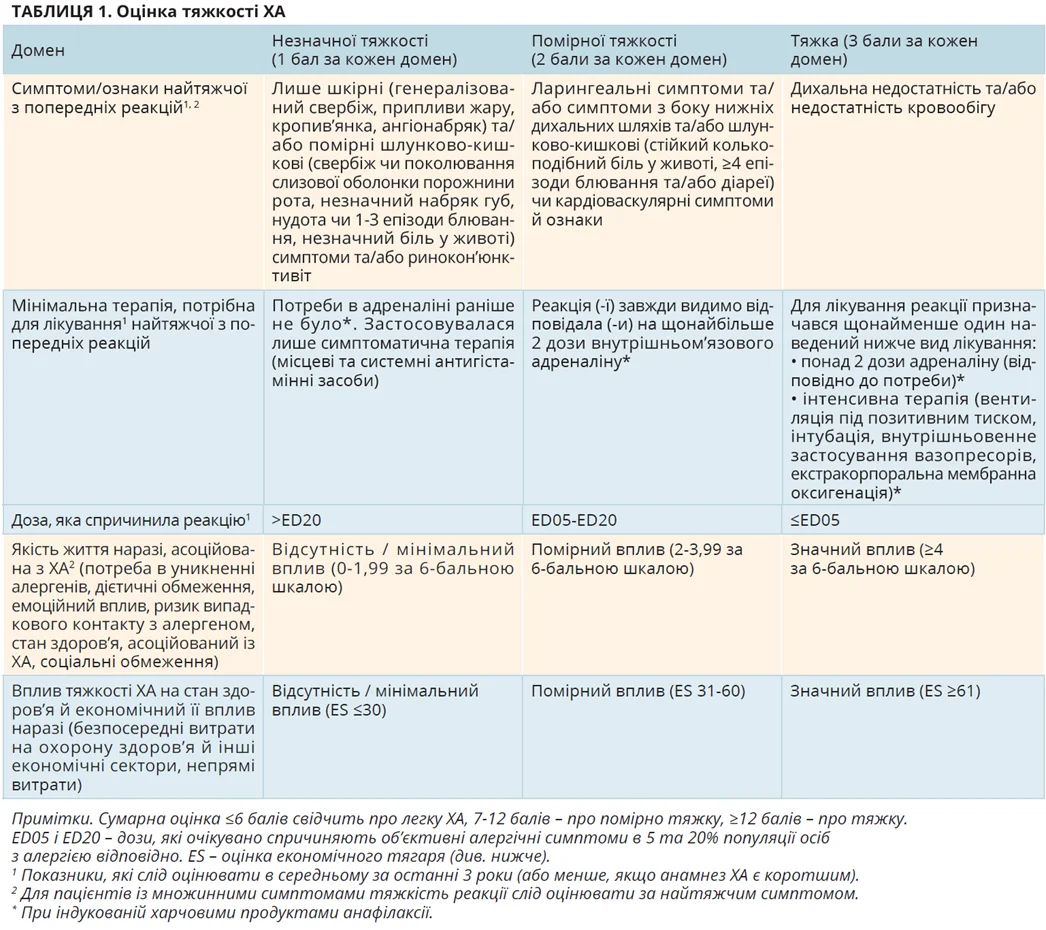
Повноцінне визначення ХА як багатогранної хвороби дотепер відсутнє, що перешкоджає наданню оптимальної медичної допомоги. У зв’язку із цим Всесвітня організація алергії започаткувала проєкт створення міжнародної системи визначення та класифікації тяжкості ХА (DEfinition of Food Allergy SEverity, DEFASE). Із цією метою робоча група з 54 експертів сформувала основні положення консенсусу й узгодила їх шляхом голосування. Зокрема, для оцінки тяжкості ХА запропоновано враховувати бальну оцінку за різними доменами (табл. 1).
Перед тим як оцінювати тяжкість ХА, слід виключити ситуації, які складно контролювати:
- неможливість визначити тригерні харчові алергени;
- відсутність підтримки щодо самоконтролю пацієнта, його батьків або родини (тобто відсутність навчання та підтримувальних заходів, які медичний персонал проводить для підвищення впевненості й покращення навиків пацієнта стосовно контролю свого алергічного захворювання, в тому числі регулярної оцінки прогресу та проблем, установлення цілей і допомоги у вирішенні проблем);
- невдача самоконтролю, відсутність підготовки до менеджменту алергічних реакцій (відсутність плану дій на випадок їх виникнення), неможливість уникнення тригерних алергенів, неможливість пролікувати реакцію належним чином, неспроможність пацієнта чи його батьків/родини ефективно контролювати алергічне захворювання, включаючи симптоми, реакції, їхні фізичні й соціальні наслідки, неспроможність проводити лікування та впроваджувати зміни способу життя (уникати алергенів, читати підписи на упаковках харчових продуктів, носити із собою адреналін тощо).
Якщо наведені вище чинники відсутні, алергічні реакції пацієнта можна поділяти на легкі, помірно тяжкі й тяжкі. Натомість, якщо наявний будь-який із цих чинників, тяжкість алергічної реакції можна визначати лише після його усунення.
Пацієнти, в яких спостерігалася близька до фатальної алергічна реакція, що потребувала лікування у відділенні інтенсивної терапії, протягом життя вважаються особами з тяжкою ХА.
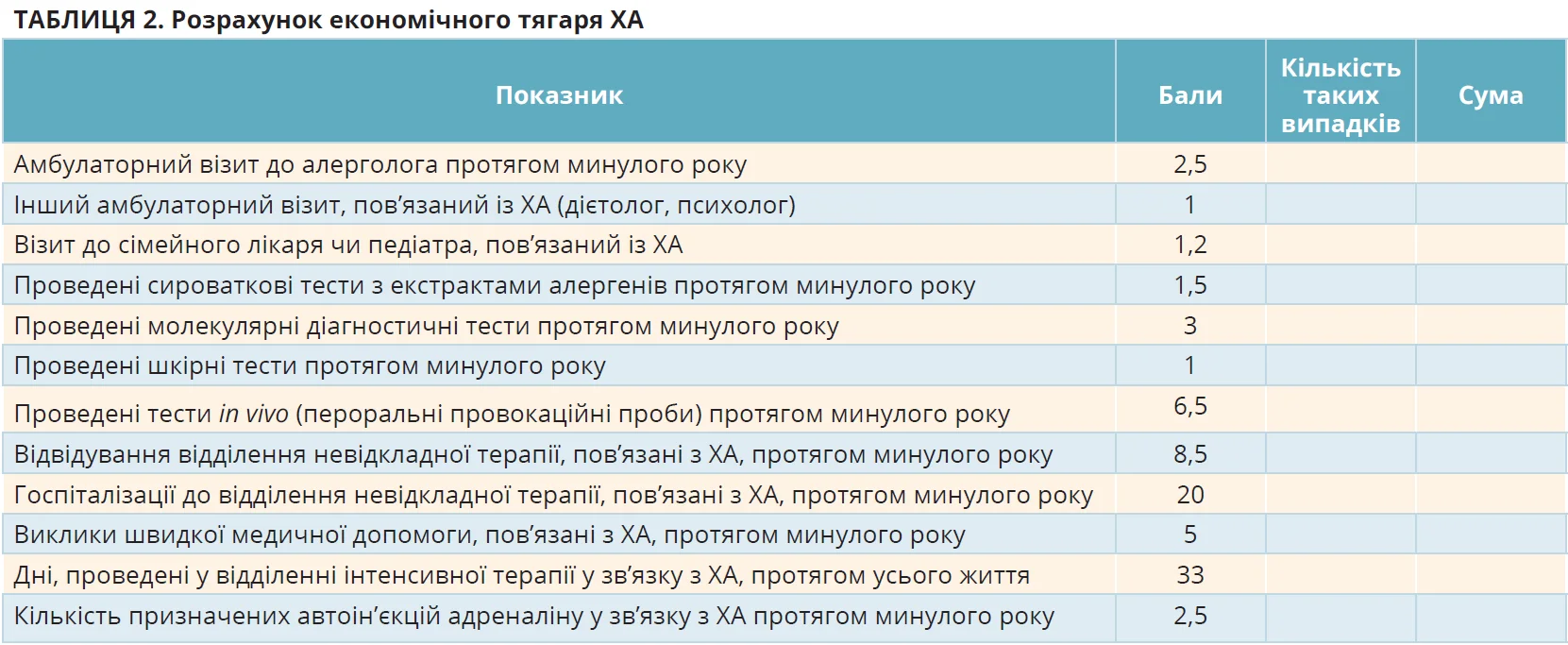
Окрема робоча група, яка включала фахівців із 15 країн, працювала з економічним аспектом оцінки тяжкості ХА, сформувавши шкалу тяжкості економічного впливу ХА (табл. 2). Для оцінки економічного тягаря ХА значення кожного показника слід помножити на кількість таких випадків протягом останнього року.
Висновки
Цей консенсус являє собою першу спробу узгодження визначення тяжкості ХА в дорослих і дітей на підставі симптомів й аспектів, не пов’язаних із симптомами. Незважаючи на обмеження, асоційовані зі складністю питання, це визначення буде корисним для встановлення меж необхідних діагностичних і лікувальних заходів у разі ХА.
Запропонована шкала ґрунтується на наявній доказовій базі й експертних поглядах і може виступати основою для визначення тягаря ХА, хоча для встановлення методів вибору пацієнтів – кандидатів для специфічних лікувальних підходів потрібні подальші дослідження. Ця шкала також потребує зовнішньої валідації й адаптації до різних харчових алергенів, різних популяцій і різних умов. Удосконалення та стандартизація визначень і підходів до класифікації ХА разом зі спільним прийняттям рішень у співпраці з пацієнтами та їхніми сім’ями дадуть змогу прицільніше допомагати особам із ХА, мінімізуючи тягар хвороби.
Література
Arasi S., et al. WAO consensus on DEfinition of Food Allergy SEverity (DEFASE). World Allergy Organization Journal. 2023; 16: 100753. doi: 10.1016/j.waojou.2023.100753.
Антигістамінні препарати в лікуванні ХА
Як було вказано в консенсусі, важливим завданням лікаря є навчання пацієнта самостійному менеджменту алергічних реакцій. Із цією метою доцільно скласти разом із пацієнтом план дій і оформити його в письмовому вигляді. Наприклад, нетяжкі ХА пацієнт може долати самостійно, приймаючи антигістамінні препарати (АГП).
Відомим АГП II покоління є цетиризин, який було схвалено Управлінням із контролю продовольства та медикаментів США (FDA) як рецептурний препарат у 1995 р. і як безрецептурний – у 2007 р. Цетиризин схвалено для лікування цілорічного алергічного риніту та кропив’янки в дорослих і дітей віком понад 6 місяців (у відповідній дитячій формі) та для лікування сезонних алергій у дорослих і дітей віком понад 2 роки (Naqvi A., Gerriets V., 2023). Відповідно до рекомендацій Американської академії алергії, астми й імунології / Американського коледжу алергії, астми й імунології (ААААІ/АСААІ, 2015) цетиризин може застосовуватися при анафілаксії як доповнення до адреналіну.
Цетиризин являє собою антагоніст периферичних гістамінових Н1-рецепторів швидкої дії, який є одним із найселективніших у своєму класі (Gillard M. et al., 2003). Цетиризину притаманний малий обсяг розподілу, що є вагомою перевагою для АГП, оскільки препарати з малим обсягом розподілу протягом тривалого часу перебувають поблизу клітин, а це дає змогу активно впливати на позаклітинні рецептори та реалізувати антигістамінний ефект (Tillement J.-P., 2000). Висока афінність і селективність до Н1-рецепторів забезпечують цетиризину швидкий початок дії, потужний ефект і більшу тривалість дії порівняно з іншими АГП (Gillard M. et al., 2003). Завдяки антагонізму до Н1-рецепторів цетиризин протидіє реалізації ефектів гістаміну та зменшує проникність судин, запобігаючи виходу рідини з капілярів у тканини. Продемонстровано також протизапальні властивості цетиризину та його здатність запобігати міграції нейтрофілів й еозинофілів (Naqvi A., Gerriets V., 2023).
Концентрація цетиризину сягає піку приблизно через 1 годину після вживання, а його ефекти розвиваються через 20-60 хвилин після прийому таблетки та зберігаються протягом 24 годин. Важливо, що цетиризин не є субстратом системи цитохрому Р450, що мінімізує ймовірність міжлікарських взаємодій для цього препарату.
На біодоступність цетиризину не впливає вживання їжі (Naqvi A., Gerriets V., 2023), тому цей препарат можна вживати одразу після того, як продукт, що спровокував алергічну реакцію, потрапив у шлунок.
У рандомізованому подвійному сліпому дослідженні за участю 64 пацієнтів із ХА порівнювалися ефективність і безпека цетиризину та дифенгідраміну. Середній час до зникнення висипки та свербежу, які виникали після пероральної провокаційної проби, на тлі застосування цетиризину становив 40,8±22,11 та 31,3±20,07 хвилини відповідно; для дифенгідраміну результати були подібними. На відміну від профілю ефективності профіль побічних ефектів порівнюваних препаратів відрізнявся: в групі дифенгідраміну седацію відзначали 28,6% учасників, а в групі цетиризину – лише 17,1%. Автори дійшли висновку, що в лікуванні гострих ХА цетиризин має перевагу над дифенгідраміном, оскільки має такі переваги, як довша тривалість дії та менша ймовірність седативного впливу (Park J.H. et al., 2011).
Підсумовуючи вищесказане, можна дійти висновку, що основою лікування всіх алергічних захворювань лишаються модифікація способу життя з уникненням алергенів і застосування АГП. Одним із найширше застосовуваних ефективних АГП II покоління є цетиризин.