Індукована стресом кропив’янка
Автор: Сергій Вікторович ЗАЙКОВ, доктор медичних наук, професор кафедри фтизіатрії і пульмонології Національного університету охорони здоров’я України ім. П.Л. Шупика (м. Київ), президент ВГО «Асоціація алергологів України»
 Кропив’янка є глобальною й актуальною проблемою клінічної практики. Це дерматологічний стан з раптовою появою сверблячих червоних опуклих пухирів або нерівностей на шкірі. Висипання можуть з’являтися на будь-якій ділянці тіла та відрізнятися за розміром і формою, часто зумовлюють дискомфорт і страждання в пацієнтів. Окрім фізичних симптомів, кропив’янка може суттєво впливати на якість життя пацієнтів, їхній соціальний і психологічний добробут, тривожність і проблеми зі сном. Глобальний тягар кропив’янки викликає дедалі більше занепокоєння останніми роками, що пов’язано з її високою поширеністю й потенціалом спричиняти тяжкі алергічні реакції та навіть анафілаксію [1].
Кропив’янка є глобальною й актуальною проблемою клінічної практики. Це дерматологічний стан з раптовою появою сверблячих червоних опуклих пухирів або нерівностей на шкірі. Висипання можуть з’являтися на будь-якій ділянці тіла та відрізнятися за розміром і формою, часто зумовлюють дискомфорт і страждання в пацієнтів. Окрім фізичних симптомів, кропив’янка може суттєво впливати на якість життя пацієнтів, їхній соціальний і психологічний добробут, тривожність і проблеми зі сном. Глобальний тягар кропив’янки викликає дедалі більше занепокоєння останніми роками, що пов’язано з її високою поширеністю й потенціалом спричиняти тяжкі алергічні реакції та навіть анафілаксію [1].
Кропив’янка є не просто симптомом або проблемою шкіри. Вона розглядається як гетерогенна група хвороб/порушень/станів, для котрих характерна певна шкірна реакція, що проявляється швидкою появою пухирів та/або ангіоневротичного набряку (АНН). Останній характеризується тимчасовим локальним набряком, який може вражати всі шари шкіри чи стінки порожнистих внутрішніх органів, як-от ротоглотки, дихальної системи чи шлунково-кишкового тракту. У 50% пацієнтів кропив’янка перебігає ізольовано, у 40% – у поєднанні з АНН, у 10% відзначається тільки АНН. АНН може нести загрозу для життя пацієнта [2]. Деякі хворі на кропив’янку відчувають позашкірні ознаки й симптоми, як-от діарея, біль або набряк суглобів, серцебиття, головний біль, утома та хрипи [3].
Кропив’янка має високу поширеність. Серед усього населення світу 15-20% осіб мали хоча б один епізод кропив’янки в житті. Тягар кропив’янки вищий у молодших вікових групах, дещо зменшується з віком, з незначним збільшенням серед найстарших осіб. Між 1990 і 2019 роками захворюваність і поширеність кропив’янки зросли в більшості вікових категорій, особливо у людей молодого віку і жінок. Більший тягар кропив’янки серед жінок пов’язаний з гормональними відмінностями (коливання рівня естрогену асоційовані з регуляцією імунних реакцій) і генетичною схильністю (певні гени, пов’язані з імунною функцією, розташовані на Х-хромосомі) [1].
До зростання поширеності кропив’янки призводять збільшення впливу алергенів, хімічних речовин і подразників, забруднення повітря, а також зміни в способі життя (харчування, стрес і гіподинамія). Покращення діагностики та підвищення обізнаності про цей стан сприяли вищому рівню виявлення кропив’янки [1].
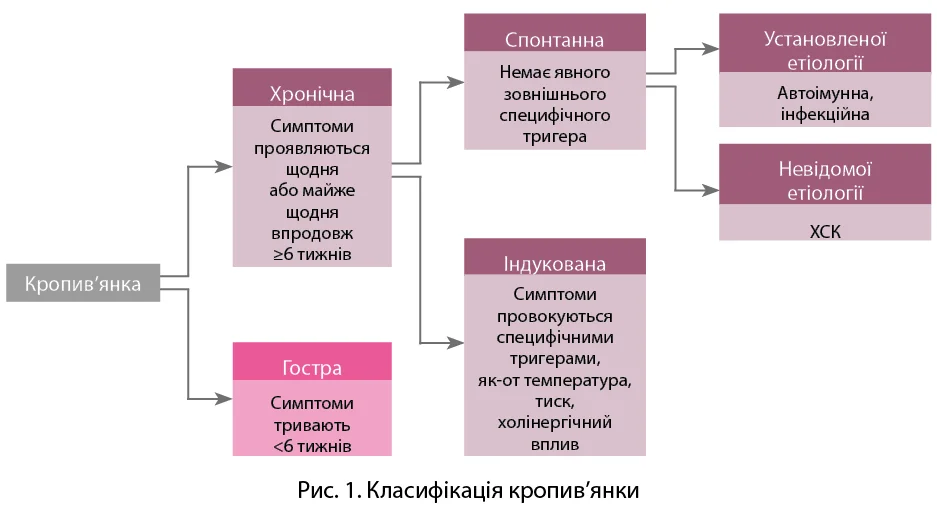
За тривалістю кропив’янка класифікується на гостру та хронічну. Гостра кропив’янка (ГК) визначається як поява пухирів та/або АНН, що тривають 6 тижнів або менше. Хронічна кропив’янка (ХК) визначається як поява пухирів та/або АНН, що тривають понад 6 тижнів. ХК може проявлятися щоденними чи майже щоденними ознаками та симптомами чи періодичним/рецидивним перебігом і може загострюватися після місяців або років повної ремісії [4].
За впливом певних тригерів кропив’янка класифікується на індуковану та спонтанну (рис. 1). Хронічна індукована кропив’янка (ХІК) характеризується певними специфічними тригерами розвитку пухирів та/або АНН. Ці тригери є певними, оскільки патологія завжди виникає, коли тригер присутній, і ніколи не виникає за його відсутності. Тригери є специфічними, оскільки кожен підтип індукованої кропив’янки має свій відповідний тригер (наприклад, холод для холодової кропив’янки), який не є релевантним для інших форм. Існують рідкісні підтипи індукованої кропив’янки, за яких для появи симптомів потрібна комбінація двох або більше певних специфічних тригерів (наприклад, холодова холінергічна кропив’янка) [4].
Тригерами ХІК є фізичні фактори (як-от температура, тиск, ультрафіолетове випромінювання, вода, фізичні вправи), алергени, укуси комах, ліки, препарати крові, харчові продукти, хімічні подразники, хвороби шлунково-кишкового тракту, інфекції, гриби, паразити, ендокринна патологія, пухлини, стрес тощо. За хронічної спонтанної кропив’янки (ХСК) стимули зазвичай не встановлені. Проте є варіанти ХСК з відомими чинниками: автоімунна ХСК I типу з утворенням автоантитіл IgE до автоантигенів або автоімунна ХСК ІІb типу з автоантитілами, які активують мастоцити [5]. Серед усіх випадків ХК превалює ХСК (приблизно 67%), ХІК становить близько 22%, а в 11% випадків відзначається змішаний варіант [5].
Патогенез кропив’янки головним чином пов’язаний з вивільненням гістаміну й інших медіаторів активованими мастоцитами шкіри. Це призводить до активації сенсорних нервів, розширення судин і екстравазації плазми, а також залучення клітин запалення та виникнення висипу [4]. Основним медіатором, відповідальним за прояви кропив’янки, є гістамін, який зв’язується з рецепторами H1 і H2 на судинному ендотелії та визначає ефекти вазодилатації, підвищеної проникності капілярів і свербіж. Із часом, окрім попередньо синтезованих речовин (гістаміну, триптази й інших протеаз), що вивільняються пошкодженими гранулами мастоцитів, мастоцити вивільняють de novo синтезовані медіатори, як-от ліпідні похідні (простагландини та лейкотрієни) й цитокіни/хемокіни, що активує шкірний судинний ендотелій і призводить до хемотаксису інших клітин (базофілів, лімфоцитів, еозинофілів і нейтрофілів) до шкіри. Ці клітини визначають установлення хронічних і періодичних запальних реакцій у різних ділянках шкіри, які є рецидивними [6]. Крім гістаміну, повідомлялося про підвищення рівнів LTE4, PGD2, ΤΝF, TGF-β, IL-1, IL-4, IL-5, IL-6, IL-25, IL-33, TSLP, а також PAF у пацієнтів із кропив’янкою [3].
Дослідження послідовно показують, що стрес і психологічна травма є значними факторами, які спричиняють розвиток і загострення ХК. Підвищений рівень стресу не тільки провокує загострення кропив’янки, але й зумовлює хронізацію та тяжкість хвороби. Нейрональні молекули, нейропептиди та нейромедіатори відіграють вирішальну роль у патофізіології кропив’янки. Ці молекули виробляються й вивільняються нейронами або середніми клітинами, спричиняють нейрогенне запалення та свербіж у разі кропив’янки [7].
Під час воєнних дій пацієнти дедалі частіше пов’язують розвиток кропив’янки зі стресом. Одним з основних медіаторів для розвитку кропив’янки та тлі стресу (поряд з гістаміном) вважають субстанцію P. Саме рівень цієї субстанції найбільшою мірою підвищується при виникненні кропив’янки внаслідок стресу. Накопичення субстанції Р також пов’язують з розвитком депресії та тривожних розладів, що певною мірою «ріднить» шкірні прояви та психічні розлади. Подекуди розвиток кропив’янки на тлі стресу пов’язують з підвищеним виробленням норадреналіну або ацетилхоліну (так звані адренергічна й холінергічна кропив’янки), які є основними медіаторами симпатичної та парасимпатичної систем відповідно й підвищене вироблення одного з яких спостерігається при тих чи інших психічних реакціях і розладах [7].
Характерними рисами кропив’янки на тлі стресу є дратівливість, емоційна напруженість, високий рівень тривожності, депресія, страх, загальне нездужання, втомлюваність, підвищення температури тіла, біль у суглобах, вегетативні реакції з боку серцево-судинної, травної, сечостатевої систем. Індукована стресом кропив’янка частіше виникає в молодих жінок і дітей, а специфічним маркером психогенної кропив’янки є субстанція P (нейропептид). Особливостями індукованої стресом кропив’янки є сильний свербіж, печіння й ураження великих ділянок шкіри з тенденцією до злиття пухирів. Це підсилює нервозність: елементи кропив’янки довго не зникають, супроводжуються появою нових висипань, що створює замкнене коло. Небезпекою при індукованій стресом кропив’янці є можливий розвиток анафілаксії [7].
Діагностика ХК передбачає збір алергологічного анамнезу та фізичне обстеження. Для алергологічного тестування застосовують тести in vivo: шкірні тести з алергенами (прик-тести, внутрішньошкірні, аплікаційні) та провокаційні тести з алергенами (назальний, кон’юнктивальний, бронхіальний, сублінгвальний з медикаментами, оральний з харчовими алергенами та медикаментами, парентеральний з медикаментами). Також застосовують тести in vitro. У всіх пацієнтів з ознаками або симптомами ХК рекомендовано проведення диференційної діагностики [4].
Діагностичні тести, рекомендовані при різних підтипах ХК, представлено в таблиці 1. При ГК рутинна діагностика не рекомендується [4].
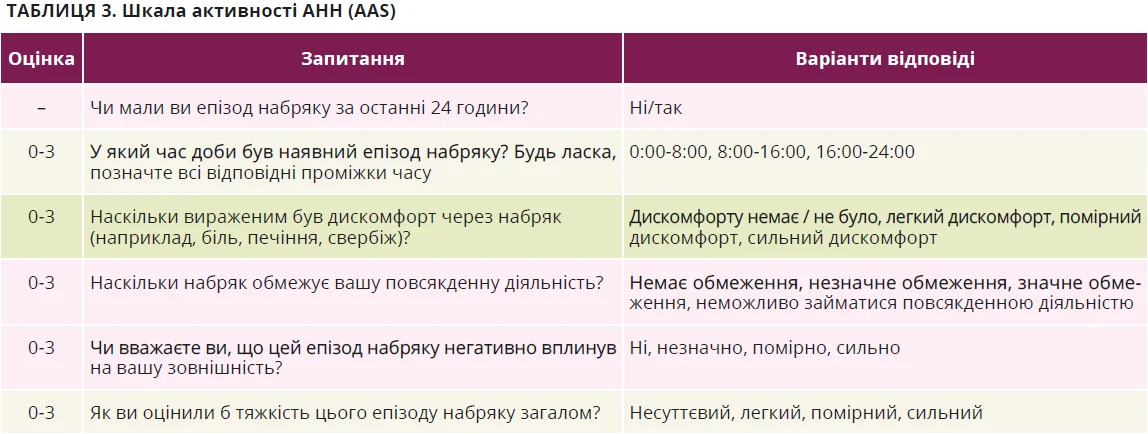
Основною метою ведення пацієнтів з ХК є лікування хвороби до повного зникнення симптомів. Терапія має бути якомога ефективнішою та безпечнішою, що дає змогу повного контролю хвороби й нормалізації якості життя. Фармакологічне лікування має тривати доти, доки в ньому не зникне потреба. Контроль над симптомами оцінюють за шкалами активності кропив’янки (Urticaria Activity Score – UAS) й АНН (Angioedema Activity Score – AAS) (табл. 2 та 3) [4].
Оптимальний терапевтичний підхід до лікування пацієнтів з ХК має охоплювати пошук і, якщо змога, елімінацію основних причин хвороби, уникнення впливу провокувальних факторів, індукцію толерантності, фармакологічне лікування для запобігання вивільненню медіаторів мастоцитів та/або дії останніх [4].
Механізм дії лікарських засобів, що застосовують для лікування кропив’янки, спрямований на медіатори мастоцитів (гістамін) й активатори (автоантитіла). Фармакодинаміка новітніх методів лікування, котрі наразі перебувають на етапі розроблення, спрямована на пригнічення мастоцитів за допомогою гальмівних рецепторів або зменшення кількості мастоцитів [4].
Згідно з рекомендаціями EAACI/GA²LEN/EuroGuiDerm/APAAACI антигістамінні препарати ІІ покоління (АГП ІІ) рекомендується застосовувати як засоби терапії першої лінії всіх типів кропив’янки [4].
Сучасні АГП IІ виявляють мінімальний седативний ефект або не мають його зовсім і не проявляють антихолінергічної активності. Більшість, але не всі АГП IІ було випробувано в пацієнтів із кропив’янкою. Отримані дані підтверджують доцільність застосування левоцетиризину, цетиризину, дезлоратадину, ебастину, фексофенадину, біластину, лоратадину та рупатадину [4].
Неседативні АГП ІІ потрібно застосовувати регулярно щодня, а не за потреби. Доцільність застосування такої схеми лікування підтверджується профілем безпеки цих лікарських засобів, а також їхнім механізмом дії, а саме зворотними агоністичними ефектами на H1-рецептор і стабілізацією неактивного стану останнього. Деякі пацієнти з ХІК можуть мати користь від короткочасного профілактичного застосування АГП перед імовірною зустріччю з відповідним тригерним чинником [4].
АГП ІІ демонструють протисвербіжні й антиексудативні властивості. На ранній стадії алергічної реакції вони пригнічують її активний розвиток, на пізнішій – обмежують вивільнення медіаторів запалення, знижують рівень міграції еозинофілів, нейтрофілів і базофілів, знімають спазм гладкої мускулатури, зменшують проникність капілярів, запобігають або пригнічують розвиток набряку тканин, усувають шкірні реакції. Завдяки своїй селективності препарати не пригнічують зворотного захоплення норадреналіну, не чинять антихолінергічної й антисеротонінергічної дії, не впливають на серцево-судинну систему, майже не мають седативного ефекту в терапевтичних дозах, не взаємодіють з алкоголем і психотропними препаратами [8].
У дослідженнях було продемонстровано переваги та доцільність щоденного застосування доз, які вчетверо перевищують стандартні для левоцетиризину, цетиризину, дезлоратадину, ебастину, фексофенадину, біластину й рупатадину. Результати досліджень демонструють, що деякі пацієнти з кропив’янкою, в яких спостерігається недостатня відповідь на лікування стандартними дозами АГП IІ, можуть отримати користь від підвищення дози, і це є кращим варіантом, аніж комбінувати різні АГП IІ. Відповідно, таким пацієнтам рекомендується збільшити дозу до 4 разів [4].
Під час ведення пацієнтів слід використовувати методику «крок уверх – крок униз» для корекції алгоритму лікування відповідно до перебігу хвороби за принципом «оцінювання, корекція, дія, повторне оцінювання». Методика передбачає початок лікування зі стандартної дози АГП ІІ. За потреби дозу останнього збільшують до 4 разів. За умови недостатнього контролю або нестерпних симптомів до лікування додають омалізумаб, а за його неефективності – циклоспорин (рис. 2) [4].
Пацієнтам з ХК на тлі стресу можуть бути показані психотропні препарати (нейролептики, антидепресанти) та психотерапія [7].
Висновки
Попри те що дані офіційної статистики щодо поширеності кропив’янки в Україні відсутні, збільшилося число пацієнтів, які пов’язують розвиток кропив’янки зі стресом. Основою лікування хворих на кропив’янку залишаються неседативні АГП ІІ. Левоцетиризин посідає чинне місце в лікуванні пацієнтів із кропив’янкою. Він має фармакодинамічно та фармакокінетично сприятливі характеристики, швидкий початок дії, високу спорідненість до H1-рецепторів, мінімальний метаболізм у печінці разом з мінімальними побічними ефектами та сприятливим профілем ефективності й безпеки.
Література
- Liu X., et al. Burden of and trends in urticaria globally, regionally, and nationally from 1990 to 2019: systematic analysis. JMIR Public Health Surveill. 2023; 9: e50114. doi: 10.2196/50114.
- Radonjic-Hoesli S., et al. Urticaria and angioedema: an update on classification and pathogenesis. Clin. Rev. Allergy Immunol. 2018; 54 (1): 88-101. doi: 10.1007/s12016-017-8628-1.
- Elieh-Ali-Komi D., et al. Chronic urticaria and the pathogenic role of mast cells. Allergol. Int. 2023; 72 (3): 359-368. doi: 10.1016/j.alit.2023.05.003.
- Zuberbier T., et al. The international EAACI/GA²LEN/EuroGuiDerm/APAAACI guideline for the definition, classification, diagnosis, and management of urticaria. Allergy. 2022; 77 (3): 734-766. doi: 10.1111/all.15090.
- Soong W., et al. Clinical profile, prevalence, and burden of chronic spontaneous urticaria in the United States. World Allergy Organ. J. 2025; 18 (8): 101081. doi: 10.1016/j.waojou.2025.101081.
- Criado P.R., et al. Chronic spontaneous urticaria: update on pathogenesis and therapeutic implications. An. Bras. Dermatol. 2025; 100 (5): 501198. doi: 10.1016/j.abd.2025.501198.
- Xiang Y.K., et al. Psychological stress and urticaria: pathophysiologic and therapeutic updates. Curr. Treat. Options Allergy. 2024; 11: 194-210. doi: 10.1007/s40521-024-00375-8.
- Lisiecka M.Z. Evolution, mechanism of action, and clinical applications of three generations of antihistamines. Innovaciencia. 2024; 12: 1. doi: 10.15649/2346075X.3651.
- Walsh G.M. The anti-inflammatory effects of levocetirizine – are they clinically relevant or just an interesting additional effect? Allergy Asthma Clin. Immunol. 2009; 5 (1): 14. doi: 10.1186/1710-1492-5-14.