Харчова алергія крізь призму кишкового мікробіому: міфи, запитання й ілюстровані відповіді
Підготувала канд. мед. наук Тетяна Можина
Нині відомо чимало фактів про харчову алергію (ХА) й алергени, які її спричиняють, але відносно нещодавно з’явилися нові відомості щодо ролі кишкового мікробіому (КМ) у виникненні цього атопічного захворювання. Спробуємо розвінчати поширені міфи, відповісти на розповсюджені запитання згідно з отриманими доказовими даними.
Міф. ХА зазвичай виникає 1-2 рази протягом життя та не являє собою значну проблему для сучасної медицини.
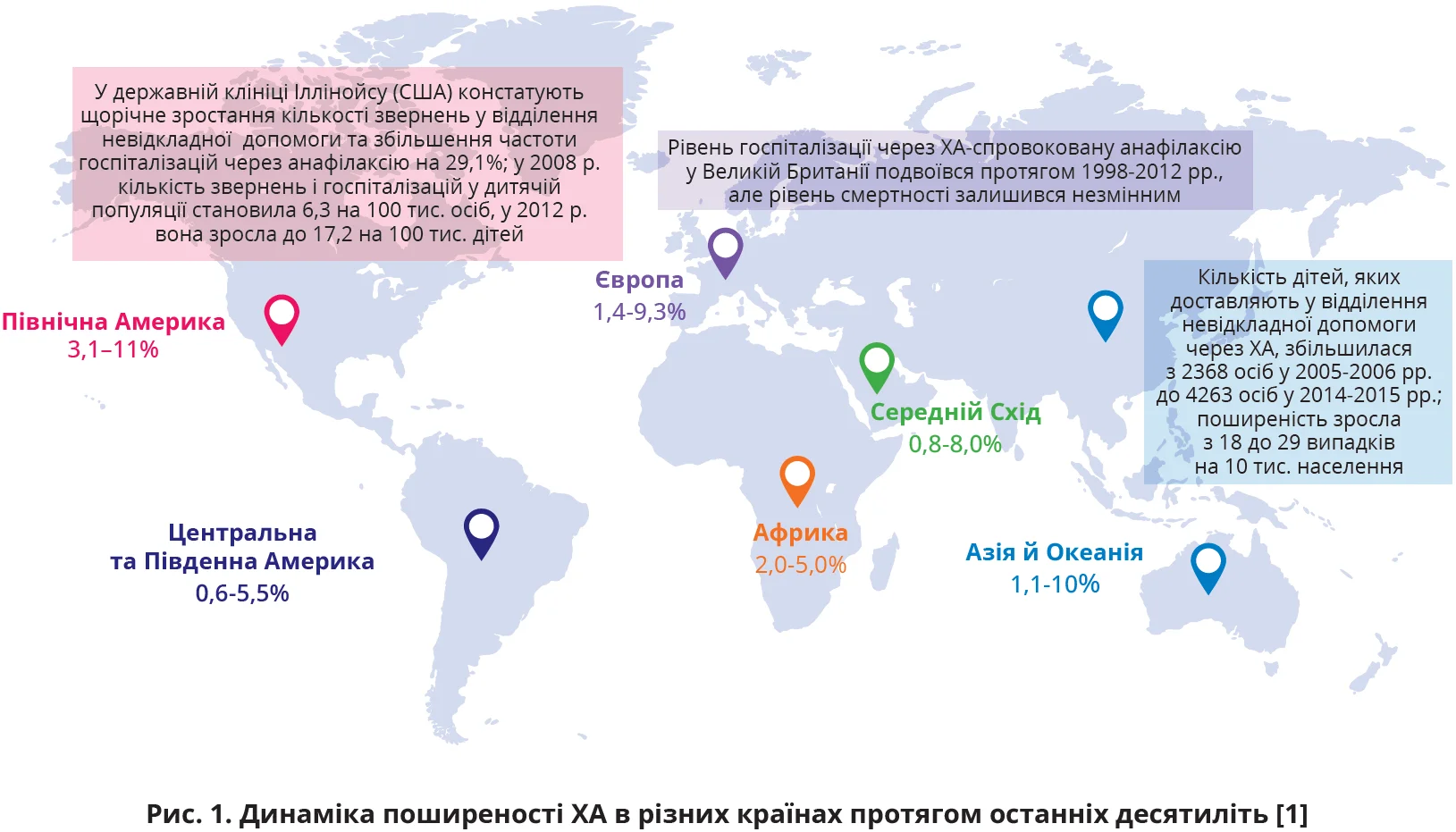
Відповідь. Такий атопічний розлад, як ХА, виникає внаслідок впливу певних харчових алергенів, призводить до розвитку життєво небезпечних алергічних реакцій і здатний багатократно повторюватися протягом життя. На сьогодні ХА являє собою поширену та серйозну проблему для системи охорони здоров’я (рис. 1), від якої страждає майже 10% дітей і 4% дорослих у всьому світі [1].
Міф. ХА клінічно проявляється ураженням шлунка, кишківника й інколи шкіри.
Відповідь. Перебіг ХА не обмежується ураженням травної системи у вигляді нудоти, блювання, абдомінального болю, діареї, вона здатна проявлятися ураженням шкіри (еритема, кропив’янка, ангіонабряк, свербіж, печіння, екзема), слизових оболонок очей (гіперемія та набряк кон’юнктиви, свербіж, сльозотеча, набряк), носа (ринорея, закладеність, чхання) та ротової порожнини (дискомфорт/набряк ротової порожнини, губ, язика, глотки), органів дихання (дискомфорт/свербіж у глотці, хрипота, дисфагія, кашель, хрипи, відчуття стиснення в грудях, задишка, ціаноз), нервової системи (головний біль, зниження бадьорості, неспокій, порушення свідомості, нетримання сечі) та циркуляторних порушень (зниження артеріального тиску, тахікардія, брадикардія, аритмія, похолодання кінцівок, блідість), які потенційно здатні призвести до анафілактичного шоку та смерті [2]. Тому дедалі більше уваги приділяють вивченню патогенезу та лікуванню ХА.
Міф. Переважна більшість випадків ХА являє собою IgE-опосередковані реакції, які маніфестують протягом 2 годин після вживання харчового антигену, невелика кількість ХА не пов’язана з надлишковим синтезом IgE, але жодна з цих типів реакцій не асоційована з кишковим дисбіозом.
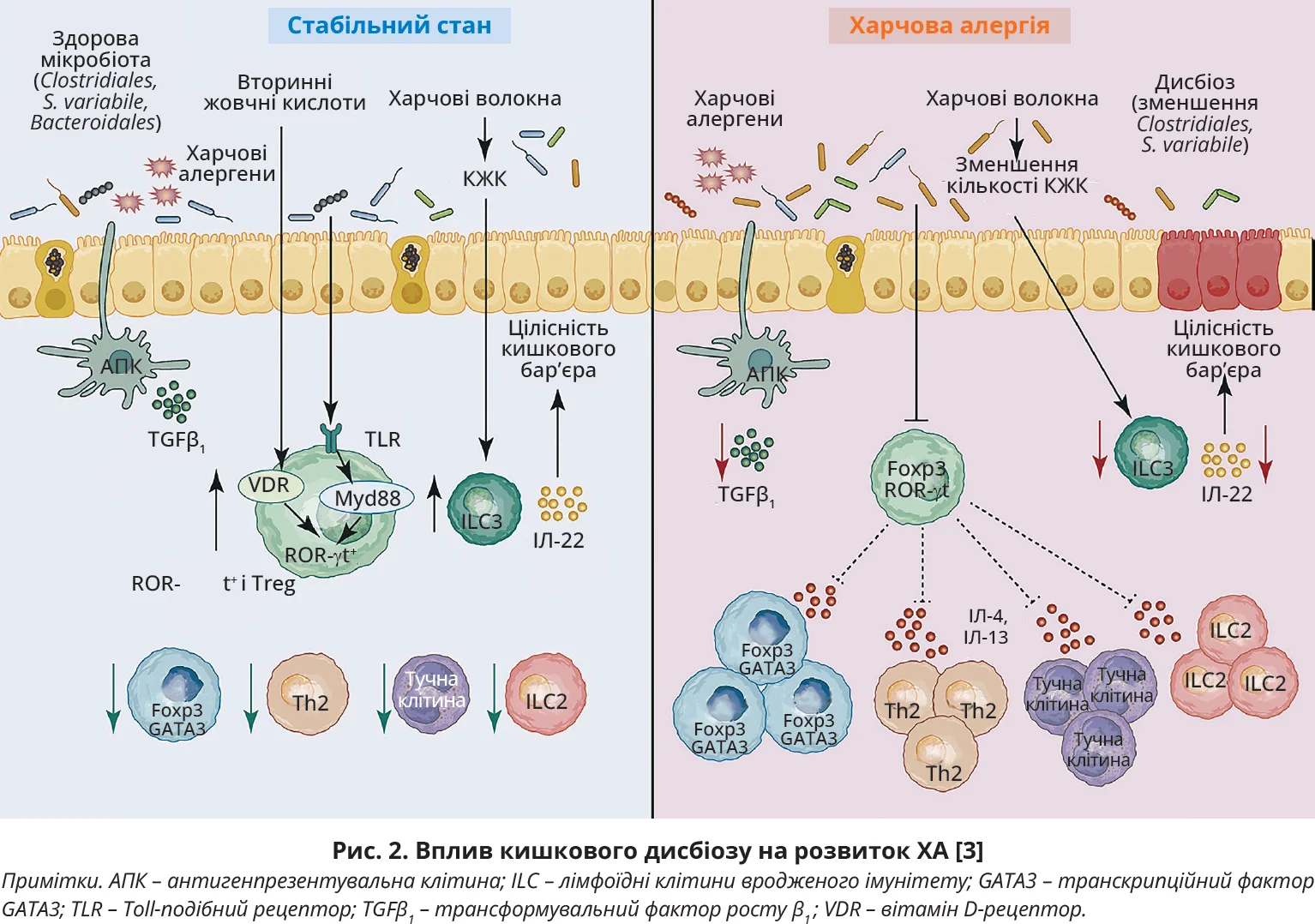
Відповідь. Дослідження, виконані протягом останніх десятиліть, дали змогу розкрити значну роль КМ у розвитку ХА (рис. 2). Встановлено, що у здоровому стані антигенпрезентувальні клітини реагують із харчовими антигенами та сприяють утворенню антигеноспецифічних iTreg-клітин. КМ, переважно представники родини Clostridiales і Bacteroidales, передають відповідні сигнали через Myd88-рецептори, що розташовані на iTreg, і стимулюють експресію транскрипційного фактора ROR-gt. Посиленню експресії ROR-gt також сприяють метаболіти жовчних кислот, які активують вітамін-D-рецептор, розташований на iTreg. Активовані ROR-gt+ Treg-клітини забезпечують толерантність до харчових антигенів, пригнічуючи антигеноспецифічні Th2-клітини, перешкоджаючи патогенній трансформації Treg, інгібуючи активацію тучних і лімфоїдних клітин (ILC)-2. З іншого боку, коротколанцюгові жирні кислоти (КЖК), які утворюються за допомогою КМ, активують ILC3-залежний синтез протизапального інтерлейкіну (ІЛ)-22, що посилює бар’єрну функцію кишківника.
Встановлено, що кишковий дисбіоз лежить в основі ХА, зумовлюючи порушення цілісності кишкового бар’єра та погіршення процесів диференціювання ROR-gt+ і Treg-клітин, посилення експансії Treg-клітин за Th2-фенотипом, які експресують транскрипційний фактор GATA3 й ІЛ-4, стимулюючи таким чином імунну відповідь кишківника за участю Th2-клітин, тучних клітин, ILC2 та спричиняючи прогресування ХА [3].
Запитання. Яким чином КМ здатна впливати на імунну систему?
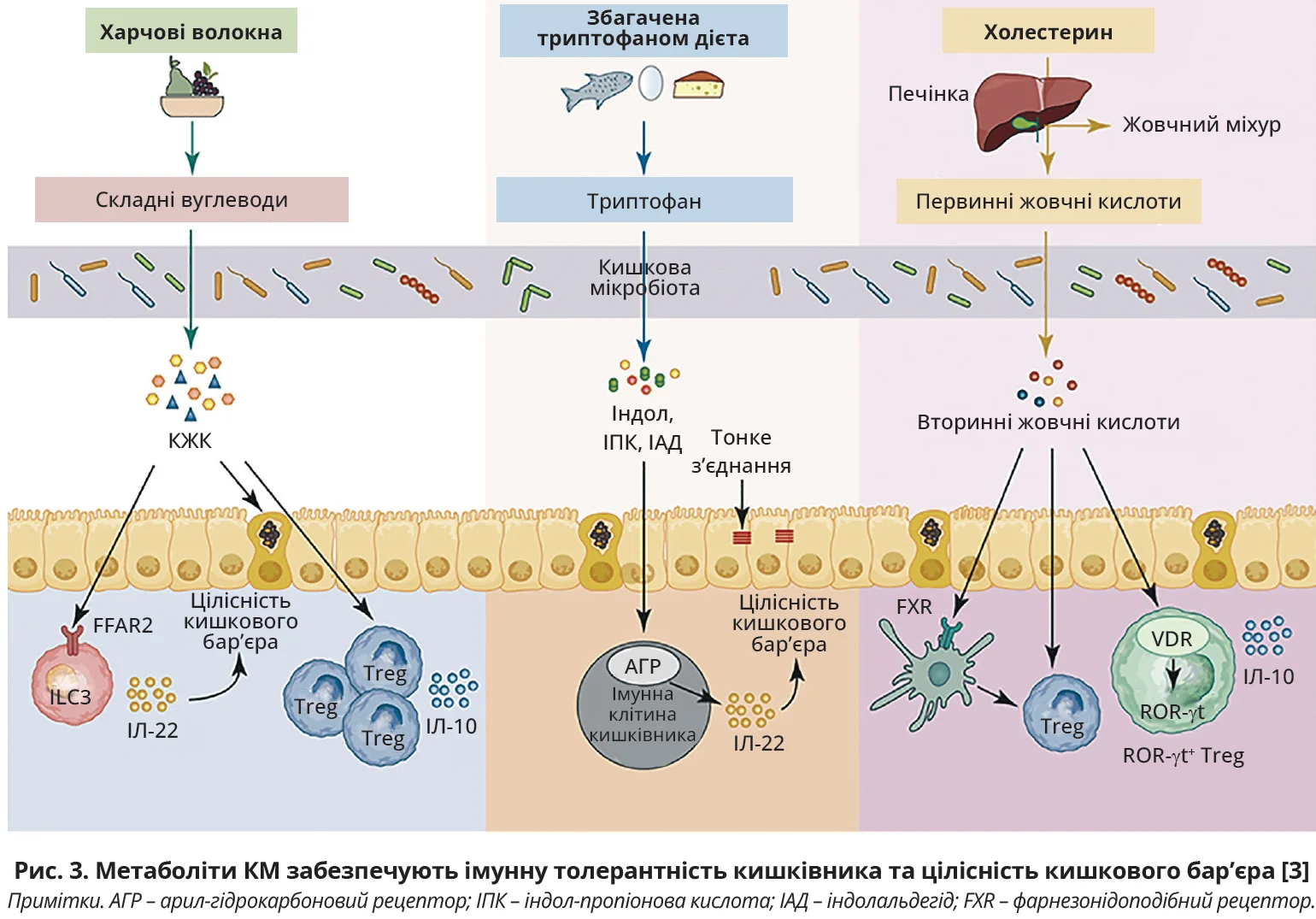
Відповідь. КМ сприяє перетравленню харчових волокон, білків і жирів, а точніше складних вуглеводів, триптофану та первинних жовчних кислот, котрі утворюються з вихідних продуктів. КМ забезпечує синтез КЖК, індолу, індол-пропіонової кислоти, вторинних жовчних кислот, метаболіти яких мають різноманітну біологічну активність. КЖК індукують диференціацію кишкових Treg-клітин і зумовлюють зростання протизапального ІЛ-10; КЖК сприяють імунній толерантності, активуючи вироблення протизапального ІЛ-22 ILC3-клітинами завдяки FFAR2-залежному механізму та забезпечують цілісність кишкового бар’єра, індукуючи секрецію слизу келихоподібними клітинами (рис. 3). Індол, індол-пропіонова кислота й індолальдегід, метаболіти триптофану, які утворюються за допомогою КМ, знижують проникність кишківника, забезпечують зростання щільності міжклітинних контактів, збільшуючи цілісність кишкового бар’єра. Похідні індолу активують арил-гідрокарбонові рецептори в імунних клітинах, сприяючи синтезу захисного ІЛ-22. Первинні жовчні кислоти, що синтезуються в печінці, далі модифікуються КМ до вторинних жовчних кислот, які індукують диференціацію ROR-gt Treg-клітин, котра забезпечує підвищення імунної толерантності кишківника [3].
Міф. Із метою корекції КМ у разі ХА досить нормалізувати дієту, інші засоби застосовувати недоцільно.
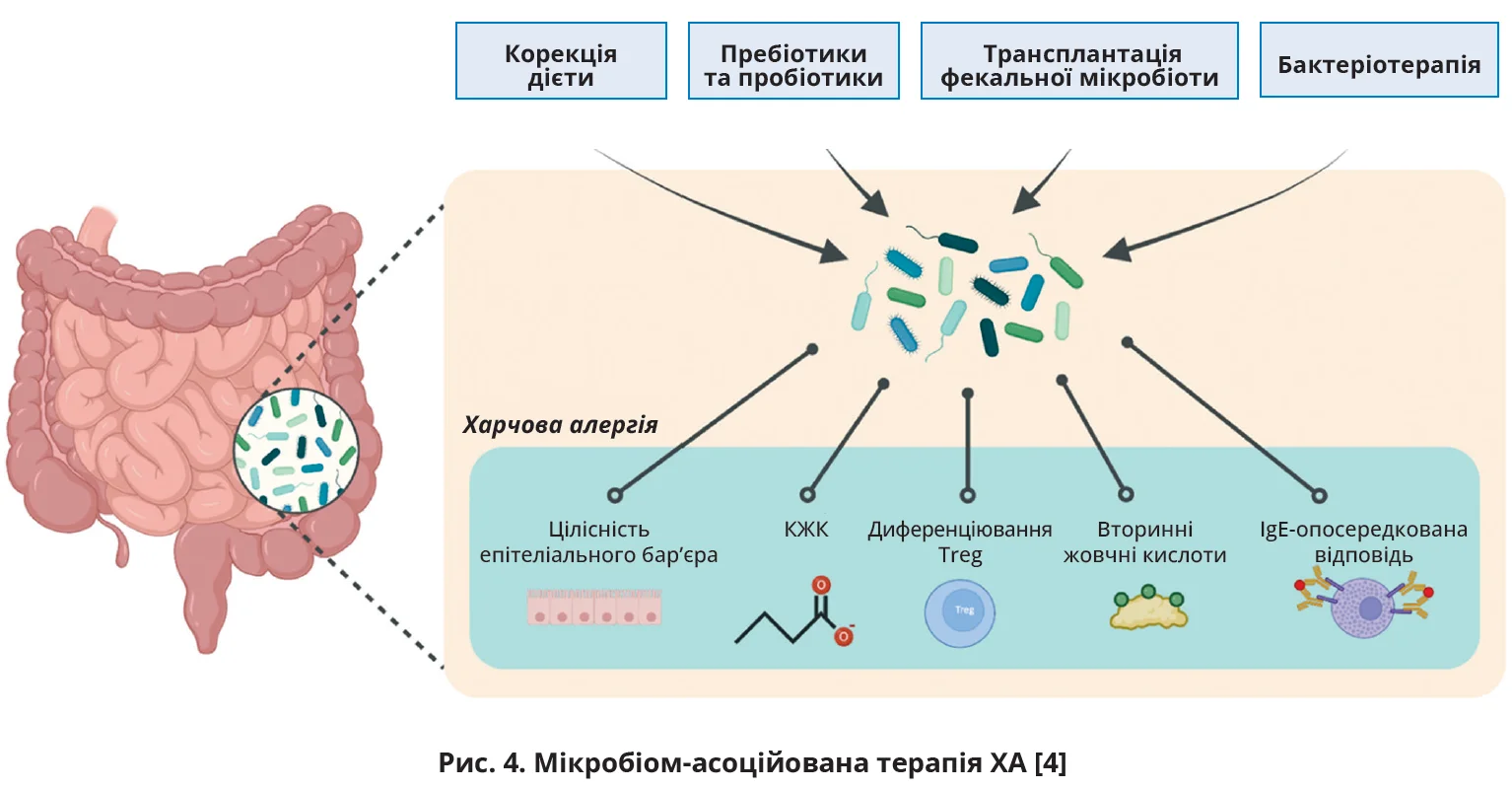
Відповідь. Сучасні уявлення щодо відновлення КМ у разі ХА передбачають не лише корекцію звичного харчового раціону, а й застосування пробіотиків і пребіотиків, проведення трансплантації фекальної мікробіоти та бактеріотерапії (рис. 4) [4]. Новітній мультитаргетний мікробіом-асоційований підхід до лікування ХА пропонує одночасно з пероральною/епікутанною/сублінгвальною імунотерапією використовувати пробіотичні засоби [5].
Міф. Ефективність пробіотиків у разі ХА ґрунтується лише на думках експертів, застосування пробіотиків за ХА не має доказової бази.
Відповідь. Результативність пробіотиків у разі ХА заснована не лише на думках експертів, а й на даних клінічних досліджень і декількох метааналізів. Нещодавно опублікований метааналіз підтверджує, що пробіотики зменшують клінічні явища харчової гіперчутливості завдяки імуномодуляції, зниженню рівня прозапальних цитокінів, сироваткового рівня IgE [6]. В іншому метааналізі 17 досліджень доведено, що пренатальне та постнатальне застосування пробіотиків дає змогу знизити ймовірність розвитку атопії (відносний ризик, ВР 0,78; 95% довірчий інтервал, ДІ 0,66-0,92) та харчової гіперчутливості (ВР 0,77; 95% ДІ 0,61-0,98) [7]. Висловлюються думки, що пробіотики слід застосовувати в схемах імунотерапії ХА з метою підвищення її ефективності [8]. Представляючи нові міжнародні рекомендації щодо лікування ХА, провідні експерти Японського товариства педіатричної алергології та клінічної імунології [2] та представники Європейської мережі GA2LEN [9] поки що не змогли сформувати положення, які підтримували би застосування пробіотиків/пребіотиків або, навпаки, забороняли їх використання при ХА, провідні спеціалісти наполягають на доцільності проведення великих рандомізованих досліджень [2, 9].
Запитання. Чи визначено пробіотичні штами або пребіотики, які здатні мінімізувати явища ХА та покращувати стан хворих на ХА?
Відповідь. Експериментальні дослідження підтверджують здатність Lactobacillus rhamnosus знижувати рівень сироваткового IgЕ, прозапального ІЛ-4 та підвищувати вміст протективного TGFβ1 [10]. Клінічні дослідження довели, що ад’ютанте застосування L. rhamnosus сприяє нівелюванню ознак атопічного дерматиту, котрий виник на тлі ХА [11]. L. rhamnosus, якій притаманна низька антигенність і мінімальна потенційна алергенність [12], рекомендована для щоденного використання як гіпоалергенний засіб для розвитку імунної толерантності, зменшення вірогідного алергенного потенціалу білка коров’ячого молока (БКМ) [12]. L. rhamnosus вважають пробіотиком першого вибору для лікування ХА на БКМ, який здатний зменшити ймовірність розвитку алергічного маршу в майбутньому [13]. Ефективність L. rhamnosus у разі ХА доведена в декількох метааналізах: цей штам сприяє підвищенню імунологічної толерантності в дітей з алергією на БКМ (ВР 0,41; 95% ДІ 0,28-0,62) [14]; в іншій роботі, заснованій на аналізі 10 досліджень, отримано докази помірного рівня щодо зростання толерантності до БКМ порівняно з контролем (ВР 2,22; 95% ДІ 1,86-2,66) [15].
Доведено імуномодулювальні властивості L. acidophilus: ця лактобактерія здатна інгібувати імунну відповідь у кишківнику шляхом блокування прозапального шляху TLR4/NF-kB – основного шляху виникнення ХА на БКМ [16], а також регулювати КМ за ХА [17]. Застосування L. acidophilus визнано доцільним із метою інгібування алергічної відповіді [18]. L. rhamnosus і L. acidophilus є поширеними компонентами сумішей для годування немовлят, що дає змогу запобігти виникненню дисбіозу, ХА на БКМ.
Ідеальний пребіотик для корекції ХА поки що невизначений; допускається, що застосування будь-якого пребіотика сприятиме покращенню стану хворих на ХА [19].
Запитання. Який пробіотик/пребіотик буде доцільно призначати дітям і дорослим у разі ХА?
Відповідь. Нині панує думка, що ефективній профілактиці та лікуванню ХА сприятиме не просто застосування специфічного пробіотичного штаму, а одночасне використання комбінації пробіотиків із пребіотиком, тобто синбіотика; вважається, що таке поєднання забезпечить значніший протективний ефект [19]. Доведено, що застосування синбіотиків сприяє помітнішому збагаченню складу КМ і забезпечує тривалий сприятливий ефект у дітей із ХА на БКМ порівняно з монотерапією пробіотиком/пребіотиком [20].
Згідно з оновленою настановою Міжнародної наукової асоціації пробіотиків і пребіотиків (ISAPP, 2020) синбіотики являють собою «суміш, що складається з живих мікроорганізмів і субстрату (-ів),
які селективно утилізуються мікроорганізмами-хазяїнами та надають користь для здоров’я макроорганізму» [21]. Експерти вважають, що взаємодоповнювальні (комбінація пребіотика та пробіотика, де обидва компоненти працюють незалежно) й синергічні (субстрат селективно утилізується спільно введеними мікроорганізмами) синбіотики регулюють співвідношення Firmicutes до Bacteroidetes, пригнічують шкідливі бактерії шляхом прямого антагонізму, прискорюють відновлення КМ [21]. Використання синбіотика при ХА на БКМ сприяє зменшенню виразності абдомінального болю, здуття, риніту, свербежу очей, атопічного дерматиту, а також покращує якість життя, знижує кількість госпіталізацій і частоту використання лікарських засобів (у всіх випадках р<0,05) [22].
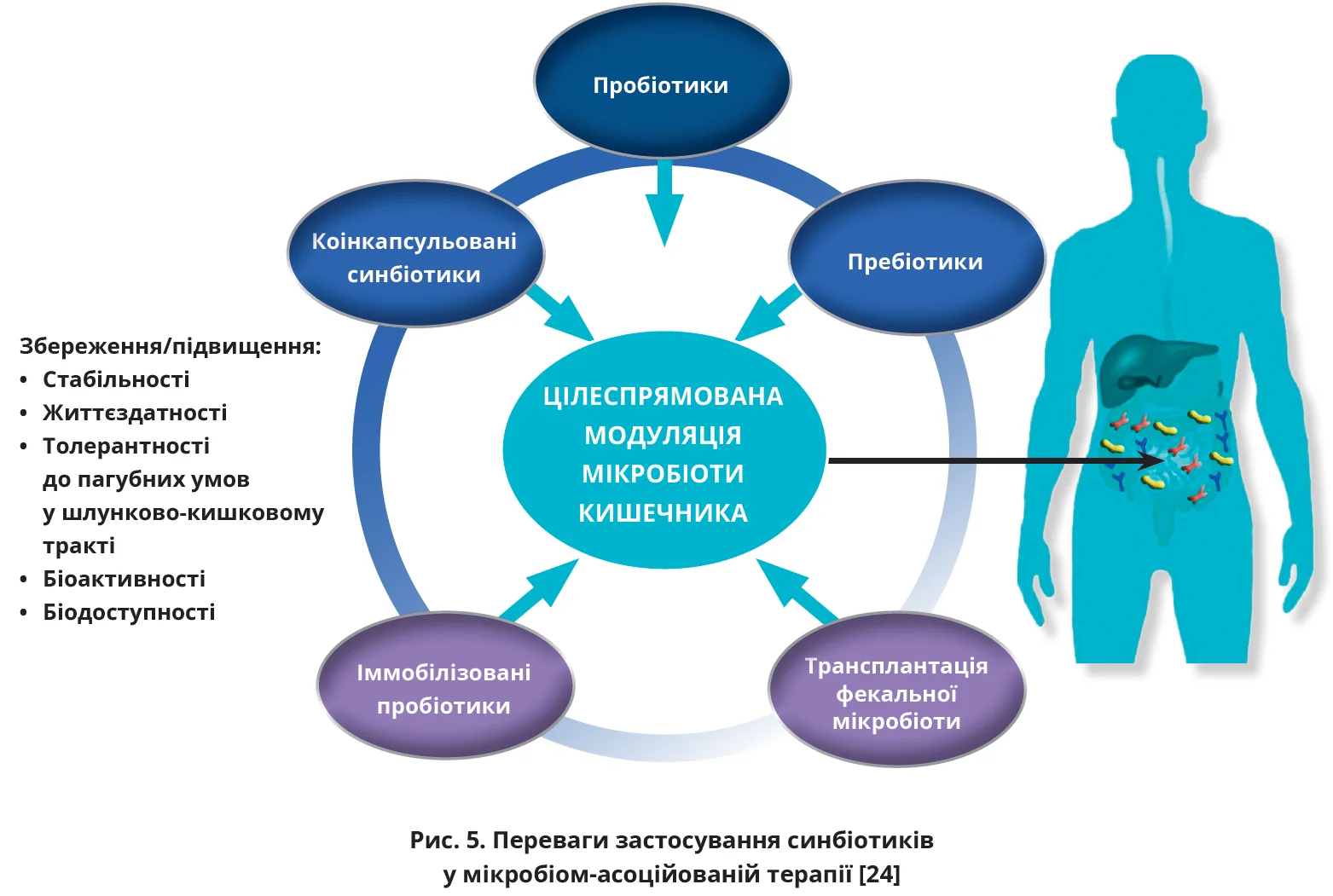
Нині на вітчизняному фармацевтичному ринку представлений комплементарний синбіотик Бажана (фірма-виробник – Sopharma), пробіотична складова якого репрезентована L. rhamnosus, L. acidophilus, Saccharomyces boulardii та взаємодоповнюється субстратом, пребіотиком інуліном, при цьому обидва компоненти синбіотика розташовані всередині капсули [23]. Вважається, що капсулювання, особливо мікрокапсулювання (розташування пробіотиків усередині мікрокапсул), захищає пробіотики від несприятливих умов під час транзиту шлунково-кишковим трактом, сприяє їх контрольованому вивільненню переважно в товстій кишці [24]. Мікрокапсулювання також дає змогу підвищити біодоступність, покращити органолептичні властивості, замаскувати неприємний присмак і подовжити термін придатності синбіотика (рис. 5). Капсульна форма випуску Бажани допомагає підтримувати стабільність і життєздатність усіх її компонентів [23].
Запитання. Чи доцільне застосування синбіотика Бажана при ХА?
Відповідь. Комбінований склад взаємодоповнювального синбіотика Бажана робить патогенетично обґрунтованим і раціональним його використання при ХА. Кожна капсула Бажани містить два штами лактобактерій – L. rhamnosus (1×109 КОЕ) та L. acidophilus (2,5×109 КОЕ), які продемонстрували свою ефективність у корекції ХА [10-18], а також пребіотик інулін (25 мг), що підтримує та підсилює протизапальну дію пробіотиків, захищає організм від оксидативного стресу [24]. Додатковою перевагою Бажани можна вважати наявність ліофілізованих дріжджів S. boulardii (2,5×109 КОЕ), які надають синбіотику прямі протимікробні властивості та здатність виводити патогенні мікроорганізми, створюючи умови для розмноження власної сапрофітної мікрофлори. L. rhamnosus і S. boulardii є найвивченішими пробіотичними штамами, які визнані безпечними та рекомендовані для використання в педіатричній і дорослій популяціях для зменшення явищ ХА [25, 26].
Низька антигенність і мінімальна потенційна алергенність L. rhamnosus [12], доведена ефективність L. acidophilus [17, 18] і L. rhamnosus у профілактиці/лікуванні ХА [14, 15], здатність інуліну посилювати дію лактобактерій [24], добрий профіль безпеки L. rhamnosus, L. acidophilus, S. boulardii, інуліну [25, 26] та їх багаторічне використання в різних вікових групах, а також у немовлят (як компонентів сумішей для годування), в тому числі з ХА на БКМ, робить доцільним застосування Бажани в педіатричній і дорослій популяціях як профілактичного засобу або препарату ад’ювантної терапії ХА. Синбіотик Бажана можна рекомендувати дітям від 3 років і дорослим, призначаючи відповідну форму випуску: порошок-саше або капсули [23]. Згідно з інструкцією дітям призначають 1 капсулу/саше Бажани 1 р/добу, дорослим – 2 капсули 1 р/добу натще [23].
Ключові положення
- КМ перебуває в постійній фізіологічній взаємодії з імунною системою кишківника та являє собою сполучну ланку між імунною системою й розвитком ХА.
- КМ сприяє виникненню та підтриманню імунологічної толерантності, забезпечує цілісність кишкового бар’єра, запобігає розвитку ХА й мінімізує її прояви.
- Мікробіом-асоційований підхід до лікування ХА заснований на корекції дієти, призначенні пробіотиків/пребіотиків, проведенні трансплантації фекальної мікробіоти, бактеріотерапії.
- Сучасні міжнародні рекомендації не підтримують і не заперечують призначення пробіотиків/пребіотиків у разі ХА.
- Серед різноманітних пробіотичних штамів найефективнішими в профілактиці ХА визнані L. rhamnosus і L. acidophilus.
- Протизапальні властивості пробіотиків (L. rhamnosus, L. acidophilus) і пребіотика (інулін), які є основними складовими синбіотика Бажана, роблять можливим його призначення при ХА як профілактичного засобу або препарату ад’ювантної терапії.
Література
- Yang H., Qu Y., Gao Y., et al. Research progress on the correlation between the intestinal microbiota and food allergy. Foods. 2022; 11: 2913. doi: 10.3390/foods11182913.
- Ebisawa M., Ito K., Fujisawa T.; Committee for Japanese Pediatric Guideline for Food Allergy, the Japanese Society of Pediatric Allergy and Clinical Immunology; Japanese Society of Allergology. Japanese guidelines for food allergy 2020. Allergol. Int. 2020; 69 (3): 370-386. doi: 10.1016/j.alit.2020.03.004.
- Stephen-Victor E., Crestani E., Chatila T.A. Dietary and microbial determinants in food allergy. Immunity. 2020; 53 (2): 277-289. doi: 10.1016/j.immuni.2020.07.025.
- Chernikova D.A., Zhao M.Y., Jacobs J.P. Microbiome therapeutics for food allergy. Nutrients. 2022; 14 (23): 5155. doi: 10.3390/nu14235155.
- Sindher S.B., Long A., Chin A.R., et al. Food allergy, mechanisms, diagnosis and treatment: innovation through a multi-targeted approach. Allergy. 2022; 77 (10): 2937-2948. doi: 10.1111/all.15418.
- Santos S.C.D., Konstantyner T., Cocco R.R. Effects of probiotics in the treatment of food hypersensitivity in children: a systematic review. Allergol. Immunopathol. (Madr.). 2020; 48 (1): 95-104. doi: 10.1016/j.aller.2019.04.009.
- Zhang G.Q., Hu H.J., Liu C.Y., et al. Probiotics for prevention of atopy and food hypersensitivity in early childhood: a PRISMA-compliant systematic review and meta-analysis of randomized controlled trials. Medicine (Baltimore). 2016; 95 (8): e2562. doi: 10.1097/MD.0000000000002562.
- Furci F., Caminati M., Crisafulli E., et al. The intriguing possibility of using probiotics in allergen-specific immunotherapy. World Allergy Organ. J. 2023; 16 (2): 100751. doi: 10.1016/j.waojou.2023.
- Muraro A., de Silva D., Halken S., et al. Managing food allergy: GA2LEN guideline 2022. World Allergy Organ. J. 2022; 15 (9): 100687. doi: 10.1016/j.waojou.2022.100687.
- Dehghani S., Edalatian Dovom M.R., Yavarmanesh M., Sankian M. Effect of Lacticaseibacillus rhamnosus and Lactiplantibacillus plantarum isolated from food and human origin on reduction of IgE-dependent hypersensitivity in Balb/c mice. Immunobiology. 2022; 227 (6): 152292. doi: 10.1016/j.imbio.2022.152292.
- Carucci L., Nocerino R., Paparo L., et al. Therapeutic effects elicited by the probiotic Lacticaseibacillus rhamnosus GG in children with atopic dermatitis. The results of the ProPAD trial. Pediatr. Allergy Immunol. 2022; 33 (8): e13836. doi: 10.1111/pai.13836.
- Huang M., Li X., Wu Y., et al. Potential allergenicity and hydrolysis assessment of bovine casein and β-casein by treatment with lactic acid bacteria. J. Food Biochem. 2022; 46 (12): e14424. doi: 10.1111/jfbc.14424.
- Guest J.F., Fuller G.W. Effectiveness of using an extensively hydrolyzed casein formula supplemented with Lactobacillus rhamnosus GG compared with an extensively hydrolysed whey formula in managing cow’s milk protein allergic infants. J. Comp. Eff. Res. 2019; 8 (15): 1317-1326. doi: 10.2217/cer-2019-0088.
- Tan-Lim C., Esteban-Ipac N. Probiotics as treatment for food allergies among pediatric patients: a meta-analysis. World Allergy Organ. J. 2018; 11 (1): 25. doi: 10.1186/s40413-018-0204-5.
- Tan W., Zhou Z., Li W., et al. Lactobacillus rhamnosus GG for cow’s milk allergy in children: a systematic review and meta-analysis. Front. Pediatr. 2021; 9: 727127. doi: 10.3389/fped.2021.727127.
- Li A., Yang J., Zhang C., et al. Lactobacillus acidophilus KLDS 1.0738 inhibits TLR4/NF-kB inflammatory pathway in β-lactoglobulin-induced macrophages
via modulating miR-146a. J. Food Biochem. 2021; 45 (10): e13662. doi: 10.1111/jfbc.13662. - Yang C., Zhu J., Bai J., et al. Effects of Lactobacillus on the differentiation of intestinal mucosa immune cells and the composition of gut microbiota in soybean-sensitized mice. Foods. 2023; 12 (3): 627. doi: 10.3390/foods12030627.
- Ni W.W., Zhang Q.M., Zhang X., et al. Modulation effect of Lactobacillus acidophilus KLDS 1.0738 on gut microbiota and TLR4 expression in β-lactoglobulin-induced allergic mice model. Allergol. Immunopathol. (Madr.). 2020; 48 (2): 149-157. doi: 10.1016/j.aller.2019.06.002.
- Sestito S., D’Auria E., Baldassarre M., et al. The role of prebiotics and probiotics in prevention of allergic diseases in infants. Front. Pediatr. 2020; 8: 583946. doi: 10.3389/fped.2020.583946.
- Phavichitr N., Wang S., Chomto S., et al. Impact of synbiotics on gut microbiota during early life: a randomized, double-blind study. Sci. Rep. 2021 Feb 11; 11 (1): 3534. doi: 10.1038/s41598-021-83009-2.
- Swanson K.S., Gibson G.R., Hutkins R., et al. The International Scientific Association for Probiotics and Prebiotics (ISAPP) consensus statement on the definition and scope of synbiotics. Nat. Rev. Gastroenterol. Hepatol. 2020; 17 (11): 687-701. doi: 10.1038/s41575-020-0344-2.
- Hubbard G.P., Atwal K., Graham L., et al. Synbiotic containing extensively hydrolyzed formula improves gastrointestinal and atopic symptom severity, growth, caregiver quality of life, and hospital-related healthcare use in infants with cow’s milk allergy. Immun. Inflamm. Dis. 2022; 10 (6): e636. doi: 10.1002/iid3.636.
- Бажана. Інструкція [Електронний ресурс]. – Режим доступу: https://compendium.com.ua/dec/526752.
- Kvakova M., Bertkova I., Stofilova J., Savidge T.C. Co-encapsulated synbiotics and immobilized probiotics in human health and gut microbiota modulation. Foods. 2021 Jun 4; 10 (6): 1297. doi: 10.3390/foods10061297.
- Vandenplas Y., Huys G., Daube G. Probiotics: an update. J. Pediatr. (Rio J.). 2015; 91 (1): 6-21. doi: 10.1016/j.jped.2014.08.005.
- Boggio Marzet C., Burgos F., Del Compare M., et al. Approach to probiotics in pediatrics: the role of Lactobacillus rhamnosus GG. Arch. Argent. Pediatr. 2022; 120 (1): e1-e7. doi: 10.5546/aap.2022.eng.e1.