Фактор активації тромбоцитів як медіатор запалення: від досліджень до рутинної клінічної практики
Підготувала д-р мед. наук Лариса Стрільчук
Минуло понад 50 років, відтоді як термін «фактор активації тромбоцитів» (ФАТ) був уперше запроваджений Бенвеністом, Генсоном і Кокрейном (1972) для опису активації й агрегації тромбоцитів під впливом цієї активної речовини. Хімічну структуру ФАТ було встановлено лише в 1979 р. Ця сполука являє собою гліцериловий ефірний ліпід (1-O-алкіл-2-ацетил-sn-гліцеро-3-фосфохолін). У наш час ФАТ визнано ліпідним медіатором, який має широкий спектр дій у майже всіх системах організму людини та задіяний у різноманітних фізіологічних і патологічних процесах.
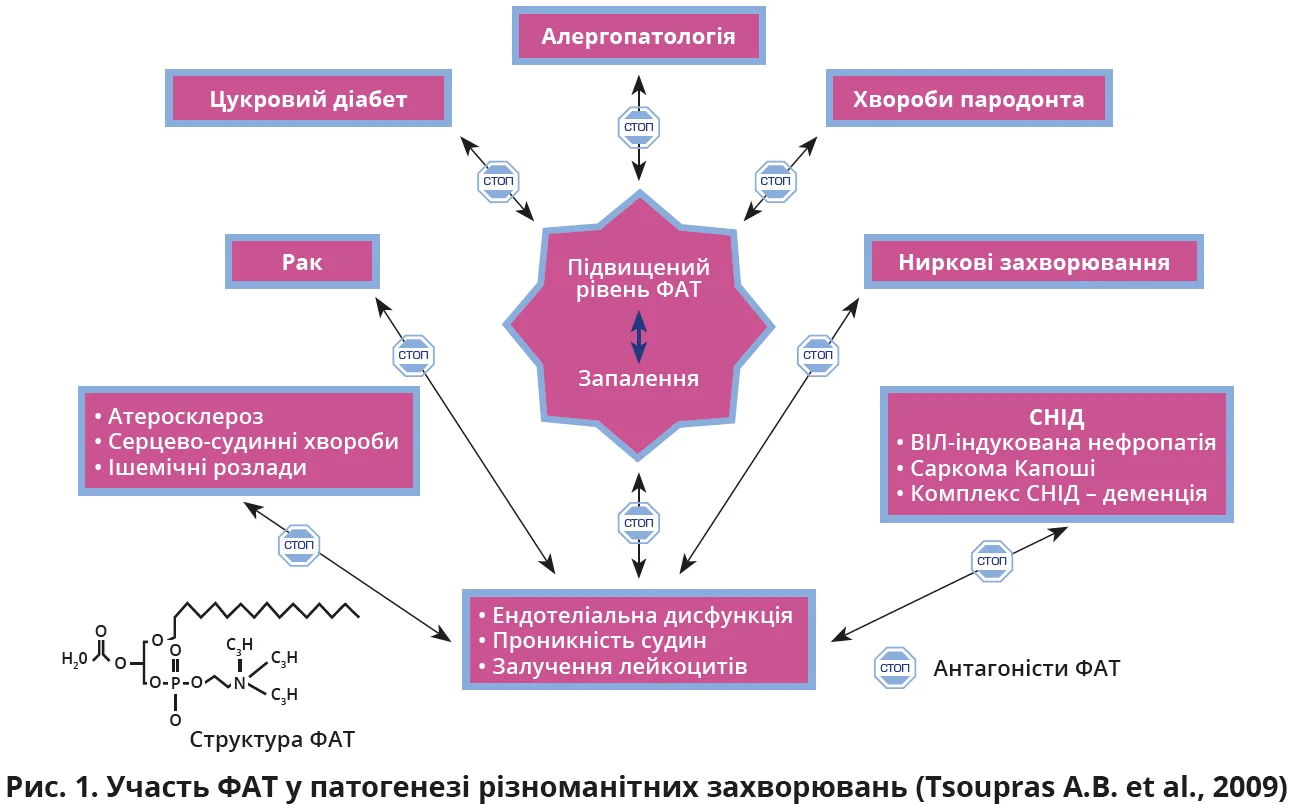
Зокрема, ФАТ є потужним медіатором запалення, що бере участь у розвитку низки захворювань: алергічних, інфекційних, онкологічних, ниркових, цереброваскулярних, бронхіальної астми тощо. Відповідно, блокатори ФАТ можуть успішно застосовуватися при цих хворобах (рис. 1).
Наприклад, у разі COVID-19 ФАТ спричиняє підвищення проникності судин і розвиток набряку легень. Водночас, як свідчить назва цього медіатора, він зумовлює агрегацію тромбоцитів, як зворотну, так і незворотну, через що може провокувати коронарні та тромботичні події, які супроводжують тяжкий перебіг коронавірусної інфекції. Ще однією характеристикою тяжкої COVID-19 є гемодинамічна нестабільність і розвиток гіпотензивного шоку, подібного до анафілактичного. Подальше вивчення цієї подібності дало змогу висловити гіпотезу, що спільними ланками патогенезу цих видів шоку є неконтрольована вазодилатація та підвищена проникність капілярів, зумовлена дегрануляцією опасистих клітин і впливом прозапальних цитокінів. Як відомо, саме ці процеси опосередковані ФАТ, тому блокаду цього медіатора можна вважати доцільною терапевтичною стратегією в лікуванні COVID-19 (Klein M. et al., 2021).
Окрім участі в гострому запаленні, ФАТ залучений до механізмів клітинної сигналізації, які забезпечують низку фізіологічних процесів, включно з апоптозом, загоєнням ран, репродукцією й ангіогенезом (Antonopoulou S., 2024). Різнопланові ефекти ФАТ зумовлюють його роль у патогенезі сепсису, злоякісних новоутворень, ускладнень цукрового діабету, хвороб нирок, алергопатологій тощо (Ashraf M.A., Nookala V., 2023). У пацієнтів зі злоякісними пухлинами ФАТ здатен взаємодіяти з хіміотерапевтичними препаратами. Зокрема, цей медіатор посилено екскретується в разі призначення цитотоксичних засобів, що може зумовлювати доцільність призначення інгібіторів ФАТ як ад’ювантних засобів у лікуванні новоутворень (Tsoupras A. et al., 2024).
ФАТ реалізує свою дію шляхом зв’язування з відповідним рецептором, розташованим на плазматичній та ядерній мембрані й експресованим у багатьох типах клітин і тканин. Рецептор ФАТ також взаємодіє з окисненими фосфоліпідами, подібними до ФАТ, і розпізнає компоненти бактерійної стінки, як-от ліпотейхоєва кислота та ліпополісахариди. На активність і метаболізм ФАТ впливають різні чинники, зокрема дієта, спосіб життя та вплив довкілля. У зв’язку з важливою роллю ФАТ у розвитку хронічних захворювань, він є перспективною терапевтичною мішенню, у зв’язку з чим ведуться активні дослідження природних і синтетичних антагоністів ФАТ (Antonopoulou S., 2024).
Однією з речовин, що досліджуються в контексті впливу на ФАТ, зокрема в онкології, є рупатадин. Наприклад, у разі раку яєчників відзначається надмірна експресія рецепторів ФАТ, яку пов’язують з розвитком, метастазуванням і ангіогенезом пухлини, а також із захистом пухлинних клітин від апоптозу. E. Deuster і співавт. (2021) дослідили зразки тканин раку яєчників, отримані від 156 пацієнток, оцінивши в них експресію рецепторів ФАТ. Було з’ясовано, що цей показник виступає незалежним прогностичним чинником: середня виживаність жінок з підвищеною експресією рецепторів ФАТ становила 83,48 місяця, а жінок з низькою експресією цих рецепторів – 155,03 місяця. Крім того, пацієнтки з підвищеною експресією рецепторів ФАТ мали достовірно вищу ймовірність рецидивів раку. Автори також виявили, що обробка пухлинних клітинних ліній раку яєчників in vitro асоціювалася зі зниженням проліферації, міграції та виживаності клітин. Отримані дані стосувалися світлоклітинного, серозного, з мутацією BRCA1 та ендометріоїдного раку яєчників. На думку дослідників, цей антипроліферативний вплив рупатадину зумовлений не лише антагонізмом до рецепторів ФАТ, а й антагонізмом до Н1-гістамінових рецепторів, підвищена експресія котрих відзначається при раку ендометрія. Численні клінічні випробування рупатадину як антиалергічного засобу довели його довготермінову безпеку, на відміну від інших експериментальних блокаторів ФАТ, дослідження котрих поки що не проводилися. У зв’язку з цим доцільне подальше вивчення рупатадину як засобу для протидії пухлинному росту за раку яєчників, а також інших видів раку, оскільки, наприклад, у разі меланоми для антагоністів рецепторів ФАТ було продемонстровано здатність потенціювати ефект хіміотерапії. Описано також синергію антагоністів ФАТ і цисплатину.
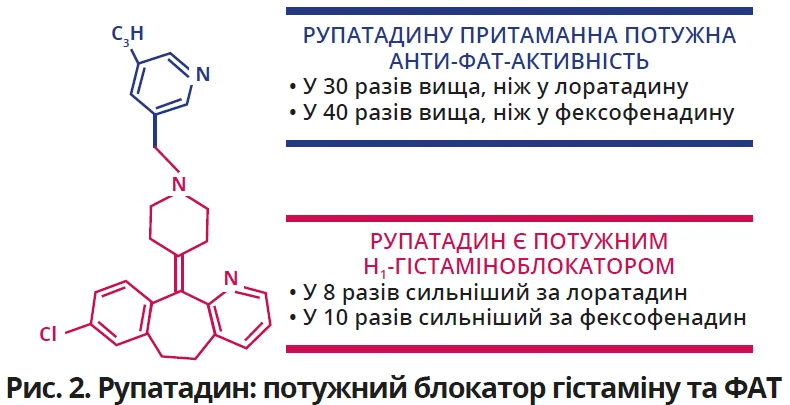
Важливо, що потужність і антигістамінної, й анти-ФАТ-активності рупатадину перевищує показники інших антигістамінних препаратів (рис. 2; Church M.K. et al., 2010).
Рупатадин демонструє активність не лише при новоутвореннях, а й у разі інших патологічних станів, наприклад діабетичної нефропатії. Експериментальне дослідження H.M. Hafez і співавт. (2020) продемонструвало, що при стрептозоцин-індукованому цукровому діабеті застосування рупатадину знижувало всі патологічно підвищені сироваткові маркери дисглікемії, а також покращувало гістопатологічну картину. Крім того, рупатадин нормалізував окисно-відновний баланс і знижував уміст фактора некрозу пухлин-α та фактора росту пухлин-β1. Експериментальний діабет зумовлював передчасне старіння клітин, натомість застосування рупатадину протидіяло цьому несприятливому ефекту. Отже, рупатадин чинить значну протизапальну, антиоксидантну та ренозахисну дію.
У разі ожиріння – пандемії нашого часу – ФАТ відіграє подвійну роль. Фізіологічні рівні ФАТ у жировій тканині та її мікрооточенні чинять сприятливий автокринний ефект, забезпечуючи підтримання належного стану жирової тканини. Водночас в умовах надмірного окисного стресу та запалення клітини крові й ендотеліоцити виробляють підвищену кількість ФАТ, який за рахунок пара- та юкстакринних механізмів призводить до подальшого посилення запалення й тромбозу (Antonopoulou S., 2025).
Роль ФАТ добре вивчена при алергічних захворюваннях. Цей медіатор виступає найпотужнішим індуктором судинної проникності, внаслідок чого відіграє головну роль у розвитку ринореї та закладеності носа. У зразках плазми крові та промивних вод носа пацієнтів з алергічним ринітом і бронхіальною астмою було виявлено підвищений уміст ФАТ. Провокаційні проби з ФАТ відтворюють симптоми риніту й астми, погіршують прохідність носових ходів, спричиняють еозинофільну та нейтрофільну інфільтрацію верхніх дихальних шляхів, підвищують гіперчутливість носової порожнини. ФАТ бере участь також у імунній і запальній відповіді при бронхіальній астмі, індукуючи бронхоконстрикцію, підвищуючи гіперчутливість бронхів, спричиняючи вироблення слизу та підвищуючи проникність легеневих судин. Експериментальні дослідження свідчать, що терапевтичні стратегії, спрямовані на блокаду ФАТ й інших, відмінних від гістаміну медіаторів, мають потенціал покращення контролю астми та зменшення бронхоспазму. Проте дотепер існує потреба в клінічних дослідженнях (Munoz-Cano R.M. et al., 2019).
У пацієнтів із кропив’янкою ФАТ підвищує проникність судин шкіри, посилюючи ефект інших медіаторів і спричиняючи утворення пухирів. Дослідження свідчать, що в пацієнтів зі спонтанною хронічною кропив’янкою спостерігаються вищий рівень ФАТ і нижчий уміст ферменту ацетилгідролази, який його руйнує, порівняно з відносно здоровими особами. Цікаво, що підвищення вмісту ФАТ (>5000 пг/мл) корелює з відсутністю відповіді на антигістамінні препарати (Munoz-Cano R.M. et al., 2019).
Для того щоб підтвердити вищу ефективність комбінованої гістамінової блокади та блокади ФАТ порівняно зі стандартною гістаміновою блокадою, R.M. Munoz-Cano та співавт. (2013) провели подвійно сліпе рандомізоване плацебо-контрольоване дослідження, в якому пацієнтам, які протягом 4 днів до того отримували левоцетиризин або рупатадин, проводилася провокаційна проба з ФАТ. Результати показали, що рупатадин, на відміну від левоцетиризину, достовірно зменшував ФАТ-індуковані симптоми в пацієнтів з алергічним ринітом. Найпотужнішим виявився вплив на закладеність носа та ринорею.
За умови застосування рупатадину сумарне зниження оцінки за шкалою 4 основних назальних симптомів (T4SS) через 1 годину становило 73%, а на тлі застосування левоцетиризину – лише 23%. Проведене тими самими авторами дослідження in vitro виявило, що рупатадин у концентрації 5, 10 і 25 мкмоль інгібував дегрануляцію опасистих клітин – один із ключових елементів патогенезу алергічних захворювань – на 40, 53 та 46%. Натомість левоцетиризин і дезлоратадин (обидва в концентрації 1 мкмоль) інгібували процес дегрануляції лише на 3 та 3,5% відповідно. У висновку наукової роботи дослідники вказали, що завдяки цьому ефекту рупатадин може бути ефективнішим у лікуванні анафілаксії, ніж інші антигістамінні засоби (Munoz-Cano R.M. et al., 2012).
Загалом ФАТ відіграє важливу роль у патогенезі алергічного риніту, а блокада цього медіатора, відповідно, зменшує вираженість клінічної симптоматики. Антигістамінні засоби з анти-ФАТ-активністю можуть забезпечувати кращий контроль назальних симптомів порівняно із застосуванням протиалергічних препаратів, яким не притаманний анти-ФАТ-ефект. Науковцями світу вивчалася велика кількість антигістамінних препаратів з анти-ФАТ-потенціалом (рупатадин, азеластин, кетотифен, епінастин), але лише рупатадин продемонстрував здатність інгібувати вивільнення ФАТ у носовій порожнині в кількох дослідженнях in vitro й in vivo (Munoz-Cano R.M. et al., 2019).
Отже, медична наука продовжує з’ясовувати нюанси патогенетичного підґрунтя найпоширеніших захворювань (алергічних, серцево-судинних, злоякісних тощо), оскільки з огляду на ці нюанси можливими стають відкриття нових терапевтичних мішеней і створення нових фармакопрепаратів чи переосмислення старих. Один з фокусів уваги науковців – це ФАТ, який не лише активує тромбоцити, а й бере участь у процесах запалення, дегрануляції опасистих клітин, апоптозу. Серед досліджуваних молекул зі впливом на ФАТ багатий потенціал має рупатадин – відомий антигістамінний препарат, якому притаманна анти-ФАТ-активність, що зумовлює доцільність подальшого його вивчення як протипухлинного, протизапального й антиоксидантного засобу.
Література
- New Insights into Platelet-Activating Factor. Available at: https://www.imrpress.com/journal/FBL/special_issues/platelet-activating_factor.
- Tsoupras A.B., Iatrou C., Frangia C., Demopoulos C.A. The implication of platelet activating factor in cancer growth and metastasis: potent beneficial role of PAF-inhibitors and antioxidants. Infect. Disord. Drug Targets. 2009; 9 (4): 390-399. doi: 10.2174/187152609788922555. PMID: 19689381.
- Deuster E., Hysenaj I., Kahaly M., Schmoeckel E., Mayr D., et al. The platelet-activating factor receptor’s association with the outcome of ovarian cancer patients and its experimental inhibition by rupatadine. Cells. 2021 Sep 7; 10 (9): 2337. doi: 10.3390/cells10092337.
- Church M.K. Efficacy and tolerability of rupatadine at four times the recommended dose against histamine- and platelet-activating factor-induced flare responses and ex vivo platelet aggregation in healthy males. Br. J. Dermatol. 2010 Dec; 163 (6): 1330-1332. doi: 10.1111/j.1365-2133.2010.10029.x.
- Hafez H.M., Abdel-Hakeem E.A., Hassanein H. Rupatadine, a dual antagonist of histamine and platelet-activating factor (PAF), attenuates experimentally induced diabetic nephropathy
in rats. Naunyn Schmiedebergs Arch. Pharmacol. 2020 Aug; 393 (8): 1487-1500. doi: 10.1007/s00210-020-01856-8. Epub 2020 Mar 21. PMID: 32200462. - Muñoz-Cano R.M., Casas-Saucedo R., Valero Santiago A., Bobolea I., Ribó P., Mullol J. Platelet-activating factor (PAF) in allergic rhinitis: clinical and therapeutic implications. Journal of Clinical Medicine. 2019; 8 (9): 1338. doi: 10.3390/jcm8091338.
- Muñoz-Cano R., Valero A., Izquierdo I., Sánchez-López J., Doménech A., et al. Evaluation of nasal symptoms induced by platelet activating factor, after nasal challenge in both healthy
and allergic rhinitis subjects pretreated with rupatadine, levocetirizine or placebo in a cross-over design. Allergy Asthma Clin. Immunol. 2013; 9: 43. - Munoz-Cano R., et al. Effects of rupatadine on platelet activating factor (PAF)-induced human mast cell degranulation compared with desloratadine and levocetirizine. Journal of Allergy and Clinical Immunology. 2012 Feb; Vol. 129; Issue 2; AB122.
- Antonopoulou S. Platelet-activating factor-induced inflammation in obesity: a two-sided coin of protection and risk. Cells. 2025; 14 (7): 471. doi: 10.3390/cells14070471.
- Klein M., Dao V., Khan F. A review of platelet-activating factor as a potential contributor to morbidity and mortality associated with severe COVID-19. Clinical and Applied Thrombosis/Hemostasis. 2021; 27. doi: 10.1177/10760296211051764.
- Biochemistry of Platelet Activating Factor. Available at: https://www.ncbi.nlm.nih.gov/books/NBK557392.
- Tsoupras A., Adamantidi T., Finos M.A., Philippopoulos A., Detopoulou P., et al. Re-assessing the role of platelet activating factor and its inflammatory signaling and inhibitors in cancer
and anti-cancer strategies. Front. Biosci. (Landmark Ed.). 2024; 29 (10): 345. doi: 10.31083/j.fbl2910345.