Цілорічний алергічний риніт: клінічні виклики, фармакотерапія та вплив на якість життя
Підготувала канд. біол. наук Олександра Демецька
Цілорічний алергічний риніт (ЦАР) є хронічним запальним захворюванням слизової оболонки носа, що виникає внаслідок сенсибілізації до постійно присутніх алергенів, як-от кліщі домашнього пилу, шерсть тварин або пліснява. На відміну від сезонного алергічного риніту (САР), симптоми ЦАР проявляються протягом усього року, що значно погіршує якість життя пацієнтів, спричиняє порушення сну, зниження працездатності й підвищує ризик розвитку супутніх захворювань, зокрема бронхіальної астми та хронічного синуситу. Незважаючи на високу поширеність, ефективний контроль симптомів ЦАР залишається викликом, що зумовлює потребу в глибшому розумінні його факторів ризику та клінічних особливостей, а також оптимізації терапевтичних підходів.
Епідеміологія, фактори ризику та вплив на якість життя
Загальна поширеність АР коливається від 5 до 50% залежно від країни, віку, методів діагностики й визначення, тоді як ЦАР трапляється в 10-20% загальної популяції [1, 2].
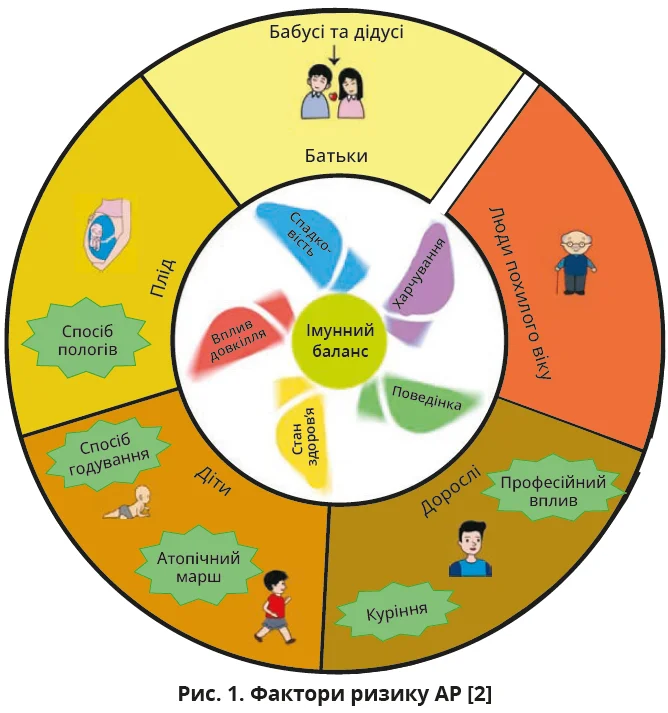
Встановлені на сьогодні фактори ризику АР можуть впливати на розвиток хвороби протягом усього життя людини (рис. 1).
На рисунку 1 вітряк у внутрішньому кільці має п’ять лопатей, які відповідають спадковості, навколишньому середовищу, поведінці, харчуванню та стану здоров’я. Усі зазначені аспекти так чи інакше впливають на імунний баланс людини, що в підсумку провокує розвиток АР. Зовнішнє кільце відображає різні етапи життя людини, протягом яких можуть впливати ті чи інші фактори ризику АР.
Отже, спадкові фактори й сімейний анамнез, стан матері та спосіб пологів і годування, особисті характеристики, харчування та споживання їжі, особиста поведінка та звички, набутий вплив довкілля й хімічних речовин, хвороби та стан здоров’я – все це впливає на схильність до АР. Зокрема, відомо, що материнська тривожність і депресія під час вагітності, гестаційний цукровий діабет, ожиріння, а також пологи через кесарів розтин можуть збільшити ризик алергічних захворювань у людини протягом її життя [2].
ЦАР часто недооцінюється клініцистами, оскільки більшість епідеміологічних досліджень фокусується на сезонному риніті, а не на цілорічному. Відомо, що ЦАР має стійкіший негативний вплив на якість життя та вищий ризик розвитку супутніх захворювань, тоді як САР хоча й може спричиняти гостріші симптоми, але їхній вплив є менш тривалим [3].
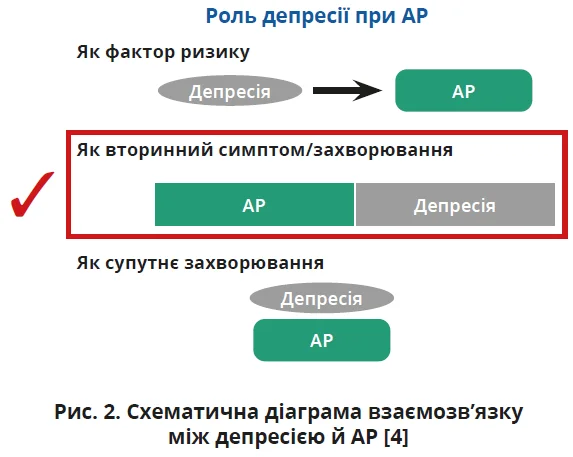
ЦАР має вираженіший негативний вплив на якість життя та частіше асоціюється з хронічними ускладненнями, як-от синусит, бронхіальна астма (особливо при алергії на кліщів домашнього пилу), отити та дисфункція євстахієвої труби. Крім того, серед потенційно серйозних коморбідних станів, пов’язаних із ЦАР, виділяється депресія (рис. 2). Хоча сам по собі ЦАР не є небезпечним для життя захворюванням, він може суттєво впливати на якість життя й навіть призводити до зниження працездатності. У певної кількості пацієнтів він може спровокувати депресію, тривогу й інші психічні розлади через стрес, спричинений самим АР або іншими негативними подіями, що певною мірою збільшує навантаження на сім’ю та суспільство. Ризик розвитку депресивних симптомів у пацієнтів з АР у 1,82 раза вищий, аніж у здорових людей [4].
Патогенез, симптоматика та диференціація АР
АР виникає, коли порушення епітеліального бар’єра дає алергенам змогу проникати через слизовий епітелій носових ходів, спричиняючи запальну реакцію Т-хелперів 2-го типу та вироблення алергенспецифічного імуноглобуліну Е (IgE). Здебільшого він проявляється симптомами закладеності носа, ринореї, виділень з носа, чхання та свербіння очей, носа й горла.
У пацієнтів із САР зазвичай під час фізикального огляду виявляються набряклі та бліді носові раковини. У пацієнтів із ЦАР зазвичай спостерігаються еритематозні й запалені носові раковини із серозними виділеннями, які при фізикальному огляді видаються подібними до інших форм хронічного риніту. Персистивний АР визначають як симптоми, що виникають частіше 4 днів поспіль на тиждень і понад 4 тижні поспіль на рік [5].
Антигістамінні препарати як терапія першої лінії ЦАР
Насамперед пацієнтам з АР слід уникати контакту з алергенами. Терапія охоплює антигістамінні препарати другого покоління – АГП ІІ (наприклад, цетиризин, фексофенадин, дезлоратадин, лоратадин), інтраназальні антигістамінні препарати (наприклад, азеластин, олопатадин) та інтраназальні кортикостероїди (наприклад, флутиказон, тріамцинолон, будесонід, мометазон) і має бути вибрана на підставі тяжкості та частоти симптомів, а також уподобань пацієнта [5].
Антигістамінні препарати, що є H1-блокаторами другого покоління, блокують гістамінові рецептори, зменшуючи свербіж, чхання та ринорею. Гістамін є ключовим медіатором алергічної реакції.
Концентрація гістаміну особливо висока в опасистих клітинах, які розташовані в дихальному дереві, шлунково-кишковому тракті та шкірі. H1-антигістамінні препарати широко використовуються в пацієнтів для лікування симптомів, які є вторинними до вивільнення гістаміну, що типово для певних алергічних станів. На відміну від представників першого покоління, АГП ІІ мають менше побічних ефектів, оскільки вони селективніші до периферичних H1-рецепторів [1].
Деякі АГП ІІ також мають низку важливих протизапальних і протиалергічних ефектів, які виникають шляхом зменшення вироблення цитокінів і вивільнення інших медіаторів мастоцитами та базофілами; залучення еозинофілів у пізній фазі алергічних реакцій; експресії мембранних рецепторів в епітеліальних клітинах носа та судинному ендотелії тощо [6].
Пацієнти із ЦАР часто не досягають належного контролю симптомів за стандартної фармакотерапії, що підкреслює важливість вибору антигістамінного препарату з доведеною ефективністю, доброю переносимістю та належним профілем безпеки.
Цетиризин: фармакологічний профіль і клінічна ефективність
Цетиризин – АГП ІІ, який з’явився на фармацевтичному ринку 1989 року. Відтоді він утвердився як одна з ключових молекул у своєму класі та досі залишається широко застосовуваним у клінічній практиці [6].
Фармакодинамічні властивості
Цетиризин є високоселективним антагоністом H1-рецепторів з мінімальною спорідненістю до інших рецепторів, як-от α1-адренергічні, допамінові, серотонінові та мускаринові. У дозі 10 мг він ефективно пригнічує гістамін-індуковані шкірні реакції, перевершуючи за цим показником деякі інші антигістаміни. Крім того, цетиризин краще за лоратадин зменшує назальний опір після гістамінового навантаження. Його протизапальна дія проявляється в зниженні клітинної інфільтрації й експресії молекул адгезії. Завдяки обмеженому проникненню в центральну нервову систему препарат не спричиняє клінічно значущої седації. Він також не впливає на інтервал QT, навіть у високих дозах, і не взаємодіє з препаратами, що метаболізуються системою цитохрому P450 [6].
Фармакокінетичні властивості
Цетиризин характеризується швидким і повним усмоктуванням у шлунково-кишковому тракті, високою біодоступністю та швидким початком дії. Він має низький об’єм розподілу, активно зв’язується з альбуміном і практично не проникає в мозок чи міокард, що зумовлює низький ризик кардіо- та нейротоксичності. Препарат не піддається значному печінковому метаболізму й виводиться переважно в незміненому вигляді із сечею, що знижує ризик лікарських взаємодій. Період напіввиведення становить приблизно 10,5 годин, що дає змогу застосовувати його 1 раз на добу. У літніх пацієнтів концентрація препарату в сироватці крові більше залежить від функції нирок, аніж від віку [6].
Терапевтична ефективність
Ефективність цетиризину в пацієнтів із ЦАР доведено в численних клінічних випробуваннях. У подвійно сліпому рандомізованому плацебо-контрольованому дослідженні було оцінено вплив цетиризину на тяжкість симптомів та якість життя в дорослих пацієнтів із ЦАР. Протягом 4 тижнів приймання препарату в дозі 10 мг 1 раз на добу спостерігалися достовірне зниження загального комплексу симптомів (TSSC) та покращення показників за шкалою якості життя при риніті (RQLQ) порівняно з плацебо. Вже після першого тижня лікування відзначалися покращення носових симптомів, зменшення практичних труднощів і підвищення рівня активності, а наприкінці курсу – покращення емоційного стану [6].
Порівняльні характеристики антигістамінних препаратів свідчать на користь цетиризину в лікуванні АР, зокрема ЦАР. У клінічних дослідженнях цетиризин показав вищу ефективність у зменшенні симптомів алергії порівняно з лоратадином (Claritin): 48% зменшення симптомів у пацієнтів, які приймали цетиризин, проти 33% у групі лоратадину [7] (рис. 3).
Інше дослідження порівнювало різні режими дозування цетиризину з хлорфеніраміном і плацебо в пацієнтів з АР. Усі схеми приймання цетиризину (ранкова, вечірня, двічі на день) забезпечували достовірне зниження тяжкості симптомів через 12 і 24 години після введення дози. Найвираженіше полегшення спостерігалося в нічний і ранковий час, що свідчить про ефективний контроль симптомів протягом доби незалежно від режиму дозування [6].
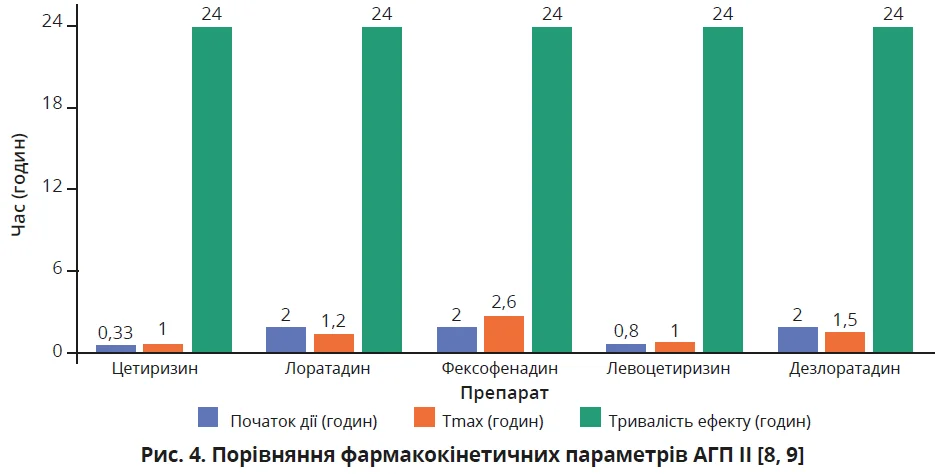
Цетиризин має один з найшвидших початків дії серед АГП ІІ, що може мати вирішальне значення при гострих симптомах. Препарат починає діяти через 20-60 хвилин, у 50% пацієнтів ефект починається вже через 20 хвилин (0,33 години) [8] (рис. 4).
Результати систематичного огляду 22 клінічних досліджень, які охопили 5867 педіатричних пацієнтів із ЦАР і САР, свідчать, що цетиризин забезпечує достовірне зниження симптомів уже з 1-го тижня лікування з поступовим покращенням до 12-го тижня. Також відзначено позитивний вплив на якість життя дітей. Ефективність препарату була порівнянною або вищою за інші антигістамінні засоби та монтелукаст, хоча при атопічному дерматиті переваги були менш вираженими [10].
Цетиризин – оптимальний вибір у разі ЦАР завдяки швидкому початку дії та високій ефективності при назальних симптомах. Він демонструє високу ефективність у контролі симптомів ЦАР з позитивним впливом на якість життя пацієнтів.
Профіль безпеки
Метааналіз 13 рандомізованих досліджень показав, що приймання цетиризину 10 мг щодня не спричиняє клінічно значущої сонливості порівняно з плацебо. Його профіль безпеки підтверджено також у контексті взаємодії з їжею й алкоголем: цетиризин демонструє низький ризик фармакокінетичних змін, що важливо для пацієнтів з алергічними захворюваннями [6].
У межах великого європейського дослідження ARITMO не було виявлено підвищеного ризику шлуночкових аритмій при застосуванні цетиризину, на відміну від деяких інших антигістамінних препаратів [6].
Відповідно до даних бази безпеки UCB Pharma використання цетиризину під час вагітності не асоціюється зі збільшенням ризику несприятливих наслідків, зокрема вроджених вад розвитку [6].
При застосуванні в педіатричній практиці цетиризин продемонстрував добру переносимість: не виявлено підвищеного ризику серйозних побічних ефектів, включно з кардіо-, нейро- та гастротоксичністю [10].
Висновки
ЦАР являє собою хронічне запальне захворювання, що може призводити до серйозних коморбідних ускладнень, як-от бронхіальна астма, хронічний синусит, отити, а також психоемоційні порушення, включно з депресією. Його персистивний перебіг значно знижує якість життя пацієнтів, впливає на сон, працездатність і соціальну активність. Тому своєчасне й ефективне лікування ЦАР має не лише симптоматичне, а й профілактичне значення, спрямоване на зменшення ризику ускладнень і покращення якості життя.
Цетиризин – АГП ІІ, який ефективно зменшує тяжкість симптомів АР і покращує якість життя. Препарат має швидкий початок дії та тривалий період напіввиведення, що дає змогу приймати його 1 раз на день. Він не спричиняє клінічно значущої седації, не впливає на інтервал QT і не має суттєвих взаємодій з їжею чи алкоголем. Завдяки поєднанню ефективності, безпеки та зручності застосування цетиризин залишається препаратом першого вибору при лікуванні ЦАР.
Література
- Chen R., An W., Liu X., et al. Risk factors of allergic rhinitis and its prevention strategies. Front. Allergy. 2024; 5: 1509552. doi: 10.3389/falgy.2024.1509552.
- Savouré M., Bousquet J., Jacquemin B., et al. Worldwide prevalence of rhinitis in adults: a review of definitions and temporal evolution. Clinical and Translational Allergy. 2022; 12 (1): e12130. doi: 10.1002/clt2.12130.
- Nuhi A., Jintu A., Amresh K., Harinderjit S. Allergic rhinitis: impact on quality of life. Ann. Pulm. Res. Med. 2024; 2 (1): 1007.
- Mou Y.K., Wang H.R., Zhang W.B., et al. Allergic rhinitis and depression: profile and proposal. Front. Psychiatry. 2022 Jan 4; 12: 820497. doi: 10.3389/fpsyt.2021.820497.
- Bernstein J.A., Bernstein J.S., Makol R., Ward S. Allergic rhinitis: a review. JAMA. 2024; 331 (10): 866-877. doi: 10.1001/jama.2024.0530.
- Corsico A.G., Leonardi S., Licari A., et al. Focus on the cetirizine use in clinical practice: a reappraisal 30 years later. Multidiscip. Respir. Med. 2019; 14. doi: 10.1186/s40248-019-0203-6.
- Clearvue Health. Cetirizine (Zyrtec) vs loratadine (Claritin): effectiveness & side effects. Reviewed by The Clinical Committee, May 8, 2019. Available at: https://www.clearvuehealth.com/b/cetirizine-loratadine.
- Naqvi A., Patel P., Gerriets V. Pharmacology, Cetirizine. In StatPearls. StatPearls Publishing. 2024. Available at: https://www.ncbi.nlm.nih.gov/books/NBK549776.
- Simons F.E.R. Advances in H1-antihistamines. New England Journal of Medicine. 2004; 351 (21): 2203-2217. doi: 10.1056/NEJMra033121.
- Zhang Y., Liu Y., Wang Y., et al. Efficacy, acceptability, and safety of cetirizine for treating allergic diseases in children: a systematic review and meta-analysis of randomized controlled trials. Frontiers in Pediatrics. 2022; 10: 940213. doi: 10.3389/fped.2022.940213.