Атопічний дерматит: вибір пробіотичного штаму та порівняння ефективності пробіотиків і синбіотиків
Переклала й адаптувала канд. мед. наук Тетяна Можина
Атопічний дерматит (АтД) являє собою хронічний запальний дерматоз, який схильний до рецидивування та виникає в осіб із генетичною схильністю [1]. Протягом останніх років реєструють зростання щорічної захворюваності на АтД: згідно з Фінською національною базою даних найчастіше на АтД страждають діти та підлітки віком 0-14 років (47,46%), а також працездатні хворі віком 15-60 років (43,74%) [2].
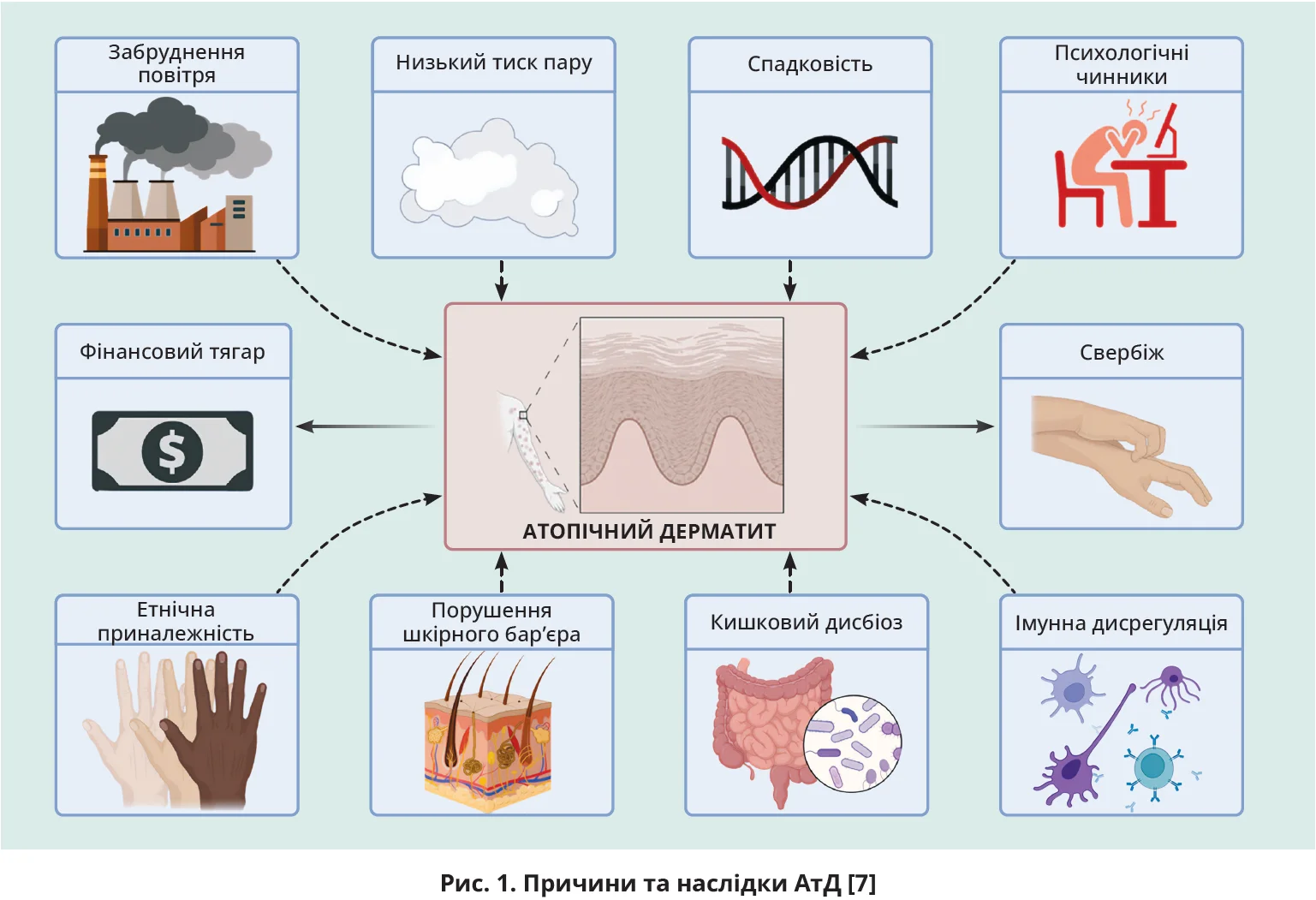
Незважаючи на те що механізми розвитку АтД остаточно не з’ясовані, ключовими патогенетичними ланками вважають порушення імунологічної функції та дисрегуляцію шкірного бар’єра [3]. Водночас такі фактори навколишнього середовища (рис. 1), як нераціональні харчові звички, різкі зміни способу життя, вплив алергенів, також асоційовані з розвитком АтД. До кліматичних умов, пов’язаних із підвищенням ризику АтД, відносять низький тиск повітряних парів [4]; психологічні чинники відіграють важливу роль у розвитку АтД: згодом АтД призводить до появи депресії [5].
Патогенез АтД: короткі відомості
Хоча патогенез АтД продовжує вивчатися, десятиліття досліджень указують на патогенетичний зв’язок АтД із генетичною схильністю, впливом навколишнього середовища, порушенням цілісності шкірного бар’єра, імунною дисрегуляцією та мікробним дисбалансом (рис. 1).
Розвиток АтД спричиняють різні чинники: забруднення повітря, низький тиск пару, спадковість, психологічні чинники, етнічна приналежність, дисрегуляція шкірного бар’єра, кишковий дисбактеріоз, імунна дисрегуляція. АтД зумовлює виникнення свербежу та збільшення фінансового тягаря.
Це свідчить про те, що АтД є системним органозалежним алергічним захворюванням, за якого після ушкодження поверхневого шару шкіри та порушення цілісності епідермального бар’єра антигени проникають у шкіру, продукуючи хемокіни й медіатори запалення (інтерлейкін-25 (ІЛ-25), ІЛ-33 та тимічний стромальний лімфопоетин). Th-клітини трансформуються в Th2 та виробляють ІЛ-4, ІЛ-13, ІЛ-5 [6]. Активуються Th1, Th17, Th22 й інші сигнальні шляхи; синтезуються різноманітні цитокіни та фактори росту, залучені в запальну імунну відповідь через сигнальний шлях янус-кінази (JAK), посилюючи диференціацію Th2-клітин. Подряпини разом з ендогенними й іншими екзогенними тригерами (гістамін, протеази, субстанція P, різні інтерлейкіни, алергени навколишнього середовища) призводять до активації кератиноцитів і посилення запалення шкіри [6]. Прозапальні медіатори та запальний процес спричиняють інтенсивне розчухування, подальше пошкодження шкірного бар’єра, яке посилюють патогенні й умовно-патогенні бактерії.
Кишківник відіграє важливу роль в імунній відповіді. Природні кілери, лімфоїдні клітини вродженого імунітету, кишкова мікрофлора регулюють одне одного задля підтримки кишкового гомеостазу, належного функціонування імунітету [8]. Здорова мікрофлора кишківника чинить захисний ефект [9], тоді як порушення кишкового мікробіому в ранньому дитинстві погіршує імунну дисфункцію в дітей з АтД [10]. Різноманітні способи відновлення екології кишківника, навіть трансплантацію фекальної мікробіоти, розглядають як методи лікування АтД [11]. Доцільність такого підходу підтверджує низьке мікробне різноманіття, асоційоване зі зростанням захворюваності на АтД [12]. Збільшення тяжкості клінічної симптоматики у хворих на АтД пов’язане зі зменшенням кількості біфідобактерій у кишківнику [7]. І навпаки, велика кількість патогенних Clostridium difficile у фекаліях пацієнтів з АтД свідчить про зменшення кількості корисних бактерій, імунну дисфункцію, підвищення проникності кишківника. Дослідження продемонстрували, що колонізація кишкової флори передує виникненню АтД [12], тому своєчасне підтримання кишкового мікробіому в здоровому стані розглядають як перспективний лікувально-профілактичний захід.
Лікування та профілактика АтД: місце пробіотиків
Метою лікування АтД вважають зменшення інтенсивності запалення, підсилення та відновлення бар’єрної функції шкіри, зменшення свербежу, запобігання виникненню суперінфекції, спричиненої деградацією рогового шару [7]. Різноманітні експериментальні та клінічні дослідження довели, що призначення пробіотиків при АтД є патогенетично обґрунтованим через їхню здатність зменшувати запалення завдяки зниженню вмісту прозапальних цитокінів (ІЛ-4, IЛ-6, фактор некрозу пухлини-α), інтерферону-γ, високочутливого С-реактивного білка та збільшенню експресії IЛ-10, протизапальних цитокінів у мезентеріальних лімфатичних вузлах [13]. Нормалізація мікробного складу забезпечує захист слизової оболонки від хвороботворних мікроорганізмів; окрім цього, застосування пробіотиків пов’язане з позитивними метаболічними змінами у вигляді покращення травлення, поліпшенням засвоєння харчових інгредієнтів, тенденцією до зниження сироваткового вмісту глікемії, інсулінемії та резистентності до інсуліну [13].
Такі патогенетичні механізми дії пробіотиків зумовлюють вірогідні клінічні ефекти, що передусім дають змогу зменшити активність запального процесу: метааналіз 7 рандомізованих контрольованих досліджень – РКД (n=241) підтвердив, що призначення пробіотиків хворим на АтД асоційовано зі зниженням тяжкості захворювання, котру оцінювали за допомогою шкали SCORAD (середня різниця, СР 7,90; 95% довірчий інтервал, ДI від -7,25 до -6,92; p<0,00001) і покращенням якості життя (СР -7,68; 95% ДI від -14,08 до -1,29; p=0,02) [14] (рис. 2).
Аналогічні дані отримано ще в декількох роботах: метааналіз 13 досліджень довів, що застосування пробіотиків сприяє покращенню значень шкали SCORAD порівняно з контролем (СР -3,07; 95% ДІ від -6,12 до -0,03; р<0,001) [15]. Причому пероральний прийом Lactobacillus-умісних пробіотиків забезпечує вірогідне зменшення тяжкості АтД
та зниження кількості балів за шкалою SCORAD (СР -2,90; 95% ДІ від -4,21 до -1,59; p<0,00001) [16].
Метааналіз 22 статей (n=3280) підтвердив, що прийом пробіотиків під час вагітності та/або в грудному віці асоційований зі значним зниженням захворюваності на АтД (відносний ризик, ВР 0,81; 95% ДІ 0,70-0,93; р<0,05), причому найефективнішим виявилося застосування пробіотиків, які містили штами Lactobacillus і Bifidobacterium (ВР 0,68; 95% ДІ 0,52-0,90; р<0,05) [17]. Автори цієї роботи відзначили цікавий факт: профілактична ефективність пробіотиків зберігалася незалежно від географічного ареалу – вони чинили свою благотворну дію як у США, Європі (ВР 0,74; 95% ДІ 0,61-0,91; р<0,05), так і в Австралії (ВР 0,83; 95% ДІ 0,73-0,96; р<0,05) [17].
Метааналіз 7 РКД довів, що пробіотики перевершують плацебо не тільки в лікуванні, а й у профілактиці АтД (ВР 0,83; 95% ДІ 0,73-0,94), особливо при застосуванні штамів L. rhamnosus або змішаних пробіотиків [18]. Отже, накопичено достатню кількість даних, що демонструють доцільність застосування Lactobacillus-умісних пробіотиків.
Lactobacillus у лікуванні АтД: яким штамам віддати перевагу?
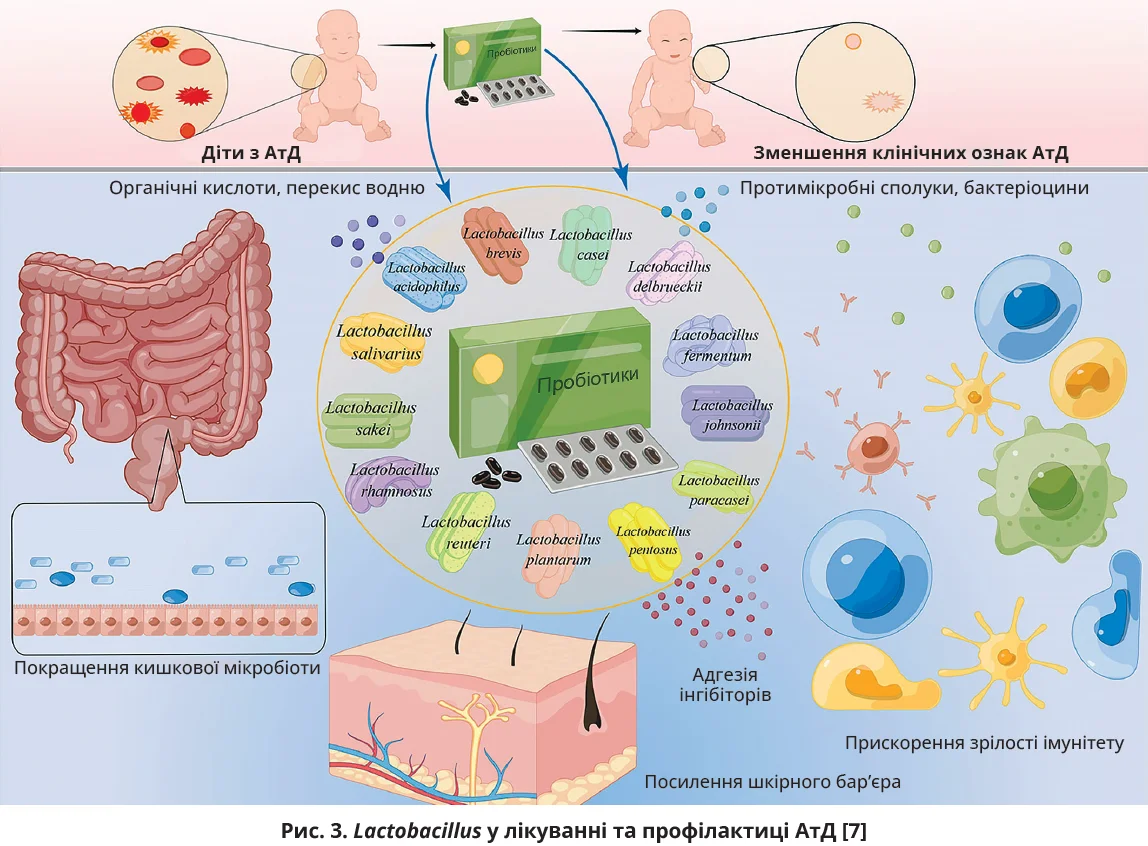
Рід Lactobacillus надзвичайно чисельний і представлений, зокрема, L. rhamnosus, L. acidophilus, L. sakei, L. reuteri, L. salivarius, L. paracasei, L. casei, L. delbrueckii, L. fermentum, L. johnsonii, L. Pentosus і L. brevis, ефективність яких у лікуванні та профілактиці АтД оцінювалася в різноманітних дослідженнях (рис. 3). Доведено, що Lactobacillus виробляють різні речовини (органічні кислоти, перекис водню, низькомолекулярні протимікробні препарати, бактеріоцини й інгібітори адгезії), які стимулюють уроджений імунітет і сприяють формуванню збалансованих мікробних спільнот завдяки конкурентному відторгненню та протимікробній активності щодо патогенних бактерій [7]. Прийом Lactobacillus знижує рівень IgE в сироватці крові, сприяє балансу Th1/Th2 та відновленню кишкового бар’єра, покращенню імунної функції та шкірного бар’єра [7].
L. rhamnosus
Найвивченішим видом Lactobacillus є L. rhamnosus, який має переконливу доказову базу своєї ефективності. В експериментах доведено, що пептидоглікан L. rhamnosus здатний регулювати імунну функцію епітеліальних і дендритних клітин кишківника людини, а призначення L. rhamnosus знижує концентрацію еозинофільного катіонного білка, еозинофілів, IЛ-3 та сироваткового IgE, підтримує баланс Th1/Th2, прискорює імунне дозрівання, стимулює клітини периферичної крові синтезувати ІЛ-10, перетворює фактор росту-β та регулює вироблення інтерферону-γ в шкірі [7].
Клінічні дослідження також підкреслюють безпечність і результативність L. rhamnosus: у межах багатоцентрового педіатричного РКД встановлено, що 3-місячне застосування комбінованого L. rhamnosus-умісного пробіотика сприяє зменшенню тяжкості АтД, оціненого за допомогою SCORAD (відношення шансів 2,56; 95% ДІ 1,13-5,8; p=0,012) [19]. У клінічних дослідженнях у немовлят віком 0-2 роки спостерігали зниження частоти виникнення атопічної екземи, якщо їхні матері приймали L. rhamnosus під час вагітності, а профілактичний ефект зберігався до 4 років [20]. Застосування L. rhamnosus не тільки сприяє зменшенню тяжкості захворювання, покращенню якості життя, а й зниженню добового дозування топічних кортикостероїдів [21].
АтД є поширеним захворюванням у дітей. Lactobacillus прискорюють дозрівання імунної системи, підтримують кишковий гомеостаз, покращують кишковий мікробіом і в підсумку нівелюють симптоми АтД.
Здатність L. rhamnosus поліпшувати перебіг АтД має найвищий рівень доказовості: метааналіз 11 РКД, в яких для лікування АтД використовували L. rhamnosus як моноштам або в комбінації з іншими пробіотиками, довів статистично значуще зниження захворюваності на АтД у дітей ≤2 років (ВР 0,60; 95% ДІ 0,47-0,75; p<0,00001)
і в дітей 6-7 років (ВР 0,62; 95% ДІ 0,50-0,75; p<0,00001) [22].
L. acidophilus
L. acidophilus, інший представник родини Lactobacillus, відомий доведеною здатністю знижувати судинну проникність, пригнічує запальну відповідь шляхом активації регуляторних Т-лімфоцитів і Th1-клітин, зменшує рівень загального IgE в сироватці крові, а також нівелює ознаки АтД у дітей і дорослих [7]. У клінічних дослідженнях L. acidophilus довів добрий профіль безпеки та високу ефективність у лікуванні АтД.
Бажана: Lactobacillus-умісний синбіотик
Протягом останніх років поповнюється доказова база доцільності застосування синбіотиків у лікуванні АтД. Термін «синбіотик» було запроваджено відносно нещодавно; згідно з положеннями міжнародного консенсусу це «суміш, що складається з живих мікроорганізмів і субстрату (субстратів), які вибірково використовуються мікробами організму господаря, що дає користь для здоров’я господаря» [23], тобто синбіотик являє собою поєднання пробіотичних штамів із пребіотиком. Результати клінічних досліджень підтверджують ефективність синбіотиків у лікуванні АтД: доведено, що застосування багатокомпонентних синбіотиків сприяє поліпшенню функціонування шкірного бар’єра [24], знижує тяжкість захворювання [25] та зменшує виразність симптомів [26]. Зазначені результати підтвердив метааналіз 6 досліджень, у якому доведено, що використання синбіотика протягом 8 тижнів сприяє значному зниженню індексу SCORAD (-6,56; 95% ДІ від -11,43 до -1,68; р=0,008), причому ефективність синбіотиків у лікуванні АтД перевищує таку пробіотиків [27]. Прийом синбіотика асоційований із тенденцією до зменшення сумарного відносного ризику АтД (0,44; 95% ДІ 0,11-1,83; р=0,26) [27].
Бажана, сучасний високодозовий Lactobacillus-умісний синбіотик (виробник – Sopharma), може бути успішно застосований у лікуванні та профілактиці АтД. Його пробіотична складова представлена двома штамами лактобактерій: L. rhamnosus і L. acidophilus, безпечність та ефективність яких у терапії АтД доведено в межах експериментальних і клінічних досліджень, а також підтверджено систематичними оглядами та метааналізами. Протизапальна й імуномодуляторна активність комбінації L. rhamnosus, L. acidophilus дає змогу відновити цілісність кишкового бар’єра, зменшити рівень прозапальних цитокінів, IgE та нівелювати клінічні ознаки АтД. Пребіотичну складову Бажани представляє інулін, який слугує субстратом для мікробної ферментації та вироблення коротколанцюгових жирних кислот. Доведено, що інулін сприяє відновленню кишкового бар’єра, детоксикації канцерогенів, розквіту «корисних» мікробів [28], посилюючи таким чином дію штамів L. rhamnosus, L. acidophilus і мінімізуючи вплив оксидативного стресу. Наявність у складі Бажани ліофілізованих дріжджів Saccharomyces boulardii надає препарату додаткові переваги завдяки їхній здатності виводити патогенні мікроорганізми, створювати умови для розмноження власної сапрофітної мікрофлори. Активні речовини Бажани розташовані в капсулі, яка захищає пробіотики під час транзиту верхніми відділами шлунково-кишкового тракту та допомагає підтримувати стабільність і життєздатність усіх її компонентів. Кожна капсула Бажани містить L. rhamnosus (1×109 КУО), L. acidophilus (2,5×109 КУО), інулін (25 мг) і S. boulardii (2,5×109 КУО). Синбіотик Бажана можна використовувати як у дітей ≥3 років, так і в дорослих, призначаючи відповідну форму випуску (капсули/порошок-саше) та дозування (2 капсули або 1 капсула/саше відповідно), та рекомендуючи приймати препарат 1 раз на добу протягом 4 тижнів.
Висновки
Згідно з даними доказової медицини пробіотики здатні запобігти виникненню АтД та зменшити тяжкість захворювання. Застосування Lactobacillus-умісних пробіотиків дає змогу відновити цілісність кишкового бар’єра, знизити рівень прозапальних цитокінів, сироваткового IgE та зменшити клінічні ознаки АтД; найдієвішими пробіотичними лактобактеріями є L. rhamnosus, L. acidophilus. Результативність використання багатокомпонентних синбіотиків (комбінації пробіотиків і пребіотика) перевищує ефективність пробіотиків. Високодозовий синбіотик Бажана, який містить пробіотичні штами з доведеною ефективністю L. rhamnosus, L. acidophilus, пребіотик інулін і S. boulardii, може використовуватися в схемах лікування та профілактики АтД.
Література
- Armario-Hita J.C., Galán-Gutiérrez M., Dodero-Anillo J., et al. Updated review on treatment of atopic dermatitis. J. Investig. Allergol. Clin. Immunol. 2023; 33 (3): 158-167. doi: 10.18176/jiaci.0906.
- Salava A., Rieppo R., Lauerma A., et al. Age-dependent distribution of atopic dermatitis in primary care: a nationwide population-based study from Finland. Acta Derm. Venereol. 2022; 102: adv00738. doi: 10.2340/actadv.v102.2287.
- Yang G., Seok J.K., Kang H., et al. Skin barrier abnormalities and immune dysfunction in atopic dermatitis. Int. J. Mol. Sci. 2020; 21 (8): 2867. doi: 10.3390/ijms21082867.
- Yokomichi H., Mochizuki M., Shinohara R., et al. Association of the incidence of atopic dermatitis until 3 years old with climate conditions in the first 6 months of life: Japan Environment and Children’s Study (JECS). PLoS One. 2022; 17 (5): e0268204. doi: 10.1371/journal.pone.0268204.
- Chatrath S., Lei D., Yousaf M., et al. Longitudinal course and predictors of depressive symptoms in atopic dermatitis. J. Am. Acad. Dermatol. 2022; 87 (3): 582-591. doi: 10.1016/j.jaad.2022.04.061.
- Cosmi L., Maggi L., Mazzoni A., et al. Biologicals targeting type 2 immunity: lessons learned from asthma, chronic urticaria and atopic dermatitis. Eur. J. Immunol. 2019; 49 (9): 1334-1343. doi: 10.1002/eji.201948156.
- Xie A., Chen A., Chen Y., et al. Lactobacillus for the treatment and prevention of atopic dermatitis: clinical and experimental evidence. Front. Cell. Infect. Microbiol. 2023; 13: 1137275. doi: 10.3389/fcimb.2023.1137275.
- Cairo C., Webb T.J. Effective barriers: the role of NKT cells and innate lymphoid cells in the gut. J. Immunol. 2022; 208 (2): 235-246. doi: 10.4049/jimmunol.2100799.
- Méndez C.S., Bueno S.M., Kalergis A.M. Contribution of gut microbiota to immune tolerance in infants. J. Immunol. Res. 2021; 2021: 7823316. doi: 10.1155/2021/7823316.
- Lee M.J., Park Y.M., Kim B., et al. Disordered development of gut microbiome interferes with the establishment of the gut ecosystem during early childhood with atopic dermatitis. Gut Microbes. 2022; 14 (1): 2068366. doi: 10.1080/19490976.2022.2068366.
- Kim J.H., Kim K., Kim W. Gut microbiota restoration through fecal microbiota transplantation: a new atopic dermatitis therapy. Exp. Mol. Med. 2021; 53 (5): 907-916. doi: 10.1038/s12276-021-00627-6.
- Galazzo G., van Best N., Bervoets L., et al. Development of the microbiota and associations with birth mode, diet, and atopic disorders
in a longitudinal analysis of stool samples, collected from infancy through early childhood. Gastroenterology. 2020; 158 (6): 1584-1596. doi: 10.1053/j.gastro.2020.01.024. - Rusu E., Enache G., Cursaru R., et al. Prebiotics and probiotics in atopic dermatitis. Exp. Ther. Med. 2019; 18 (2): 926-931. doi: 10.3892/etm.2019.7678.
- Umborowati M.A., Damayanti D., Anggraeni S., et al. The role of probiotics in the treatment of adult atopic dermatitis: a meta-analysis of randomized controlled trials. J. Health Popul. Nutr. 2022; 41 (1): 37. doi: 10.1186/s41043-022-00318-6.
- Huang R., Ning H., Shen M., et al. Probiotics for the treatment of atopic dermatitis in children: a systematic review and meta-analysis of randomized controlled trials. Front. Cell. Infect. Microbiol. 2017; 7: 392. doi: 10.3389/fcimb.2017.00392.
- Tanojo N., Citrashanty I., Utomo B., et al. Oral postbiotics derived from Lactobacillus sp. in treatment of atopic dermatitis: a meta-analysis. Acta Dermatovenerol. Alp. Pannonica Adriat. 2023; 32 (2): 41-47.
- Yin D.G., He Z., Duan X., et al. Effect of probiotic supplementation during pregnancy and infancy in preventing atopic dermatitis in children: a meta analysis. Zhongguo Dang Dai Er Ke Za Zhi. 2019; 21 (1): 82-88. doi: 10.7499/j.issn.1008-8830.2019.01.015.
- Wang F., Wu F., Chen H., et al. The effect of probiotics in the prevention of atopic dermatitis in children: a systematic review and meta-analysis. Transl. Pediatr. 2023; 12 (4): 731-748. doi: 10.21037/tp-23-200.
- Cukrowska B., Ceregra A., Maciorkowska E., et al. The effectiveness of probiotic Lactobacillus rhamnosus and Lactobacillus casei strains in children with atopic dermatitis and cow’s milk protein allergy: a multicenter, randomized, double blind, placebo controlled study. Nutrients. 2021; 13 (4): 1169. doi: 10.3390/nu13041169.
- Kalliomäki M., Salminen S., Poussa T., et al. Probiotics and prevention of atopic disease: 4-year follow-up of a randomised placebo-controlled trial. Lancet. 2003; 361 (9372): 1869-71. doi: 10.1016/S0140-6736(03)13490-3.
- Carucci L., Nocerino R., Paparo L., et al. Therapeutic effects elicited by the probiotic Lacticaseibacillus rhamnosus GG in children with atopic dermatitis. The results of the ProPAD trial. Pediatr. Allergy Immunol. 2022; 33 (8): e13836. doi: 10.1111/pai.13836.
- Voigt J., Lele M. Lactobacillus rhamnosus used in the perinatal period for the prevention of atopic dermatitis in infants: a systematic review and meta-analysis of randomized trials. Am. J. Clin. Dermatol. 2022; 23 (6): 801-811. doi: 10.1007/s40257-022-00723-x.
- Swanson K.S., Gibson G.R., Hutkins R., et al. The International Scientific Association for Probiotics and Prebiotics (ISAPP) consensus statement on the definition and scope of synbiotics. Nat. Rev. Gastroenterol. Hepatol. 2020; 17 (11): 687-701. doi: 10.1038/s41575-020-0344-2.
- Kim S., Han S.Y., Lee J., et al. Bifidobacterium longum and galactooligosaccharide improve skin barrier dysfunction and atopic dermatitis-like skin. Allergy Asthma Immunol. Res. 2022; 14 (5): 549-564. doi: 10.4168/aair.2022.14.5.549.
- Aldaghi M., Tehrani H., Karrabi M., et al. The effect of multistrain synbiotic and vitamin D3 supplements on the severity of atopic dermatitis among infants under 1 year of age: a double-blind, randomized clinical trial study. J. Dermatolog. Treat. 2022; 33 (2): 812-817. doi: 10.1080/09546634.2020.1782319.
- Ibáñez M.D., Rodríguez Del Río P., González-Segura Alsina D., et al. Effect of synbiotic supplementation on children with atopic dermatitis: an observational prospective study. Eur. J. Pediatr. 2018; 177 (12): 1851-1858. doi: 10.1007/s00431-018-3253-4.
- Chang Y.S., Trivedi M.K., Jha A., et al. Synbiotics for prevention and treatment of atopic dermatitis: a meta-analysis of randomized clinical trials. JAMA Pediatr. 2016; 170 (3): 236-42. doi: 10.1001/jamapediatrics.2015.3943.
- Hutchinson N.T., Wang S.S., Rund L., et al. Effects of an inulin fiber diet on the gut microbiome, colon, and inflammatory biomarkers in aged mice. Exp. Gerontol. 2023; 176: 112164. doi: 10.1016/j.exger.2023.112164.