Антигістамінні препарати в терапії алергічного риніту: місце в клінічних алгоритмах та раціональний вибір
Автор: Сергій Вікторович ЗАЙКОВ, доктор медичних наук, професор кафедри фтизіатрії та пульмонології Національного університету охорони здоров’я України ім. П.Л. Шупика (м. Київ), президент ВГО «Асоціація алергологів України»
 Алергічний риніт (АР) є поширеним хронічним захворюванням, яке суттєво впливає на якість життя, продуктивність праці та навчання, а також соціальну активність [1]. АР зумовлений IgE-опосередкованими реакціями на інгаляційні алергени, часто поєднується з кон’юнктивітом, бронхіальною астмою (БА), синуситом, обструктивним апное й іншими коморбідними станами та є глобальною проблемою охорони здоров’я.
Алергічний риніт (АР) є поширеним хронічним захворюванням, яке суттєво впливає на якість життя, продуктивність праці та навчання, а також соціальну активність [1]. АР зумовлений IgE-опосередкованими реакціями на інгаляційні алергени, часто поєднується з кон’юнктивітом, бронхіальною астмою (БА), синуситом, обструктивним апное й іншими коморбідними станами та є глобальною проблемою охорони здоров’я.
Клінічно АР проявляється чханням, закладеністю носа, свербежем і ринореєю [2]. За визначенням ECRHS (дослідження Європейської спілки щодо здоров’я дихальної системи), поширеність АР є варіативною (медіана становила 22,7% – від 7,0 до 47,5), і цей показник не стає меншим до сьогодні [3, 4].
Традиційний поділ АР на сезонний і цілорічний поступився місцем класифікації ARIA (Allergic Rhinitis and its Impact on Asthma), що враховує тривалість симптомів та їхній вплив на якість життя [5, 6].
Сезонний АР найчастіше відповідає інтермітивній формі за класифікацією ARIA. Проте частина пацієнтів із чутливістю до кількох сезонних алергенів з послідовним пилкуванням може мати симптоми протягом більшої частини року. Також у країнах з меншою вираженістю сезонів (теплим кліматом) може згладжуватися класична, притаманна країнам з контрастними порами року, сезонність пилкування.
Саме тому сучасні настанови рекомендують оцінювати не лише тригер, а й тривалість і тяжкість симптомів.
Класифікація АР за тривалістю симптомів:
- інтермітивний – симптоми тривають менш ніж 4 дні на тиждень або менш ніж 4 послідовні тижні;
- персистивний – симптоми тривають більш ніж 4 дні на тиждень і більш ніж 4 послідовні тижні.
Кожна з форм може мати легкий або помірно тяжкий / тяжкий перебіг залежно від наявності порушень сну, денної активності, навчання чи роботи.
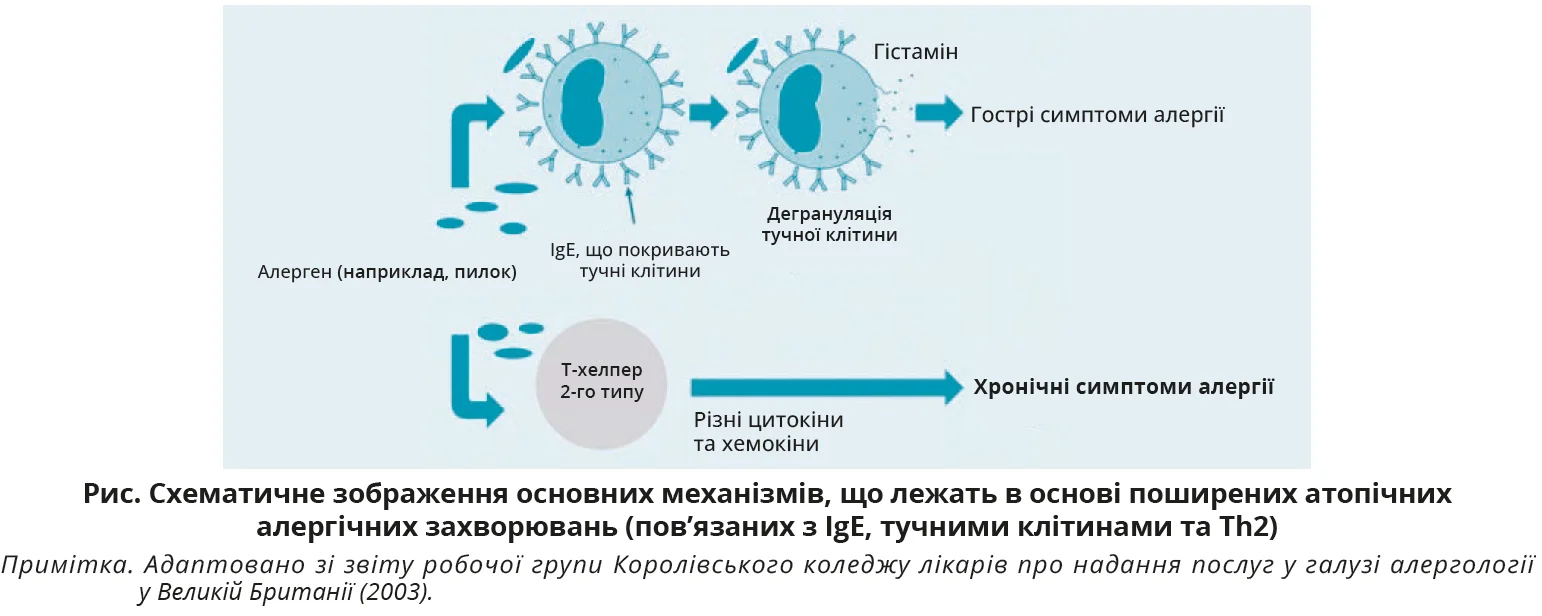
В основі патогенезу АР лежить IgE-опосередкована імунна відповідь на інгаляційні алергени в сенсибілізованих людей. При контакті з алергеном (пилок рослин, частинки пилових кліщів, спори цвілевих грибів та ін.) фіксований на поверхні тучних клітин IgE запускає їхню дегрануляцію з вивільненням гістаміну, лейкотрієнів та інших медіаторів (рис.).
Медіатори й цитокіни ранньої фази зумовлюють підвищення судинної проникності, чхання, ринорею, гіперсекрецію слизу та бронхоспазм. Ця рання фаза реакції розгортається протягом хвилин після контакту з алергеном. Гістамін, який вивільняється при дегрануляції тучних клітин, активує H1-рецептори та спричиняє основні симптоми АР. Це обґрунтовує застосування H1-антагоністів як одного з базових елементів симптоматичної терапії АР.
Проте не варто забувати про реакції пізньої фази, що зумовлюють тривале збереження симптомів. Через 4-8 годин відбувається повторна хвиля клітинної інфільтрації, що клінічно проявляється переважно стійкою закладеністю носа та нерідко зберігається тривалий час [6]. Унаслідок тривалого запалення, інфільтрації імунними клітинами слизова оболонка стає чутливішою до алергену та реагує яскравіше на подальший його вплив, а також стає гіперчутливою до іритантів і атмосферних змін [7]. Через це, наприклад, наприкінці сезону пилкування набагато менша кількість пилку може спричиняти таку саму або сильнішу реакцію, ніж на початку (феномен праймінгу).
Міжнародні рекомендації щодо ведення АР
Ініціатива ARIA регулярно оновлює рекомендації щодо ведення пацієнтів з АР: останню редакцію на основі методології GRADE та даних реальної клінічної практики було опубліковано 2019 року [8]. Додатково у 2024-2025 роках вийшла оновлена редакція з окремими рекомендаціями щодо інтраназальних препаратів [1].
У настанові ARIA 2019 року зазначається можливість використання покрокового підходу до лікування на підставі тяжкості симптомів:
- за легкого та помірно тяжкого АР – пероральні антигістамінні препарати ІІ покоління (АГП ІІ), особливо коли пацієнт віддає перевагу пероральним препаратам, або інтраназальні АГП (ІнАГП) за потреби;
- за помірно тяжких / тяжких симптомів – інтраназальні кортикостероїди (ІнКС) є препаратами першого вибору для лікування або в комбінації з ІнАГП;
- за недостатнього контролю – додатково алергенспецифічна імунотерапія.
Депо-кортикостероїди для внутрішньом’язового введення також не рекомендовано при АР у сучасних настановах.
Рекомендації Британського товариства алергології та клінічної імунології (BSACI, 2017), японські клінічні настанови 2020 року [9], канадські практичні рекомендації 2024 року [10] пропонують практичні алгоритми ведення АР, що збігаються з рекомендаціями ARIA.
Окремо підкреслюється раціональність регулярного використання АГП ІІ при персистивному риніті, а не за потреби.
Фармакотерапія АР: класи препаратів
- АГП ІІ посідають провідну позицію в симптоматичному лікуванні легкого та помірно тяжкого АР. Їхніми ключовими перевагами є:
- приймання 1 раз на добу (період напіввиведення АГП ІІ довший порівняно з I першим поколінням – 12-24 проти 4-12 годин);
- швидкий початок дії;
- мінімальний седативний ефект;
- відсутність значущих антихолінергічних властивостей і клінічно важливих взаємодій з іншими ліками;
- діють переважно на свербіння, чхання, ринорею, що є основними симптомами АР.
Велика частина пацієнтів перевагу віддає саме пероральній фармакотерапії, тому призначення АГП ІІ позитивно впливає на прихильність до лікування. До класу належать цетиризин, левоцетиризин, лоратадин, дезлоратадин, фексофенадин, ебастин, біластин, рупатадин. Незважаючи на спільний механізм дії, представники класу відрізняються фармакокінетикою, тривалістю дії та клінічним профілем.
- ІнКС є препаратами вибору при помірно тяжкому й персистивному АР завдяки потужній протизапальній дії. Вони ефективніші за АГП щодо усунення закладеності носа та загального контролю симптомів у тяжчих випадках. Водночас їм притаманний відтермінований початок дії (оптимальний ефект через 1-2 тижні регулярного застосування), що варто враховувати при призначенні.
- Місце комбінованої терапії: при недостатньому контролі симптомів на тлі монотерапії допускається поєднання перорального АГП з ІнКС.
Левоцетиризин: фармакологія та клінічна характеристика
Левоцетиризин – R-енантіомер цетиризину гідрохлориду, селективний антагоніст H1-рецепторів гістаміну ІІ покоління. Препарат міцніше зв’язується з H1-рецепторами та діє довше при нижчій дозі. Має високу біодоступність у разі перорального приймання, швидше всмоктується (забезпечує відчутний ефект уже через 1 годину), діє повні 24 години при прийманні 1 раз на добу.
Клінічні переваги
Клінічну ефективність левоцетиризину при інтермітивному та персистивному АР підтверджено в численних рандомізованих контрольованих дослідженнях і метааналізах. У метааналізі 7 подвійно сліпих плацебо-контрольованих досліджень левоцетиризин як монотерапія достовірно перевершував лоратадин у зменшенні загальної оцінки симптомів АР: розмір ефекту порівняно з плацебо становив -0,59 (95% довірчий інтервал (ДІ) від -0,89 до -0,29) для левоцетиризину проти -0,21 (95% ДІ від -0,31 до -0,1) для лоратадину [11].
Із практичного погляду левоцетиризин зменшував симптоми майже втричі ефективніше за лоратадин порівняно з ефектом плацебо. Для пацієнта це означає помітне полегшення: чхання, свербіж і нежить контролюються краще та надійніше.
У найбільшому на сьогодні мережевому метааналізі, що охопив дані понад 90 тисяч пацієнтів з АР, левоцетиризин виявився єдиним АГП, який достовірно перевершував інші препарати свого класу – дезлоратадин, ебастин і фексофенадин – за контролем як носових, так і очних симптомів [12]. Це клінічно важливо для пацієнтів з ринокон’юнктивітом, адже левоцетиризин діяв на обидва компоненти одночасно.
Також цікаво, що ефект монотерапії левоцетиризином виявився потужнішим, аніж комбінації цього АГП з ІнКС. Автори пояснюють це погіршенням прихильності при двошляховому режимі введення.
Швидкість початку та тривалість дії
Порівняльне дослідження в провокаційній камері показало, що левоцетиризин почав достовірно полегшувати симптоми вже через 1 годину, тоді як дезлоратадин – лише через 3 години. Через добу ефект левоцетиризину також залишався вираженішим [13].
Для пацієнта це може означати, що, прийнявши таблетку вранці перед виходом на вулицю, він може розраховувати на захист протягом усього дня.
В іншому дослідженні в провокаційній камері порівнювалася тривалість дії левоцетиризину та фексофенадину. Через 2 години після приймання ефективність обох препаратів була зіставною, але через 22-24 години середнє зменшення симптомів АР дорівнювало 5,1±0,3 бала після левоцетиризину проти 3,8±0,3 бала після фексофенадину: перевага левоцетиризину становила ≈1,3 раза (95% ДІ 0,7-1,9) і зберігалася до кінця спостереження (28 годин) [14].
Левоцетиризин демонструє зіставну ефективність з біластином, зберігаючи високий рівень безпеки та переносимості. У порівняльному рандомізованому дослідженні (Vanitha M. et al., 2020) левоцетиризин 5 мг не поступався біластину 20 мг за ефективністю: обидва препарати продемонстрували порівнянний ефект щодо загального бала назальних симптомів (TNSS), рівня IgE й абсолютної кількості еозинофілів у крові в пацієнтів з АР після 2 тижнів лікування (p>0,05) [15].
Вплив на якість життя
Дослідження XPERT – одне з найдовших у своєму класі: 551 пацієнт з персистивним АР отримував левоцетиризин або плацебо протягом 6 місяців. Уже через тиждень лікування пацієнти відзначали помітне покращення за такими аспектами якості життя: менше порушувався сон, краща денна активність, менше носових і очних симптомів [16]. Важливо, що покращення фіксувалося й за загальними показниками здоров’я (SF-36), тобто пацієнти почувалися краще не лише з огляду на носові симптоми, а й загалом.
Окрім того, аналіз економічних витрат (Yogesh D. et al., 2023) показав: лікування левоцетиризином скорочує втрати продуктивності на роботі, що актуально для роботодавців і загалом для системи охорони здоров’я [17].
Ефективність за коморбідності АР і БА
У пацієнтів з поєднанням АР і БА левоцетиризин продемонстрував ефект, важливий не лише для носових симптомів: уже з 2-го тижня лікування зменшилася кількість еозинофілів і нейтрофілів у назоцитограмі, що вказувало на протизапальну дію препарату. Протягом 8 тижнів препаратів порятунку (сальбутамол, кромолін) потребували лише 2 пацієнти групи активного лікування проти 13 у групі плацебо [18]. Це може свідчити про те, що ефективний контроль запалення у верхніх дихальних шляхах позитивно позначається й на перебігу БА.
Порівняльна ефективність АГП ІІ й ІнКС
Порівняння пероральних АГП ІІ й ІнКС є принципово важливим для лікаря-практика. ІнКС залишаються основним вибором для лікування помірно тяжкого та тяжкого персистивного АР, зокрема коли домінувальним симптомом є закладеність носа [14].
Водночас АГП ІІ мають низку переваг, що зумовлює їхню незамінність у клінічній практиці:
- швидкий початок дії: ефект настає вже через 1 годину після приймання, тоді як для ІнКС характерний поступовий розвиток ефекту протягом 1-2 тижнів;
- зручність застосування (1 таблетка 1 раз на добу) та високий профіль безпеки підвищують прихильність до лікування;
- ефективність проти очних симптомів (свербіж, сльозотеча), щодо яких ІнКС значно поступаються.
Використання АГП ІІ за показаннями в терапії АР укладається в ступінчастий підхід рекомендацій ARIA, даючи змогу враховувати вподобання пацієнта при легких і помірно тяжких формах АР.
Левоцетиризин є оптимальним вибором у таких клінічних ситуаціях:
- легкий або помірно тяжкий АР з домінуванням свербежу, чхання та ринореї;
- необхідність швидкого контролю симптомів (початок дії через ~1 годину);
- поєднання носових і очних симптомів (ринокон’юнктивіт);
- пацієнти, що потребують щоденної безпечної терапії АГП з мінімальним ризиком седації;
- превентивне (передсезонне) застосування для зменшення праймінгу та пом’якшення дебюту сезонних симптомів;
- пацієнти з коморбідними АР і кропив’янкою, АР і БА.
При недостатньому контролі симптомів на тлі монотерапії можливе поєднання левоцетиризину з ІнКС, насамперед у пацієнтів з вираженою закладеністю носа чи тяжчим перебігом АР.
Висновки
АР залишається однією з найпоширеніших хронічних хвороб з вираженим негативним впливом на якість життя пацієнтів.
Сучасні рекомендації ARIA, BSACI й інші підкреслюють необхідність індивідуалізованого ступінчастого лікування з огляду на тяжкість симптомів, провідні скарги та вподобання пацієнта.
Левоцетиризин як R-енантіомер цетиризину поєднує в собі переваги найновіших антигістамінних молекул: швидкий початок дії, тривалий ефект протягом 24 годин, відсутність седативного ефекту, низький потенціал фармакологічних взаємодій.
Левоцетиризин є препаратом вибору при легкому та помірно тяжкому сезонному АР, ринокон’юнктивіті, а також як компонент комбінованої терапії при тяжчих або персистивних формах захворювання.
Висока прихильність пацієнтів до терапії одним пероральним препаратом 1 раз на добу, доведений вплив на якість життя та фармакоекономічна ефективність зміцнюють позицію левоцетиризину як важливого елементу алгоритму лікування АР у щоденній практиці лікаря.
Література
- Sousa-Pinto B., Bousquet J., Vieira R.J., et al. Allergic Rhinitis and Its Impact on Asthma (ARIA)-EAACI guideline 2024-2025 revision: part I – guidelines on intranasal treatments. Allergy. 2025; 0: 1-23. doi: 10.1111/all.70131.
- Bousquet J., Anto J.M., Bachert C., et al. Allergic rhinitis. Nat. Rev. Dis. Primers. 2020 Dec 3; 6 (1): 95. doi: 10.1038/s41572-020-00227-0. PMID: 33273461.
- Campello C., Ferrari M., Poli A., et al. Prevalence of asthma and asthma-like symptoms in an adult population sample from Verona. ECRHS Verona. European Community Respiratory Health Survey. Monaldi Arch. Chest Dis. 1998 Oct; 53 (5): 505-509. PMID: 9861808.
- Savouré M., Bousquet J., Jaakkola J.J.K., et al. Worldwide prevalence of rhinitis in adults: a review of definitions and temporal evolution. Clin. Transl. Allergy. 2022 Mar; 12 (3): e12130. doi: 10.1002/clt2.12130. PMID: 35344304; PMCID: PMC8967272.
- Bousquet J.J., Schünemann H.J., Togias A., et al. Next-generation ARIA care pathways for rhinitis and asthma: a model for multimorbid chronic diseases. Clin. Transl. Allergy. 2019 Sep 9; 9: 44. doi: 10.1186/s13601-019-0279-2. PMID: 31516692; PMCID: PMC6734297.
- Rosenfield L., Keith P.K., Quirt J., et al. Allergic rhinitis. Allergy Asthma Clin. Immunol. 2024; 20 (Suppl. 3): 74. doi: 10.1186/s13223-024-00923-6.
- Sin B., Togias A. Pathophysiology of allergic and nonallergic rhinitis. Proc. Am. Thorac. Soc. 2011 Mar; 8 (1): 106-114. doi: 10.1513/pats.201008-057RN. PMID: 21364228.
- Klimek L., Bachert C., Pfaar O., et al. ARIA guideline 2019: treatment of allergic rhinitis in the German health system. Allergol. Select. 2019 Dec 30; 3 (1): 22-50. doi: 10.5414/ALX02120E. PMID: 32176226; PMCID: PMC7066682.
- Okano M., Fujieda S., Gotoh M., et al. Executive summary: Japanese guidelines for allergic rhinitis 2020. Allergol. Int. 2023; 72 (1): 41-53. doi: 10.1016/j.alit.2022.11.003.
- Ellis A.K., Cook V., Keith P.K., et al. Focused allergic rhinitis practice parameter for Canada. Allergy Asthma Clin. Immunol. 2024 Aug 8; 20 (1): 45. doi: 10.1186/s13223-024-00899-3. PMID: 39118164; PMCID: PMC11311964.
- Mösges R., König V., Köberlein J. The effectiveness of levocetirizine in comparison with loratadine in treatment of allergic rhinitis – a meta-analysis. Allergol. Int. 2011 Dec; 60 (4): 541-546. doi: 10.2332/allergolint.10-OA-0300. Epub 2011 Sep 25. PMID: 21918368.
- Mösges R., König V., Köberlein J. The effectiveness of modern antihistamines for treatment of allergic rhinitis – an IPD meta-analysis of 140,853 patients. Allergol. Int. 2013 Jun; 62 (2): 215-222. doi: 10.2332/allergolint.12-OA-0486. Epub 2013 Mar 25. PMID: 23524648.
- Day J.H., Briscoe M.P., Rafeiro E., Ratz J.D. Comparative clinical efficacy, onset and duration of action of levocetirizine and desloratadine for symptoms of seasonal allergic rhinitis in subjects evaluated in the Environmental Exposure Unit (EEU). Int. J. Clin. Pract. 2004 Feb; 58 (2): 109-118. doi: 10.1111/j.1368-5031.2004.0117.x. PMID: 15055856.
- Horak F., Zieglmayer P.U., Zieglmayer R., et al. Levocetirizine has a longer duration of action on improving total nasal symptoms score than fexofenadine after single administration. Br. J. Clin. Pharmacol. 2005 Jul; 60 (1): 24-31. doi: 10.1111/j.1365-2125.2005.02377.x. PMID: 15963090; PMCID: PMC1884902.
- Vanitha M., Sowmini K., Santha Sheela Kumari K., Resu Neha Reddy. Efficacy of oral bilastine in comparison with levocetirizine in allergic rhinitis: a randomised clinical study. Journal of Clinical and Diagnostic Research. 2021 Aug; 15 (8): FC01-FC04.
- Canonica G.W., Bousquet J., Van Hammée G., et al.; XPERT study group. Levocetirizine improves health-related quality of life and health status in persistent allergic rhinitis. Respir. Med. 2006 Oct; 100 (10): 1706-1715. doi: 10.1016/j.rmed.2006.03.039. Epub 2006 May 24. PMID: 16723217.
- Yogesh D., Tanush S., Roheet R., et al. Effectiveness of levocetirizine in treating allergic rhinitis while retaining work efficiency. Arch. Asthma Allergy Immunol. 2023; 7: 005-011.
- Pasquali M., Baiardini I., Rogkakou A., et al. Levocetirizine in persistent allergic rhinitis and asthma: effects on symptoms, quality of life and inflammatory parameters. Clin. Exp. Allergy. 2006 Sep; 36 (9): 1161-1167. doi: 10.1111/j.1365-2222.2006.02548.x. PMID: 16961716.