Антигістамінні препарати другого покоління: ключова роль у лікуванні алергічного риніту
 Автор: Сергій Вікторович ЗАЙКОВ, доктор медичних наук, професор кафедри фтизіатрії і пульмонології Національного університету охорони здоров’я України ім. П.Л. Шупика (м. Київ), президент ВГО «Асоціація алергологів України»
Автор: Сергій Вікторович ЗАЙКОВ, доктор медичних наук, професор кафедри фтизіатрії і пульмонології Національного університету охорони здоров’я України ім. П.Л. Шупика (м. Київ), президент ВГО «Асоціація алергологів України»
Алергічний риніт (АР) виникає внаслідок опосередкованої імуноглобулінами (Ig) E відповіді на інгальовані алергени й характеризується чханням, закладеністю носа, свербежем носа та ринореєю.
Цій хворобі властиві значний несприятливий вплив на якість життя, сон, робочу та навчальну працездатність, емоційний стан, соціальні взаємодії, а також часте сполучення з такими коморбідними станами, як кон’юнктивіт і бронхіальна астма (БА). Коморбідностями АР також виступають випітний середній отит, синусит, ларингіт, обструктивне апное сну, бруксизм і навіть порушення оклюзії зубів [1, 2, 6].
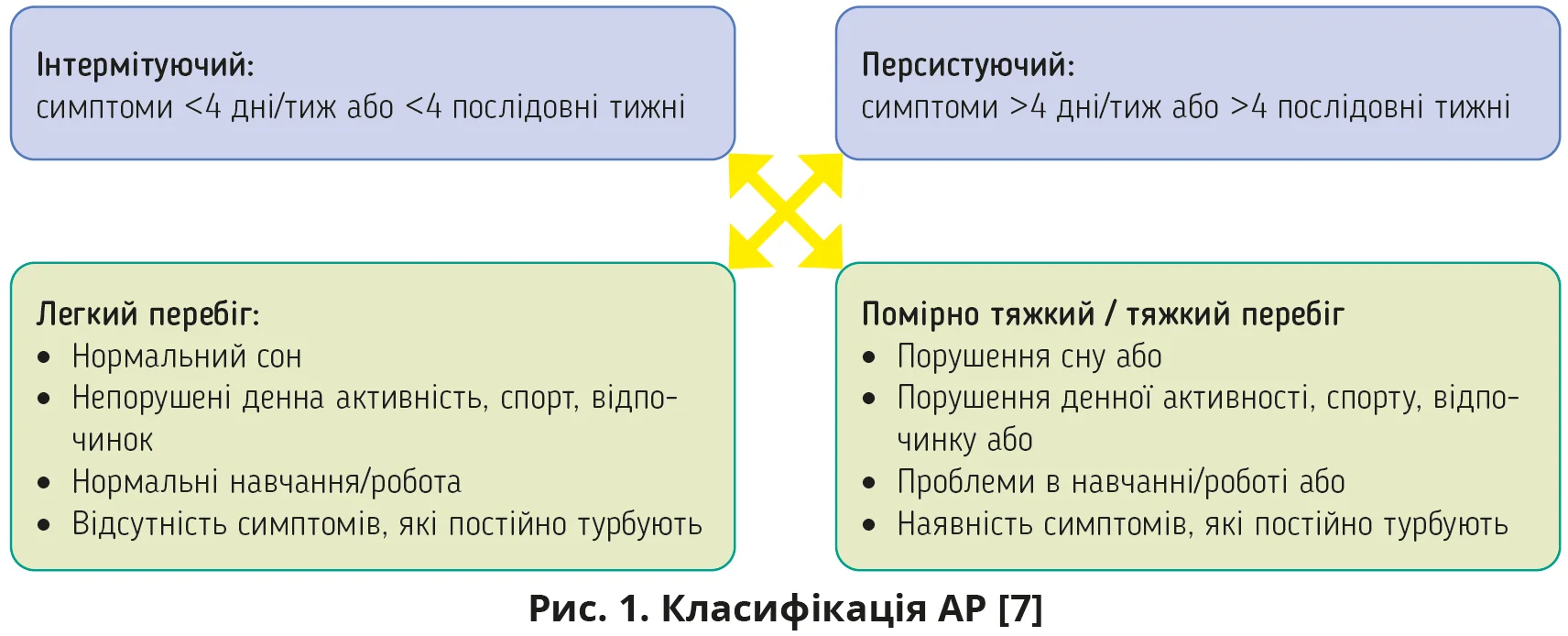
Раніше АР поділяли на сезонний і цілорічний, але з огляду на значну поширеність полісенсибілізації ініціатива ARIA («АР і його вплив на БА») запропонувала натомість поділ на інтермітуючий і персистуючий АР (рис. 1). Також виділяють два додаткові класи АР: професійний, асоційований з алергенами робочого місця, та локальний з доказами вироблення IgE слизовою оболонкою носа без системної атопії [1, 2].
АР є загальносвітовою проблемою, оскільки його поширеність у деяких країнах сягає 50%.
Наприклад, за даними дослідження ECRHS (35 центрів, 15 країн), поширеність АР у пацієнтів віком 20-44 роки становить від 11,8 до 46,0% [1]. Цікаво, що серед чоловіків АР поширеніший до статевого дозрівання, а серед жінок – після. Зафіксовано й інші статеві відмінності в патогенезі, перебігу та коморбідностях АР (рис. 2) [2].
Порівняно з 1960-ми рр. поширеність АР у всьому світі значно зросла. Експерти пов’язують цю епідеміологічну тенденцію з атопією – схильністю виробляти антитіла класу IgE у відповідь на різні чинники довкілля [1].
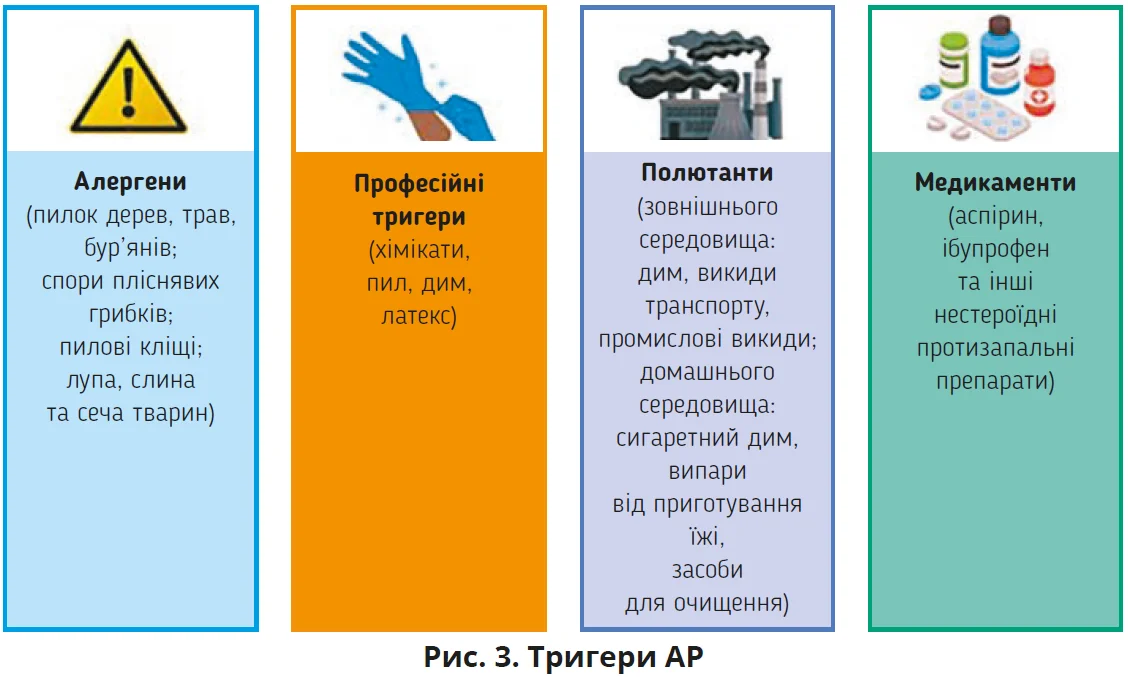
Факторами ризику АР виступають уживання антибіотиків, забруднення повітря, контакт зі свійськими тваринами, котами та собаками, куріння батьків. Більшість цих факторів ризику також збільшують імовірність розвитку БА й атопічного дерматиту [1]. Тригери АР, які безпосередньо спричиняють клінічну симптоматику, поділяють на кілька груп: алергени, професійні тригери, полютанти та фармакопрепарати (рис. 3) [6].
Патогенез АР передбачає не лише гостру реакцію на контакт з алергеном, а й так звані реакції пізньої фази, котрі зумовлюють тривале збереження симптомів. Часті повторні контакти з алергеном спричиняють іще один притаманний АР феномен – так званий праймінг, суть якого полягає в тому, що з часом алергічну реакцію провокує дедалі менша кількість алергену. Наприклад, наприкінці сезону пилкування пацієнти з АР реагують уже на дуже малі кількості пилку в повітрі. Праймінг зумовлений накопиченням опасистих клітин і базофілів у слизовій оболонці носа та гіперреактивністю назальної слизової оболонки [1].
Окремою проблемою, яку не слід недооцінювати, є АР у дітей. У віці 2-3 років симптоми АР спостерігаються приблизно у 20% дитячого населення, у віці до 6 років – у 40%, у підлітковому періоді – в 30%. У дітей АР часто спричиняє втомлюваність, зменшує тривалість концентрації уваги, погіршує пам’ять і здатність до навчання, що батьки нерідко помилково трактують як поведінкові розлади [4].
За відсутності лікування АР не лише погіршує фізичний і психосоціальний стан дитини, а й може спричиняти розвиток таких тяжких наслідків, як БА, синусит і середній отит [13].
Лікування АР передбачає уникнення алергенів, застосування Н1-антигістамінних препаратів (АГП), інтраназальних глюкокортикостероїдів і алергенспецифічної імунотерапії. Незважаючи на різні можливості лікування, значна кількість пацієнтів залишається незадоволеною, оскільки абсолютне вилікування неможливе, а закріплений лікар не завжди враховує особисті побажання пацієнта. Для ефективного лікування АР потрібний високий ступінь прихильності, проте значна кількість пацієнтів не дотримується рекомендацій лікаря й тому не отримує бажаного результату [1].
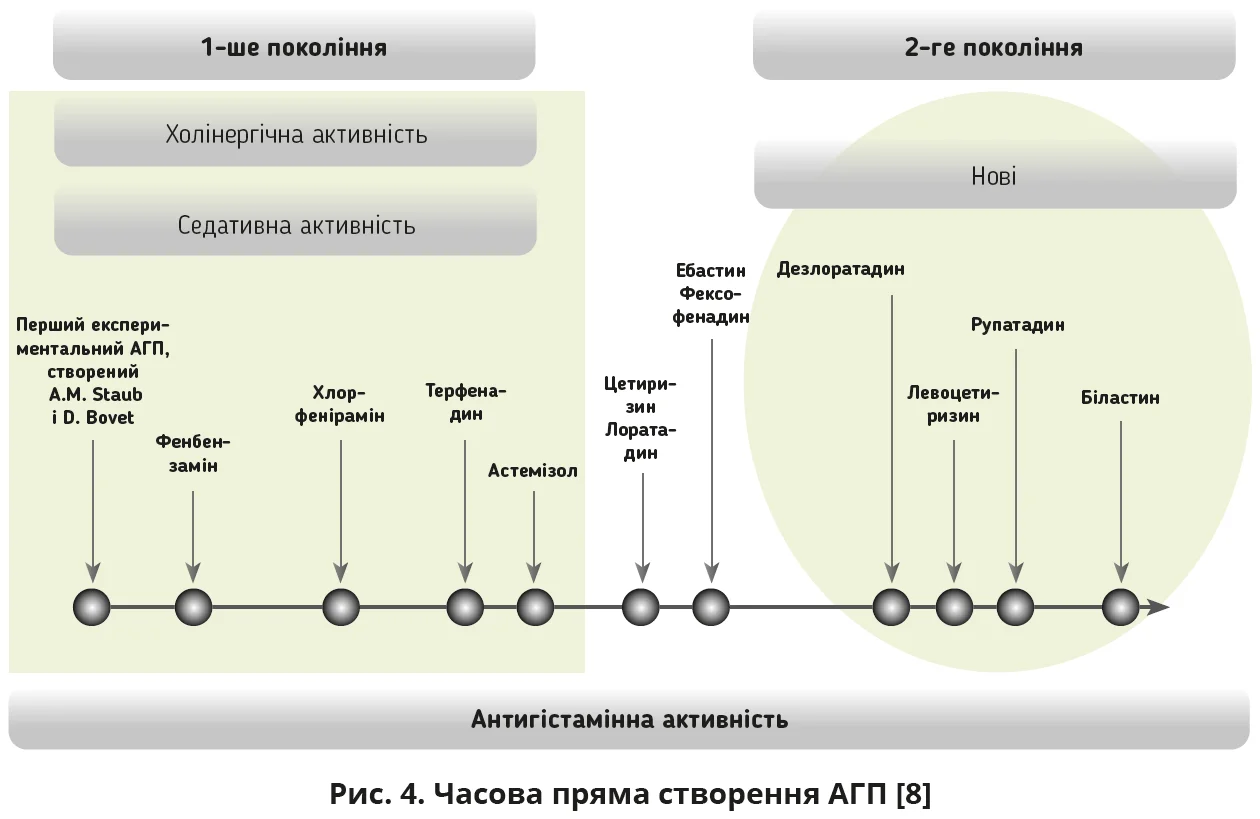
Одну з провідних позицій у лікуванні АР посідають пероральні АГП. Окрім високої ефективності, перевагами цих препаратів є застосування 1 раз на добу, швидке настання ефекту. До того ж велика частина пацієнтів віддає перевагу саме пероральній фармакотерапії. Різним представникам класу пероральних АГП притаманні різні хімічна структура, фармакокінетика й потенціал взаємодій з іншими ліками та продуктами харчування. Традиційно АГП поділяють на два покоління [1, 3, 5]. Однією з останніх синтезованих молекул АГП є левоцетиризин (рис. 4) – R-енантіомер цетиризину гідрохлориду, який продемонстрував відмінні показники ефективності та безпеки при лікуванні АР і хронічної кропив’янки в дорослих і дітей у низці досліджень і великих метааналізів.
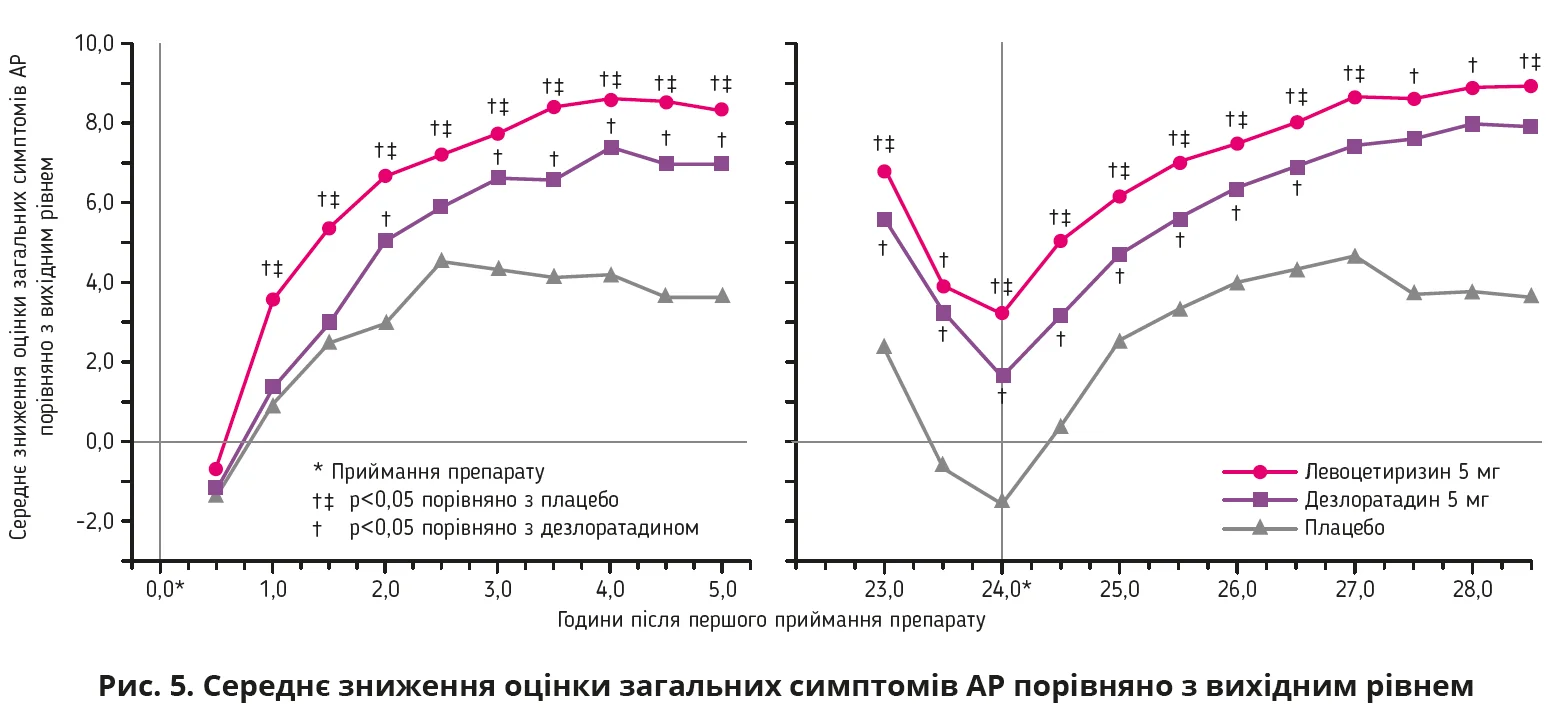
Наприклад, один із цих метааналізів продемонстрував, що в пацієнтів з АР левоцетиризину слід віддавати перевагу над дезлоратадином, оскільки левоцетиризину властиві швидший початок дії та стійкіший ефект [9]. Порівняння левоцетиризину з дезлоратадином, проведене в камері для провокаційних алергопроб, виявило, що левоцетиризин починає діяти через 1 годину, а дезлоратадин – лише через 3 години. Крім того, через 24 години після застосування препарату ефект левоцетиризину є вираженішим (рис. 5) [19].
За даними іншого масштабного метааналізу (n=18 014), левоцетиризин характеризувався меншою кількістю проявів седації та менш вираженою зміною часу реакції порівняно з АГП 1-го покоління [10]. Метааналіз 7 подвійно сліпих плацебоконтрольованих досліджень виявив, що як монотерапія левоцетиризин є достовірно ефективнішим за лоратадин у зменшенні загальної оцінки симптомів АР. За підрахунками авторів метааналізу, розмір ефекту порівняно з плацебо для левоцетиризину становив -0,59 (95% довірчий інтервал [ДІ] від -0,89 до -0,29), а для лоратадину – лише -0,21 (95% ДІ від -0,31 до -0,1) [17].
Надважливим елементом доказової бази левоцетиризину є метааналіз даних понад 90 тисяч пацієнтів, у якому левоцетиризин виявився єдиним АГП, що продемонстрував значущу перевагу над іншими (дезлоратадином, ебастином, фексофенадином) за загальною шкалою назальних симптомів АР (Total Nasal Symptoms Score, TNSS) і загальною шкалою очних симптомів АР (Total Ocular Symptoms Score, TOSS). Автори радять застосовувати при АР, особливо в тяжких випадках, монотерапію левоцетиризином, оскільки її ефект виявився навіть потужнішим за комбінацію цього ж АГП з інтраназальними глюкокортикостероїдами. На думку науковців, такий парадоксальний висновок пояснюється погіршенням прихильності на тлі застосування двох препаратів з різними шляхами введення (рис. 6) [11]. Слід зауважити, що перевага левоцетиризину над фексофенадином може бути зумовлена більшою тривалістю дії першого. За даними дослідження, проведеного в провокаційних камерах, через 2 години після приймання цих АГП покращення було приблизно однаковим, але через 22-24 години середнє зменшення провідних симптомів АР (ринорея, чхання, свербіж очей і носа) становило 1,9±0,3 бала після вживання плацебо, 3,8±0,3 бала після вживання фексофенадину та 5,1±0,3 бала після вживання левоцетиризину. Отже, левоцетиризин був приблизно в 1,3 раза (95% ДІ 0,7-1,9) ефективнішим за фексофенадин. Ця перевага зберігалася до кінця спостереження (28 годин) [18].
Оскільки проявам АР властива певна варіабельність протягом доби, зокрема посилення симптоматики вночі та рано-вранці, запропоновано застосовувати левоцетиризин увечері. За даними D. Yogesh і співавт. (2023), вечірнє призначення левоцетиризину в дозі 5 або 10 мг забезпечувало контроль симптомів протягом 24 годин і відсутність значущого впливу на сонливість протягом дня та денну активність.
Ба більше, було зафіксовано сприятливий вплив лікування левоцетиризином на робочу продуктивність (за індексом порушень робочої продуктивності й активності – Work Productivity and Activity Impairment, WPAI). Левоцетиризин достовірно зменшував вираженість основних симптомів АР: закладеності носа, назального свербежу, чхання, виділень з носа [14].
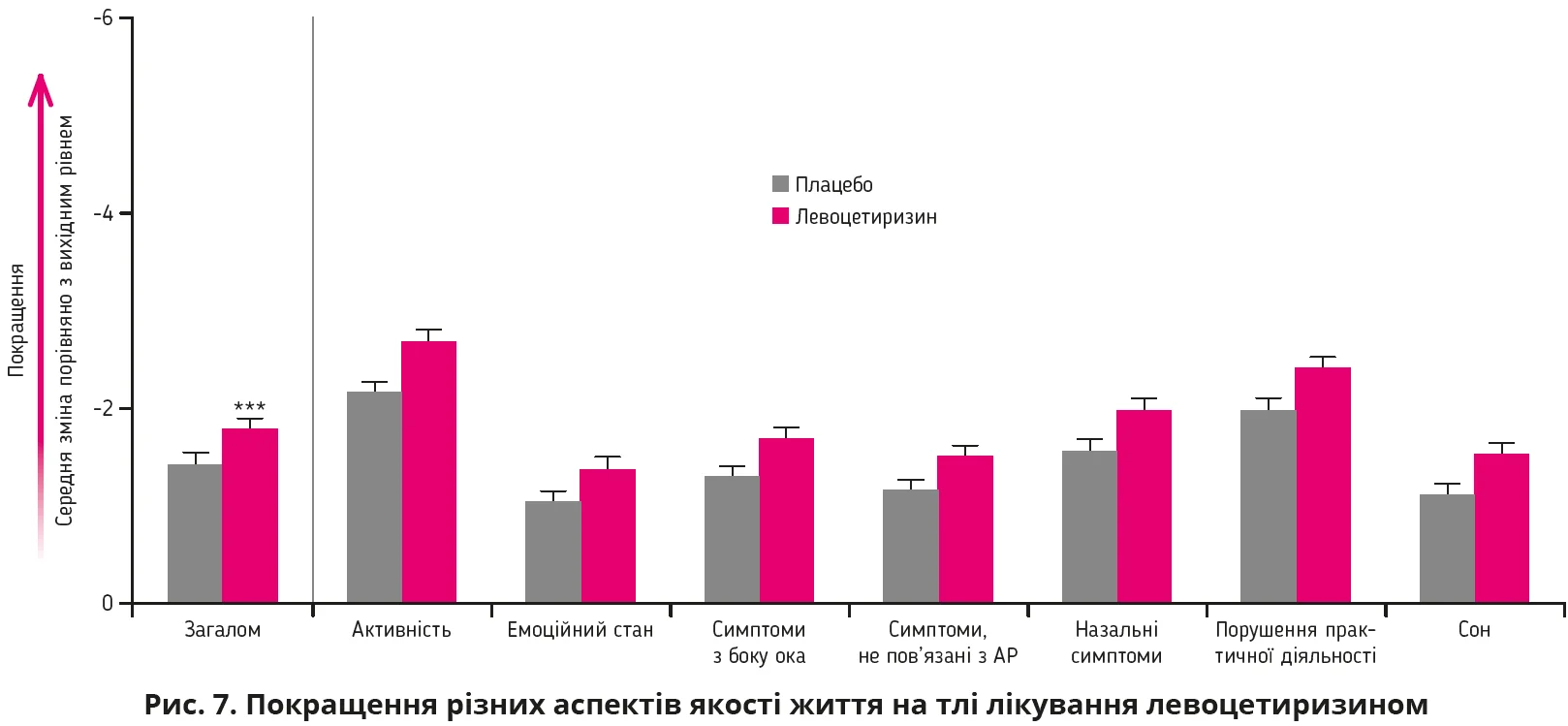
Провідною метою ведення пацієнта з АР є усунення тих розладів і симптомів, які вважає значущими сам пацієнт. Вважається, що при оцінюванні ефективності терапії вплив на якість життя має навіть більше значення, ніж безпосередньо тяжкість симптомів хвороби. Передусім це стосується персистуючого АР, при якому симптоми за визначенням є хронічними та значно погіршують загальну якість життя пацієнта. У дослідженні XPERT оцінювався довгостроковий вплив левоцетиризину на якість життя та загальний стан здоров’я пацієнтів з персистуючим АР. Для оцінювання якості життя застосовувалися два найпоширеніші валідовані опитувальники – RQLQ (Rhinoconjunctivitis Quality of Life Questionnaire – спеціалізована анкета щодо якості життя пацієнтів з ринокон’юнктивітом) і SF-36 (Short Form Health Survey – короткий опитувальник щодо стану здоров’я). Лікування левоцетиризином достовірно покращувало оцінку за RQLQ порівняно з плацебо вже через 1 тиждень. Водночас спостерігалося покращення як фізичного, так і психічного компонента здоров’я за SF-36 (рис. 7) [15].
Левоцетиризин також продемонстрував свою ефективність у пацієнтів з типовим кластером коморбідності – поєднанням АР і БА. Вже на другий тиждень лікування різниця у вираженості симптомів між групами левоцетиризину та плацебо стала достовірною й залишалася такою до кінця дослідження. Важливо, що в назальних мазках пацієнтів групи левоцетиризину зменшилася кількість еозинофілів і нейтрофілів – це свідчить про протизапальну дію. Протягом 8 тижнів дослідження препаратів порятунку (сальбутамол, кромолін) потребували лише 2 пацієнти групи левоцетиризину та 13 осіб групи плацебо. Автори дійшли висновку, що левоцетиризин здатен забезпечити контроль симптомів і покращення якості життя в пацієнтів з комбінацією АР і БА [16].
Загалом левоцетиризину властиві сприятливі фармакодинамічні й фармакокінетичні характеристики, зокрема швидкий початок дії, висока біодоступність, добрі показники афінності та здатності захоплювати Н1-рецептори, обмежений розподіл в організмі, мінімальний печінковий метаболізм, мала кількість побічних ефектів. На додачу до застосування левоцетиризину для усунення короткотермінових проявів алергічних хвороб активно поширюється тренд використання цього препарату як довгострокової терапії. Однією з причин цього є те, що для левоцетиризину продемонстровано протизапальний ефект in vitro й in vivo.
Механізм цього ефекту дотепер остаточно не вивчений, але вважається, що в його основі лежить пригнічення експресії молекул адгезії ендотеліальними клітинами [12].
Отже, левоцетиризин можна вважати одним з оптимальних пероральних АГП для лікування АР.
Фармакодинамічні та фармакокінетичні переваги, швидке настання ефекту, здатність усувати назальні й очні симптоми АР, а також низький потенціал седації та міжлікарських взаємодій виводять левоцетиризин на провідну позицію серед представників свого класу.
Література
- Bousquet J., Anto J.M., Bachert C., Baiardini I., Bosnic-Anticevich S., et al. Allergic rhinitis. Nat. Rev. Dis. Primers. 2020; 6 (1): 95. doi: 10.1038/s41572-020-00227-0.
- De Carli M., Capezzali E., Tonon S., Frossi B. Mechanism and clinical evidence of immunotherapy in allergic rhinitis. Front. Allergy. 2023; 4: 1217388. doi: 10.3389/falgy.2023.1217388.
- Oppenheimer J.J., Casale T.B. Next generation antihistamines: therapeutic rationale, accomplishments and advances. Expert Opin. Investig. Drugs. 2002; 11 (6): 807-817. doi: 10.1517/13543784.11.6.807.
- Cheng M., Dai Q., Liu Z., Wang Y., Zhou C. New progress in pediatric allergic rhinitis. Front. Immunol. 2024; 15: 1452410. doi: 10.3389/fimmu.2024.1452410.
- Sur D.K., Plesa M.L. Treatment of allergic rhinitis. Am. Fam. Physician. 2015; 92 (11): 985-992.
- Narasimhan R., Roy S., Koralla M., et al. Expert panel consensus recommendations for allergic rhinitis in patients with asthma in India. Pulm. Ther. 2024. doi: 10.1007/s41030-024-00273-z.
- Rosenfield L., Keith P.K., Quirt J., et al. Allergic rhinitis. Allergy Asthma Clin. Immunol. 2024; 20 (Suppl. 3): 74. doi: 10.1186/s13223-024-00923-6.
- Kuna P., Jurkiewicz D., Czarnecka-Operacz M.M., et al. The role and choice criteria of antihistamines in allergy management – expert opinion. Postepy Dermatol. Alergol. 2016 Dec; 33 (6): 397-410. doi: 10.5114/pdia.2016.63942.
- Passalacqua G., Canonica G.W. A review of the evidence from comparative studies of levocetirizine and desloratadine for the symptoms of allergic rhinitis. Clin. Ther. 2005 Jul; 27 (7): 979-992. doi: 10.1016/j.clinthera.2005.07.011. Erratum in: Clin. Ther. 2005 Oct; 27 (10): 1669.
- Snidvongs K., Seresirikachorn K., Khattiyawittayakun L., Chitsuthipakorn W. Sedative effects of levocetirizine: a systematic review and meta-analysis of randomized controlled studies. Drugs. 2017; 77 (2): 175-186. doi: 10.1007/s40265-016-0682-0.
- Mösges R., König V., Köberlein J. The effectiveness of modern antihistamines for treatment of allergic rhinitis – an IPD meta-analysis of 140,853 patients. Allergol. Int. 2013 Jun; 62 (2): 215-222. doi: 10.2332/allergolint.12-OA-0486.
- Walsh G.M. The anti-inflammatory effects of levocetirizine – are they clinically relevant or just an interesting additional effect? Allergy Asthma Clin. Immunol. 2009 Dec 17; 5 (1): 14. doi: 10.1186/1710-1492-5-14.
- Fireman P. Therapeutic approaches to allergic rhinitis: treating the child. J. Allergy Clin. Immunol. 2000; 105 (6 Pt. 2): S616-621. doi: 10.1067/mai.2000.106152.
- Yogesh D., Tanush S., Roheet R., Akhila P., Chaitanya V.K., et al. Effectiveness of levocetirizine in treating allergic rhinitis while retaining work efficiency. Arch. Asthma Allergy Immunol. 2023; 7: 005-011.
- Walter Canonica G., Bousquet J., Van Hammée G., et al.; XPERT Study Group. Levocetirizine improves health-related quality of life and health status in persistent allergic rhinitis. Respir. Med. 2006; 100 (10): 1706-1715. doi: 10.1016/j.rmed.2006.03.039.
- Pasquali M., Baiardini I., Rogkakou A., Riccio A.M., Gamalero C., et al. Levocetirizine in persistent allergic rhinitis and asthma: effects on symptoms, quality of life and inflammatory parameters. Clin. Exp. Allergy. 2006; 36 (9): 1161-1167. doi: 10.1111/j.1365-2222.2006.02548.x.
- Mösges R., König V., Köberlein J. The effectiveness of levocetirizine in comparison with loratadine in treatment of allergic rhinitis – a meta-analysis. Allergol. Int. 2011; 60 (4): 541-546. doi: 10.2332/allergolint.10-OA-0300.
- Horak F., Zieglmayer P.U., Zieglmayer R., Kavina A., Lemell P. Levocetirizine has a longer duration of action on improving total nasal symptoms score than fexofenadine after single administration. Br. J. Clin. Pharmacol. 2005; 60 (1): 24-31. doi: 10.1111/j.1365-2125.2005.02377.x.
- Day J.H., Briscoe M.P., Rafeiro E., Ratz J.D. Comparative clinical efficacy, onset and duration of action of levocetirizine and desloratadine for symptoms of seasonal allergic rhinitis in subjects evaluated in the Environmental Exposure Unit (EEU). Int. J. Clin. Pract. 2004; 58 (2): 109-118. doi: 10.1111/j.1368-5031.2004.0117.x.