Алгоритми в алергології: патогенез, діагностика та лікування хронічної спонтанної кропив’янки
Переклала й адаптувала д-р мед. наук Лариса Стрільчук
Хронічна кропив’янка (ХК), яку визначають як кропив’янку тривалістю понад 6 тижнів, поділяється на індуковану та хронічну спонтанну (ХСК).
Індукованим кропив’янкам властиві наявність початкового ініціювального стимулу, часто фізичного, а також інтермітивний перебіг, хоча загальна тривалість симптомів може становити багато років. Натомість ХСК притаманні хронічний перебіг, наявність уртикарних висипок у більшість днів тижня та відсутність екзогенної причини. Алгоритм діагностики ХСК представлено на рисунку 1.
Ангіонабряк, який зазвичай асоціюється з ХСК, уражає обличчя, кінцівки, геніталії, губи, язик і рідко глотку, але не гортань, тому ризик асфіксії є нульовим. ХСК тісно пов’язана з автоімунними процесами, зокрема з перехресним зв’язуванням антитіл класу імуноглобулінів (Ig) G з вільними рецепторами до IgE на опасистих клітинах і базофілах із подальшою активацією цих клітин і секрецією гістаміну, лейкотрієнів, цитокінів і хемокінів. Окрім того, активується система комплементу та вивільнення компоненту C5a додатково підсилює секреторні властивості опасистих клітин.
Існує також другий сценарій, за якого в пацієнтів наявні антитіла класу IgE до широкого спектра автоантигенів, включаючи тиреопероксидазу й інтерлейкін-24. Однак те, які саме антитіла є патогенними, дотепер не встановлено. Клінічно цей сценарій характеризується одночасною наявністю інших автоімунних розладів, передусім тиреоїдиту Хашімото. Антитиреоїдні антитіла (наприклад, IgG до мікросомального антигену та тиреоглобуліну) визначаються у 25% пацієнтів незалежно від тиреоїдного статусу. У цій популяції пацієнтів спостерігається підвищений уміст загальних IgE, хоча він є набагато нижчим, аніж за умов астми чи атопічного дерматиту. Можуть також спостерігатися низькі або дуже низькі рівні IgE; такі пацієнти гірше відповідають на омалізумаб.
Окрім вивільнення хімічних медіаторів з опасистих клітин і базофілів, активується також зовнішній каскад коагуляції, хоча асоціація з тромбозом відсутня. Фактор Xa та тромбін можуть безпосередньо розщеплювати компонент С5із вивільненням С5а, якому притаманна й анафілатоксична активність, і хемотаксична. Взаємодія фактора Ха та тромбіну з PAR-рецепторами здатна підвищувати проникність судин незалежно від вивільнення медіаторів опасистих клітин. Стимуляція ендотеліальних клітин гістаміном (наприклад) запускає секрецію ендотеліальними клітинами цитокінів і хемокінів, а також урокінази або тканинного активатора плазміногену. Ці ферменти перетворюють плазміноген на плазмін, а розщеплення фібрину призводить до підвищення вмісту D-димерів за цієї хвороби.
Ці процеси, однак, не є специфічними для ХСК.
ХСК асоціюється з появою навколо малих венул шкіри ненекротичного периваскулярного інфільтрату, який містить нейтрофіли, еозинофіли, базофіли, моноцити та Т-лімфоцити (переважно СD4+ із переважанням Т-хелперів 2-го типу над Т-хелперами 1-го типу).
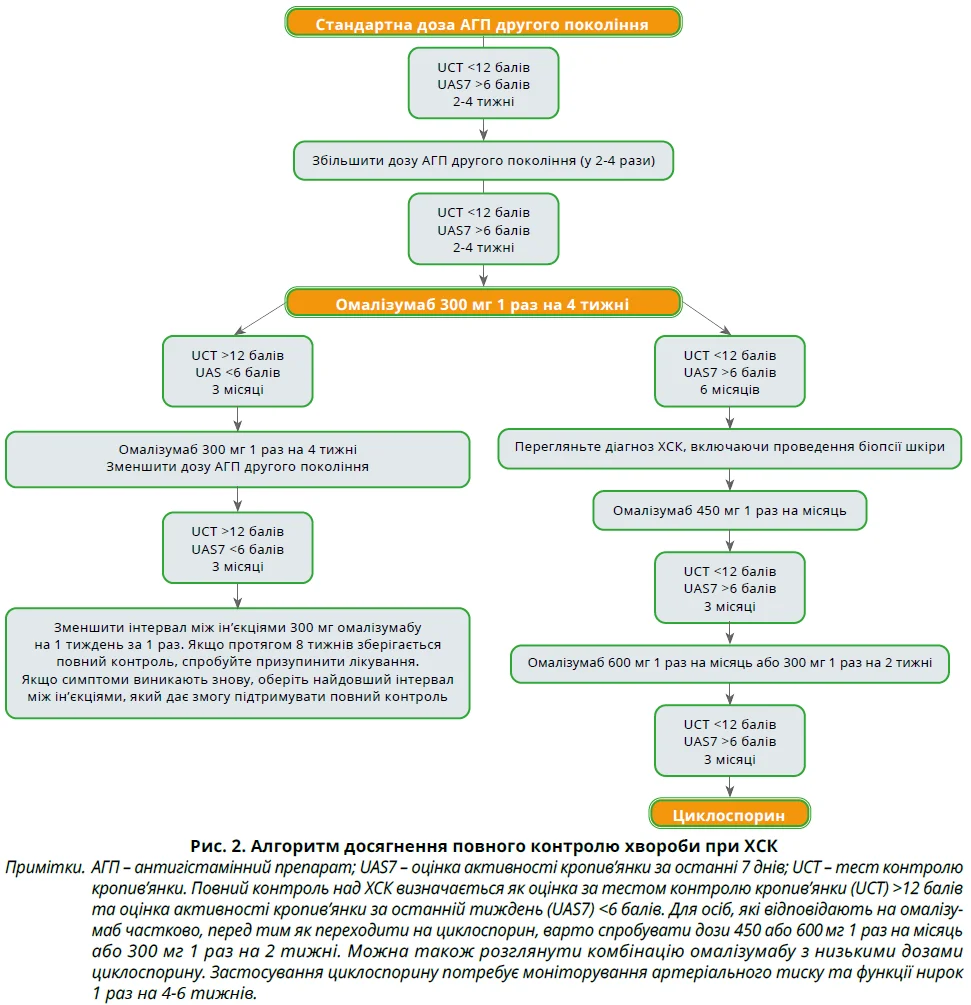
Лікування ХСК узагальнено на рисунку 2.
Загалом рекомендовано три види фармакотерапії: високі дози антигістамінних препаратів (АГП), омалізумаб і циклоспорин. Вивчається також низка нових засобів із відмінними від попередніх препаратів механізмами дії, як-от інгібітори секреції та/або дозрівання опасистих клітин.
У разі невдачі лікування АГП (близько 50% випадків) рекомендовано розпочати лікування омалізумабом, ефективність якого в таких випадках сягає 65-70%. Загалом АГП або омалізумаб дають можливість досягти успіху терапії у 80% пацієнтів. Третім кроком алгоритму лікування є циклоспорин, дієвий приблизно в 70% пацієнтів, які не відповіли на попередні два етапи лікування. Циклоспорин пригнічує Т-лімфоцити в інфільтраті, а також інгібує секрецію базофілів та опасистих клітин, впливаючи на кальциневрин.
Значна частка препаратів, які застосовувалися для лікування кропив’янки в минулому, вже не рекомендуються, оскільки частка успіху лікування була занадто низькою, а дослідження – занадто малими або недосконалими за дизайном. До таких препаратів належать Н2-АГП, антагоністи лейкотрієнів, сульфасалазин, метотрексат, гідроксихлорохін і дапсон.
Один із найсучасніших АГП – біластин (Ніксар, «Берлін-Хемі Менаріні АГ», Німеччина) – є високоселективним до Н1-гістамінових рецепторів препаратом, схваленим для симптоматичного лікування кропив’янки й алергічного ринокон’юнктивіту в дорослих і дітей від 12 років у багатьох країнах світу.
Біластин не є структурним похідним, метаболітом або енантіомером якогось іншого АГП, натомість він являє собою оригінальну молекулу, створену з метою виконання всіх вимог до ідеального АГП другого покоління (Holgate S.T. et al., 2003). Біластин не метаболізується в клітинах печінки та не пригнічує й не індукує активність ізоферментів цитохрому P450. Йому також притаманне повільне виведення з організму; період напіврозпаду препарату становить 10-14 годин (Sologuren A. et al., 2009). Біластину властива дозозалежна тривала антигістамінна активність, а також додаткова здатність інгібувати вивільнення інтерлейкіну-4 та фактора некрозу пухлин-α з опасистих клітин і гранулоцитів крові (Jáuregui I. et al., 2013).
У дослідженні R. Antonijoan і співавт. (2017) здорових добровольців рандомізували в групи біластину (20 мг), дезлоратадину (5 мг), рупатадину (10 мг) і плацебо. В учасників провокували алергічну відповідь шляхом інтрадермальної ін’єкції 5 мкг гістаміну й оцінювали наслідки через 0,5; 1; 2; 4; 6; 9; 12 і 24 години. Біластин пригнічував алергічну реакцію вже через 1 годину, натомість значуще інгібування висипів і свербежу за допомогою дезлоратадину та рупатадину спостерігалося лише через 4 години. На відміну від останніх, біластин достовірно зменшував свербіж порівняно з плацебо.
Клінічні дослідження III фази продемонстрували, що при ХК біластин у дозі 20 мг на добу є ефективнішим за плацебо щодо усунення симптомів, покращення якості життя та контролю розладів сну (Zuberbier T. et al., 2010). Зокрема, подвійне сліпе рандомізоване дослідження за участю пацієнтів із ХК виявило, що біластин має перевагу над плацебо в усіх досліджуваних дозах (10, 20 і 30 мг), ефективно зменшує загальну оцінку симптомів, інтенсивність свербежу та кількість/діаметр уртикарних висипань (Audicana M.T. et al., 2007). Клінічне дослідження фази III підтвердило ефективність біластину (20 мг) при ХСК (зниження загальної оцінки симптомів на 4,23 бала в групі біластину та на 2,99 бала в групі плацебо; p<0,001). Результат лікування біластином був зіставним із показниками для левоцетиризину та не залежав від статі, віку й етнічної приналежності пацієнта (Sadaba B. et al., 2011).
Важливо, що біластину властивий відмінний профіль безпеки, передусім відсутність впливу на серцеву провідність, пильність і здатність керувати автомобілем, причому цей вплив відсутній і при перевищенні терапевтичної дози вдвічі (Scaglione F., 2012). Оскільки гістамін є нейротрансмітером, що бере участь у контролі циклів сну та неспання, процесів уваги, пам’яті й навчання, регуляції голоду, АГП можуть мати несприятливий вплив на ці процеси. Ступінь цього несприятливого впливу залежить від здатності препаратів проходити крізь гематоенцефалічний бар’єр і зв’язуватися з центральними Н1-рецепторами. Своєю чергою, ця здатність залежить від ліпофільності препарату, його молекулярної маси й афінності до Р-глікопротеїну. Біластин практично не проникає в тканини мозку, що було підтверджено численними експериментальними та клінічними (із застосуванням позитронно-емісійної томографії) дослідженнями, не впливає на психомоторні функції та не взаємодіє з алкоголем (Jáuregui I. et al., 2013).
Отже, біластин (Ніксар) являє собою новий високоселективний Н1-АГП, який відповідає багатьом властивостям потужних АГП другого покоління. Біластин зменшує активність кропив’янки, знижуючи вираженість симптомів і покращуючи якість життя. Профіль побічних ефектів біластину відповідає показникам плацебо; цей препарат не впливає на серцеву провідність, пильність і здатність керувати автомобілем, навіть у дозах до 40 мг. Біластин успішно застосовується при різних видах кропив’янки: гострій і хронічній, спонтанній та індукованій. Відсутність метаболізму в організмі та збалансований профіль виведення (67% із калом, 33% із сечею) зумовлює відсутність потреби в корекції дози біластину (Jáuregui I. et al., 2013).
Література
Kaplan A.P., Ferrer M. Algorithms in allergy: diagnosis, pathogenesis, and treatment of chronic spontaneous urticaria. Allergy. 2024. doi: 10.1111/all.16113.