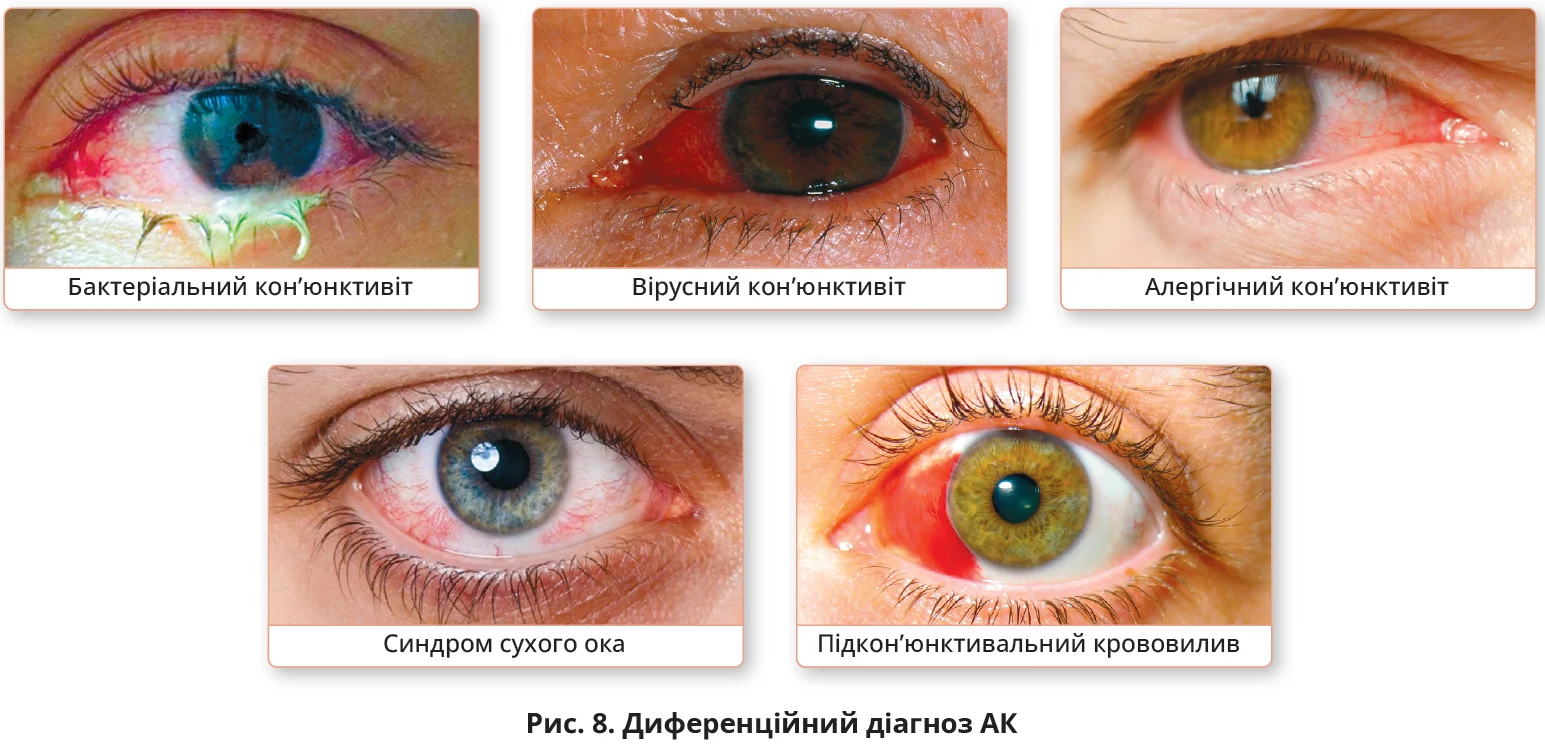
Алергічний кон’юнктивіт: офтальмологічні аспекти, принципи лікування
Автор: Сергій Вікторович ЗАЙКОВ, доктор медичних наук, професор кафедри фтизіатрії і пульмонології Національного університету охорони здоров’я України ім. П.Л. Шупика (м. Київ), президент ВГО «Асоціація алергологів України»
 Алергія справедливо вважається хворобою цивілізації, оскільки її поширеність неухильно зростає, особливо в урбанізованих районах [1]. За підрахунками, від алергії може страждати від 10 до 30% населення планети [2]. За даними Європейської академії алергології та клінічної імунології, 30% європейців мають симптоми алергії, причому майже половина випадків не діагностується [3]. За даними Національного центру статистики охорони здоров’я Центру контролю та профілактики захворювань США, станом на 2021 рік майже 1 із 3 дорослих та понад 1 із 4 дітей мали прояви сезонної алергії, екземи або харчової алергії [4, 5]. Схожа статистика спостерігається і в Україні: поширеність алергічних захворювань у різних регіонах становить 15-30%, останніми роками відзначається тенденція до збільшення кількості пацієнтів з алергією [6, 7].
Алергія справедливо вважається хворобою цивілізації, оскільки її поширеність неухильно зростає, особливо в урбанізованих районах [1]. За підрахунками, від алергії може страждати від 10 до 30% населення планети [2]. За даними Європейської академії алергології та клінічної імунології, 30% європейців мають симптоми алергії, причому майже половина випадків не діагностується [3]. За даними Національного центру статистики охорони здоров’я Центру контролю та профілактики захворювань США, станом на 2021 рік майже 1 із 3 дорослих та понад 1 із 4 дітей мали прояви сезонної алергії, екземи або харчової алергії [4, 5]. Схожа статистика спостерігається і в Україні: поширеність алергічних захворювань у різних регіонах становить 15-30%, останніми роками відзначається тенденція до збільшення кількості пацієнтів з алергією [6, 7].
Точні цифри алергічного ураження очей достеменно не встановлено ні у світі, ні в Україні з декількох причин. По-перше, недостатня діагностика. Пацієнти часто займаються самолікуванням і не звертаються по медичну допомогу з приводу очних симптомів, що призводить до поганого контролю симптомів, зниження якості життя та продуктивності праці [8]. По-друге, більшість алергічних уражень очей насправді є доброякісними та не становлять загрози для життя на відміну від анафілактичних реакцій або бронхіальної астми, а отже, недооцінюються. По-третє, більшість пацієнтів з алергічними ураженнями очей мають інші прояви алергії, як-от сезонний або цілорічний алергічний риніт, астму, екзему (атопічний дерматит), кропив’янку, медикаментозну, харчову або інсектну алергію, еозинофільний езофагіт, на тлі яких алергічний кон’юнктивіт (АК) часто не береться до уваги як самостійна значуща алергічна хвороба [9-11]. Відомо, що понад 90% осіб з алергією мають супутнє ураження очей і лише 6% – ізольовані очні симптоми [9]. Для прикладу, 44% дітей і 20% дорослих з астмою мають симптоми АК [12]. Отже, очним проявам приділяється значно менше уваги порівняно з іншими алергічними хворобами. Через недостатню обізнаність як пацієнтів, так і медичних працівників діагностика й лікування цих станів залишаються неадекватними [13]. Врешті, алергічні ураження очей є доволі неоднорідною групою, про що йтиметься далі. Вчасне виявлення й обґрунтоване лікування мають важливе значення для забезпечення контролю хвороби, швидкого полегшення симптомів і запобігання ускладненням, зокрема інфікуванню, помутнінню рогівки, васкуліту, які призводять до істотного зниження гостроти зору. Як гострий, так і затяжний перебіг АК значно погіршує якість життя пацієнтів [13].
Цей огляд присвячено найпоширенішій формі алергічного ураження очей – АК і включає обговорення епідеміології, патофізіології, клінічних особливостей, діагностики, варіантів лікування з акцентом на топічні засоби та підкреслює важливу роль співпраці різних фахівців для покращення догляду за пацієнтами.
Визначення та чинники ризику
АК – це гостре інтермітивне або хронічне запалення кон’юнктиви, спричинене причинно-значущим алергеном у сенсибілізованих людей.
Око зазнає постійного впливу екзогенних чинників, зокрема пилкових алергенів, епідермісу й екскрементів тварин і птахів, алергенів пліснявих і дріжджоподібних грибів і домашнього пилу (кліщі роду Dermatophagoides). Рідше АК пов’язаний із сенсибілізацією до харчових, медикаментозних і хімічних алергенів [13]. Певне значення можуть мати інфекції дихальних шляхів, які виснажують неспецифічні та специфічні чинники захисту, спричиняючи додаткову сенсибілізацію [14]. До відомих чинників ризику АК відносять також використання контактних лінз, очних протезів або накладання офтальмологічних швів [15]. Гіперчутливість до тих чи інших алергенів може бути генетично детермінована [16]. Певне значення мають також пренатальний вплив парацетамолу та недостатність вітаміну D
у постнатальному періоді [17, 18].
Епідеміологія
Епідеміологія алергічних захворювань очей на сьогодні вивчена недостатньо. За оцінками, від очних проявів алергії страждає від 5 до 22% населення залежно ід географічного положення та віку досліджуваної популяції [19]. У Сполучених Штатах Національне дослідження здоров’я та харчування III (NHANES III) виявило, що очні симптоми, визначені як «епізоди сльозотечі та свербіння очей», уражають 40% дорослого населення [20].
В Італії серед пацієнтів, які відвідали алергологічну клініку, симптоми АК виявлено в 40% осіб, із них у 66% також було діагностовано сезонний алергічний риніт [21]. Дослідження, проведене в Японії, виявило АК у 90% пацієнтів з алергією на пилок [22]. Що стосується віку, то спостерігаються два піки захворюваності на АК: перший – у віці до 15 років, другий – у віці 35-40 років [23].
Вплив аероалергенів (епітелій тварин, кліщі, пилок, гриби) частіше спричиняє очні симптоми, ніж носові [20]. Для сенсибілізації до епідермальних і кліщових алергенів характерне погіршення під час безпосереднього контакту з алергеном (прибирання приміщення, робота в бібліотеці, гра з тваринами) та покращення при перебуванні на свіжому повітрі. У разі грибкової сенсибілізації симптоми АК можуть спостерігатися впродовж усього теплого періоду року, але найчастіше в березні-квітні та вересні, коли спороутворення грибів максимальне; симптоми погіршуються при контакті з прілим сіном або травою, при перебуванні в сирих приміщеннях із поганою вентиляцією та вживанні харчових продуктів, які зазнали ферментації (сири, дріжджове тісто, квас, пиво). У разі пилкової алергії очні симптоми часто переважають у період цвітіння, коли концентрація пилку в довкіллі найвища; стан погіршується при перебуванні на природі або на вулиці, особливо в суху вітряну погоду, але покращується після дощу та в закритих приміщеннях. Симптоми також можуть погіршуватися при вживанні харчових продуктів, які містять перехресні алергени з пилком рослин або при використанні косметичних засобів чи ліків, які містять рослинні компоненти. Нещодавно проведене дослідження в Україні серед пацієнтів віком 19-45 років із сезонним алергічним ринокон’юнктивітом виявило, що дві третини пацієнтів сенсибілізовані до харчових алергенів, які у своїй структурі містять перехресні алергени з амброзією (шоколад, яйця, диня, кавун, кабачки, баклажани, огірки, капуста), третина пацієнтів була сенсибілізована до епідермальних алергенів домашнього пилу, шерсті собаки або кішки [14].
Класифікація
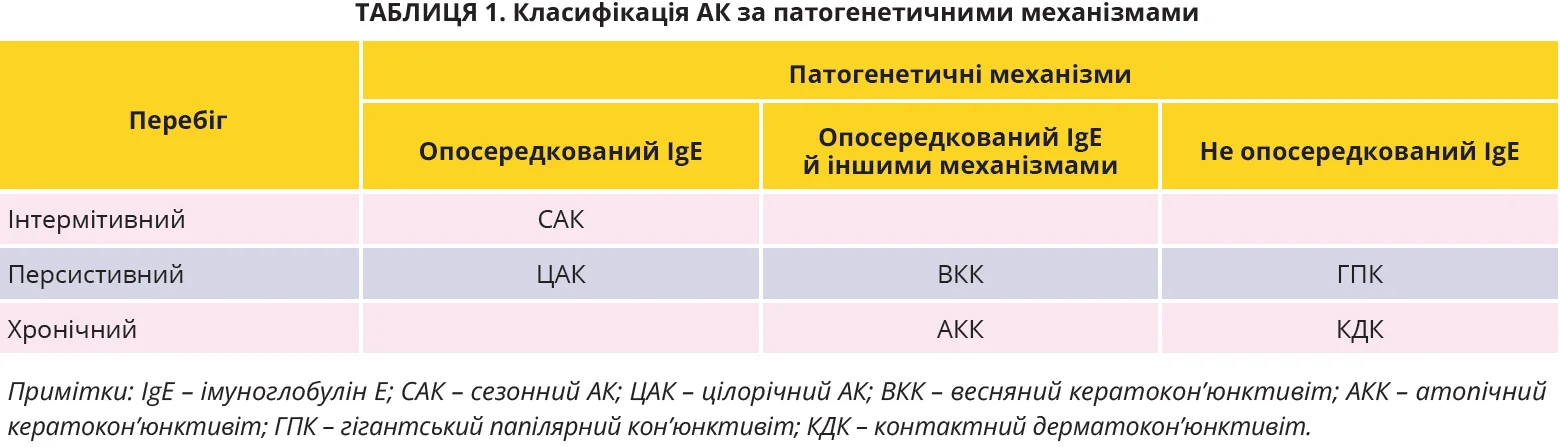
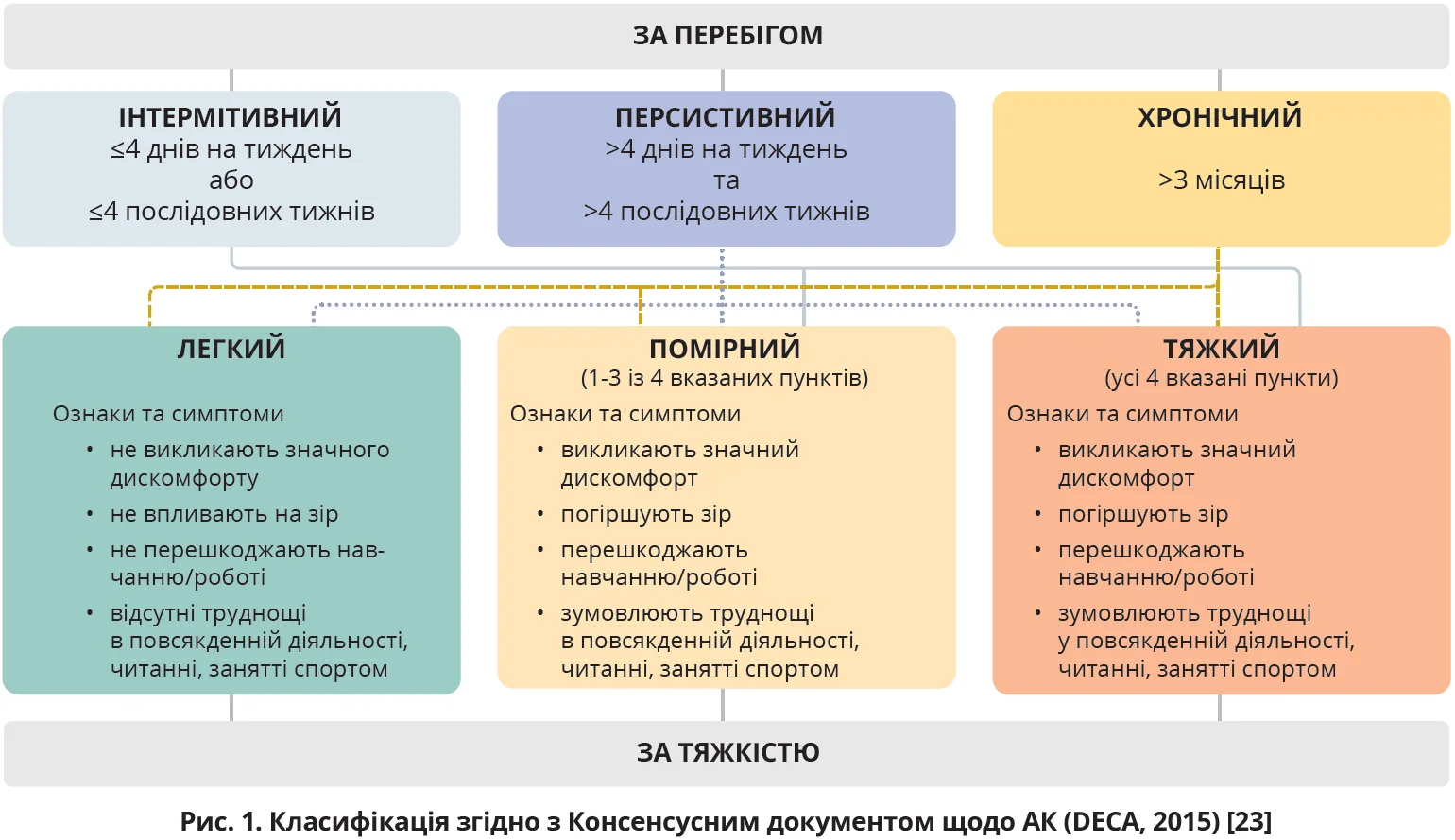
Єдиної класифікації АК не існує. Запропоновано класифікацію за перебігом і тяжкістю (рис. 1), а також патофізіологічними механізмами (табл. 1).
Патофізіологія
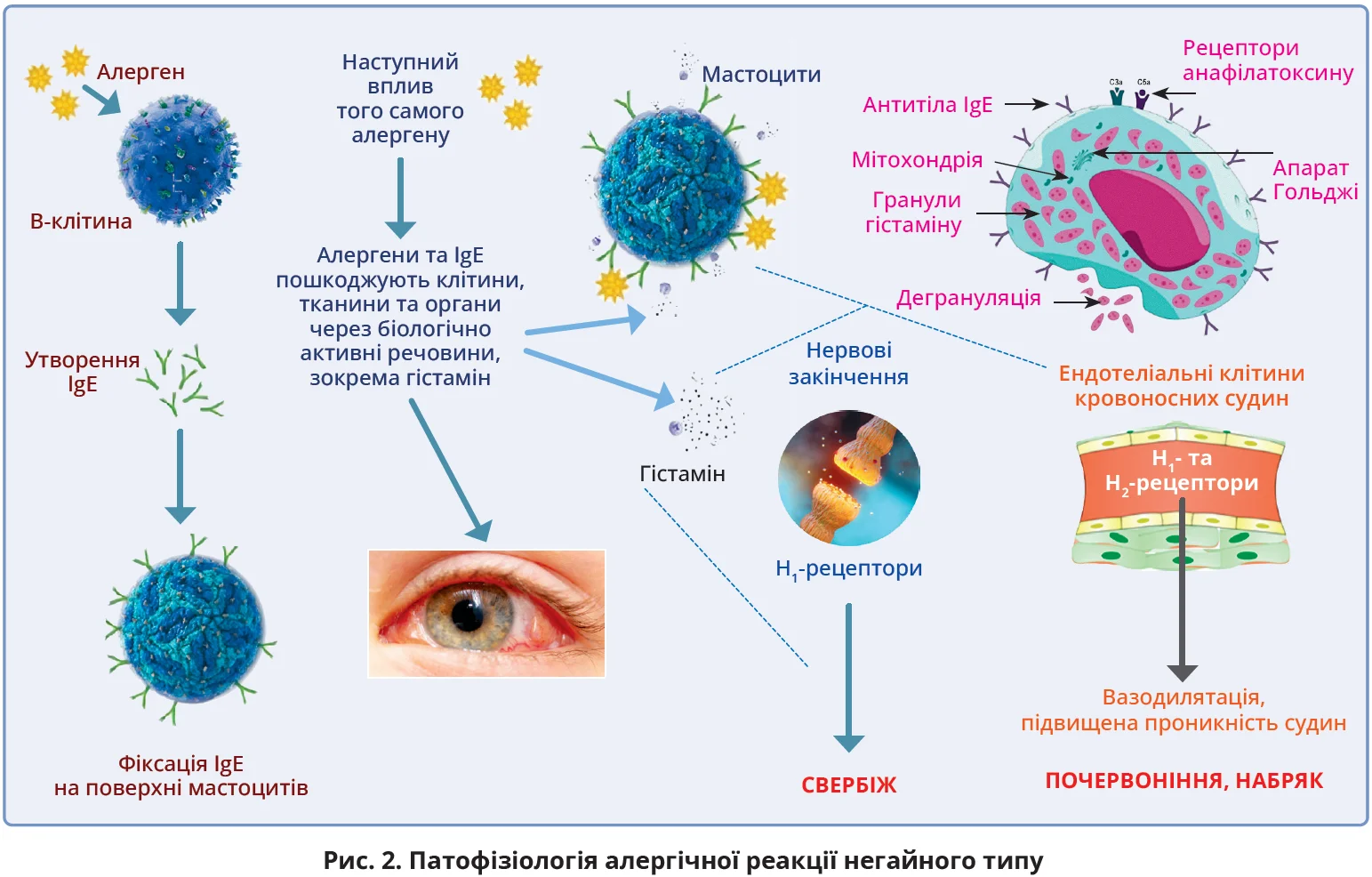
Зазвичай АК – це двобічний запальний процес, що іноді минає самостійно після елімінації причинних алергенів. Запалення часто спричинене IgE-опосередкованим імунним механізмом або механізмом негайної гіперчутливості внаслідок прямого контакту алергену з поверхнею кон’юнктиви в сенсибілізованих пацієнтів, що зумовлює активацію тучних клітин, відомих також як мастоцити, лаброцити або тканинні базофіли, з вивільненням різних медіаторів, насамперед гістаміну (рис. 2) [23]. Проте певну роль у запальному процесі можуть відігравати й інші механізми та медіатори, зокрема нейрогенні механізми, молекули адгезії й інші системні імунні механізми [24].
Механізм гіперчутливості негайного типу
В ініціації алергічного процесу важливу роль відіграють антигенпрезентувальні клітини – кон’юнктивальні макрофаги, дендритні клітини тощо [25, 26]. Коли алерген разом із молекулами гістосумісності ІІ класу контактує з CD4+ Т-лімфоцитами (Th), популяція Th2-лімфоцитів розширюється та виділяє низку цитокінів, які сприяють синтезу В-лімфоцитами специфічних IgE, а також секреції цитокінів (IL-4, IL-13), які полегшують ріст і диференціацію В-клітин. Синтезований специфічний IgE зв’язується з мембраною тучних клітин кон’юнктиви через специфічні високоафінні рецептори FcεRI (рис. 2) [23]. Зауважимо, що кон’юнктива людського ока містить 50 млн мастоцитів [27].
Новий контакт з алергеном супроводжується його зв’язуванням із двома специфічними молекулами IgE на поверхні мастоцитів, що зумовлює дегрануляцію та вивільнення різних медіаторів алергічної реакції негайного типу (рис. 2). Деякі з цих медіаторів попередньо сформовані та пов’язані з гранулами, наприклад гістамін, протеоглікани (гепарин, хондроїтину сульфат), нейтральні протеази (триптаза, хімаза), кислотні гідролази або певні окислювальні ферменти, тоді як інші синтезуються de novo, наприклад ліпідні медіатори (простагландини, лейкотрієни), тромбоцитарний фактор (PAF), певні інтерлейкіни (IL-4, IL-5, IL-6, IL-8, IL-13) і фактор некрозу пухлини-α (TNF-α) [23].
Пізня відповідь здебільшого залежить від залучення й активації еозинофілів і Т-лімфоцитів [28]. За сезонного й цілорічного АК розвиток пізньої фази різниться серед пацієнтів. У деяких випадках реакція відбувається за класичною схемою, коли через 4-8 годин після контакту з алергеном клінічні симптоми з’являються знову та спостерігається другий пік концентрації медіатора. В інших випадках симптоми можуть бути постійними або періодичними. Імовірно, така мінливість залежить від інтенсивності негайної реакції. Провокації низькими дозами алергену часто призводять до негайних реакцій, які обмежуються самостійно, натомість провокації високими дозами алергену або провокації у високочутливих осіб викликають інтенсивнішу та тривалішу відповідь із залученням клітинних механізмів і розвитком пізньої відповіді [29].
Для чіткого розуміння всіх механізмів пізньої відповіді в оці потрібні подальші дослідження.
Найважливішу роль у патогенезі АК відіграють мастоцити. Як клітини-мішені алергії, вони є джерелом цілого спектра медіаторів, зокрема гістаміну, які визначають клінічну картину гострого АК.
В організмі людини виявлено чотири класи гістамінових рецепторів, два з них – в оці (H1 та H2). Зв’язування гістаміну з H1-рецепторами на нервових закінченнях спричиняє свербіж. Зв’язування гістаміну з Н1– та Н2-рецепторами клітин ендотелію зумовлює вазодилятацію, підвищення проникності судин, що клінічно проявляється набряком і почервонінням (рис. 2).
Клінічна картина
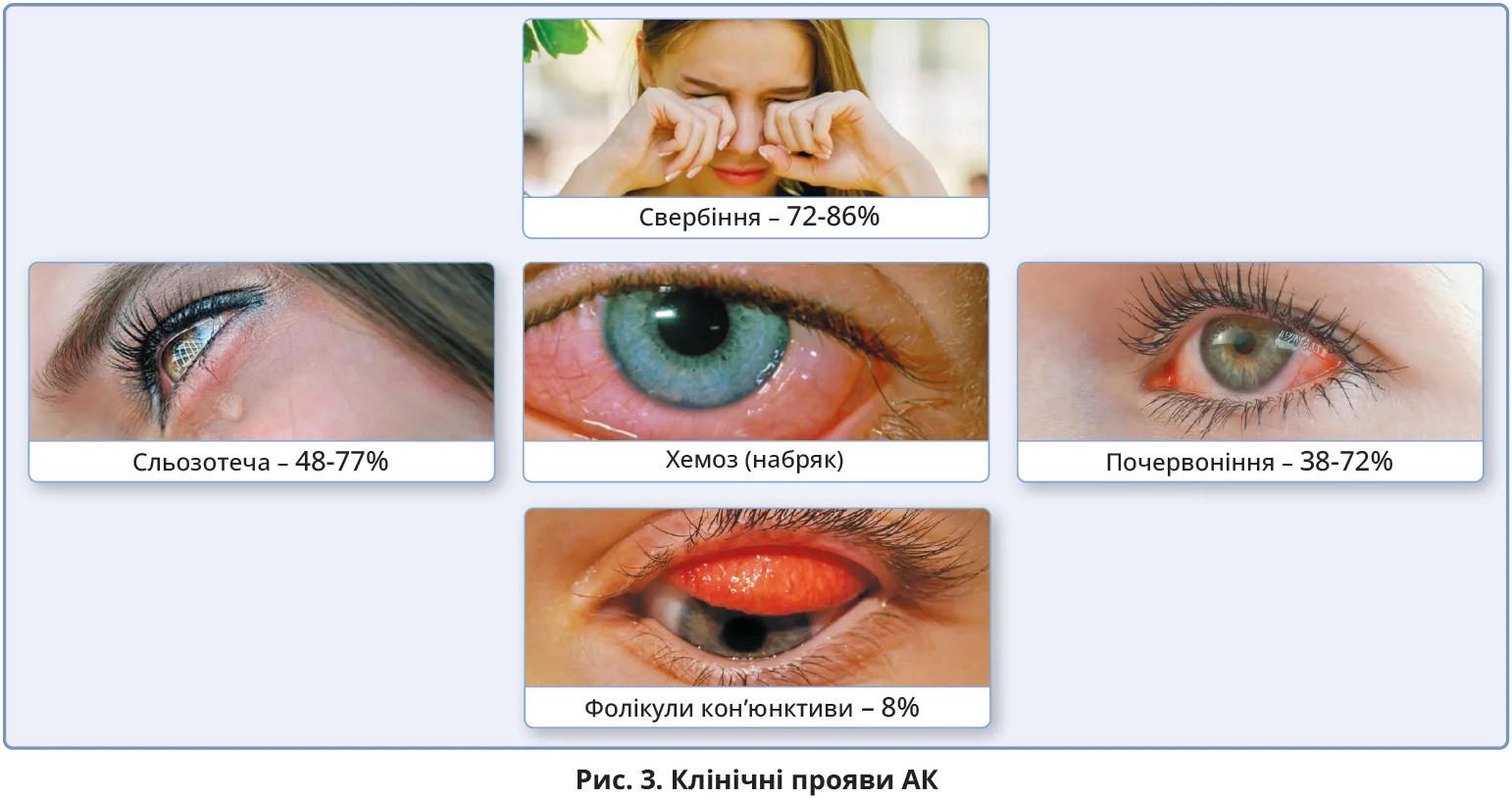
Симптоми АК частіше розвиваються гостро, зазвичай через декілька хвилин і максимум до 12 годин після контакту з причинно-значущим алергеном. Ураження очей здебільшого двобічне. Особливо обтяжливим симптомом для більшості пацієнтів є свербіння повік, яке посилюється через розтирання. Свербіж – постійне джерело роздратування багатьох пацієнтів, що значно погіршує якість життя [30]. Часто спостерігається сльозотеча внаслідок спазму м’язів сльозовивідних шляхів і гіперсекреції слізної рідини під впливом медіаторів алергії. Інші симптоми включають гіперемію та набряк кон’юнктиви, відчуття наявності стороннього тіла в очах (рис. 3).
Виокремлюють такі клінічні форми АК: сезонний АК (САК), цілорічний АК (ЦАК), весняний кератокон’юнктивіт (ВКК), атопічний кератокон’юнктивіт (АКК), гігантський папілярний кон’юнктивіт (ГПК) та контактний дерматокон’юнктивіт (КДК). Близько 95% усіх АК припадає на САК і ЦАК [13, 23, 31].
САК здебільшого спричиняється впливом пилку (полінозний кон’юнктивіт), іноді спорами пліснявих грибів. Переважає серед молодих людей віком 20-40 років без гендерних відмінностей. Час появи симптомів залежить від причинного алергену та періоду цвітіння. В Україні виділяють три періоди цвітіння рослин, а отже, три хвилі полінозу: березень-травень – цвітіння вільхи, берези, тополі; з кінця травня до середини липня – цвітіння злаків, лугових і газонних трав (жито, тимофіївка, костриця лучна, тонконіг); серпень-вересень – цвітіння кукурудзи, соняшника та бур’янів (амброзія, полин, лобода). У пацієнтів із САК часто виявляють алергічний риніт і/або астму. Ураження зазвичай двобічне. Основним симптомом є свербіж, можливі також відчуття печіння та сльозотеча. У тяжких випадках можливі скарги на затуманення зору та світлобоязнь, що може бути наслідком зміни складу та стабільності слізної плівки [32]. Клінічними ознаками САК є легка або помірна гіперемія кон’юнктиви з набряком. Очна кон’юнктива блідо-рожева, з молочним відтінком, білуватим ексудатом, іноді з дифузними ділянками злегка гіпертрофованих сосочків, розташованих переважно на верхній тарзальній кон’юнктиві. Рогівка здебільшого не страждає.
Діагноз підтверджується сімейним або особистим анамнезом атопічних станів і позитивними шкірними пробами на підозрювані сезонні алергени. Проте не завжди шкірні проби є визначальними, оскільки, за даними досліджень, близько 47% пацієнтів можуть виявляти сенсибілізацію до цілорічних алергенів [33]; 24% пацієнтів можуть мати полісенсибілізацію [34]; іноді шкірні проби можуть бути негативними, особливо за відсутності супутнього риніту [35]. Іншими діагностичними критеріями є підвищення рівня IgE в сироватці крові та слізній рідині, а також клінічна відповідь на протиалергічну терапію. Еозинофільна інфільтрація в зразках мазка з кон’юнктиви спостерігається лише у чверті пацієнтів і не є специфічною для САК.
ЦАК зазвичай спричиняється впливом пилових кліщів (≥50% випадків), а також епітелію тварин і/або грибкових та професійних алергенів [36]. Симптоми можуть проявлятися протягом року, хоча в 79% випадків перебіг інтермітивний із загостреннями в умовах досить тісного контакту з причинно-значущими алергенами. Іноді можлива сезонність, що зумовлено активізацією розмноження кліщів домашнього пилу, тарганів, спороутворенням грибів або наявністю супутньої пилкової сенсибілізації.
Із часом у таких пацієнтів можлива поява невеликих сосочків на кон’юнктиві верхньої повіки, які надають їй оксамитового вигляду. У тяжких випадках тарзально-кон’юнктивальні сосочки на кон’юнктиві досягають великих розмірів; спостерігається також неоваскуляризація рогівки з подальшим рубцюванням і зниженням гостроти зору.
Вікової та статевої схильності не спостерігається. Понад 95% пацієнтів мають супутні алергічні хвороби, наприклад цілорічний риніт [37]. Для ЦАК характерна невелика еозинофілія в кон’юнктивальних мазках. Іноді для встановлення діагнозу проводиться кон’юнктивальний провокаційний тест, особливо корисний у пацієнтів із негативними шкірними тестами або відсутністю підвищення IgE в сироватці крові, але з анамнезом, що вказує на ЦАК. Тест проводиться тільки в період ремісії лікарем-алергологом в умовах стаціонару. У нижній кон’юнктивальний мішок закрапують контрольну рідину. За відсутності реакції в кон’юнктивальний мішок іншого ока послідовно закрапують по 1 краплі алергену в дворазових розведеннях (1:2048, 1:1024, 1:512 тощо) з інтервалами не менш як 20-30 хвилин за відсутності реакції на попереднє розведення. Тест вважається позитивним за появи симптомів кон’юнктивіту.
ВКК переважає в осіб чоловічої статі віком 5-25 років. Симптоми хвороби досягають максимуму на початку статевого дозрівання, що може вказувати на патогенетичну роль гормональних змін, а потім поступово зменшуються. Часто поєднується з екземою, астмою або полінозом. Характерна сезонність із загостреннями з весни до осені, які змінюються періодами ремісії взимку. Поширеність хвороби вища в країнах із тривалою природною сонячною інсоляцією, можлива патогенетична роль гіперчутливості до ультрафіолетового випромінювання. Пацієнти здебільшого скаржаться на свербіння й почервоніння очей, сльозотечу, світлобоязнь у сонячну погоду, зорову втому, відчуття важкості повік, густі та в’язкі виділення.
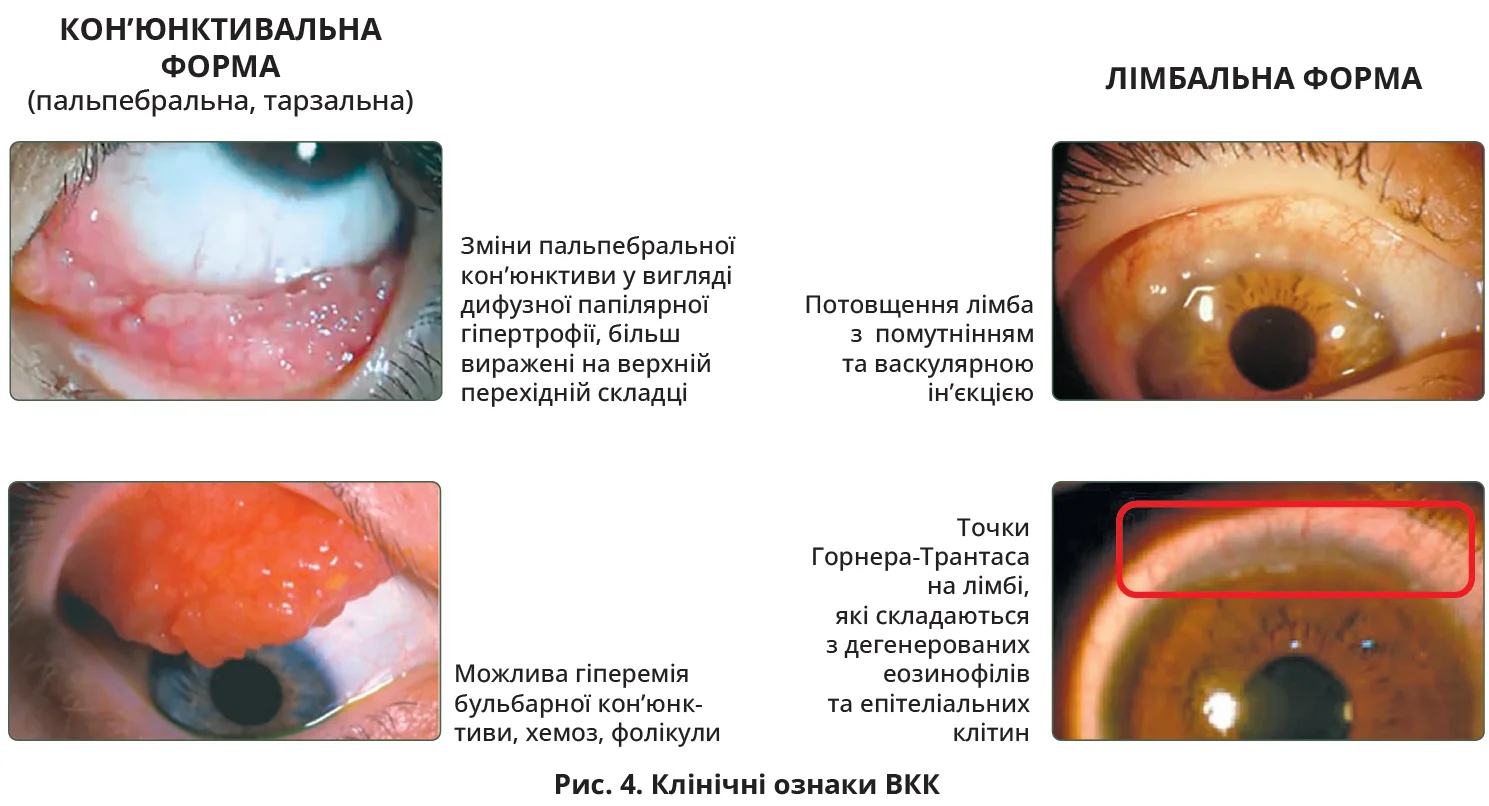
За локалізацією виділяють кон’юнктивальну (тарзальну, пальпебральну), лімбальну та змішану форми (рис. 4). Через потовщення повік вигляд ока нагадує частковий птоз або заспаність. Кон’юнктива хряща верхньої повіки до перехідної складки має своєрідний молочний відтінок, каламутна, з великими пласкими епітеліальними розростаннями, що нагадують бруківку. Сосочки щільні квадратні пласкі блідо-рожевого або сіруватого кольору, можуть спричиняти мікротравми рогівки. Унаслідок цього можливі клінічні прояви з боку рогівки та лімбальної зони. Лімбальна форма характеризується ураженням кон’юнктиви очного яблука, гіпертрофією прекорнеальної кон’юнктиви, яка набуває сірого кольору. Перилімбально можуть спостерігатися желеподібне кільце, розташоване під кон’юнктивою, або точки Горнера – Трантаса (рис. 4). Виділення стають в’язкими та слизуватими, в ділянці перехідних складок – у вигляді ниток. Типові морфологічні зміни включають субепітеліальну інфільтрацію еозинофілами, плазматичними клітинами, лімфоцитами, що вказує на алергічну природу [38].
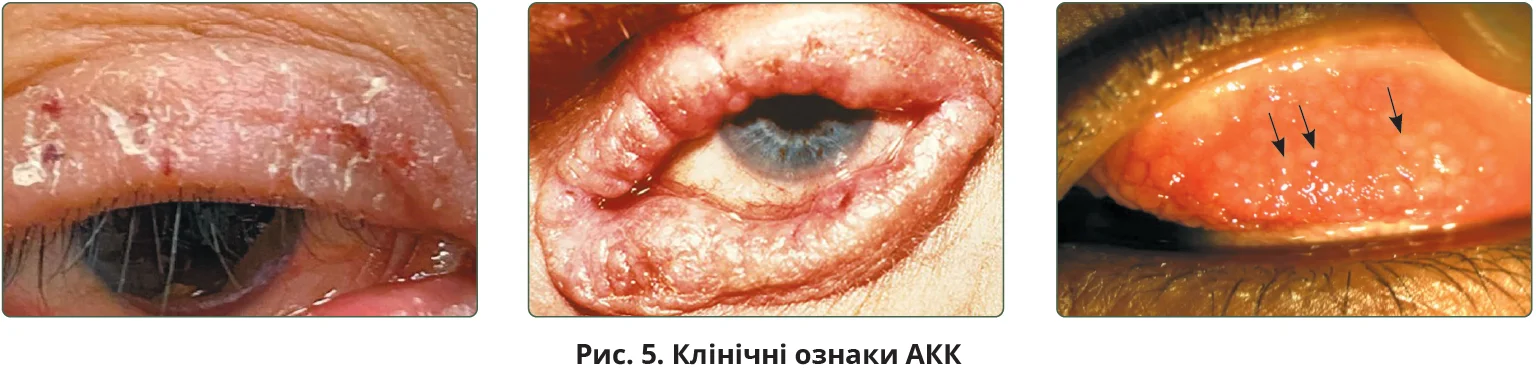
АКК – двобічне хронічне, але циклічне запальне захворювання, що може знижувати гостроту зору. Етіопатогенез, очевидно, включає механізми гіперчутливості I та IV типів з активацією лімфоцитів Th1, Th2 і зменшенням келихоподібних клітин [39]. Хвороба переважає в чоловіків; трапляється в дітей, але значно частіша та серйозніша в дорослих віком 20-50 років [40]. Близько 95% пацієнтів мають особистий або сімейний анамнез атопії (атопічний дерматит, риніт, астма). Очні прояви подібні до таких за ВКК, але сосочки склепінь не є гігантськими, часто виявляється молочний набряк кон’юнктиви. Можлива васкуляризація слизової та рогівки (рис. 5). Повіки зазвичай мають екзематозний вигляд, характерний хронічний блефарит. Хронічний набряк ока призводить до ознаки, відомої як складка Денні – Моргана, під очною ямкою. Розчісування може спричинити випадання вій із зовнішнього боку, відоме як знак Гертоге.
У цій когорті часто спостерігаються невиразковий блефарит і пальпебральні стафілококові інфекції, мейбоміт, трихіаз, ектропіон та ентропіон [30].
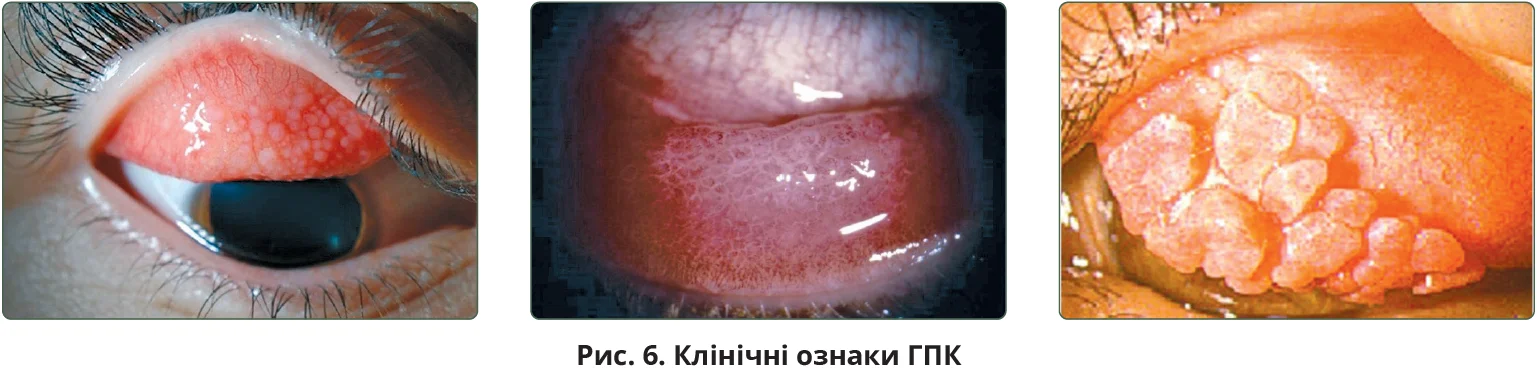
ГПК може розвиватися поступово або гостро впродовж короткого часу після первинного введення лікарського засобу. Часто зумовлений використанням контактних лінз. Вважається, що постійна травма від носіння контактних лінз може ускладнитися алергією з переважанням гіперчутливості сповільненого типу. Типові скарги включають свербіння, почервоніння, сльозотечу, слизові виділення, неможливість використання лінз або відчуття присутності лінзи та її підвищену рухливість, посилення болю та затуманення зору. При об’єктивному обстеженні спостерігаються птоз, наліт на контактній лінзі, гіперемія кон’юнктиви, гігантські сосочки >1 мм у діаметрі, які складаються з лімфоцитів і плазматичних клітин, на кон’юнктиві верхньої повіки, поверхнева васкуляризація рогівки в зоні верхнього лімба (рис. 6). Диференційну діагностику проводять із вірусним, бактеріальним кон’юнктивітами, полінозом. Збираючи анамнез, акцентують увагу на дотриманні строків використання контактних лінз, їх чищення, застосування зволожувальних крапель тощо [30, 31].
Диференційна діагностика
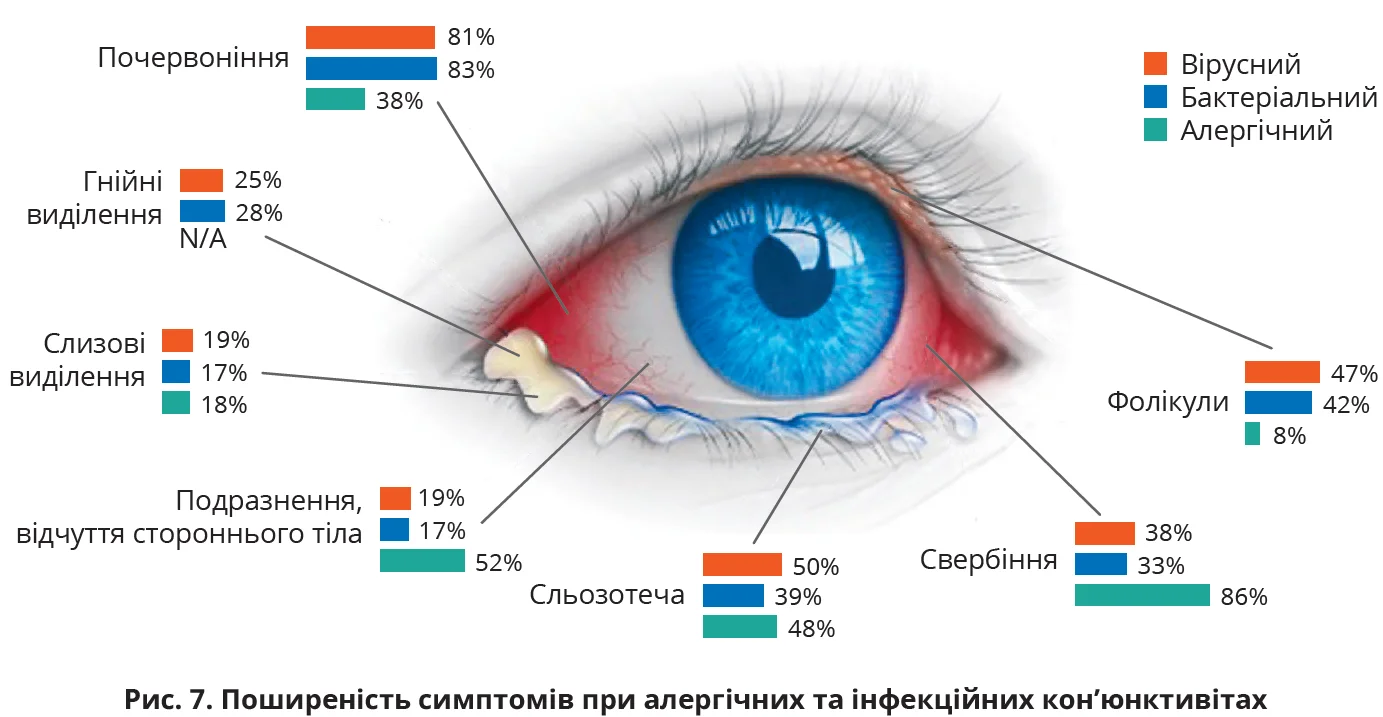
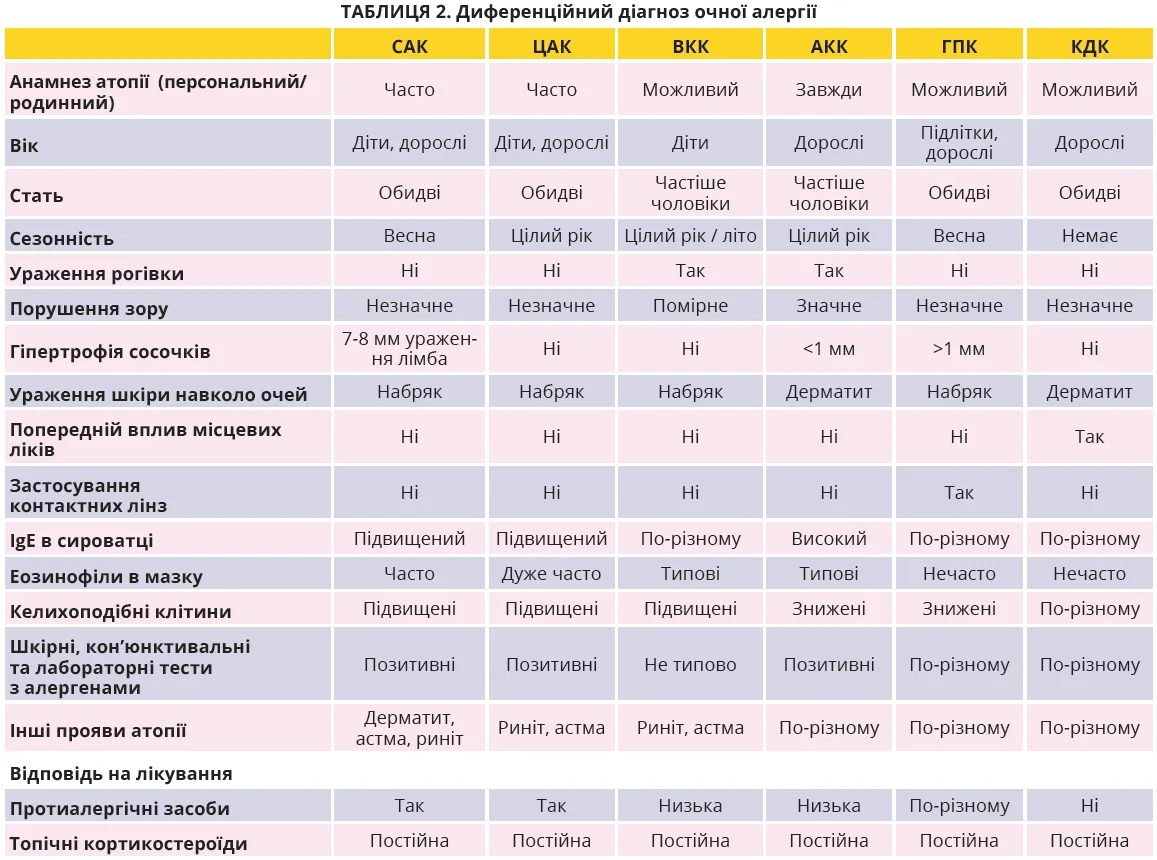
Диференційний діагноз алергічних захворювань очей підсумовано в таблиці 2, відмінності з кон’юнктивітами іншої етіології підсумовано на рисунках 7 і 8.
Лікування
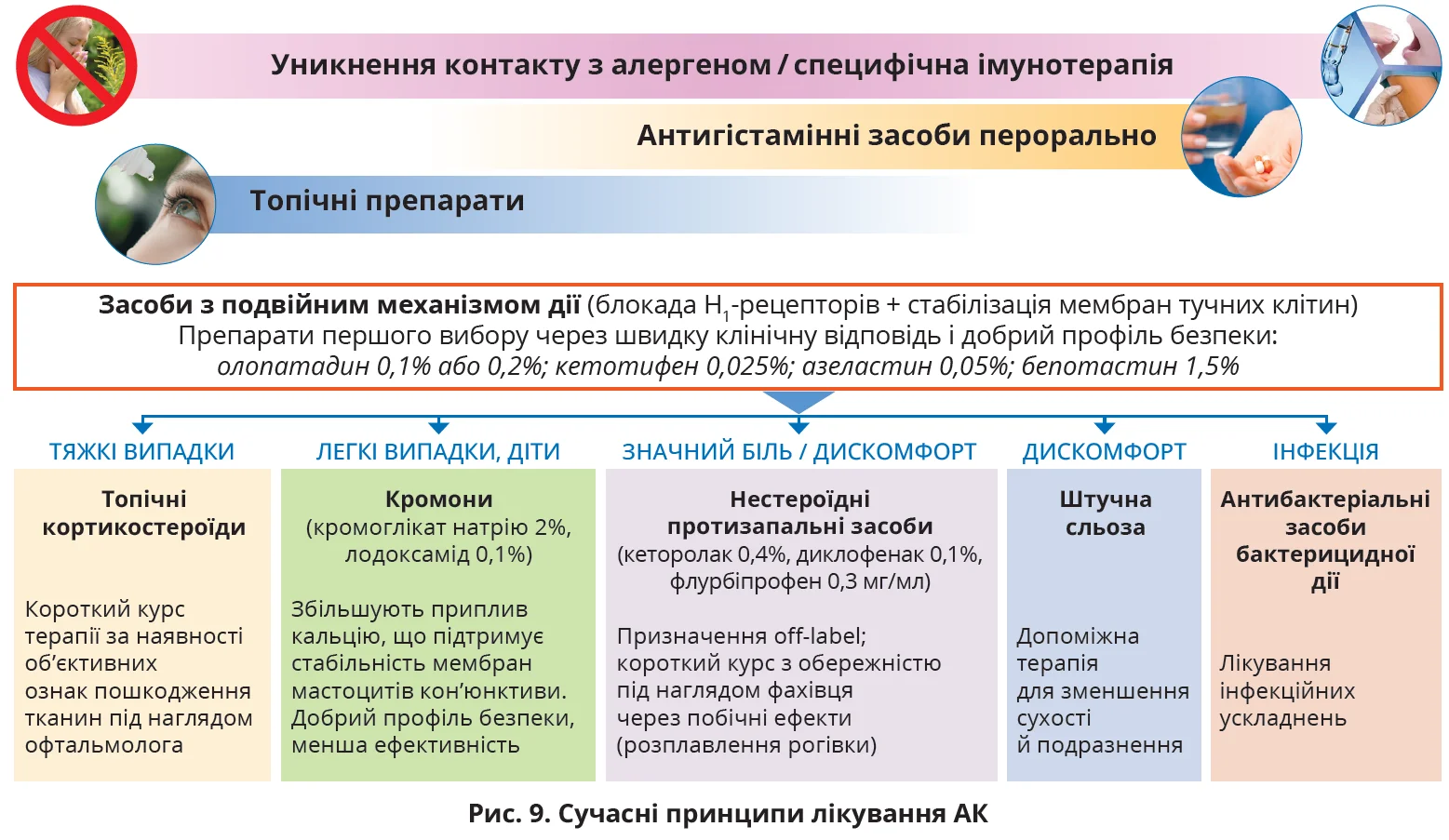
Першим кроком у лікуванні АК є уникнення контакту з алергеном і його елімінація за можливості (рис. 9). Рекомендовано вмивання обличчя, промивання очей і носа, сонцезахисні окуляри, уникнення певних харчових продуктів, вологе прибирання приміщень, відсутність домашніх тварин тощо. Рекомендується також застосовувати препарати, котрі містять ектоїн. Відомо, що ектоїн утворює ектоїнгідрокомплекс – бар’єр, який захищає очі від шкідливої дії бактерій, алергенів та інших подразників [13, 23, 31].
Важливим компонентом є алергеноспецифічна імунотерапія, що проводиться в пацієнтів із чітко визначеними пилковими, епідермальними або побутовими причинно-значущими алергенами в період ремісії під наглядом алерголога (рис. 9). Метод полягає в підшкірному або сублінгвальному введенні алергенних препаратів у зростальних концентраціях, що дає змогу змінити чутливість пацієнта до алергену та забезпечує стійкий тривалий результат [13, 23, 31].
Антигістамінні засоби системної дії включають препарати І покоління (клемастин, хлоропірамін, прометазин), які нині практично не застосовуються через седативний ефект. Перевага віддається неседативним засобам II покоління (цетиризин, лоратадин, астемізол, ебастин, фексофенадин) та їхнім активним метаболітам (дезлоратадин, левоцетиризин) [13, 23, 31].
Основний акцент у цьому огляді зроблено на топічні засоби лікування. Око – це орган, що має вирішальне значення для виживання, але зазнає безпосереднього впливу довкілля та може пошкоджуватися алергенами. Відносно велика площа поверхні кон’юнктиви, потужне кровопостачання й щільна концентрація тучних клітин роблять АК особливо дратівливою формою алергії. Тож лікування очної алергії є важливим терапевтичним завданням. Багато досліджень продемонстрували переваги цілеспрямованої й ефективної місцевої терапії очної алергії порівняно із системною терапією. Адекватне місцеве лікування забезпечує швидке усунення симптомів, позитивно впливає на якість життя та не супроводжується системними проявами побічної дії [23].
Тактика лікування АК залежить від тяжкості клінічних проявів і скарг пацієнта. Топічні кортикостероїди у формі очних крапель і мазей рекомендовано застосовувати лише за тяжких форм АК. Місцеві форми кортикостероїдів високоефективні та виявляють мінімальні побічні ефекти, проте їх треба призначати з обережністю пацієнтам із тяжкими бактеріальними, грибковими та вірусними (герпетичними) інфекціями очей. Топічні кортикостероїди на вітчизняному ринку переважно містять дексаметазон або гідрокортизон. Перевагу варто віддавати препаратам, що не містять антибіотик як консервант. Рекомендовано короткі курси впродовж 2 діб що 2 години з поступовим скасуванням упродовж 1-2 тижнів. Тривале застосування кортикостероїдів небажане через ризик підвищення внутрішньоочного тиску та порушення епітелізації рогівки [13, 23, 31]. У разі приєднання вторинної інфекції показано топічні антибіотики широкого спектра дії, а якщо ускладнення поєднується з кератокон’юнктивітом або блефарокон’юнктивітом – топічні комбіновані засоби, що містять антибіотик і кортикостероїд [13, 23, 31].
Відповідно до сучасних рекомендацій препаратами першої лінії є новий клас місцевих протиалергічних ліків із подвійною дією, які поєднують сильну антигістамінну активність унаслідок селективної блокади Н1-рецепторів (рис. 9), забезпечуючи швидке полегшення симптомів, зі здатністю стабілізації мембран тучних клітин, що збільшує тривалість полегшення симптомів [13, 23, 31].
Прикладом препарату подвійної дії є олопатадин, який швидко покращує стан слизової оболонки очей і характеризується сприятливим профілем безпеки. Призначення олопатадину в режимі монотерапії може бути достатнім за наявності симптомів АК без виразних ознак запалення кон’юнктиви. Препарат не впливає на α-адренергічні, допамінові, мускаринові, серотонінові рецептори та не змінює діаметр зіниць. Специфічність і висока активність олопатадину щодо Н1-рецепторів дають змогу розглядати цю сполуку окремо від інших антигістамінних засобів. Висока селективна зв’язувальна здатність олопатадину до Н1-рецепторів зумовлена унікальним зв’язувальним комплексом із залишком аспартату [41]. Іншим механізмом протиалергічної дії олопатадину є здатність пригнічення тучних клітин і дегрануляції базофілів. Пригнічення вивільнення гістаміну олопатадином дозозалежне – десятикратна максимально ефективна доза забезпечує пригнічення вивільнення гістаміну на понад 90% без будь-яких цитотоксичних реакцій у тучних клітинах [42]. Окрім того, олопатадин пригнічує вивільнення інших медіаторів алергії – лейкотрієнів, тромбоксанів і факторів, що активують тромбоцити [43]. Забезпечення цілісності мембран запобігає вивільненню гемоглобіну, лактатдегідрогенази та гістаміну, що забезпечує більше відчуття комфорту очей після застосування препарату [44]. Високі концентрації олопатадину ефективніше запобігають вивільненню гістаміну з тучних клітин кон’юнктиви людини, ніж кромони – недокроміл, пеміроласт і кромолін-натрій [45]. Дослідження in vitro вказують на здатність олопатадину блокувати вивільнення медіаторів запалення TNF-α, молекул ICAM-1 та ефективніше, ніж фенірамін і антазолін, зменшувати секрецію ІL-6, IL-8 епітеліальними клітинами кон’юнктиви [46-48].
Клінічні дослідження продемонстрували, що ефективність зменшення свербіння й почервоніння очей під впливом олопатадину більша, ніж у недокромілу, кромоліну натрію та левокабастину, зокрема в дітей віком до 4 років [49-52]. Більша ефективність олопатадину спостерігалася також порівняно з кетотифеном і азеластином щодо усунення свербіння, а також порівняно з епінастином щодо зниження інтенсивності свербіння, набряку та почервоніння кон’юнктиви й епісклерального простору [53-55]. Крім того, олопатадин продемонстрував вищу ефективність і кращу переносимість порівняно з кортикостероїдом лотепреднолом у разі лікування САК [56]. Порівняння з нестероїдним протизапальним засобом кеторолаком указує на значне зменшення свербіння та почервоніння очей під впливом олопатадину [57]. Отже, рекомендація олопатадину як препарату першої лінії зумовлена його перевагами над багатьма іншими топічними протиалергічними засобами [23, 31].
Антигістамінні препарати системної дії для перорального застосування зменшують симптоми сухості очей завдяки неспецифічній взаємодії з рецепторами, спряженими з G-білком (G-Protein Coupled Receptor – GPCR). Гістамінові та мускаринові рецептори є GPCR- і М3-рецепторами, які беруть участь у регуляції функцій слізної залози. Будучи антагоністами М3-рецепторів, неселективні антигістамінні засоби знижують секрецію слізної залози, що спричиняє висихання поверхневих відділів ока. Зневоднення слізної плівки зменшує захисні бар’єрні властивості, що полегшує проникнення алергенів через поверхню очей і посилює симптоми алергії [58]. При супутньому застосуванні олопатадину в пацієнтів, які приймали лоратадин перорально, спостерігалося значуще зменшення інтенсивності свербіння очей без появи сухості [58, 59]. Тож поєднане застосування пероральних антигістамінних засобів у разі риніту й олопатадину при очних алергіях є безпечним і запобігає виникненню синдрому сухого ока.
Відомо, що вдихання аероалергенів спричиняє як очні, так і носові симптоми. При потраплянні в очі аероалергени також проникають через носовий канал у порожнину носа, зумовлюючи носові симптоми алергії. За аналогією місцеве введення офтальмологічних розчинів може впливати на симптоми алергічного риніту [60]. За даними досліджень, олопатадин значно краще зменшує алергічні симптоми риніту порівняно з плацебо. Комбінована терапія олопатадином і назальним спреєм дає змогу зменшити інтенсивність свербіння й почервоніння очей значно більше, ніж у разі застосування назального спрею в комбінації з антигістамінним препаратом системної дії [59]. Інше дослідження продемонструвало, що комбінація олопатадину, назального спрею й антигістамінного засобу системної дії ефективно зменшує очні симптоми алергії [60]. Крім того, додавання олопатадину пацієнтам з алергічним ринітом, які вже використовували назальний спрей або антигістамінний засіб системної дії, суттєво покращувало показники якості життя [61]. Отже, місцеве лікування алергічних захворювань певної локалізації є значущим, а олопатадин може зменшувати носові алергічні симптоми.
Після отримання доказів клінічної ефективності та безпеки очних крапель олопатадину 0,1% у режимі застосування двічі на добу з’явилися докази доклінічних випробувань про збереження певного рівня лікарського засобу через 24 години після одноразового введення в кон’юнктивальний мішок 1 краплі олопатадину 0,2% об’ємом 30 мкл. Через 24 години після одноразового місцевого введення олопатадину в дозі 1 мг/кг блокада Н1-рецептора зберігалася на рівні 50%, а ефективність контролю зумовлених гістаміном симптомів алергії була більшою при застосуванні вищих концентрацій олопатадину в режимі 1 раз на добу. Концентрація розчину 0,2% вибрана з урахуванням граничних параметрів розчинності водного розчину. Олопатадин 0,2% демонструє таку саму ефективність, як 0,1% розчин у перші 5 хвилин після введення, але значно більший ефект після 24 годин. Дослідження клінічної моделі САК продемонструвало статистично більшу ефективність олопатадину 0,2% щодо зменшення інтенсивності свербіння, почервоніння й набряку кон’юнктиви та сльозотечі порівняно з плацебо з розвитком дії через 5 хвилин і тривалістю дії ≈24 години [62]. Після одноразового використання крапель олопатадину 0,2% свербіж очей припинився в 63% пацієнтів упродовж 3 хвилин [63]. Отож олопатадин 0,2% – це єдиний засіб подвійної дії, який показаний для застосування 1 раз на добу, що забезпечує потенційну перевагу над ліками, котрі потрібно застосовувати частіше.
У відкритому багатоцентровому клінічному дослідженні оцінювали сприйняття олопатадину 0,2% у режимі введення по 1 краплі в кожне око 1 раз на добу впродовж 28 днів у пацієнтів з наявними симптомами АК. Дослідження завершили 328 пацієнтів віком 5-94 роки, які раніше застосовували олопатадин 0,1%. У 1-й та 7-й дні пацієнти заповнювали анкету якос-ті життя при ринокон’юнктивіті, реєстрували своє сприйняття олопатадину 0,1% (у 1-й день) та олопатадину 0,2% (на 7-й день). На 28-й день пацієнти повернулися до дослідного центру, повідомили про своє сприйняття лікування та пройшли оцінку виразності симптомів алергії з боку очей. Пацієнти були більш задоволені олопатадином 0,2%, ніж олопатадином 0,1% (87,6 проти 77,8%; p<0,05). Серед 48 пацієнтів, які носили контактні лінзи, 42 учасники (88%) вважали, що вони можуть надалі їх носити. В усіх категоріях анкети якості життя при ринокон’юнктивіті пацієнти відзначили значуще покращення (p<0,0001).
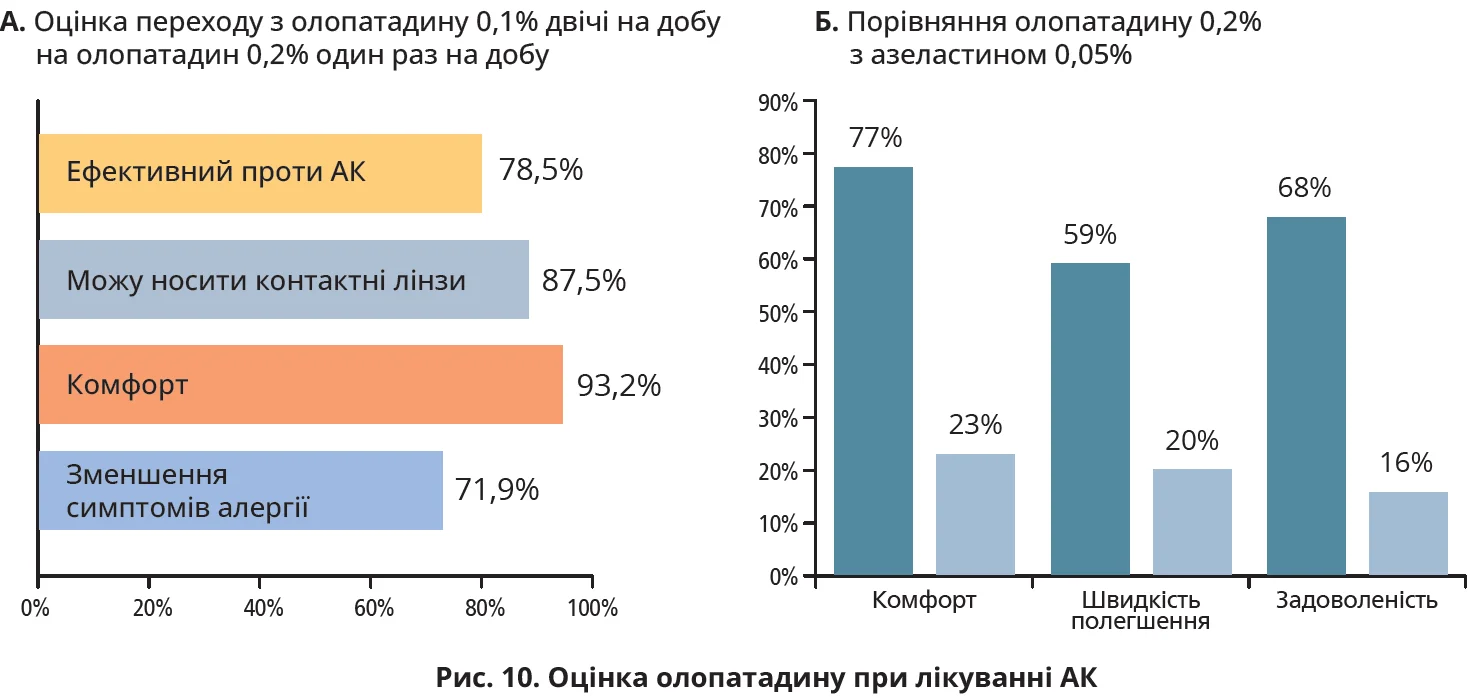
Не було жодних повідомлень щодо побічних ефектів терапії. Пацієнти вважали, що олопатадин 0,2% ефективний і добре переноситься (рис. 10А) [64].
РАСЕ (оцінка АК з Pataday олопатадин 0,2%) – багатоцентрове проспективне відкрите дослідження в одній групі, проведене в 10 клінічних центрах алергії, офтальмології й оптометрії по всій території США впродовж весни 2008 року за участю пацієнтів віком понад 18 років з активними ознаками та/або наявними симптомами АК за оцінкою дослідника, які лікувалися протягом останніх 6 місяців місцевими очними формами протиалергічних препаратів в режимі двічі на добу. Метою дослідження була оцінка сприйняття пацієнтом олопатадину 0,2% порівняно з азеластином 0,05%, який застосовувався впродовж попередніх 6 місяців. У 1-й день (візит 1) пацієнти заповнювали анкету з питаннями щодо алергопатології та оцінки ефективності попереднього лікування, а дослідники заповнювали історію хвороби. Потім пацієнтам було рекомендовано використовувати олопатадин 0,2% 1 раз на добу. На 7-й день пацієнти заповнювали аналогічну анкету з метою оцінки ефекту олопатадину 0,2%; дослідники відзначали будь-які небажані явища або зміни супутньої терапії за цей час. В анкеті пацієнти оцінювали своє сприйняття ефективності препаратів за впливом на такі симптоми: свербіння очей, почервоніння, сльозотеча та набряки за 5-бальною шкалою («дуже ефективно», «певною мірою ефективно» «не визначено», «певною мірою неефективно», «дуже неефективно»; а також задоволеність протиалергічною терапією щодо трьох параметрів (комфорт крапель, швидкість настання полегшення та загальна задоволеність) за допомогою дескрипторів: «дуже задоволений», «певною мірою задоволений», «не визначився», «певною мірою незадоволений», «дуже незадоволений». Велика частка пацієнтів повідомили, що олопатадин виявився «дуже ефективним» порівняно з азеластином (46 проти 20% для свербіння, р=0,069; 42 проти 17% для почервоніння, р=0,071; 25 проти 9% для сльозотечі, р>0,05; 47 проти 8% для набряку, р=0,040). Олопатадин 0,2% продемонстрував чудову переносимість порівняно з азеластином 0,05% через значно більший комфорт після закрапування. Причини підвищеної комфортності олопатадину порівняно з азеластином чітко не визначені, але вони можуть пояснюватися відмінностями рН (для азеластину 5,0-6,5; для олопатадину ≈7,1, тобто фізіологічний рівень рН) і різним впливом цих препаратів на цілісність клітинних мембран. На відміну від азеластину й інших засобів подвійної дії олопатадин не порушує мембрани епітеліальних клітин очної поверхні, пошкодження котрих може пояснити появу печіння після закрапування. Завдяки застосуванню 1 раз на добу олопатадин 0,2% виявився зручнішим для пацієнтів і сприймався ними як клінічно ефективніший порівняно з азеластином 0,05%. Пацієнти оцінювали себе як «дуже задоволені» після використання олопатадину 0,2% у 3-4 рази частіше, ніж після застосування азеластину 0,05% (рис. 10Б) [65]. Сприйняття пацієнтом є критично важливим для забезпечення безперервного дотримання прийому та досягнення загальної задоволеності як лікуванням, так і якістю послуг.
Пацієнтам, які носять контактні лінзи, можна безпечно призначати олопатадин за відсутності почервоніння очей перед використанням препарату та з інтервалом 10 хвилин до встановлення лінзи [66].
За дотримання таких рекомендацій декілька досліджень указують на успішне пригнічення симптомів АК в осіб, які носять контактні лінзи [67]. Використання контактних лінз може стимулювати появу симптомів, характерних для сухого ока, зокрема дефіцит слізної рідини та прискорення часу розриву слізної плівки [68]. Дослідження, в якому олопатадин покращував функціональні характеристики слізної рідини та сприяв підтримці стійкості бар’єрних характеристик слізної плівки, вказує на можливість застосування препарату в осіб, що носять контактні лінзи, а також у пацієнтів із синдромом сухого ока [69]. Дослідження, в якому порівнювали ефекти олопатадину 0,2% з ефектами фізіологічного розчину, продемонструвало однакові зміни в симптоматиці синдрому сухого ока під впливом обох препаратів і схожі показники переносимості в пацієнтів з алергічними хворобами та супутнім синдромом сухого ока [70]. Інше дослідження вказує, що частота синдрому сухого ока після застосування олопатадину 0,2% була меншою або рівноцінною відносно показника при застосуванні плацебо [71].
Цікаво, що олопатадин 0,2% здатний впливати на носові симптоми алергії. В одному з досліджень пацієнти з алергічним ринітом і ринокон’юнктивітом самостійно закрапували олопатадин 0,2% або плацебо в обидва ока 1 раз на добу з квітня по серпень. У групі олопатадину спостерігалися нижчі середні показники інтенсивності свербіння та почервоніння очей, аніж у групі плацебо, незалежно від рівня запиленості повітря. Олопатадин 0,2% також сприятливо впливав на середні показники інтенсивності свербіння та почервоніння очей у періоди максимальних середніх рівнів пилкових алергенів у повітрі. Переносимість лікарського засобу була доброю, жоден пацієнт не припинив лікування достроково через небажані явища [72].
Вплив олопатадину 0,2% на носові симптоми алергії в пацієнтів із САК вивчали два плацебо-контрольовані дослідження: одне тривало 12 тижнів із липня по грудень, інше – 10 тижнів із квітня по серпень. Пацієнти щотижня відвідували клініку для отримання лікування та реєстрації симптомів. Дослідження, котре проводилося восени, виявило, що олопатадин 0,2% ефективно зменшував частоту випадків чхання та свербіння в порожнині носа, а також інтенсивність чхання, свербіння й виділень із носа. Дослідження, котре проводилося у весняно-літній період, виявило значуще зменшення частоти випадків чхання та виділень із носа під впливом олопатадину 0,2%. Синдром сухого ока – небажане явище, що найчастіше виникає внаслідок терапії, – виявлено з однаковою частотою (1,7%) у групах олопатадину та плацебо. Отже, результати досліджень указують на безпечність і добру переносимість олопатадину 0,2% у пацієнтів із носовими симптомами алергії [73].
При порівнянні олопатадину 0,2% та епінастину 0,05% обидва препарати ефективно зменшували інтенсивність свербіння й почервоніння очей, але показники ефективності та переносимості олопатадину перевищували такі епінастину. У групі олопатадину виявлено значно нижчі середні показники інтенсивності свербіння та почервонінні очей, аніж у групі епінастину. В обох групах зареєстровано зіставні оцінки ступенів комфортності застосування в усіх часових точках, за винятком часової точки через 1 хвилину після введення, коли застосування олопатадину було статистично комфортнішим, аніж застосування епінастину [74].
Що стосується переносимості й безпеки, то в дослідженнях установлено добру переносимість очних крапель олопатадину 0,1 та 0,2% [41, 62, 74, 75]. Порівняльні дослідження вказують, що комфортність застосування та переносимість олопатадину вища, ніж у недокромілу натрію 2% [49], кромоліну натрію 2% [51, 76], левокабастину 0,05% [50], лотепреднолу 0,2% [56], кеторолаку 0,5% [57], кетотифену 0,05% [77] та епінастину 0,05% [74]. Чудовий профіль комфортності застосування олопатадину 0,2% робить цей препарат варіантом терапії, якому віддають перевагу лікарі та пацієнти.
При лікуванні олопатадином не спостерігали серйозних небажаних явищ, а місцеві небажані явища були вкрай рідкісними. Препарат можна призначати дітям віком від 3 років [41].
Отже, препаратами першого вибору для лікування симптомів алергічних захворювань очей є засоби подвійної дії, зокрема олопатадин 0,2%, який можна використовувати 1 раз на добу. Препарат швидко усуває симптоми алергії, зокрема свербіння, набряк, сльозотечу, позитивно впливає на супутні прояви алергічного риніту та не посилює сухості ока. Може застосовуватися тривало починаючи з 3-річного віку. На українському ринку очні краплі олопатадину 0,2% доступні у формі препарату Візаллергол («Сентісс Фарма Пвт. Лтд.», Індія), переваги якого підсумовано на рисунку 11.
Література
- Mazur M., Czarnobilska M., Dyga W., Czarnobilska E. Trends in the epidemiology of allergic diseases of the airways in children growing up in an urban agglomeration. J. Clin. Med. 2022 Apr 14; 11 (8): 2188. doi: 10.3390/jcm11082188.
- Aldakheel F.M. Allergic diseases: a comprehensive review on risk factors, immunological mechanisms, link with COVID-19, potential treatments, and role of allergen bioinformatics. Int. J. Environ. Res. Public Health. 2021 Nov 18; 18 (22): 12105. doi: 10.3390/ijerph182212105.
- The European Academy of Allergy and Clinical Immunology (EAACI). Advocacy Manifesto Tackling the Allergy Crisis in Europe-Concerted Policy Action Needed. June 2015 Version [Accessed on 18 December 2021]. Available at: http://www.eaaci.org/outreach/public-declarations.html.
- Ng A.E., Boersma P. Diagnosed allergic conditions in adults: United States, 2021. NCHS Data Brief, no 460. Hyattsvi
- lle, MD: National Center for Health Statistics. 2023. doi: https://dx.doi.org/10.15620/cdc:122809.
- Zablotsky B., Black L.I., Akinbami L.J. Diagnosed allergic conditions in children aged 0-17 years: United States, 2021. NCHS Data Brief, no 459. Hyattsville, MD: National Center for Health Statistics. 2023. doi: https://dx.doi.org/10.15620/cdc:123250.
- Дуда Л.В., Охотнікова О.М. Клініко-епідеміологічна характеристика найпоширеніших алергічних захворювань у дітей. Здоров’я дитини. 2018; Т. 13, № 4: С. 345-355.
- Кузнецова Л.В. Клініко-імунологічна характеристика та сучасні аспекти антигістамінної терапії сезонного алергічного риніту. Український медичний часопис. 2014; № 3 (101): С. 35-39.
- Rosario N., Bielory L. Epidemiology of allergic conjunctivitis. Curr. Opin. Allergy Clin. Immunol. 2011; 11 (5): 471-476.
- Singh K., Axelrod S., Bielory L. The epidemiology of ocular and nasal allergy in the United States, 1988-1994. J. Allergy Clin. Immunol. 2010; 126 (4): 778-783.
- Gradman J., Wolthers O.D. Allergic conjunctivitis in children with asthma, rhinitis and eczema in a secondary outpatient clinic. Pediatr. Allergy Immunol. 2006; 17 (7): 524-526.
- Brown-Whitehorn T.F., Spergel J.M. The link between allergies and eosinophilic esophagitis: implications for management strategies. Expert Rev. Clin. Immunol. 2010; 6 (1): 101-109.
- Neto H.J., Rosario N.A., Westphal G.L., Riedi C.A., Santos H.L. Allergic conjunctivitis in asthmatic children: as common as underreported. Ann. Allergy Asthma Immunol. 2010; 105 (5): 399-400.
- Dupuis P., Prokopich C., Hynes A., et al. A contemporary look at allergic conjunctivitis. Allergy Asthma Clin. Immunol. 2020; 16 (5). doi: 10.1186/s13223-020-0403-9.
- Кузнецов О.Г. Клінічна характеристика хворих на сезонний алергічний ринокон’юнктивіт. Анамнестичні дані та структура супутньої патології. Імунологія й алергологія: наука та практика. 2020; № 2: С. 72-81.
- Комплексний і мультидисциплінарний підхід у диференційній діагностиці та лікуванні кон’юнктивіту в дітей. Здоров’я України. 2020; Тематичний номер № 4 (55): С. 28-29.
- Kabesch M., Tost J. Recent findings in the genetics and epigenetics of asthma and allergy. Semin. Immunopathol. 2020; 42: 43-60. doi: 10.1007/s00281-019-00777-w.
- Fan G., Wang B., Liu C., Li D. Prenatal paracetamol use and asthma in childhood: a systematic review and meta-analysis. Allergol. Immunopathol. (Madr.). 2017 Nov-Dec; 45 (6): 528-533. doi: 10.1016/j.aller.2016.10.014.
- Mirzakhani H., Al-Garawi A., Weiss S.T., Litonjua A.A. Vitamin D and the development of allergic disease: how important is it? Clin. Exp. Allergy. 2015 Jan; 45 (1): 114-25. doi: 10.1111/cea.12430.
- Bogacka E. Epidemiology of allergic eye diseases. Pol. Merkur. Lekarski. 2003; 14 (84): 714-15.
- Singh K., Bielory L., Hackensack N.J., Newark N.J. Epidemiology of ocular allergy symptoms in United States adults (1988-1994). Ann. Allergy Asthma Immunol. 2007; 98: 34-A22.
- Bonini S. Allergic conjunctivitis: the forgotten disease. Chem. Immunol. Allerg. 2006; 91:110-20.
- Takano Y., Narita S., Kobayashi K. Seasonal allergic rhinitis in Hakodote. Nippon Ganka Gakkai Zasshi. 2004; 108: 606-11.
- Sánchez M.C., Fernández Parra B., Matheu V., Navarro A., Ibáñez M.D., Dávila I., Dordal M.T., Lluch Bernal M., Rondón C., Montoro J., Antón E., Colás C., Valero A. (SEAIC Rhinoconjunctivitis Committee 2010). Allergic Conjunctivitis. J. Investig. Allergol. Clin. Immunol. 2011; 21 (Suppl. 2): 1-19.
- Offiah I., Calder V.L. Immune mechanisms in allergic eye diseases: what is new? Curr. Opin. Allergy Clin. Immunol. 2009; 9 (5): 477-81.
- Ishida W., Fukuda K., Kajisako M., Takahashi A., Sumi T., van Rooijen N., Fukushima A. Conjunctival macrophages act as antigen-presenting cells in the conjunctiva during the development of experimental allergic conjunctivitis. Mol. Vis. 2010 Jul 10; 16: 1280-5.
- McConchie B.W., Norris H.H., Bundoc V.G., Trivedi S., Boesen A., Urban J.F., Jr., Keane-Myers A.M. Ascaris suum-derived products suppress mucosal allergic inflammation in an interleukin-10-independent manner via interference with dendritic cell function. Infect. Immun. 2006; 74 (12): 6632-41.
- Abelson M.B. Comparison of the conjunctival allergen challenge model with the environmental model of allergic conjunctivitis. Acta Ophthalmol. Scand. Suppl. 1999; 228: 38-42. doi: 10.1111/j.1600-0420.1999.tb01172.x.
- Ozaki A., Seki Y., Fukushima A., Kubo M. The control of allergic conjunctivitis by suppressor of cytokine signalling (SOCS)3 and SOCS5 in a murine model. J. Immunol. 2005; 175 (8): 5489-97.
- Bonini S., Bucci M.G., Berruto A., Adriani E., Balsano F., Allansmith M.R. Allergen dose response and late symptoms in a human model of ocular allergy. J. Allergy Clin. Immunol. 1990; 86 (6 Pt. 1): 869-76.
- Baab S., Le P.H., Kinzer E.E. Allergic conjunctivitis. 2022 May 23. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2023 Jan.
- SEAIC 2010 Rhinoconjunctivitis Committee; Spanish Group Ocular Surface-GESOC. Consensus document on allergic conjunctivitis (DECA). J. Investig. Allergol. Clin. Immunol. 2015; 25 (2): 94-106.
- Suzuki S., Goto E., Dogru M., Asano-Kato N., Matsumoto Y., Hara Y., Fujishima H., Tsubota K. Tear film lipid layer alterations in allergic conjunctivitis. Cornea. 2006; 25 (3): 277-80.
- Buckley R.J. Allergic diseases: a clinical challenge. Clin. Exp. Allergy. 1998; 28 (6): 39-43.
- Pallasaho P., Ronmark E., Haahtela T., Sovijarvi A.R., Lundback B. Degree and clinical relevance of sensitization to common allergens among adults: a population study in Helsinki, Finland. Clin. Exp. Allergy. 2006; 36 (4): 503-9.
- Berdy G.J., Berdy S.S. Ocular allergic disorders: disease entities and differential diagnosis. Curr. Allergy Asthma Reports. 2009; 9: 297-303.
- El-Nahas H.A., El-Beshbishi S.N., Azab M.S., Zaalouk T., Elsheikha H.M., Saleh A.B., El-Shazly A.M. Diagnostic criteria for house dust mites sensitized allergic patients. J. Egypt Soc. Parasitol. 2007; 37 (3 Suppl.): 1113-24.
- Kosrirukvongs P., Visitsunthorn N., Vichyanond P., Bunnag C. Allergic conjunctivitis. Asian Pac. J. Allergy Immunol. 2001; 19 (4): 237-44.
- Leonard A. Management of vernal keratoconjunctivitis. Ophthalmol. Ther. 2013 Dec; 2 (2): 73-88.
- Hu Y., Matsumoto Y., Dogru M., Okada N., Igarashi A., Fukagawa K., Tsubota K., Fujishima H. The differences of tear function and ocular surface findings in patients with atopic keratoconjunctivitis and vernal keratoconjunctivitis. Allergy. 2007; 62 (8): 917-25.
- Bonini S. Atopic keratoconjunctivitis. Allergy. 2004; 59 (supp. 78): 71-73.
- Abelson M.B., Gomes P.J. Olopatadine 0.2% ophthalmic solution: the first ophthalmic antiallergy agent with once-daily dosing. Expert Opinion on Drug Metabolism & Toxicology. 2008; 4 (4): 453-461. doi: 10.1517/17425255.4.4.453.
- Yanni J.M., Stephens D.J., Miller S.T., et al. The in vitro and in vivo ocular pharmacology of olopatadine (AL-4943A), an effective anti-allergic/antihistaminic agent. J. Ocul. Pharmacol. Ther. 1996; 12: 389-400.
- Ikemura T., Manabe H., Sasaki Y., et al. KW-4679, an antiallergic drug, inhibits the production of inflammatory lipids in human polymorphonuclear leukocytes and guinea pig eosinophils. Int. Arch. Allergy Immunol. 1996; 110: 57-63.
- Brockman H.L., Momsen M.M., Knudtson J.R., et al. Interactions of olopatadine and selected antihistamines with model and natural membranes. Ocul.
Immunol. Inflamm. 2003; 11: 247-68. - Yanni J.M., Miller S.T., Gamache D.A., et al. Comparative effects of topical ocular anti-allergy drugs on human conjunctival mast cells. Ann. Allergy Asthma Immunol. 1997; 79: 541-5.
- Cook E.B., Stahl J.L., Barney N.P., Graziano F.M. Olopatadine inhibits TNF-alpha release from human conjunctival mast cells. Ann. Allergy Asthma Immunol. 2000; 84: 504-8.
- Cook E.B., Stahl J.L., Barney N.P., Graziano F.M. Olopatadine inhibits anti-immunoglobulin E-stimulated conjunctival mast cell upregulation of ICAM-1 expression on conjunctival epithelial cells. Ann. Allergy Asthma Immunol. 2001; 87: 424-9.
- Cook E.B., Stahl J.L., Sedgwick J.B., et al. The promotion of eosinophil degranulation and adhesion to conjunctival epithelial cells by IgE-activated conjunctival mast cells. Ann. Allergy Asthma Immunol. 2004; 92: 65-72.
- Butrus S., Greiner J.V., Discepola M., Finegold I. Comparison of the clinical efficacy and comfort of olopatadine hydrochloride 0.1% ophthalmic solution and nedocromil sodium 2% ophthalmic solution in the human conjunctival allergen challenge model. Clin. Ther. 2000; 22: 1462-72.
- Abelson M.B., Greiner J.V. Comparative efficacy of olopatadine 0.1% ophthalmic solution versus levocabastine 0.05% ophthalmic suspension using the conjunctival allergen challenge model. Curr. Med. Res. Opin. 2004; 20: 1953-8.
- Katelaris C.H., Ciprandi G., Missotten L., et al. A comparison of the efficacy and tolerability of olopatadine hydrochloride 0.1% ophthalmic solution and cromolyn sodium 2% ophthalmic solution in seasonal allergic conjunctivitis. Clin. Ther. 2002; 24: 1561-75.
- Ciprandi G., Turner D., Gross R.D. Double-masked, randomized, parallel-group study comparing olopatadine 0.1% ophthalmic solution with cromolyn sodium 2% and levocabastine 0.05% ophthalmic preparations in children with seasonal allergic conjunctivitis. Curr. Ther. Res. 2004; 65: 186-99.
- Leonardi A., Zafirakis P. Efficacy and comfort of olopatadine versus ketotifen ophthalmic solutions: a double-masked, environmental study of patient preference. Curr. Med. Res. Opin. 2004; 20: 1167-73.
- Spangler D.L., Bensch G., Berdy G.J. Evaluation of the efficacy of olopatadine hydrochloride 0.1% ophthalmic solution and azelastine hydrochloride 0.05% ophthalmic solution in the conjunctival allergen challenge model. Clin. Ther. 2001; 23: 1272-80.
- Finegold I., Granet D.B., D’Arienzo P.A., Epstein A.B. Efficacy and response with olopatadine versus epinastine in ocular allergic symptoms: a post hoc analysis of data from a conjunctival allergen challenge study. Clin. Ther. 2006; 28: 1630-8.
- Berdy G.J., Stoppel J.O., Epstein A.B. Comparison of the clinical efficacy and tolerability of olopatadine hydrochloride 0.1% ophthalmic solution and loteprednol etabonate 0.2% ophthalmic suspension in the conjunctival allergen challenge model. Clin. Ther. 2002; 24: 918-29.
- Deschenes J., Discepola M., Abelson M. Comparative evaluation of olopatadine ophthalmic solution (0.1%) versus ketorolac ophthalmic solution (0.5%) using the provocative antigen challenge model. Acta Ophthalmol. Scand. Suppl. 1999; 38: 47-52.
- Abelson M.B., Welch D.L. An evaluation of onset and duration of action of Patanol (olopatadine hydrochloride ophthalmic solution 0.1%) compared to Claritin (loratadine 10 mg) tablets in acute allergic conjunctivitis in the conjunctival allergen challenge model. Acta Ophthalmol. Scand. Suppl. 2000; 230: 60-3.
- Abelson M.B., Lanier R.Q. The added benefit of local Patanol therapy when combined with systemic Claritin for the inhibition of ocular itching in the conjunctival antigen challenge model. Acta Ophthalmol. Scand. Suppl. 1999; 228: 53-6.
- Spangler D.L., Abelson M.B., Ober A., Gotnes P.J. Randomized, double-masked comparison of olopatadine ophthalmic solution, mometasone furoate monohydrate nasal spray, and fexofenadine hydrochloride tablets using the conjunctival and nasal allergen challenge models. Clin. Ther. 2003; 25: 2245-67.
- Berger W., Abelson M.B., Gomes P.J., et al. Effects of adjuvant therapy with 0.1% olopatadine hydrochloride ophthalmic solution on quality of life in patients with allergic rhinitis using systemic or nasal therapy. Ann. Allergy Asthma Immunol. 2005; 95: 361-71.
- Vogelson C.T., Abelson M.B., Pasquine T., et al. Preclinical and clinical antiallergic effect of olopatadine 0.2% solution 24 hours after topical ocular administration. Allergy Asthma Proc. 2004; 25: 69-75.
- Granet D.B., Amin D., Tort M.J. Evaluation of olopatadine 0.2% for the elimination of ocular itching in the conjunctival allergen challenge (CAC) model. Poster presented at: Western Society of Allergy, Asthma and Immunology; January 2010.
- Scoper S.V., Berdy G.J., Lichtenstein S.J., Rubin J.M., Bloomenstein M., Prouty R.E., Vogelson C.T., Edwards M.R., Waycaster C., Pasquine T., Gross R.D., Robertson S.M. Perception and quality of life associated with the use of olopatadine 0.2% (Pataday) in patients with active allergic conjunctivitis. Adv. Ther. 2007 Nov-Dec; 24 (6): 1221-32. doi: 10.1007/BF02877768.
- Epstein A.B., Van Hoven P.T., Kaufman A., Carr W.W. Management of allergic conjunctivitis: an evaluation of the perceived comfort and therapeutic efficacy of olopatadine 0.2% and azelastine 0.05% from two prospective studies. Clin. Ophthalmol. 2009; 3: 329-36. doi: 10.2147/opth.s5223.
- Alcon. Olopatadine hydrochloride solution, 0.2%, package insert. Fort Worth, TX: Alcon Laboratories, Inc. 2004.
- Brodsky M. Allergic conjunctivitis and contact lenses: experience with olopatadine hydrochloride 0.1% therapy. Acta Ophthalmol. Scand. Suppl. 2000; 230: 56-9.
- du Toit R., Situ P., Simpson T., Fonn D. The effects of six months of contact lens wear on the tear film, ocular surfaces, and symptoms of presbyopes. Optom. Vis. Sci. 2001; 78: 455-62.
- Dogru M., Ozmen A., Erturk H., et al. Changes in tear function and the ocular surface after topical olopatadine treatment for allergic conjunctivitis: an open-label study. Clin. Ther. 2002; 24: 1309-21.
- Mah F.S., O’Brien T., Kim T. Evaluation of olopatadine hydrochloride 0.2% in an allergic conjunctivitis patient population with dry eye. In: Western Society of Allergy, Asthma and Immunology 2007 Scientific Session, January 14-18, 2007, Wailea Maui, HI.
- Krokhmal L., Gomes P., Welch D., Abelson M.B. The incidence of dry eye with topical anti-allergic therapies. In: Association for Research in Vision and Ophthalmology Annual Meeting, May 6-10, 2007, Fort Lauderdale, FL, Poster #2300.
- Abelson M.B., Gomes P.J., Vogelson C.T., et al. Clinical efficacy of olopatadine hydrochloride ophthalmic solution 0.2% compared with placebo in patients with allergic conjunctivitis or rhinoconjunctivitis: a randomized, double-masked environmental study. Clin. Ther. 2004; 26: 1237-48.
- Abelson M.B., Gomes P.J., Vogelson C.T., et al. Effects of a new formulation of olopatadine ophthalmic solution on nasal symptoms relative to placebo in two studies involving subjects with allergic conjunctivitis or rhinoconjunctivitis. Curr. Med. Res. Opin. 2005; 21: 683-91.
- Mah F.S., Rosenwasser L.J., Townsend W.D., et al. Efficacy and comfort of olopatadine 0.2% versus epinastine 0.05% ophthalmic solution for treating itching and redness induced by conjunctival allergen challenge. Curr. Med. Res. Opin. 2007; 23: 1445-52.
- Abelson M.B., Spitalny L. Combined analysis of two studies using the conjunctival allergen challenge model to evaluate olopatadine hydrochloride, a new ophthalmic antiallergic agent with dual activity. Am. J. Ophthalmol. 1998; 125: 797-804.
- Scandashree K., Patil M., Udaykumar P. Comparative study of the efficacy and safety of olopatadine eyedrops and sodium cromoglycate in clinical practice: a prospective study. International Journal of Basic & Clinical Pharmacology. 2017; 5 (5): 1764-1769. doi: 10.18203/2319-2003.ijbcp20163047.
- Aguilar A.J. Comparative study of clinical efficacy and tolerance in seasonal allergic conjunctivitis management with 0.1% olopatadine hydrochloride versus 0.05% ketotifen fumarate. Acta Ophthalmol. Scand. Suppl. 2000; 230: 52-5.