Алергічний кон’юнктивіт: сучасні підходи до класифікації, діагностики та лікування
Переклала й адаптувала лікарка-алерголог Ірина Калікіна
Алергічний кон’юнктивіт (АК) – поширений і часто недооцінений стан, який характеризується імунологічним запальним процесом на передній поверхні ока й істотно знижує якість життя пацієнтів. Його поширеність зростає протягом останніх десятиліть, що пов’язано з комбінованим впливом генетичних чинників, забруднення довкілля, змін у складі пилку рослин і урбанізації. За різними оцінками, хвороба виявляється в 10-40% загальної популяції, однак реальні цифри можуть бути вищими через значний рівень недіагностованості [1, 2].
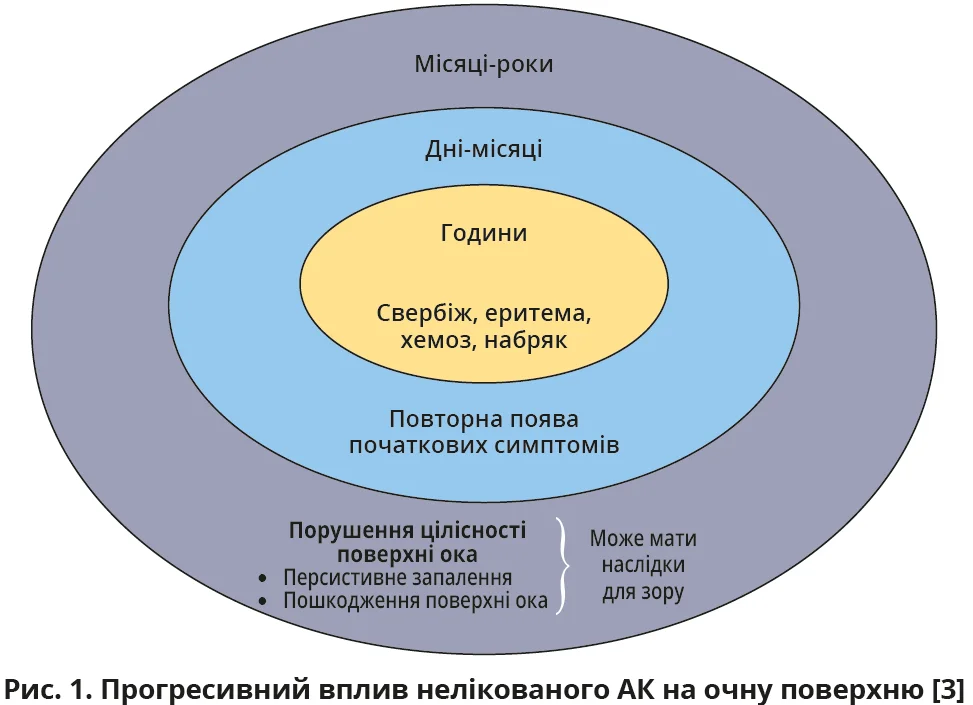
Незважаючи на переважно доброякісний перебіг, АК нерідко поєднується з алергічним ринітом, атопічним дерматитом і бронхіальною астмою, утворюючи єдиний атопічний синдром. Недостатньо лікований або нелікований АК має прогресивний характер: від гострої фази зі свербежем, гіперемією та хемозом до хронічного запалення з пошкодженням тканин унаслідок токсичного впливу метаболітів еозинофілів й інших медіаторів, що може мати незворотні наслідки для зору [3] (рис. 1).
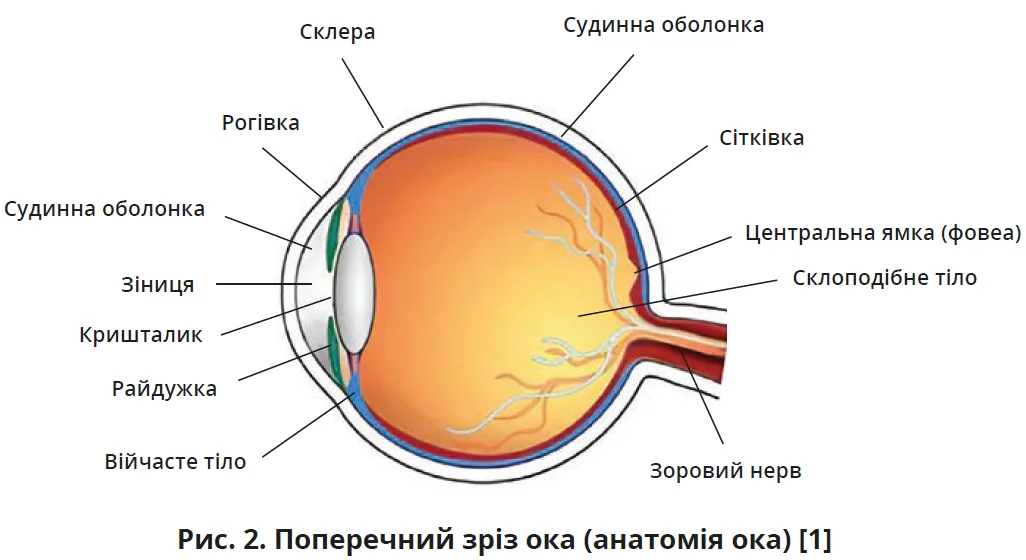
Око є складним органом, кожна структура якого виконує специфічну імунологічну роль. Кон’юнктива та рогівка є зовнішніми структурами, що безпосередньо контактують з алергенами. У нормі тучні клітини локалізуються під епітелієм кон’юнктиви в поверхневому шарі власної пластинки, при АК їхня кількість разом з еозинофілами істотно зростає в кон’юнктиві [1] (рис. 2).
Класифікація й етіологія
АК є гетерогенною групою захворювань. Відповідно до сучасної класифікації виділяють такі основні форми [2, 4]:
- простий АК – більшість випадків АК виникають унаслідок простого контакту алергену з поверхнею ока. Прості форми АК поділяються на три підтипи:
- гострий АК – минущий епізод із чіткою причинно-наслідковою картиною, виникає при контакті з алергеном: хімічним, косметичним тощо;
- сезонний АК – найпоширеніша форма, загострення виникають переважно навесні та влітку (мають чітку сезонність) і зумовлені контактом з пилком дерев і трав, склад яких варіюється залежно від географічного регіону;
- цілорічний АК – менш поширена, персистивна форма. Тригерами виступають алергени кліщів домашнього пилу, лупа тварин і спори грибків. При контакті алергену з поверхнею ока відбувається дегрануляція тучних клітин з вивільненням гістаміну й інших медіаторів запалення, саме гістамін визначає провідний симптом хвороби – свербіж очей;
- весняний кератокон’юнктивіт (ВКК) – хронічне запальне захворювання, патогенез якого включає IgE-опосередковану гіперчутливість і Т-клітинні імунні реакції. У теплих і сухих кліматичних зонах (Близький Схід, тропічна Африка, Середземномор’я) може набувати цілорічного характеру;
- атопічний кератокон’юнктивіт (АКК) – хронічна двобічна форма, тісно пов’язана з атопічним дерматитом (більш ніж у 90% випадків). Поєднує риси гіперчутливості I та IV типів [2];
- гігантський папілярний кон’юнктивіт (ГПК) – виникає внаслідок механічного подразнення кон’юнктиви контактними лінзами, очними протезами, швами або сторонніми тілами. Оскільки патофізіологія та підходи до лікування суттєво перетинаються з іншими формами алергічного ураження, ця нозологія включена до групи очних алергій [1, 6].
Клінічна картина
Прості форми АК
Провідними симптомами всіх форм АК є свербіж очей, сльозотеча та гіперемія кон’юнктиви. Виділення прозорі, водянисті. Симптоматика часто поєднується з проявами алергічного риніту [1, 2].
Весняний кератокон’юнктивіт
ВКК маніфестує переважно навесні й характеризується вираженішою симптоматикою: густими слизовими виділеннями, болем, світлобоязню, розмитістю зору та відчуттям стороннього тіла. Під час огляду виявляються гігантські сосочки на верхній тарзальній кон’юнктиві, жовто-білі крапки на лімбі (крапки Горнера) або кон’юнктиві (крапки Трантаса), зморшки на нижній повіці (лінії Денні – Моргана), утворення псевдомембрани на верхній повіці [2, 5].
Атопічний кератокон’юнктивіт
АКК вирізняється цілорічним, хронічним перебігом. Симптоми – біль, світлобоязнь, відчуття стороннього тіла – менш інтенсивні, ніж у разі ВКК, проте стійкіші. Характерними є виражені зміни повік і періорбітальної шкіри (ліхенізація, ектропіон, лінії Денні – Моргана, симптом Гертога – відсутність зовнішньої третини брів) [2].
Гігантський папілярний кон’юнктивіт
На відміну від простих форм АК, ГПК схильний до прогресування з формуванням тяжчої та стійкішої симптоматики. Хворі скаржаться на наростання свербежу, трансформацію виділень із прозорих водянистих у густі слизові, а також на біль, гіперемію, непереносимість контактних лінз, затуманення зору та виражене відчуття стороннього тіла. Характерно, що симптоми посилюються після зняття контактних лінз, а не під час їх носіння. При огляді – гігантські сосочки на верхній тарзальній кон’юнктиві, відкладення на лінзах [2, 6].
Діагностика
Діагноз АК встановлюється переважно клінічно на підставі анамнезу й огляду. За підозри на ушкодження рогівки виконується флюоресцеїнова проба. Шкірне прик-тестування або визначення специфічних IgE доцільне для ідентифікації тригерних алергенів. За підозри на контактну реакцію уповільненого типу (екзематозний блефарит, блефарокон’юнктивіт) показано патч-тестування; серед найпоширеніших тригерів – бензалконію хлорид і тимеросал [2, 3].
Диференційна діагностика охоплює вірусний і бактеріальний кон’юнктивіт, синдром сухого ока, блефарит і контактний алергічний блефарокон’юнктивіт.
Лікування
Незалежно від форми АК потрібно мінімізувати контакт з алергеном: носити сонцезахисні окуляри, зволожувати повітря вдома, обмежувати перебування надворі в години максимального пилкування, уникати макіяжу та контактних лінз у гострий період. Пацієнтів слід переконати не терти очі, оскільки механічне подразнення посилює дегрануляцію тучних клітин. Холодні компреси та замінники сльози зменшують дискомфорт і вимивають алергени з кон’юнктивального мішка [2].
Фармакотерапія: ступінчастий підхід
Медикаментозна терапія АК будується за ступінчастим принципом залежно від ступеня тяжкості та форми хвороби. На першому ступені застосовуються замінники сльози, при недостатній ефективності – стабілізатори тучних клітин та/або антигістамінні краплі. У тяжких випадках підключають топічні кортикостероїди під наглядом фахівця.
При системних симптомах розглядається пероральна антигістамінна терапія [1, 2].
Стабілізатори тучних клітин пригнічують дегрануляцію тучних клітин і є ефективними при тривалому застосуванні. Їхнім суттєвим недоліком є відсутність миттєвої дії: для досягнення максимального ефекту потрібні тижні регулярного використання, що обмежує їх застосування під час гострих епізодів.
Топічні антигістамінні препарати забезпечують швидке полегшення свербежу та гіперемії. Поєднання антигістамінної та мембраностабілізувальної дій в одному препараті стало важливим кроком у терапії, оскільки дає змогу одночасно впливати на гострі симптоми й запобігати подальшому вивільненню медіаторів запалення.
Топічні кортикостероїди призначаються при тяжких загостреннях і кератопатії, короткими курсами, зі спостереженням лікаря.
Імуномодулятори (циклоспорин, такролімус) призначаються при рефрактерних до стероїдів формах ВКК й АКК. Ефект розвивається протягом 6 тижнів [2].
Місце олопатадину в терапії алергічних захворювань очей: фармакологічні особливості та клінічне значення
Механізм дії та фармакологічний профіль
Олопатадину гідрохлорид є офтальмологічним препаратом з подвійним механізмом дії, що поєднує потужний селективний антагонізм H1-гістамінових рецепторів зі стабілізацією тучних клітин кон’юнктиви. Саме ця подвійна дія відрізняє олопатадин від «чистих» антигістамінних засобів або монопрепаратів – стабілізаторів тучних клітин.
Механізм антагонізму H1-рецепторів: олопатадин конкурентно блокує H1-рецептори кон’юнктиви та повік, тим самим запобігаючи зв’язуванню гістаміну й розвитку свербежу, гіперемії, хемозу та набряку. На відміну від антагоністів H1, що діють лише після дегрануляції тучних клітин, мембраностабілізувальна дія олопатадину запобігає самій дегрануляції – вивільненню не лише гістаміну, а й простагландинів, лейкотрієнів і триптази [7]. Крім того, олопатадин пригнічує хемотаксис і активацію еозинофілів – клітин, що беруть участь у хронічному алергічному запаленні (в дослідженнях in vitro) [8].
Важливою характеристикою молекули також є краща суб’єктивна переносимість олопатадину – менший дискомфорт після інстиляції [9].
Базова форма олопатадину, 0,1% розчин, призначається двічі на день. Порівняно з іншими антигістамінними очними краплями олопатадин демонструє переваги за швидкістю настання ефекту та суб’єктивним комфортом.
Дослідження Aguilar (2000) показало, що олопатадин 0,1% зменшував свербіж уже через 30 хвилин після першої інстиляції, а вища частка пацієнтів відзначала поліпшення та кращу комфортність інстиляції порівняно з кетотифеном фумаратом 0,05% [9].
Порівняно зі стабілізаторами тучних клітин олопатадин продемонстрував суттєву перевагу над недокромілом натрію в дослідженні Butrus і співавт. (2000): одна крапля олопатадину виявилася ефективнішою, ніж 29 крапель недокромілу натрію при провокаційному тесті (p <0,001). Препарат також оцінювався пацієнтами як значно комфортніший [10]. Перевага перед монопрепаратом кромоглікату натрію 2% підтверджена в міжнародному рандомізованому дослідженні за участю групи Katelaris і співавт. [11].
Важливими є результати порівняльного дослідження олопатадину та лотепреднолу (кортикостероїд): олопатадин виявився ефективнішим щодо зменшення гострих симптомів сезонного АК (свербіж, гіперемія). Водночас у групі лотепреднолу зафіксовано статистично значуще підвищення внутрішньоочного тиску вже через 2 тижні застосування (p <0,001), що підкреслює переваги олопатадину з погляду безпеки [12].
Тривале застосування 0,1% розчину олопатадину (10 тижнів) показало поступове та стійке зниження балів свербежу й гіперемії: з 3,55 до 1,63 за шкалою оцінювання свербежу. Жодних небажаних реакцій за весь період спостереження зафіксовано не було [13]. У подвійно сліпому рандомізованому дослідженні (131 пацієнт, 10 тижнів) олопатадин 0,1% двічі на день перевершував плацебо в контролі як очних, так і носових симптомів АК та ринокон’юнктивіту [14].
Наявна доказова база свідчить про високу клінічну ефективність олопатадину гідрохлориду, що в більшості порівняльних досліджень не поступається або перевершує інші топічні протиалергічні засоби, зокрема монопрепарати – стабілізатори тучних клітин, що пояснюється його подвійним механізмом дії.
Профіль безпеки та переносимість
Олопатадин характеризується сприятливим профілем безпеки при місцевому застосуванні. Системна біодоступність після закрапування в очі є мінімальною: концентрація в плазмі крові зазвичай нижча за поріг кількісного визначення (<0,5 нг/мл) при стандартних режимах дозування. Це суттєво відрізняє місцеву форму від системних антигістамінних засобів, що можуть спричиняти седацію й антихолінергічні ефекти [13].
Сприятливий профіль безпеки олопатадину підтверджується й регуляторними рішеннями: в лютому 2020 року Управління США з контролю продовольства та медикаментів (FDA) перевела обидві форми (0,1 та 0,2%) з рецептурного до безрецептурного відпуску, що свідчить про визнання їхньої безпеки для самостійного застосування під наглядом фармацевта (FDA OTC switch, 2020).
Місце олопатадину в терапевтичному алгоритмі
З огляду на описані характеристики олопатадин, як представник групи топічних препаратів з подвійним механізмом дії, посідає важливе місце в лікуванні АК. При сезонних і цілорічних АК препарати цієї групи розглядаються як терапія вибору: поєднання антигістамінного та мембраностабілізувального ефектів забезпечує як швидке купіювання симптомів, так і превентивний контроль алергічного запалення.
Початкова фармакотерапія ВКК й АКК також охоплює топічні антигістамінні препарати з мембраностабілізувальною дією (зокрема олопатадин) зазвичай у поєднанні зі штучною сльозою до призначення топічних кортикостероїдів або імуномодуляторів за рефрактерного перебігу. При ГПК олопатадин застосовується аналогічно іншим формам АК після усунення механічного подразника [2].
Висновки
АК є поширеним, клінічно гетерогенним захворюванням, що потребує диференційованого підходу залежно від форми та ступеня тяжкості. Правильна верифікація підтипу визначає стратегію лікування та прогноз для пацієнта.
У сучасному арсеналі засобів для лікування алергічних захворювань ока олопатадину гідрохлорид займає важливе місце завдяки подвійному механізму дії. Поєднання селективного антагонізму H1-рецепторів зі стабілізацією тучних клітин кон’юнктиви, пригніченням вивільнення медіаторів запалення та гальмуванням еозинофільної активності забезпечує препарату високу клінічну ефективність, підтверджену в клінічних дослідженнях, включно з рандомізованими контрольованими випробуваннями та довгостроковими спостереженнями.
Швидкий початок дії, тривалість ефекту, сприятливий профіль безпеки та відсутність ризику підвищення внутрішньоочного тиску, притаманного кортикостероїдам, роблять олопатадин обґрунтованим вибором у лікуванні простих форм АК, а також компонентом початкової терапії тяжчих персистивних форм.
Література
- Dupuis P., Prokopich C.L., Hynes A., Kim H. A contemporary look at allergic conjunctivitis. Allergy Asthma Clin. Immunol. 2020; 16: 5.
- Baab S., Le P.H., Gurnani B., Kinzer E.E. Allergic conjunctivitis. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2024 Jan 26. Available at: https://www.ncbi.nlm.nih.gov/books/NBK448118.
- Bielory L., Delgado L., Katelaris C., et al. ICON Diagnosis and management of allergic conjunctivitis. Annals of Allergy, Asthma & Immunology. 2019; 124: 118-134.
- Leonardi A., Castegnaro A., Valerio A.L., Lazzarini D. Epidemiology of allergic conjunctivitis: clinical appearance and treatment patterns in a sample of 17,919 patients. Curr. Opin. Allergy Clin. Immunol. 2015; 15 (5): 482-488.
- Bielory L., Meltzer E.O., Nichols K.K., et al. An algorithm for the management of allergic conjunctivitis. Allergy Asthma Proc. 2013; 34 (5): 408-420.
- Donshik P.C. Giant papillary conjunctivitis. Trans. Am. Ophthalmol. Soc. 1994; 92: 687-744.
- Abelson M.B., Gomes P.J. Olopatadine 0.2% ophthalmic solution: the first ophthalmic antiallergy agent with once-daily dosing. Expert Opin. Drug Metab. Toxicol. 2008; 4 (4): 453-461.
- Cook E.B., Stahl J.L., Lowe L., et al. Olopatadine inhibits anti-IgE-stimulated conjunctival mast cell upregulation of ICAM-1 expression on conjunctival epithelial cells. Ann. Allergy Asthma Immunol. 2001; 87 (5): 424-429.
- Aguilar A.J. Comparative study of clinical efficacy and tolerance in seasonal allergic conjunctivitis management with olopatadine hydrochloride 0.1% versus ketotifen fumarate 0.05%. Acta Ophthalmol. Scand. Suppl. 2000; 230: 52-55.
- Butrus S., Greiner J.V., Discepola M., Finegold I. Comparison of the clinical efficacy and comfort of olopatadine hydrochloride 0.1% ophthalmic solution and nedocromil sodium 2% ophthalmic solution in the human conjunctival allergen challenge model. Clin. Ther. 2000 Dec; 22 (12): 1462-1472. doi: 10.1016/s0149-2918(00)83044-1. PMID: 11192137.
- Katelaris C.H., Ciprandi G., Missotten L., Turner F.D., Bertin D., Berdeaux G.; International Olopatadine Study Group. A comparison of the efficacy and tolerability of olopatadine hydrochloride 0.1% ophthalmic solution and cromolyn sodium 2% ophthalmic solution in seasonal allergic conjunctivitis. Clin. Ther. 2002 Oct; 24 (10): 1561-1575. doi: 10.1016/s0149-2918(02)80060-1. PMID: 12462286.
- Berdy G.J., Spangler D.L., Bensch G., et al. A comparison of the efficacy and tolerability of olopatadine HCl 0.1% ophthalmic solution and loteprednol etabonate 0.2% ophthalmic suspension. Clin. Ther. 2000; 22 (12): 1462-1472.
- Uchio E. Treatment of allergic conjunctivitis with olopatadine hydrochloride eye drops. Clin. Ophthalmol. 2008 Sep; 2 (3): 525-531.
- Abelson M.B., Turner D. A randomized, double-blind, parallel-group comparison of olopatadine 0.1% ophthalmic solution versus placebo for controlling the signs and symptoms of seasonal allergic conjunctivitis and rhinoconjunctivitis. Clin. Ther. 2003 Mar; 25 (3): 931-947. doi: 10.1016/s0149-2918(03)80115-7. PMID: 12852709.