Ефективність, безпека та переносимість збільшених доз біластину при хронічній спонтанній кропив’янці, не контрольованій стандартними дозами інших антигістамінних препаратів другого покоління
Переклала й адаптувала лікарка-алерголог Ірина Калікіна
Хронічна спонтанна кропив’янка (ХСК) – опосередкована тучними клітинами хвороба шкіри, що проявляється рецидивними папульозними висипаннями з ангіоедемою або без неї тривалістю понад 6 тижнів за відсутності чіткого тригера. Хоча б один епізод кропив’янки протягом життя виникає приблизно у 20% людей. ХСК значно погіршує якість життя та створює значне соціальне навантаження, що потребує належного лікування.
Сучасні клінічні настанови рекомендують антигістамінні препарати другого покоління (АГП ІІ), омалізумаб і циклоспорин у межах покрокового алгоритму. АГП ІІ є засобами першої лінії завдяки їхній ефективності, безпеці та доступності. За недостатньої відповіді допускається підвищення дози АГП ІІ до чотириразової від стандартної. Препарати другої та третьої ліній – омалізумаб і циклоспорин – залишаються дорогими й мають обмежену доступність.
Біластин є сучасним високоселективним блокатором H1-гістамінових рецепторів з мінімальним проникненням крізь гематоенцефалічний бар’єр і відсутністю клінічно значущих взаємодій із системою цитохрому P450 (CYP450), що забезпечує низький седативний потенціал і сприятливий профіль лікарських взаємодій. Стандартна (ліцензована) доза біластину становить 20 мг на добу. За наявними даними, підвищення до 80 мг на добу визнано безпечним й ефективним. Разом з тим реальна клінічна практика переважно обмежується стандартною дозою, а доказова база щодо підвищення дози залишається досить обмеженою.
Метою дослідження стало оцінювання ефективності, безпеки та переносимості біластину в дозах 20, 40 і 80 мг на добу в пацієнтів з ХСК, резистентною до стандартних доз інших АГП ІІ, а також пошук предикторів, які могли б обґрунтовувати рішення про підвищення дози.
Пацієнти та методи
Дизайн дослідження й відбір пацієнтів
Інституційне відкрите одногрупове проспективне дослідження проводилося на базі кафедри дерматології медичного факультету та лікарні Sagore Dutta (м. Колката, Індія) протягом 12 місяців (з лютого 2022 по березень 2023 року) після отримання етичного схвалення (Institute/IEC/204/01-2021). Дослідження внесено до Реєстру клінічних випробувань Індії (CTRI/2021/08/035626). Дотримано вимоги належної клінічної практики (GCP), Гельсінської декларації й індійського регуляторного стандарту Schedule Y.
Скринінг пройшли 43 пацієнти з ХСК віком 18-65 років з неконтрольованим перебігом хвороби (оцінка активності кропив’янки UAS7 ≥7), незважаючи на приймання стандартних доз будь-якого АГП ІІ, крім біластину.
До критеріїв вилучення належали: вік поза діапазоном 18-65 років, індуковані або інші хронічні варіанти кропив’янки, системні коморбідності, вагітність і лактація, психічні чи неврологічні розлади, зловживання психоактивними речовинами, неграмотність, що унеможливлювала ведення щоденника UAS7, а також застосування омалізумабу протягом попередніх 6 місяців. Від кожного учасника отримано письмову інформовану згоду.
Клінічна оцінка пацієнтів з ХСК
Усі залучені пацієнти пройшли ретельне клінічне обстеження з оцінюванням тривалості хвороби, ангіоедеми, дермографізму, дисфункції щитоподібної залози, атопічного анамнезу та вихідного показника UAS7. Система оцінювання UAS7 ураховує щоденну кількість папул (0-3 бали) й інтенсивність свербежу (0-3 бали), підсумованих за 7 днів (максимальна оцінка – 42 бали). Згідно із цією шкалою кропив’янку класифікували таким чином: відсутність симптомів (0), контрольований (1-6), легкий (7-15), помірний (16-27) і тяжкий перебіг (28-42).
Базове лабораторне обстеження включало: розгорнутий аналіз крові з п’ятикомпонентною лейкоцитарною формулою, С-реактивний білок (СРБ), функціональні проби печінки та нирок, загальний імуноглобулін Е (IgE), електрокардіографію, а також нейтрофільно-лімфоцитарне (НЛС) і тромбоцитарно-лімфоцитарне співвідношення (ТЛС). Безпеку моніторували при кожному візиті шляхом реєстрації небажаних реакцій, а переносимість оцінювали на підставі підрахунку таблеток.
Хід дослідження
Перед початком активної фази було передбачено двотижневий період виведення препарату з організму (період «вимивання»), протягом якого як препарат швидкої допомоги дозволялося приймати лише біластин у дозі 20 мг.
Паралельно збирали вихідні лабораторні дані, велося щоденне записування даних за шкалою UAS7 та оформлювали інформовану згоду.
На старті всім пацієнтам призначали біластин 20 мг на добу на 2 тижні. На 14-й день оцінювали UAS7: пацієнти з повною відповіддю (UAS7 = 0) були вилучені з подальшого підвищення дози, решті підвищували дозу до 40 мг 1 раз на день. Проведено перевірку на побічні ефекти та переносимість. На 28-й день за збереження симптомів (UAS7 >0) дозу підвищували до 80 мг 1 раз на день. На 42-й день (завершення дослідження) повторно оцінювали UAS7, лабораторні показники, безпеку та переносимість терапії.
Статистичний аналіз
Дані аналізували за допомогою MedCalc v12.5.0. Результати описової статистики наведено як середнє значення ± стандартне відхилення або у відсотках. Нормальність розподілу перевіряли за критерієм Шапіро – Вілка. Для порівняння груп застосовували парний t-критерій і χ²-критерій. Предиктори підвищення дози визначали методом логістичної регресії. Статистично значущими вважали результати при p <0,05.
Результати
Клініко-демографічний профіль і лабораторні показники
До дослідження було залучено 35 пацієнтів з ХСК: 17 чоловіків і 18 жінок, середній вік – 34,5±11,4 року, найбільша вікова група – 31-40 років (40%; n=14).
Медіана тривалості хвороби – 6 місяців (міжквартильний діапазон – 4-11). Ангіоневротичний набряк спостерігався у 28,6% (10/35) пацієнтів, симптоматичний дермографізм – у 22,9% (8/35), дисфункція щитоподібної залози – в 17,1% (6/35), атопічний анамнез – у 31,4% (11/35). Середній вихідний показник UAS7 становив 25,7±11,7, помірний або тяжкий перебіг мали 71,4% (25/35) пацієнтів. У всіх пацієнтів не вдалося досягти контролю симптомів за допомогою інших АГП ІІ в рекомендованих дозах: цетиризин (n=27), левоцетиризин (n=6), фексофенадин (n=2).
Показники нейтрофілів, лімфоцитів і тромбоцитів у більшості пацієнтів були в межах норми. Гіпереозинофілія спостерігалася в 60% (21/35) пацієнтів. Середні НЛС і ТЛС становили 4,03±1,56 та 140,8±37,1 відповідно. Рівень загального IgE коливався від 199 до 748,7 МО/мл (у середньому 405,7±128,7 МО/мл), підвищені значення (>200 МО/мл) зафіксовано в третини пацієнтів.
Відповідь на біластин
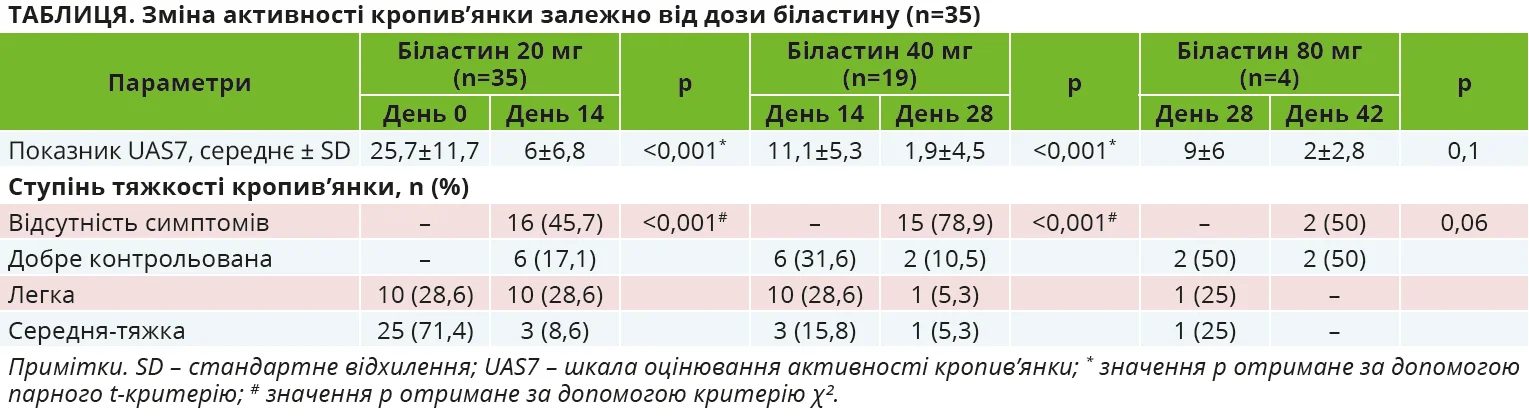
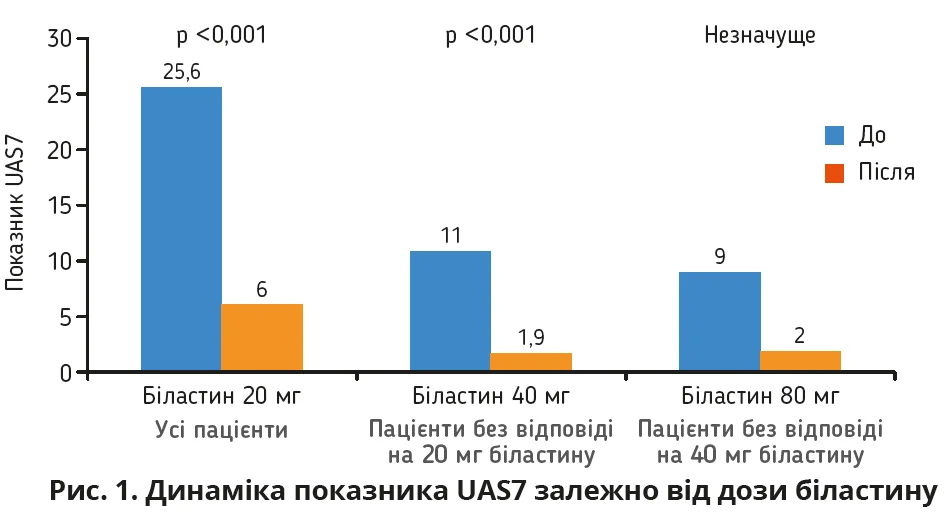
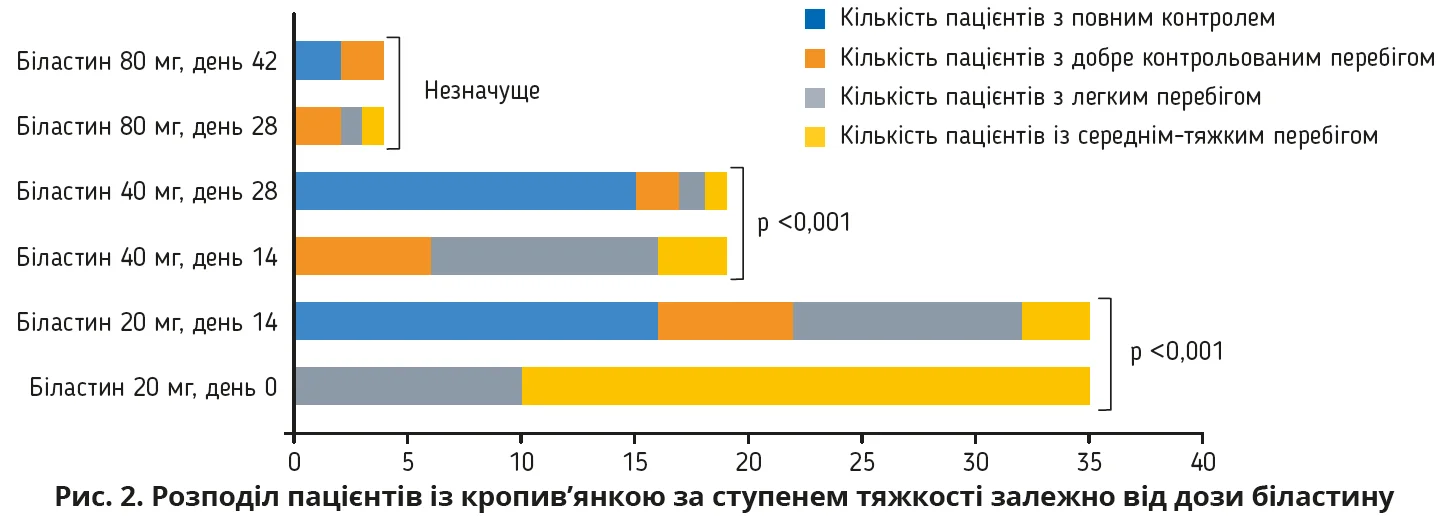
Після двотижневого періоду виведення препарату з організму всі пацієнти (n=35) отримували біластин у дозі 20 мг на добу протягом 2 тижнів. Середній показник UAS7 значно знизився з 25,7±11,7 до 6,0±6,8 на 14-й день (p <0,001). Повного контролю (UAS7 = 0) досягли 16 пацієнтів (45,7%), а 6 (17,1%) повідомили про добре контрольоване захворювання (UAS7 ≤6). Частка хворих з помірним і тяжким перебігом скоротилася із 71,4 до 8,6% (p <0,001).
Пацієнти, що досягли повного контролю, завершили участь у дослідженні, решті 19 пацієнтам підвищили дозу до 40 мг.
На 28-й день у групі біластину 40 мг середній показник UAS7 знизився з 11,1±5,3 до 1,9±4,5 (p <0,001), окрім того, 15 пацієнтів (78,9%) досягли повного контролю. Лише 4 пацієнти (11,4%) потребували подальшого підвищення дози до 80 мг. У цій підгрупі середній показник UAS7 знизився з 9,0±6,0 (день 28) до 2,0±2,8 (день 42), однак різниця не досягла статистичної значущості (p=0,1).
Серед тих, хто отримував 80 мг надалі, двоє досягли повної відповіді, двоє – задовільного контролю. Загалом лише 2 пацієнти (5,7%) залишилися рефрактерними після чотириразового підвищення дози. Отже, 88,6% (31/35) досягли повної ремісії – на дозі 20 мг (n=16) або 40 мг (n=15). Динаміка відповіді представлена в таблиці та на рисунках 1 і 2.
Біластин добре переносився в усьому діапазоні доз. На дозі 20 мг небажаних реакцій не спостерігалося. При підвищенні до 40 мг повідомлялося про сонливість (22%) та нудоту (5%). На дозі 80 мг 2 із 4 пацієнтів скаржилися на головний біль. Припинення приймання препарату не було необхідним у жодному випадку.
Прогностичні фактори для підвищення дози біластину
За результатами однофакторного регресійного аналізу, єдиним достовірним предиктором потреби в підвищенні дози виявився вищий вихідний показник UAS7 (відношення шансів 1,2; p=0,001). Низка інших параметрів – жіноча стать, тривалість хвороби, НЛС, еозинофілія, підвищений середній об’єм тромбоцитів і підвищений СРБ – демонстрували певні тенденції, проте статистичної значущості не досягли. При багатофакторному аналізі незалежних предикторів виявлено не було.
Обговорення
У цьому дослідженні оцінювали ефективність і безпеку біластину в пацієнтів з ХСК, які не реагували на стандартні дози інших АГП ІІ, зосередившись на переході на біластин і збільшенні його дози відповідно до міжнародних клінічних настанов.
Нещодавній метааналіз (Xue et al., 2023) підтвердив переваги біластину 20 мг над іншими АГП ІІ при хронічній кропив’янці. Водночас дані про перехід на біластин у пацієнтів, які не відповіли на інші АГП ІІ, залишаються обмеженими. Японське дослідження IV фази (Fukunaga et al., 2024) й індійське дослідження (De et al., 2021) продемонстрували клінічне поліпшення при переході на біластин, що узгоджується з нашими результатами. Біластин 20 мг достовірно знижував показники UAS7 (p <0,001), а 45,7% пацієнтів, рефрактерних до стандартних доз інших АГП ІІ, досягли повного контролю. Це свідчить про доцільність переходу на біластин іще до розгляду питання про підвищення дози іншого АГП ІІ, з яким не було досягнуто контролю.
Перевага біластину може бути пов’язана з його вищою специфічністю та спорідненістю до гістамінових H1-рецепторів, які приблизно втричі та вп’ятеро вищі, ніж у цетиризину й фексофенадину відповідно. Додатковими перевагами є триваліший терапевтичний ефект завдяки міцнішому зв’язку з рецептором, мінімальний ризик лікарських взаємодій і низька седація, що забезпечується субстратністю препарату до P-глікопротеїну, який обмежує його транспорт крізь гематоенцефалічний бар’єр.
Сучасні міжнародні клінічні настанови рекомендують підвищувати дозу того самого АГП ІІ до чотириразової, а не замінювати його іншим. Ця рекомендація ґрунтується на фармакодинамічних особливостях препаратів і механізмі інверсного агонізму щодо H1-рецепторів, які обґрунтовують перевагу монотерапії у вищій дозі перед комбінуванням антигістамінних засобів. Разом з тим не слід ігнорувати дані про потенційний ризик деменції при тривалому кумулятивному застосуванні АГП – це додаткова підстава для пошуку безпечніших і сучасніших варіантів, як-от біластин.
У нашій когорті біластин у дозі 40 мг забезпечував достовірне поліпшення показників за шкалою UAS7 (p <0,001), тоді як перехід до 80 мг не давав значущого додаткового ефекту (p=0,1). Схожих висновків дійшли Weller і співавт. (2018) і Sarti та співавт. (2021), тоді як De та співавт. (2023) узагалі не вдавалися до дози 80 мг. Отже, ефективність біластину при дозах понад 40 мг є обмеженою. Загалом 94,3% наших пацієнтів досягли повної відсутності симптомів – істотно більше, ніж 60-70% у західних дослідженнях навіть після чотириразового підвищення дози. Ця розбіжність може бути пов’язана з генетичною або екологічною гетерогенністю популяцій, що потребує проведення масштабних багатоцентрових міжнародних досліджень.
Біластин демонстрував добру переносимість у всіх дозах. Небажаних реакцій на стандартній дозі не виявлено, а такі симптоми, як сонливість, нудота, головний біль, за вищих доз були легкими, відповідали даним наявної літератури та не потребували скасування препарату.
Вищий вихідний показник за шкалою UAS7 виявився єдиним достовірним предиктором потреби в підвищенні дози (p=0,001), що узгоджується з попередніми дослідженнями, які визначили високу активність хвороби, СРБ та D-димер як предиктори рефрактерності до АГП. Інших предикторів виявлено не було, що, найімовірніше, пов’язано з невеликим обсягом вибірки.
Обмеження
Результати дослідження слід інтерпретувати з огляду на низку обмежень: невеликий розмір вибірки, одноцентровий дизайн дослідження, відсутність контрольної групи, відсутність даних щодо D-димеру, а також відсутність інформації про тривалість попереднього приймання АГП або дотримання пацієнтами режиму лікування, що могли вплинути на оцінку справжньої рефрактерності. Для підтвердження отриманих результатів потрібні масштабніші багатоцентрові дослідження.
Висновки
Біластин демонструє ефективність, безпеку та добру переносимість у разі ХСК – як у стандартній рекомендованій дозі 20 мг на добу, так і при подальшому підвищенні. Близько половини пацієнтів, які не відповіли на стандартні дози інших АГП ІІ, досягли повного контролю вже на дозі 20 мг біластину на добу, а доза 40 мг посилювала ефективність. Проте збільшення дози до 80 мг на добу дало мінімальну додаткову користь, що вказує на оптимальну ефективність за дози 40 мг. Вищий вихідний бал за шкалою UAS7 може слугувати клінічним орієнтиром для прогнозування потреби в підвищенні дози.
Рівень повного контролю симптомів у нашій когорті (~95%) помітно перевищив показники, отримані в західних дослідженнях (~60%), що може відображати генетичні або екологічні відмінності між популяціями.
Із практичного погляду клініцисти можуть розглянути можливість переходу на біластин перед підвищенням дози інших АГП ІІ. За потреби дозу біластину можна безпечно збільшувати до чотириразової від стандартної, як це передбачено чинними клінічними настановами.
Література
Chakraborty S.S., Podder I., Das M., Dhabal A. Effectiveness, safety, and tolerability of bilastine up-dosing in chronic spontaneous urticaria uncontrolled with licensed doses of other second-generation antihistamines – an institution-based, open-label, single-group longitudinal trial. Indian Dermatol. Online J. 2026; 17: 220-224.